孕婦梅毒血清學篩查流程探討
齊結(jié)華,張春利,吳守樂,宦 宇,陳 宇,樂江漫,蔡徐山
(上海市嘉定區(qū)婦幼保健院檢驗科,上海 201821)
梅毒是由梅毒螺旋體(Treponema pallidum,TP)引起的性傳播疾病,可通過性接觸、輸血和垂直傳播方式傳播。全球每年約有100萬TP感染孕婦,大多數(shù)是無癥狀的潛伏性感染,但有超過50%的孕婦會出現(xiàn)不良妊娠結(jié)局[1]。妊娠梅毒可導致死胎、早產(chǎn)、低出生體重兒、先天性梅毒患兒和新生兒死亡[2-3]。目前,梅毒的診斷主要根據(jù)臨床表現(xiàn)和實驗室血清學檢查。梅毒的實驗室檢測方法包括病原學檢測方法和間接的血清學檢測方法。由于病原學檢測方法存在局限性,所以血清學檢測是目前梅毒診斷和療效監(jiān)測的主要方法[4]。由于各種梅毒檢測方法的敏感性和特異性存在一定的差異,單用1種方法可能會導致漏診或誤診,因此有必要建立一個合適的篩查流程。本研究以免疫印跡法為標準,對3種常見的梅毒血清學檢測方法[甲苯胺紅不加熱血清試驗(toluidine red unheated serum test,TRUST)、化學發(fā)光法(chemiluminescence immunoassay,CLIA)、化學發(fā)光微粒子免疫分析法(chemiluminescence microparticle immunoassay,CMIA)]的聯(lián)合檢測性能進行評價,探索孕婦梅毒血清學篩查流程。
1 材料和方法
1.1 研究對象
選取2013年8月—2019年9月上海市嘉定區(qū)婦幼保健院采用Chemclin100化學發(fā)光免疫分析儀(北京科美公司)及配套試劑(CLIA)篩查抗TP抗體,且S/CO值≥1.0的孕婦548例。排除復查孕婦。采集所有孕婦靜脈血4 mL,分離血清(2 mL),-80 ℃保存待檢。
1.2 方法
1.2.1 非特異性梅毒血清學試驗 TRUST試劑盒購自上海榮盛公司。
1.2.2 抗TP抗體篩查試驗 采用ARCHITECT i2000SR全自動免疫分析系統(tǒng)(美國Abbott公司)及配套試劑(CMIA)檢測抗TP抗體,以S/CO值≥1.0為抗TP抗體陽性、<1.0為陰性。
1.2.3 抗TP抗體確證試驗 采用免疫印跡法進行結(jié)果驗證,試劑盒購自德國歐蒙公司,嚴格按試劑盒說明書操作。
1.3 統(tǒng)計學方法
采用SPSS 19.0軟件進行統(tǒng)計分析。計算各種方法聯(lián)合檢測的陽性預(yù)測值。采用受試者工作特征(receiver operating characteristic,ROC)曲線評估各種方法聯(lián)合檢測的性能。
2 結(jié)果
2.1 4種梅毒血清學試驗結(jié)果比較
CLIA檢測S/CO值≥1.0的548例孕婦血清樣本經(jīng)免疫印跡法驗證,有494例為陽性、43例為陰性,11例為不確定(該11例樣本在后續(xù)檢測中均排除)。以免疫印跡法為標準,CLIA篩查梅毒假陽性率為8.0%。在537例血清樣本中,TRUST檢出陽性295例、陰性242例;CMIA檢出陽性(S/CO值≥1.0)488例、陰性(S/CO值<1.0)49例。見表1、表2。
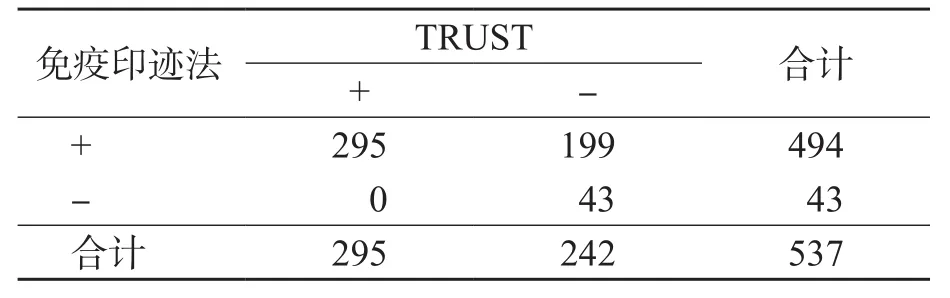
表1 TRUST與免疫印跡法結(jié)果比較 例

表2 CMIA與免疫印跡法結(jié)果比較 例
2.2 CLIA、TRUST、CMIA聯(lián)合檢測結(jié)果分析
以免疫印跡法檢測結(jié)果為標準,對3種方法的不同組合進行分析。CLIA/TRUST/CMIA(+/-/-)、CLIA/TRUST(+/-)、CLIA/TRUST/CMIA(+/-/+)、CLIA/TRUST(+/+)和CLIA/TRUST/CMIA(+/+/+)的陽性預(yù)測值分別為22.4%、82.2%、97.4%、100.0%和100.0%。CLIA /CMIA(+/+)在TRUST(-)的情況下仍然有2.6%的假陽性,但在TRUST(+)的情況下,CLIA(+)的陽性預(yù)測值可達到100.0%。見表3。
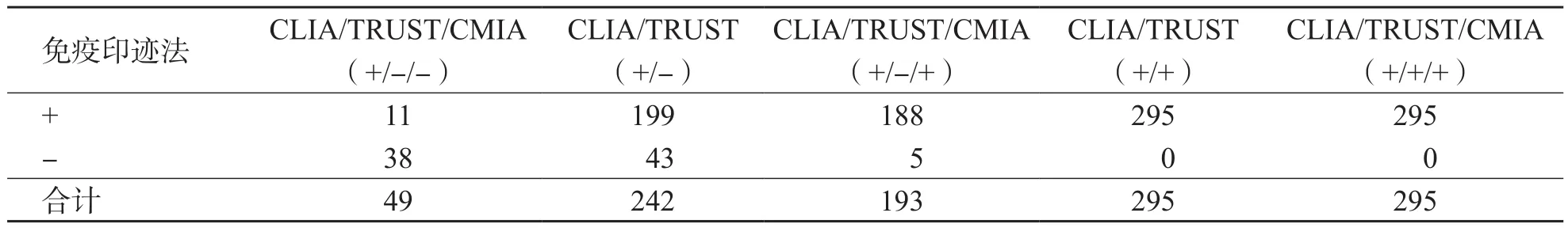
表3 各種梅毒血清學試驗聯(lián)合檢測結(jié)果分析 例
2.3 CMIA/TRUST/CLIA(+/-/+)篩查TP陽性的效能
以免疫印跡法檢測結(jié)果為標準,CMIA/TRUST/CLIA(+/-/+)檢出陽性193例。ROC曲線分析結(jié)果顯示,CMIA/TRUST/CLIA(+/-/+)篩查TP陽性的曲線下面積(area under curve,AUC)為0.964,約登指數(shù)最大(0.947)時CMIA的S/CO值為2.31,敏感性為94.7%,特異性為100.0%。見圖1、表4。
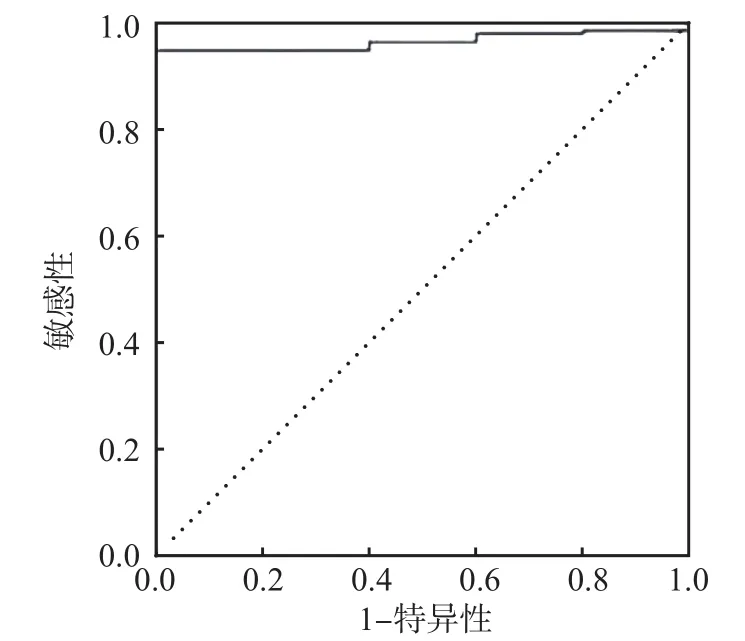
圖1 CMIA/TRUST/CLIA(+/-/+)篩查TP陽性的ROC曲線
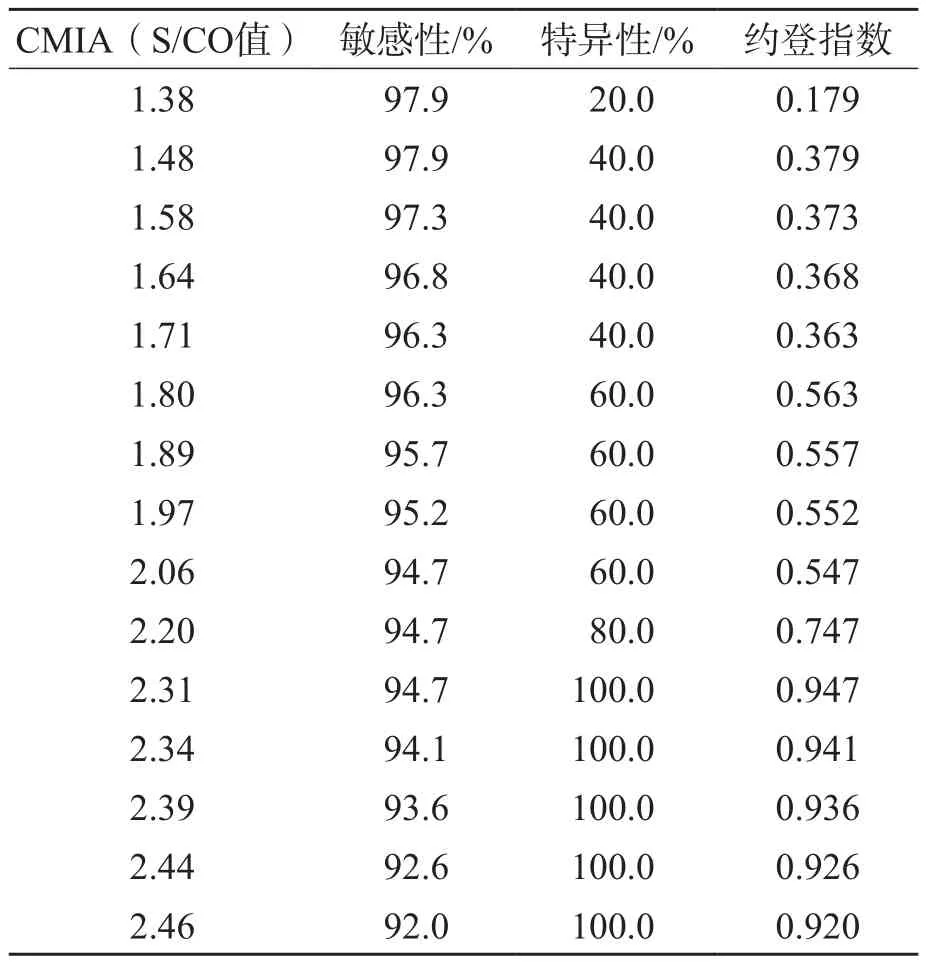
表4 CMIA/TRUST(+/-)不同臨界值篩查TP陽性的效能
2.4 孕婦梅毒血清學篩查流程的制定
根據(jù)上述結(jié)果制定孕婦梅毒血清學篩查流程。流程要點:先采用CLIA初篩抗TP抗體,如呈陰性則報告陰性,如呈陽性則加做TRUST。TRUST陽性則報告陽性,TRUST陰性則采用CMIA復檢。CMIA復檢呈陽性,且S/CO值≥2.31則報告陽性;CMIA復檢為陰性,或雖呈陽性但S/CO值<2.31時,加做免疫印跡法檢測,最后根據(jù)免疫印跡法結(jié)果出具報告。見圖2。
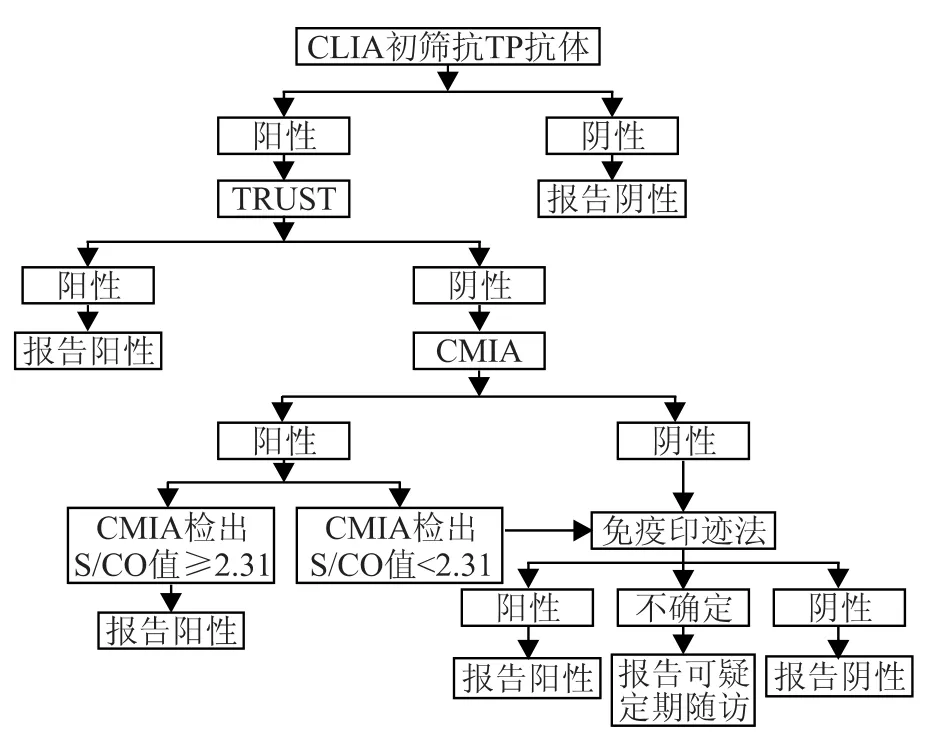
圖2 孕婦梅毒血清學試驗篩查流程圖
3 討論
目前,多數(shù)實驗室采用CLIA、CMIA、TRUST等進行梅毒篩查,但這些方法都存在各種假陰性或假陽性問題。為了排除假陽性,我國大多實驗室對抗TP抗體陽性樣本一般采用梅毒螺旋體明膠凝集試驗(Treponema pallidum particle assay,TPPA)進行確認,但TPPA敏感性低于CLIA,不建議采用[5]。免疫印跡法針對TP外膜的4種脂蛋白進行檢測,敏感性高、特異性好,是目前國際公認的梅毒確證方法[6],但由于成本以及操作方面的原因,不適合大批量樣本的檢測。蔡徐山等[7]的研究結(jié)果顯示,采用Chemclin100化學發(fā)光免疫分析儀及配套試劑(CLIA),以廠商聲明的S/CO值=1.0作為臨界值篩查抗TP抗體具有較高的敏感性,適用于大批量樣本的篩查;檢測性能與進口檢測系統(tǒng)一致,成本相對較低[7]。因此,本研究選擇該檢測系統(tǒng)篩查抗TP抗體。
本研究以免疫印跡法為標準,對不同的檢測方法組合進行了評價。結(jié)果顯示,CLIA檢測抗TP抗體的陽性預(yù)測值為92.0%,CLIA/TRUST(+/-)的陽性預(yù)測值為82.2%,CLIA/TRUST/CMIA(+/-/-)的陽性預(yù)測值僅為22.4%;采用CMIA復檢CLIA/TRUST(+/-)的樣本,結(jié)果顯示CLIA/TRUST/CMIA(+/-/+)的陽性預(yù)測值為97.4%,仍然存在2.6%的假陽性。另外,CLIA/TRUST(+/+)和CLIA/TRUST/CMIA(+/+/+)的陽性預(yù)測值均可達100.0%。蔡徐山等[7]建議將CLIA檢測孕婦抗TP抗體的陽性判斷值提高到3.32;黃文彩等[8]建議將CMIA檢測抗TP抗體的S/CO灰區(qū)設(shè)置為1.000~6.815。但以上報道均只是針對某1種檢測方法進行評價。本研究的ROC曲線分析結(jié)果顯示,CLIA /TRUST/CMIA(+/-/+)組合中CMIA S/CO值的最佳臨界值為2.31。據(jù)此,本研究借鑒抗人類免疫缺陷病毒(human immunodeficiency virus,HIV)抗體篩查試驗程序,設(shè)計了孕婦梅毒血清學試驗的篩查流程(圖2)。
孕婦梅毒篩查對優(yōu)生優(yōu)育有著重大意義,97.4%的陽性預(yù)測值無法滿足需求。為了提高孕婦梅毒檢測的準確性,防止CLIA和CMIA同時假陽性的情況發(fā)生,本研究根據(jù)最佳臨界值確定了CLIA/TRUST/CMIA(+/-/+)的復檢范圍為1.0≤S/CO值<2.31。蔡徐山等[7]對13 974例孕婦樣本進行抗TP抗體篩查,初篩陽性率為1.09%;孫斌等[9]對63 109例孕婦樣本進行抗TP抗體篩查,初篩陽性率為0.82%。考慮到復檢成本,本研究設(shè)計的篩查流程中復檢規(guī)則采用的順序是TRUST→CMIA→免疫印跡法,成本從低到高,可大大減少最終需要用免疫印跡法檢測的樣本量,合理、有效地利用醫(yī)療資源。
2015年英國發(fā)布的梅毒管理指南[10]要求當?shù)?種抗TP抗體篩查陽性時,需做另一種抗TP抗體試驗進行確證,若確證試驗陰性,需以IgG免疫印跡試驗結(jié)果為診斷標準。我國國家衛(wèi)生健康委發(fā)布的《預(yù)防艾滋病、梅毒和乙肝母嬰傳播工作實施方案(2015年版)》[11]中也提出了孕產(chǎn)婦梅毒檢測及服務(wù)流程,其中1條指出:當TP抗原血清學試驗為陽性時,應(yīng)選擇非TP抗原血清學試驗進行復檢,復檢陰性即判斷既往感染梅毒或極早期梅毒或部分晚期梅毒,隨即給予治療。但其忽略了TP抗原血清學試驗假陽性的問題。本研究提出的篩查流程與英國的梅毒管理指南[10]中采用的確證試驗一致,同時增加了非TP抗原血清學試驗,并提出了CLIA/TRUST(+/-)但CMIA為弱反應(yīng)(1.0≤S/CO值<2.31)的樣本也應(yīng)采用免疫印跡法檢測。相對于文獻[11],本研究對孕婦梅毒篩查流程進行了補充和細化,更有利于提高孕婦梅毒血清學篩查的陽性預(yù)測值和準確性,可有效避免了假陽性結(jié)果。
綜上所述,本研究結(jié)合4種梅毒血清學試驗方法建立了孕婦梅毒篩查流程:先通過CLIA篩查抗TP抗體,再采用TRUST復檢,并兼顧CMIA檢測抗TP抗體S/CO臨界值的復檢范圍,在降低復檢成本的同時,有效提升了孕婦梅毒血清學篩查的陽性預(yù)測值和準確性。

