用后即溶的起搏器
南方周末特約撰稿 陳彬
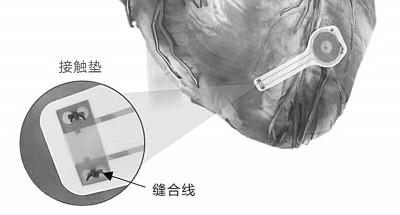
起搏器安裝在心臟上的位置。
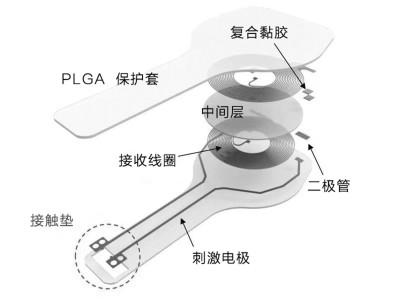
美國西北大學科學家研發的無線暫態臨時心臟起搏器,整個系統只有0.3克重,0.25毫米薄。
★美國科學家發明了一種新的心臟起搏器,這種起搏器不需要導線或者電池,而是通過無線的方式獲得能量和起搏指令。更神奇的是,起搏器會在使用結束后被體液逐漸溶解,無需取出。
2021年4月30日,國家藥品監督管理局發布通告,首次批準了國內一家企業研發生產的臨時心臟起搏器的注冊申請。第一例國產臨時心臟起搏器獲批上市將為醫療機構提供更多的選擇,并有利于降低臨時心臟起搏器的價格。
作為一種緊急或者過渡性的治療工具,臨時心臟起搏器盡管早已獲得了廣泛應用,但仍有一些不容忽視的缺陷,存在出現各類并發癥的風險。近日,美國西北大學等研究機構的科學家在國際著名學術期刊《自然生物技術》上發表了一篇論文,介紹了一種他們新研發的臨時心臟起搏器。這種起搏器不需要導線或者電池,而是通過無線的方式獲得能量和起搏指令。更神奇的是,這種起搏器在使用結束后會被體液逐漸溶解,無需取出。
這是一款用后即溶的起搏器。
心臟怎么了?
人體的組織和器官要正常運作,離不開持續而穩定的血液供應,這就要求作為泵血器官的心臟需要以恰當的頻率有節律地搏動。如果搏動異常,供血就會出問題,很多心臟病歸根結底都是這種搏動異常導致的。
人的心臟分為左右兩個心房和心室,只有心房和心室充分配合,心臟才能以最高效的方式完成泵血。在右心房上,有一個叫竇房結的區域,這個區域中有一類特殊的細胞,能夠有節奏地產生興奮信號。這些信號會使心房負責收縮的心肌細胞收縮,把血液泵入心室。另一方面,興奮信號還會傳遞到右心房鄰近右心室的一個叫房室結的區域。在正常情況下,這里是興奮信號從心房傳遞到心室的唯一途徑。房室結不僅是興奮信號的“必經之路”,還承擔著協調心房和心室收縮的任務:由于心臟結構和組織自身的特點,經過這里傳導到心室的興奮信號被“蓄意”延擱了很短的一段時間,這樣可以保證在一個心動周期中心房先充分收縮,血液進入心室,然后心室的肌肉細胞再收縮,把血液高效地泵出心臟。
如果這種有節律、講秩序的搏動出現異常,心臟就無法為全身各處的組織和器官穩定地提供充足的血液供應。以一類叫作房室傳導阻滯的心臟疾病為例,在這類疾病中,從心房傳導到心室的興奮出現了部分或完全的中斷,輕則興奮信號傳導延擱的時間變得比正常時間更長,重則興奮的傳導被完全阻滯(心室中也有一些會產生興奮信號的細胞,因此在這種情況下心室仍然會收縮,只是心房和心室的收縮變得完全各自為政)。如果阻滯程度嚴重,病人就需要植入心臟起搏器來幫助心臟正常運行。
臨時起搏
每當提到心臟起搏器,很多人的第一反應也許仍然是“笨拙”“開胸手術”這樣的字眼。但其實如今的心臟起搏技術已經非常成熟,起搏器不僅非常小巧(尺寸僅為幾厘米),而且植入也不需要開胸手術,而是以心臟介入手術的形式實現的。
在植入起搏器時,醫生會在病人胸部的皮膚上切開一個小口,在皮下做一個囊袋。接著,在X射線透視的輔助引導下,醫生會通過靜脈穿刺把起搏導線通過靜脈血管送入需要放置的心臟腔室的合適位置,并把導線連接到起搏器上。在設置好起搏器的相關參數后,醫生最后會把起搏器放在此前做好的囊袋里,并縫合切口。根據設置好的參數,起搏器會以電脈沖的形式刺激心臟,幫助心臟正常運行。這些起搏器由電池供電,在電量耗盡前就需要做手術更換(起搏器和電池是一體的)。
根據病情不同,有的時候病人并不需要植入一個永久性的起搏器,而只需要暫時性地輔助心臟的運行。比如,如果預計病人的心動異常只是短暫性的,有可能在短期后恢復正常,那么就不需要植入一個永久性的起搏器。基于這些情況,臨時心臟起搏器就應運而生了。無論是工作原理還是手術方式,這類起搏器都和永久性的起搏器非常相似,但兩個微小的差別讓這類起搏器存在一些缺陷。
首先,這種起搏器事實上并沒有被植入體內,而是置于體外的,進入體內的只是起搏導線。這些導線的一端或主動或被動地固定在心臟的相關區域,另一端則伸出體外,與起搏器相連,這大大增加了發生感染的風險。第二,當不再需要臨時起搏治療時,去除起搏導線的方式顯得非常“簡單粗暴”:硬拔。由于起搏導線是或主動或被動地固定在心臟上的(導線的頭端有螺旋或者掛鉤),這有對心臟產生傷害的風險。
這篇《自然生物技術》研究中介紹的臨時起搏器則從根本上解決了這兩個問題:這是一個無線裝置,利用無線信號來發送和接收刺激指令,大大減小了感染的風險;去除起搏裝置不會對身體造成可能的損傷,因為起搏裝置最后是被體液溶解掉的。
隔空傳遞
這個臨時起搏器分為兩個彼此分離的部分,一個是使用電脈沖對心臟給予周期性刺激的起搏元件,一個是為起搏元件供能和發送指令的指令發送元件。只需要把起搏元件通過手術植入病人的心臟,手術切口就可以被徹底縫合。病人把指令發送元件放在距離起搏元件比較近的地方,比如胸口的兜里,與外接電源相連的指令發送元件就可以向起搏元件發送起搏信號。這種方法聽起來或許很神奇,但事實上它的原理我們每天都會接觸到:無論是銀聯的閃付,手機上的虛擬門禁卡,還是無線充電,使用的都是這種被稱為無線近場通信的技術。更進一步地說,這種技術基于每個人都很熟悉的電磁感應。
在這個臨時起搏器中,指令發送元件上有一個線圈,負責發送信號,起搏元件上則有一對線圈,負責接收信號。當給指令發送元件的發射線圈通交流電時,由于電磁感應,起搏元件的接收線圈上就會產生感應電流。通過調整給發射線圈通的交流電的頻率,就能控制起搏元件上接收線圈上產生的交變電流的頻率。但起搏元件中只包含這樣的接收線圈顯然是不行的:你不能用交變電流這樣“花式”的方法去刺激心臟。因此,研究人員還在起搏元件中添加了一個二極管。二極管的根本特性是只允許電流單向通過,因此在起搏元件上添加了這個二極管的情況下,發射線圈上的交流電信號在隔空傳導到起搏元件上之后,就轉變成了直流脈沖信號。除了接收線圈和二極管外,起搏元件上還有兩根電極,當把整個起搏元件用可吸收的縫合線固定在心臟上后,起搏元件上的脈沖電流就可以通過這兩根電極刺激心臟,使心肌細胞按醫生的設置搏動。
用后即溶
很顯然,這種無線控制的原理談不上新穎,真正讓人驚嘆的是科研人員在實現這一點上的高超技藝。在美國西北大學約翰·羅杰斯教授的領導下,這個團隊把相關的技術運用到了極致,制造出的這個臨時起搏器的起搏元件超輕、超小、超薄,當不再需要時會被身體中的體液逐漸溶解,因此這樣的電子器件又被稱為暫態電子器件(tran-sient electronic device)。你甚至還能給這個起搏器的壽命“編程”,設定它最終憑空消失的時間。
羅杰斯被業界公認為柔性和暫態電子器件研究領域的領軍人物,一直在探索把這類電子器件應用于醫學領域的可能性。在制作這個臨時起搏器的起搏元件時,研究人員使用了鎂、鎢、硅等具有良好生物相容性的材料來制造起搏元件中的接收線圈、電極以及二極管等組成部分。借助光刻、轉印、氣相沉積等技術手段,最后制造出的起搏元件長寬只有大約1.5厘米,厚度只有大約50微米(0.05毫米)。這樣微小的尺度和材料使用量不僅使這個裝置有了一定的柔性,還賦予了它一種新的特性:放到液體中會慢慢溶解,最終徹底消失。在與水的反應中,元件中的鎂和硅會分別轉變為氫氧化鎂和氫氧化硅,而鎢則會轉變成鎢酸。這樣痕跡量的產物會被人體吸收或者排出體外,并且不會對機體有任何不良影響。
但如果這個信號接收和刺激裝置會被液體溶解,它又怎么正常工作呢? 研究人員的辦法是給它套上一個保護套,但這個保護套同樣會慢慢被液體溶解。研究人員使用了一種叫作聚乳酸-羥基乙酸共聚物(PLGA)的物質來制造這樣的保護套。這種高分子材料不僅無毒還很容易制備成一層層的膜或者一個包裹套,而且在液體中會逐漸水解成它的單體物質乳酸和羥基乙酸,最終消失。在用一個厚度只有100微米(0.1毫米)的保護套包裹住起搏元件之后,整個系統只有大約0.3克重,厚度只有250微米(0.25毫米)。
由于這種高分子材料本身也是會逐漸水解的,這又為研究人員提供了一個可以對起搏元件的壽命“編程”的手段:只需要通過實驗測出保護套的厚度和保護套被徹底水解需要的時間的關系,就能以此為參照制造恰當厚度的保護套,使起搏元件在指定的時間開始被體液溶解,從而停止工作。盡管在這篇論文中研究人員并沒有進一步展示這種“編程”的能力,但羅杰斯在接受科學媒體采訪時說,他們“可以為這些裝置訂制可長可短的壽命”(他的實驗室在此前的研究中曾多次實現這一點)。
糾正心臟搏動異常
在制造出這一款暫態的臨時心臟起搏器后,研究人員對這個裝置做了全面的檢測。除了未發現裝置會對機體產生不良影響外,實驗還充分證明了其有效性:利用小鼠作為實驗動物,這個起搏器成功地糾正了其心臟中出現的房室傳導阻滯。
研究人員首先從小鼠體內取出心臟,然后通過人工方法誘發心臟損傷,使小鼠出現較為嚴重的房室傳導阻滯。
心電圖是檢測心臟搏動是否正常的絕佳工具,其捕獲到的波形無比直觀,一目了然。在正常心臟的心電圖上,每出現心房的一個波形信號(P波),隨后都會出現一組心室的波形信號(QRS波群)。無論是這種一一對應的關系被破壞,還是兩種信號的時間間隔發生了變化,都意味著心臟的搏動出現了異常。在這種人為誘發房室傳導阻滯的小鼠中,心電圖顯示出現了心室漏搏的現象,也就是說有的心房波形信號后面并沒有心室的波形信號出現。
當研究人員使用這個臨時的起搏器按照設置的頻率刺激小鼠的心室時,他們發現小鼠心室的搏動會徹底恢復正常,心電圖上心房的波形信號和心室的波形信號再次建立起了一一對應的關系。進一步在實驗犬(心臟的尺寸更接近人)和自由活動的大鼠上的檢驗也發現,研究人員可以根據設置的頻率隨心所欲地刺激心房或者心室的搏動,而且起搏元件的有效工作距離可以超過20厘米,也就是說只要起搏元件和指令發送元件的距離在20厘米之內,起搏器就能正常工作。這樣的距離已經足夠滿足病人日常的需求,比如,病人只需要把指令發送元件貼身放在胸腹部就可以了。
對于包裹了100微米厚的高分子保護套的起搏元件,在動物體內的研究表明整個裝置會在植入體內5-7周后被體液徹底溶解,也就無需取出了。
安全性和功能性的檢驗都表明,與傳統的臨時起搏器相比,這種無線并且用后即溶的起搏器無疑更加理想。
仍有改進空間
除了減小感染風險、不用取出外,整個系統還有另外一個巨大的優勢:便宜。羅杰斯在接受美國媒體采訪時介紹,整個系統的成本不到100美元,甚至遠遠低于一根起搏導線的價格。如果這種臨時起搏器能夠用于臨床,商業化生產無疑還會進一步壓低成本,大大減輕病人和醫療系統的負擔。
不過這種臨時起搏器目前還處在概念驗證階段,仍然有改進的空間。比如,起搏元件仍然是通過手術植入心臟的,暫時無法通過血管植入。但羅杰斯在接受媒體采訪時表示,他的團隊目前正在探索通過優化設計,來使起搏元件可以通過血管植入心臟。
醫學界對這個暫態的臨時起搏器評價很高并寄予厚望。耶魯大學心臟病學教授、美國心臟病學學會領導理事會理事瑞秋·蘭伯特稱贊這項發明非常吸引人,并說心臟病醫師會非常期待這樣一款能夠用后即溶的起搏器。
然而羅杰斯的眼光顯然并沒有局限在這一個小小的起搏器上。在他看來,這個起搏器無線控制和用后即溶的策略完全可以被運用到更多的醫學領域,比如通過植入一個暫態的外周神經刺激裝置來輔助緩解病人在手術或者受傷后的疼痛感。用他一位合作者的話來說,他希望用暫態電子器件為生物醫學研究和臨床醫學拉開一個新篇章,創造出能夠監測病情進展和提供電刺激、化學藥物、細胞療法等各種形式治療手段的暫態電子醫療器件。

