去白細胞濾器對血液產品質量的影響
王雅卿 姚美辰
為患者輸注去除白細胞的紅細胞制品,是目前能夠有效降低或者防止一些輸血不良反應及輸血相關性疾病傳染的一項技術,這項技術能夠成功應用于臨床得益于一次性使用白細胞過濾器的誕生[1]。由于在多種去除血液中白細胞的方法中,去白細胞濾器過濾法是最有效、最便捷的[2],因此適用于血站的一次性白細胞濾器現已得到了廣泛的應用。一次性白細胞濾器通常分為隔夜過濾型和即采即濾型兩種,前者適用于采血8 h 以后進行過濾,冷藏保存的時間比較長,只能適用于制備普通冰凍血漿;后者則應用在采血2~8 h內的過濾分離,要求當天過濾,適用于新鮮冰凍血漿的制備[3]。目前相關報道中大家均比較關注白細胞過濾情況[4],但過濾也可能對其它血液成分產生不同程度的影響,其中紅細胞的回收率和血漿中的FHb 濃度也會對輸注紅細胞懸液的效果產生不同程度的影響。而全血經過濾后,血漿被分離制成新鮮漿等血漿制品,其中新鮮漿制品中的FIB 和FⅧ的活性對臨床患者輸注后療效產生決定性影響,而這些凝血因子也會受到外源性生物過濾材料的影響,對血漿中凝血因子的生物活性和血漿蛋白的含量產生一定程度的影響。因此為了解 T-200 型一次性使用白細胞過濾器血袋所采用的去白細胞濾器對相關血液產品質量的影響,作者對其去除白細胞效果、FHb 濃度、FIB 和FⅧ的活性等相關質量指標進行了檢測和分析,現將結果報告如下。
1 材料與方法
1.1 研究對象 選取2019 年9 月~2020 年1 月街頭采集的自愿無償獻血者血液全血40 袋,規格均為 200 ml,在實驗過程中均使用導管或者轉移袋,通過無菌接口機分裝實驗用血液樣本,采樣全程符合無菌操作,采樣后不影響血液產品的質量。
1.2 儀器與試劑 XT-1800i 血細胞計數儀(SYSMEX公司),CS-2000i 全自動凝血分析儀(SYSMEX 公司),Cobas-C111 全自動生化分析儀(Roche 公司),CH 光學顯微鏡(奧林帕斯),Nageotte 白細胞大容量計數池(HAUSSER SCIENTIFIC HORSHAM,PAUSA),LBG-22低溫濾白柜(天津正源公司)。血漿FHb 試劑盒(北京瑞爾達公司),FⅧ活性測定試劑盒(SYSMEX 公司),纖維蛋白原測定試劑盒(SYSMEX 公司),活化部分凝血活酶時間測定試劑盒(SYSMEX 公司),凝血因子正常值質控品(SYSMEX 公司)。
1.3 方法 根據《血站技術操作規程》2019 版要求,選擇采集過程流暢的獻血者血液(采集時間≤5 min)。采集后放置(4±2)℃環境保存,6~8 h 內完成全血過濾,分別檢測全血和過濾后去白全血的FHb 濃度、FIB 和FⅧ活性,及過濾后紅細胞回收率、白細胞計數、去白細胞濾器過濾時間。
1.4 統計學方法 采用SPSS19.0 統計學軟件處理數據。計量資料以均數±標準差()表示,采用t檢驗。P<0.05 表示差異有統計學意義。
2 結果
2.1 白細胞過濾器濾除檢測結果 對過濾后的去白全血進行檢測,紅細胞回收率均可達到>85.00%,白細胞計數均<2.5×106個/單位,且全部濾器過濾時間 <10 min。見表1。
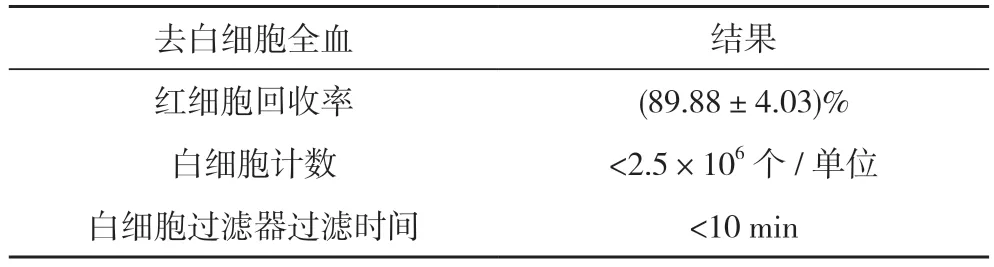
表1 白細胞過濾器濾除檢測結果
2.2 過濾前后的FHb、FIB、FⅧ水平比較 過濾后,血漿中的FHb 為(0.076±0.016)g/L,高于過濾前的(0.039±0.019)g/L;血漿中的FIB 為(1.860±0.230)g/L,低于過濾前的(2.010±0.290)g/L;血漿中的FⅧ為(91.100±7.900)%,低于過濾前的(95.300±9.200)%,差異均有統計學意義(P<0.05)。見表2。
表2 過濾前后的FHb、FIB、FⅧ水平比較()
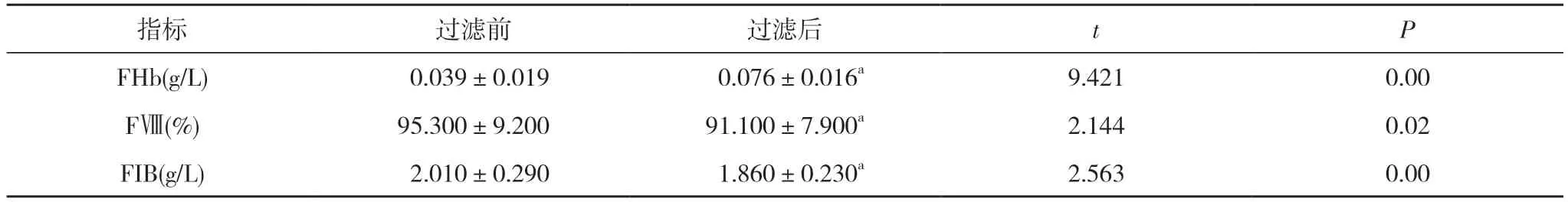
表2 過濾前后的FHb、FIB、FⅧ水平比較()
注:與過濾前比較,aP<0.05
3 討論
全血或紅細胞懸液通過去白細胞濾器過濾后,國內外標準中都對過濾后血液成分中剩余白細胞計數進行了限制,標準為≤2.5×106個/單位[5],紅細胞回收率應≥85.00%,FHb≤0.530 g/L,每單位全血過濾時間≤10 min[6]。選取適當的血袋及部位取樣,需要保證最終樣品能夠代表過濾后產品袋中的真實情況,又要方便操作,取樣過程中應兼顧血液的安全性和樣本的有效性。白細胞是血液中的一個重要組成部分,是人體免疫防御系統的重要構成,輸血反應的原因中由白細胞引起的占比最高,臨床實踐表明白細胞輸注到異體內可能產生有害的副作用,如非溶血性發熱性輸血反應(NHFTR)、人類白細胞抗原(HLA)同種異體免疫反應、血小板輸注無效等,同時還有可能引起嗜白細胞病毒傳染病的感染[7]。相關研究表明[8],血液保存過程中因為白細胞壽命比較短,隨著保存時間的不斷延長,白細胞開始釋放和生產細胞因子,而溶血反應的發生多是由于血液制品中存在的高濃度細胞因子引發的。去白細胞濾器是現有去除血液產品中白細胞的最簡單、有效的方法,采用的過濾材料一般具有吸附和濾篩作用,可將血液中的部分微聚體、白細胞等滯留在過濾材料中,但不應影響其它血液成分的通過,以達到除去大部分白細胞的目的。在本實驗中白細胞殘留量計數是很重要的判斷指標,在過濾結束后排氣過程中可將樣本打入旁路中,既不影響過濾后的下一步操作,且使用濾器下方導管中血液作為樣本,方便、安全并能夠節約血液。血細胞計數儀雖自動化程度高,適用于白細胞含量的快速批量檢測,但對過濾后的低白細胞殘留量標本檢測結果不準確[9],本實驗中所采集的全血,在經過TA-RFB T-200 型去白細胞過濾器過濾后,使用Nageotte 白細胞計數盤進行殘余白細胞計數,結果均<2.5×106個/單位,合格率為100%,可見此款去白細胞濾器對血液中白細胞的去除效果滿意,可以滿足臨床降低或消除白細胞引起輸血不良反應的需要。實驗中所有全血過濾后的紅細胞回收率檢測均>85.00%,過濾致紅細胞的損失率符合相關標準。實驗中所有抽取的全血充分混勻,沒有凝塊,避免過濾不暢等干擾因素[10],過程順暢,過濾時間均 <10 min,100%達到標準要求。紅細胞通過濾器的過程中,通過濾材孔道時會受到流體靜態壓力、切變率、孔形狀、流速等因素影響,可能會有一定的損傷[11]。不合格濾器可能導致過濾后的血漿FHb 超標,可能與紅細胞通過濾層時所受的切變力有關[12]。一般若使用的濾器合格,且按要求自然重力過濾,不會發生溶血情況;但如若濾器管路的邊緣扭結,或采血主袋管路上的易折塞入口處等也可導致紅細胞部分損傷,故應對濾白后血液及時進行質量控制。本實驗結果中過濾后血漿FHb 含量均<0.530 g/L,且遠遠小于該標準,說明該濾器對紅細胞的損傷在合格范圍內,且與過濾前的全血血漿FHb 含量相比較,具有統計學意義。新鮮冰凍血漿中包含各種凝血因子、清蛋白及免疫球蛋白等,臨床上主要應用在凝血因子的補充,幾乎包括全血中的全部凝血因子和蛋白,包括不穩定的凝血因子(如FⅤ、FⅧ等),因此凝血因子的活性高低決定著新鮮冰凍血漿的質量[13]。去白細胞過濾器產生作用的機制主要是因為阻滯作用、表面張力和電荷密度等。全血中的凝血因子因其分子大小遠遠小于濾器中濾材的孔徑,濾材阻滯作用不會對其產生影響,但濾材的表面張力與電荷密度在過濾中可能對凝血因子有一定的吸附作 用[14]。不同濾器中采用的過濾材料可能具有不同結構和表面特性,吸附作用或其它作用機制導致的凝血途徑活化,均可能造成不同程度的凝血因子消耗。本實驗中,對過濾后的去白全血進行檢測,紅細胞回收率均可達到>85.00%,白細胞計數均<2.5×106個/單位,且全部濾器過濾時間<10 min。過濾后,血漿中的FHb 高于過濾前,FIB、FⅧ低于過濾前,差異均有統計學意義(P<0.05)。
使用不同的血液保養液及濾器中采用的不同濾材都可能對通過濾器的血液成分產生質量影響,因此在選擇一次性使用白細胞過濾器血袋的時候,應綜合考慮采用的血液保養液成分類型、過濾器去白細胞效果、過濾速度、濾材介質電荷及粘附作用等。選擇過濾器的時候,濾材應具有較好的生物學相容性,使用前應評價濾器去除白細胞的效果及對紅細胞和凝血因子等有效血液成分的影響,確保去除白細胞后的血液產品能夠安全、并有效地滿足臨床需求。

