HNF-1α基因突變致MODY3型糖尿病1家系報道及文獻復習
任小燕,劉敏,閆朝麗,張少杰
先證者,男,12歲,因多飲、多尿3個月,體質量減輕2個月于2019年2月入院。3個月前出現多飲(3 000 ml/d)、多尿、消瘦(2個月內消瘦3 kg),自測空腹血糖10 mmol/L,餐后2 h血糖18 mmol/L,否認“糖尿病酮癥酸中毒”發生。既往體健。患者為第一胎第一產,足月順產,母孕期平順,無特殊藥物使用史,孕期未監測血糖,未行口服葡萄糖耐量試驗(OGTT)篩查。出生體質量4.5 kg,身長不詳,自幼生長發育正常。查體:身高150 cm,體質量40 kg,體質量指數(BMI)17.7 kg/m2,心、肺(-),腹軟,無壓痛,雙下肢無水腫,雙側足背動脈可捫及。實驗室檢查:空腹血糖(FPG)7.4 mmol/L,餐后2 h血糖(2 hPG)18.5 mmol/L,空腹胰島素8.6 μU/ml,餐后2 h胰島素18.2 μU/ml,空腹C肽1.32 ng/ml,餐后2 h C肽2.76 ng/ml,CRP 0.1 mg/L,胰島素自身抗體ICA、IA-2A、GADA-Ab(-),HbA1c9.0%。TC 5.08 mmol/L,TG 0.83 mmol/L,HDL-C 1.14 mmol/L,LDL-C 2.61 mmol/L。尿糖(+++),血、尿酮體(-)。肝腎功能正常,尿白蛋白/肌酐(-)。眼底未見視網膜病變,肌電圖未見異常。入院后予門冬胰島素(丹麥諾和諾德公司)早、午、晚各3 U+甘精胰島素8 U每晚皮下注射降糖治療,血糖控制平穩后停止胰島素改為格列美脲(亞莫利,賽諾菲安萬特中國投資有限公司)1 mg,每早口服,FPG降至5~6 mmol/L,2 h PG降至7~8 mmol/L。
家系調查:先證者爺爺60歲時診斷“糖尿病、下肢動脈粥樣硬化”。姑姑40歲時診斷“糖尿病”,目前胰島素治療中。父親30歲時診斷“糖尿病”,2019年查尿蛋白(+),眼底病變(-),診斷“糖尿病腎病”。母親孕期血糖情況不詳,24歲順產后發生產后大出血,后檢測FPG 8 mmol/L,期間飲食、運動控制血糖,5年后血糖控制于FPG 8~10 mmol/L,2 hPG 12~15 mmol/L,尿糖(+),尿微量白蛋白與肌酐的比值(ACR)升高。患者家系圖見圖1。
基因檢測結果:先證者及其母親均為攜帶HNF-1α基因突變的雜合子,HNF-1α基因2號外顯子上的錯義突變 c.G392T(p.R131L),使G堿基突變為T堿基,131位的精氨酸突變為亮氨酸,見圖2。其父系糖尿病患者未見突變,根據發病年齡及臨床特征,考慮先證者父系為2型糖尿病家系。在dbSNP137數據庫、千人基因組數據庫、HGMD 數據庫中均未檢索到c.G392T(p.R131L)位點變異。經檢索人類外顯子組整合數據庫,提示該位點G/A的最小等位基因頻率(MAF)A=0.000 009/1(rs369429452)。對該突變進行功能預測,PolyPhen-2評分為0.999,SIFT評分為0.00,Mutation Taster顯示第131位精氨酸為高度保守的氨基酸,均提示該突變為影響蛋白質功能的致病性突變。該家系3代共有5例糖尿病患者,其中2例確診MODY3,起病年齡均小于25歲,2代直系親屬中均有糖尿病患者,符合常染色體顯性遺傳的特點,達到MODY的診斷標準。由于先證者母親的父母均已失聯,無法取得母系家系血樣,根據基因檢測結果,仍考慮患者MODY3家系為母親攜帶的MODY3根據HNF-α 基因c.G392T(p.R131L)檢測結果,將先證者的胰島素注射治療更改為格列美脲1 mg 口服,每日1次,1周后,血糖控制平穩(FPG 5~6 mmol/L,2 hPG 7~8 mmol/L),HbA1c由9.0%下降為 6.5%,無低血糖發生。母親血糖升高,加用格列美脲2 mg/d治療1周后,血糖明顯較前下降,HbA1c7.6%下降為6.0%。門診規律隨訪6個月,血糖平穩,HbA1c6.0%~6.4%,未發生糖尿病微血管并發癥及大血管并發癥。
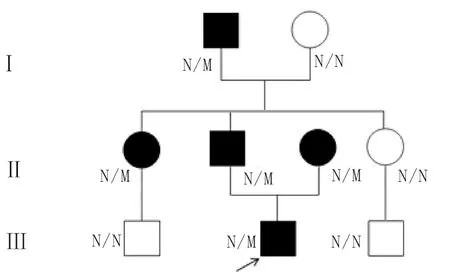
注:N/N 表示正常;N/M表示雜合突變攜帶者;□.正常男性;○.正常女性;■.男性患者;●.女性患者;↗.先證者圖1 MODY3型糖尿病家系圖
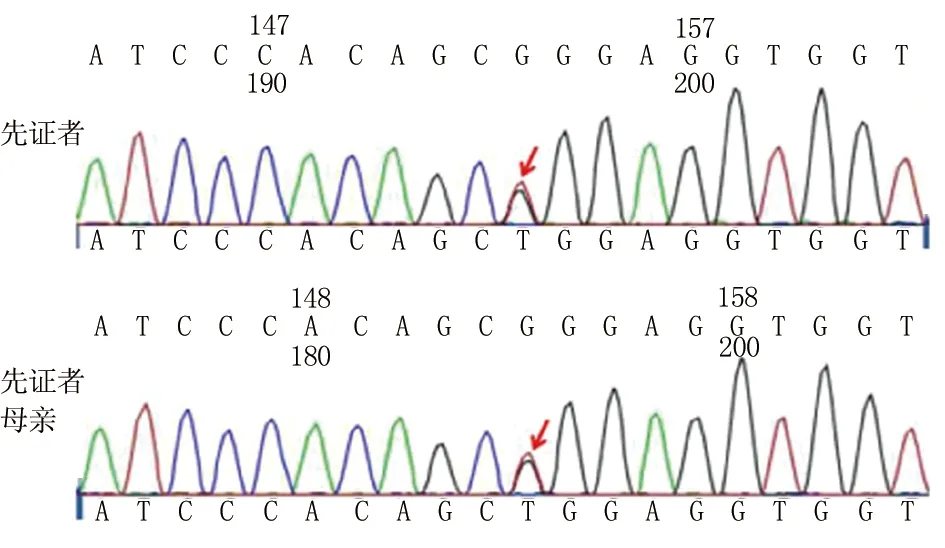
圖2 先證者及其母親均為攜帶HNF-1A基因突變的雜合子基因突變家系
討 論青少年的成人起病型糖尿病(maturity-onset diabetes of the young,MODY)是一組單基因糖尿病,目前MODY分為13種類型,以MODY3發病率最高[1]。MODY3患者起病年齡早,表現為胰島素分泌缺陷,極易被誤診為1型或2型糖尿病[2]。MODY3基因位于染色體12q24.3,其由10個外顯子組成,調節胰島素基因的轉錄[3]。至今已發現了近450種HNF1α基因突變[4]。其外顯率高,有明顯糖尿病家族史,符合常染色體顯性遺傳[5]。MODY3患者發病年齡不一,不同的外顯子區域發生糖尿病年齡不同;另一方面,如患者母親為突變攜帶者,其受特殊的宮內發育環境影響,致使MODY3患者發病年齡提早約12年。MODY3型患兒發病年齡早,有研究顯示,其在青少年時期就可表現出糖耐量異常。發病早期,監測其空腹血糖常位于正常范圍,但餐后或OGTT 2 h血糖較空腹血糖升高可達5 mmol/L[6]。隨著病情的進展,糖尿病后期會出現空腹血糖進行性升高,部分表現為糖尿病的“三多一少”癥狀,幾乎無酮癥傾向。此外,MODY3患者還具有其他臨床特征,HNF1α突變引起近端腎小管葡萄糖重吸收障礙,其可能機制是葡萄糖轉運子2(GLUT 2)介導的,因此,在糖尿病早期,患者可出現尿糖陽性[7];同時,患者可伴高敏C反應蛋白(hs-CRP)降低。研究表明,hs-CRP基因的啟動子區域有HNF1α結合位點,導致 MODY3患者hs-CRP下降[8-9]。Fu等[10]研究顯示,與1型DM相比,MODY3 C肽水平更高,hs-CRP水平更低。該家系中,先證者hs-CRP均降低至正常范圍以下,C肽水平不低。此外,MODY3對磺脲類藥物治療較為敏感[11],在早發糖尿病患者中,磺脲類藥物能平穩地控制血糖,甚至優于胰島素。通常磺脲類藥物從小劑量開始使用,約為常規起始劑量的1/4,以防治低血糖發生。臨床研究表明,磺脲類藥物對MODY3患者有獨特的降糖效果,選擇合適劑量的磺脲類藥物對血糖調整至關重要[12]。MODY3患者同樣易出現慢性并發癥,其發生幾率類似,隨著病情進展,胰島功能逐漸下降,多數患者需胰島素治療,且通常伴有大血管及微血管并發癥。此例患者家系中發現錯義突變 c.G392T(p.R131L),位于2號外顯子上,為國內首次報道。既往研究表明[13],c.391C>T(p.Arg131Trp)突變在一個英國家系中被發現,其先證者因糖尿病酮癥酸中毒(DKA)就診,因其被當做T1DM而延誤診治11年。證明胰島β細胞功能進行性惡化,此型患者病情較其他亞型嚴重。
MODY占所有糖尿病的2%~5%。臨床特點包括:(1)連續3代及以上家族史,呈常染色體顯性遺傳;(2)家族中至少1人發病年齡<25 歲;(3)至少5年不依賴胰島素治療,無酮癥傾向。MODY臨床異質性較強,由于臨床表現與T1DM 和T2DM 相似,目前約80%的MODY被誤診為T1DM或T2DM,導致其實際患病率被低估。本例患者父系及母系均有糖尿病家族史,且發病年齡小于25歲,檢查胰島功能,空腹C肽1.32 ng/ml,餐后2 h C肽2.76 ng/ml,提示患者胰島細胞仍有部分功能,1型糖尿病相關抗體陰性,故可排除1型糖尿病。患者發病年齡小,C肽水平不低,無黑棘皮征等胰島素抵抗的證據,2型糖尿病可能性不大,進而行基因檢查明確診斷MODY。
MODY經常被誤診為其他類型糖尿病,應用分子診斷技術對患者進行精準的基因診斷,對于MODY亞型患者的疾病監測、治療和預后具有重要的價值。本例基因突變位點可能參與了這個家系成員糖尿病的發生過程,但具體機制和分子病理學意義有待進一步研究。

