美羅培南用于新生兒感染安全性的Meta分析
甄路路 劉璐 劉暢 閆美興

中圖分類號 R969.3;R722.13 文獻標志碼 A 文章編號 1001-0408(2021)18-2260-07
DOI 10.6039/j.issn.1001-0408.2021.18.14
摘 要 目的:系統評價美羅培南用于新生兒感染的安全性,旨在為該藥在新生兒人群中的安全使用提供循證參考。方法:計算機檢索PubMed、Embase、Cochrane圖書館、ISI Web of Science、國際衛生技術評估機構網絡、中國期刊全文數據庫、萬方數據、中國生物醫學文獻服務系統、中文科技期刊全文數據庫等,收集美羅培南或美羅培南聯合其他藥物(試驗組)對比可替代美羅培南的同類藥物(對照組)用于新生兒感染的隨機對照試驗(RCT),檢索時限為建庫起至2021年5月1日。篩選文獻并提取資料后,采用Cochrane系統評價員手冊5.1.0推薦的偏倚風險評估工具對納入文獻質量進行評價,采用 RevMan 5.3軟件進行 Meta分析。結果:共納入25項RCT,共計2 090例患兒。Meta分析結果顯示,試驗組患兒的整體不良反應發生率顯著低于對照組[RR=0.53,95%CI(0.44,0.65),P<0.000 01]。亞組分析結果顯示,試驗組患兒的整體不良反應發生率均顯著低于對照組使用頭孢他啶[RR=0.55,95%CI(0.41,0.74),P<0.000 1]、替加環素[RR=0.37,95%CI(0.23,0.59),P<0.000 1]、頭孢曲松[RR=0.53,95%CI(0.35,0.80),P=0.003]的患兒;試驗組新生兒化膿性腦膜炎[RR=0.63,95%CI(0.44,0.92),P=0.02]、新生兒重癥多重耐藥菌感染[RR=0.37,95%CI(0.25,0.55),P<0.000 01]、新生兒重癥細菌感染[RR=0.67,95%CI(0.48,0.94),P=0.02]患兒的整體不良反應發生率均顯著低于對照組。試驗組患兒的皮疹、胃腸道反應、血紅蛋白下降等具體不良反應發生率均顯著低于對照組(P<0.05);而兩組患兒的轉氨酶升高、繼發真菌感染、腎損傷等具體不良反應發生率比較,差異均無統計學意義(P>0.05)。發表偏倚分析結果顯示,以整體不良反應發生率為指標時,本研究存在一定程度的發表偏倚;以具體不良反應發生率為指標時,本研究存在發表偏倚的可能性較小。結論:美羅培南用于新生兒感染的安全性較好,特別是用于新生兒化膿性腦膜炎、新生兒重癥多重耐藥菌感染、新生兒重癥細菌感染時的安全性優于頭孢他啶、替加環素、頭孢曲松等抗菌藥物。
關鍵詞 美羅培南;新生兒;感染;安全性;Meta分析
Meta-analysis of the Safety of Meropenem for Neonatal Infection
ZHEN Lulu1,LIU Lu2,LIU Chang2,YAN Meixing2(1. School of Medicine and Pharmacy, Ocean University of China, Shandong Qingdao 266003, China; 2. Dept. of Pharmacy, Qingdao Womens and Childrens Hospital, Shandong Qingdao 266000, China)
ABSTRACT? ?OBJECTIVE: To systematically evaluate the safety of meropenem for neonatal infection, and to provide evidence-based reference for safe use of it in the neonatal population. METHODS: Retrieved from PubMed, Embase, Cochrane Library, ISI Web of Science, International Health Technology Assessment Network Website, China Journal Full-text Database, Wanfang Database, CBM, Chinese Sci-tech Periodical Full-text Database, randomized controlled trials (RCTs) about meropenem or meropenem combined other drugs (trial group) versus the similar drugs that could replace meropenem (control group) for neonatal infection were collected during the inception to May 1st, 2021. After literature screening and data extraction, the quality of included literatures were evaluated with Cochrane systematically evaluator manual 5.1.0. Meta-analysis was conducted with RevMan 5.3 software. RESULTS: A total of 25 RCTs were included, involving 2 090 children. Results of Meta-analysis showed that the incidence of overall ADR in trial group was significantly lower than control group [RR=0.53,95%CI(0.44,0.65), P<0.000 01]. Results of subgroup analysis showed that the incidence of overall ADR in trial group was significantly lower than control group receiving ceftazidime [RR=0.55, 95%CI(0.41,0.74), P<0.000 1], tigecycline [RR=0.37, 95%CI(0.23,0.59), P<0.000 1], ceftriaxone [RR=0.53, 95%CI(0.35,0.80), P=0.003]. The incidence of overall ADR in trial group with neonatal purulent meningitis [RR=0.63,95%CI(0.44,0.92), P=0.02], severe neonatal multidrug-resistant bacterial infection [RR=0.37, 95%CI(0.25,0.55), P<0.000 01], neonatal severe bacterial infection [RR=0.67, 95%CI (0.48, 0.94), P=0.02] were significantly lower than control group. The incidence of specific ADR such as rash, gastrointestinal reaction, hemoglobin reduction in trial group were significantly lower than control group (P<0.05). There was no statistical significance in the incidence of specific ADR between 2 groups, such as elevated transaminase, secondary fungal infection and renal injury (P>0.05). Results of bias analysis showed that when the incidence of overall ADR was used as index, there was a certain degree of publication bias in this study, when the incidence of specific ADR was used as index, there was less possibility of publication bias in this study. CONCLUSIONS: Meropenem is safe in the treatment of neonatal infection, especially in the treatment of neonatal purulent meningitis, severe neonatal multidrug-resistant bacterial infection and neonatal severe bacterial infection, it is superior to ceftazidime, tigecycline, ceftriaxone and other antibacterial drugs in safety.
KEYWORDS? ?Meropenem; Newborn; Infection; Safety; Meta-analysis
美羅培南為人工合成的廣譜碳青霉烯類抗菌藥物,可通過抑制細菌細胞壁的合成而產生抗菌作用,且易穿透大多數革蘭氏陽性菌和陰性菌的細胞壁,適用于成人和兒童由單一或多種對美羅培南敏感的細菌所引起的感染[1]。同時,該藥為院內重癥感染以及以革蘭氏陰性菌為主的混合性感染、多重耐藥菌感染、產酶菌感染的首選藥物[2],在新生兒重癥感染中應用廣泛。美羅培南作為碳青霉烯類抗菌藥物的代表藥物,常見的不良反應有皮疹、胃腸道反應(惡心、嘔吐、腹瀉)等。有研究指出,碳青霉烯類抗菌藥物可以引發免疫球蛋白介導的不良反應,如過敏性休克等;也有由藥物本身代謝和排泄過程引發的不良反應,即非免疫球蛋白介導的不良反應,如胃腸道反應、腎毒性等[3]。近幾年,有研究報道了多種因使用美羅培南而出現的新發及嚴重的不良反應,如低鉀血癥、藥物性肝損傷、急性腎損傷、血小板異常、藥物熱等[2],應根據患兒自身情況和不良反應嚴重程度及時減少劑量或停藥。另外,該藥超劑量使用時出現神經系統毒性反應的可能性也很大,且伴有頭痛、神經錯亂等癥狀,特別是腎功能不全伴癲癇者,在發生神經系統毒性反應時,必須立即減少劑量或者停藥[4]。
雖然,美羅培南在治療新生兒重癥感染方面具有顯著的效果[5],但不良反應同樣不容忽視[6]。由于新生兒生理結構特殊,且正處于生長發育的關鍵階段,故更易發生藥物不良反應[7]。盡管已有多篇文獻報道了美羅培南用于新生兒感染的療效和安全性,但其樣本量較小,且研究結果存在差異[8-12]。基于此,本研究通過檢索文獻,采用Meta 分析的方法對近年來美羅培南用于新生兒感染的安全性進行系統評價,旨在為該藥在新生兒人群中的安全使用提供循證參考。
1 資料與方法
1.1 納入與排除標準
1.1.1 研究類型 本研究納入的文獻類型為國內外公開發表的隨機對照試驗(RCT);語種限定為中文和英文。
1.1.2 研究人群 本研究納入的患者為年齡≤28 d且患有細菌感染的新生兒。
1.1.3 干預措施 試驗組患兒給予美羅培南或美羅培南聯合其他藥物;對照組患兒給予可替代美羅培南的同類藥物;兩組患兒劑量、劑型、療程均不限。
1.1.4 結局指標 本研究的結局指標包括:①整體不良反應發生率;②具體不良反應發生率,如皮疹、轉氨酶升高、胃腸道反應、繼發真菌感染、血紅蛋白下降、腎損傷等。
1.1.5 排除標準 本研究的排除標準包括:①重復發表的文獻;②僅為相關研究方案的文獻;③單純介紹分析理論的文獻;④無法提取相關數據的文獻;⑤未描述安全性結局的文獻。
1.2 文獻檢索策略
計算機檢索PubMed、Embase、Cochrane圖書館、ISI Web of Science、國際衛生技術評估機構網絡(INAHTA)、中國期刊全文數據庫、萬方數據、中國生物醫學文獻服務系統、中文科技期刊全文數據庫等;同時,檢索藥監部門(包括美國FDA、國家藥品監督管理局等)官方網站的相關公示信息以及合理用藥國際網絡、臨床安全用藥監測網,并手工檢索納入文獻的參考文獻等。中文檢索詞為“美羅培南”“美平”“卓捷”“新生兒”“不良反應”“安全性”等;英文檢索詞為“meropenem”“infant”“adverse drug effect”“safety”等。檢索時限為各數據庫建庫起至2021年5月1日。
采用主題詞和自由詞相結合的檢索方式。以中國期刊全文數據庫為例,其檢索策略如下:SU=(“小兒”+“嬰兒”+“新生兒”)AND SU=(“安全性”+“不良反應”+“副作用”+“副反應”+“毒性反應”+“毒性作用”+“不良事件”+“藥物毒性”)AND SU=(“美羅培南”+“美平”+“卓捷”)。
1.3 文獻篩選與資料提取
由2名評價員獨立按納入與排除標準進行篩選,然后交叉核對,如有分歧則與第3位評價員共同討論解決。提取資料包括第一作者、發表年份、患兒感染類型、例數、性別、年齡、干預措施、結局指標等。
1.4 納入研究質量評價
采用Cochrane系統評價員手冊5.1.0推薦的偏倚風險評估工具對納入文獻質量進行評價,具體包括:隨機方法,分配隱藏,對受試者和研究者施盲、結局評估的盲法,結果數據完整性,選擇性報告結果,其他偏倚來源等方面,每個方面均分為低偏倚風險、不清楚和高偏倚風險[13]。
1.5 統計學方法
采用RevMan 5.3統計軟件進行Meta分析。二分類變量采用危險比(RR)及95%置信區間(CI)表示。采用Q檢驗判斷各納入研究結果間的異質性,以I 2值判斷異質性的大小。當P<0.05、I 2>50%時,表示各研究間存在統計學異質性,采用隨機效應模型進行Meta 分析;反之,則采用固定效應模型進行Meta分析。根據對照組患兒使用藥物種類和感染類型進行亞組分析。采用倒漏斗圖進行發表偏倚分析。檢驗水準α=0.05。
2 結果
2.1 文獻篩選流程與納入研究基本信息
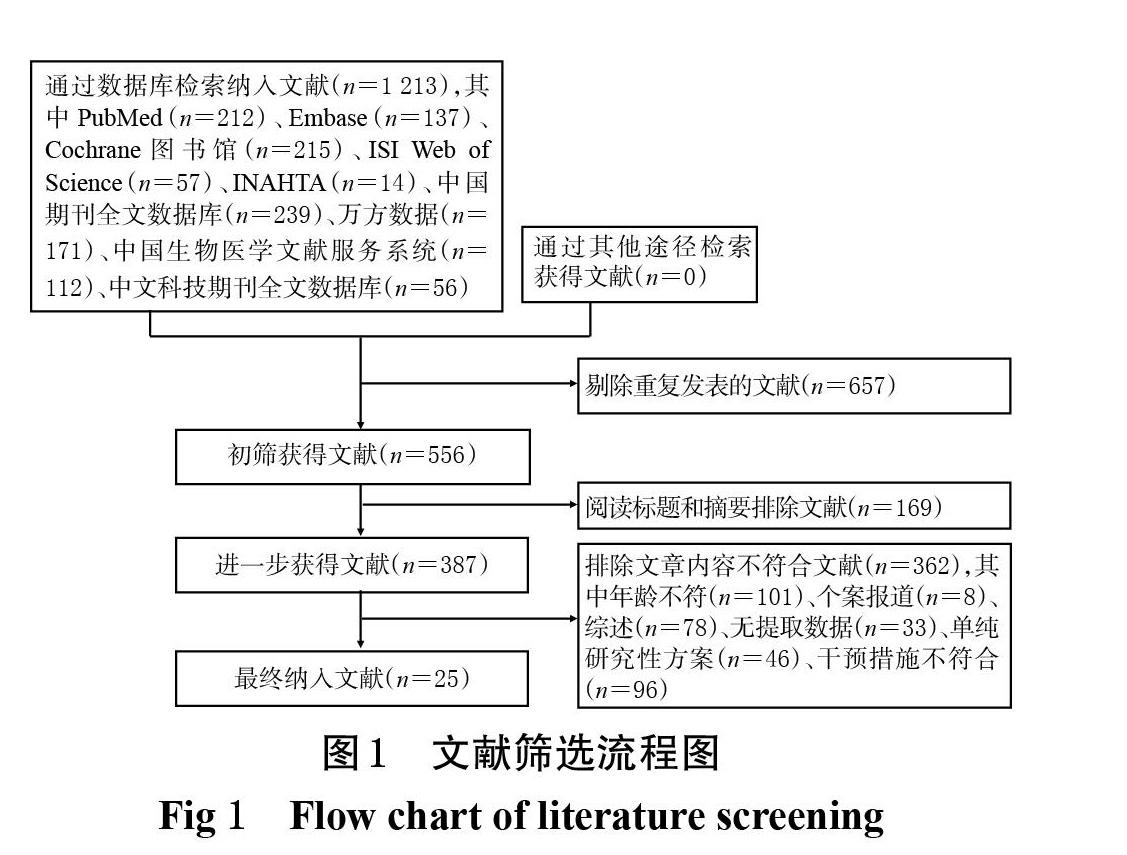
初檢共獲得相關文獻1 213篇,通過閱讀標題、摘要及全文后,最終納入文獻25篇[14-38],共計2 090例患兒,其中試驗組和對照組各1 045例。文獻篩選流程圖見圖1,納入研究基本信息見表1。
2.2 納入研究質量評價
所有研究均為RCT[14-38];12項研究描述了隨機分配方法[15-18,20,23-24,28-29,34-36];11項研究描述了分配方案隱藏[15,17-18,20,23-24,28-29,34-36];6項研究描述了對受試者和研究者施盲[15,20,24,28-29,31];10項研究描述了對結局盲法評價[14-15,17,24,28,30,32-34,37];17項研究結果數據完整[14-17,19-23,25-27,33-37];3項研究選擇性報告結果[14,36-37];所有研究均不清楚是否存在其他偏倚來源,詳見圖2、圖3。
2.3 Meta分析結果
2.3.1 整體不良反應發生率 25項研究報道了整體不良反應發生率[14-38]。各研究間無統計學異質性(P=0.20,I 2=19%),采用固定效應模型進行Meta分析,詳見圖4。Meta分析結果顯示,試驗組患兒的整體不良反應發生率顯著低于對照組[RR=0.53,95%CI(0.44,0.65),P<0.000 01]。
首先,本研究按對照組用藥的不同進行亞組分析。①頭孢他啶:8項研究的對照組患兒使用了頭孢他啶[15,18-19,21-22,28,37-38]。各研究間無統計學異質性(P=0.10,I 2=42%),采用固定效應模型進行Meta分析,詳見圖5A。Meta分析結果顯示,試驗組患兒的整體不良反應發生率顯著低于對照組使用頭孢他啶的患兒[RR=0.55,95%CI(0.41,0.74),P<0.000 1]。②替加環素:4項研究的對照組患兒使用了替加環素[14,20,25,29]。各研究間無統計學異質性(P=1.00,I 2=0),采用固定效應模型進行Meta分析,詳見圖5B。Meta分析結果顯示,試驗組患兒的整體不良反應發生率顯著低于對照組使用替加環素的患兒[RR=0.37,95%CI(0.23,0.59),P<0.000 1]。③頭孢曲松:9項研究的對照組患兒使用了頭孢曲松[16-17,23,26-27,30,32,34,36]。各研究間無統計學異質性(P=0.52,I 2=0),采用固定效應模型進行Meta分析,詳見圖5C。Meta分析結果顯示,試驗組患兒的整體不良反應發生率顯著低于對照組使用頭孢曲松的患兒[RR=0.53,95%CI(0.35,0.80),P=0.003]。
隨后,本研究按感染類型的不同進行亞組分析。①新生兒化膿性腦膜炎:11項研究的患兒為新生兒化膿性腦膜炎[16-17,23-24,26-27,30-33,36]。各研究間無統計學異質性(P=0.22,I 2=23%),采用固定效應模型進行Meta分析,詳見圖6A。Meta分析結果顯示,試驗組新生兒化膿性腦膜炎患兒的整體不良反應發生率顯著低于對照組[RR=0.63,95%CI(0.44,0.92),P=0.02]。②新生兒重癥多重耐藥菌感染:6項研究的患兒為新生兒重癥多重耐藥菌感染[15,20-21,25,29,37]。各研究間無統計學異質性(P=0.88,I 2=0),采用固定效應模型進行Meta分析,詳見圖6B。Meta分析結果顯示,試驗組新生兒重癥多重耐藥菌感染患兒的整體不良反應發生率顯著低于對照組[RR=0.37,95%CI(0.25,0.55),P<0.000 01]。③新生兒重癥細菌感染:7項研究的患兒為新生兒重癥細菌感染[14,18-19,22,28,35,38]。各研究間無統計學異質性(P=0.37,I 2=8%),采用固定效應模型進行Meta分析,詳見圖6C。Meta分析結果顯示,試驗組新生兒重癥細菌感染患兒的整體不良反應發生率顯著低于對照組[RR=0.67,95%CI(0.48,0.94),P=0.02]。
2.3.2 具體不良反應發生率 兩組患兒的轉氨酶升高、繼發真菌感染、腎損傷等具體不良反應發生率比較,差異均無統計學意義(P>0.05);試驗組患兒的皮疹、胃腸道反應、血紅蛋白下降等具體不良反應發生率均顯著低于對照組(P<0.05),詳見表2。
2.4 發表偏倚分析
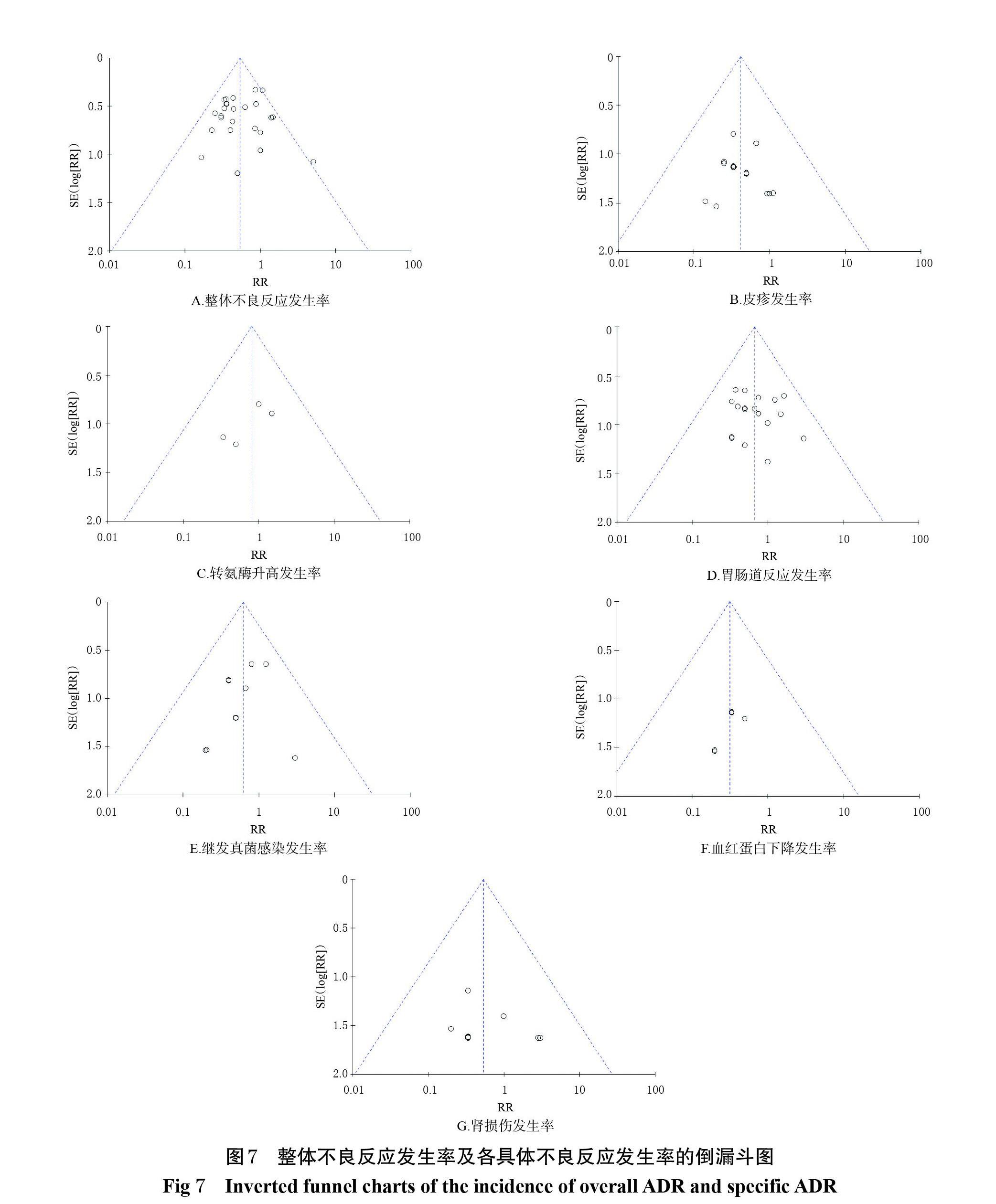
分別以整體不良反應發生率及各具體不良反應發生率為指標繪制倒漏斗圖。結果顯示,以整體不良反應為指標時,倒漏斗圖分布不對稱,各研究散點大部分集中在倒漏斗圖的中上位置,提示本研究存在一定程度的發表偏倚。以皮疹、轉氨酶升高、胃腸道反應、繼發真菌感染、血紅蛋白下降、腎損傷等具體不良反應發生率為指標時,各指標的倒漏斗圖基本對稱,各研究散點分布基本均勻對稱,提示本研究存在發表偏倚的可能性較小,詳見圖7。
3 討論
美羅培南是第二代碳青霉烯類抗菌藥物,具有抗菌譜廣、活性強等優勢,其抗菌機制為在體內與青霉素結合蛋白結合,從而使細胞壁的合成受到干擾[39]。該藥的抗菌譜包括革蘭氏陰性菌、革蘭氏陽性菌以及需氧菌、厭氧菌等多種細菌,其能夠有效抑制厭氧菌與革蘭氏陰性菌,用于新生兒重癥細菌感染的治療效果較為理想[40]。在兒科領域,美羅培南可用于病原菌尚未查明的免疫缺陷患兒的中重度感染、重癥需氧菌與厭氧菌混合感染、多重耐藥革蘭氏陰性菌所致嚴重感染,其中嚴重感染包括重癥肺炎、嚴重敗血癥、化膿性腦膜炎、重度急性膽管炎等[3]。
新生兒感染時可選擇的抗菌藥物種類較少,重癥感染時主要使用包括美羅培南在內的碳青霉烯類抗菌藥物,美羅培南在體內與血漿蛋白的結合率較低,能夠分布于多個組織和體液中,甚至在腦脊液中也能達到有效濃度[41]。藥動學研究證明,該藥在體內的清除率與肌酐清除率成正相關,年齡和體質量可影響肌酐清除率,由于新生兒的肌酐清除率較成人偏低,因此能間接影響美羅培南的體內代謝[1]。新生兒作為一類特殊群體,其身體機能以及器官功能尚未完善,胃腸功能較弱,肝臟的藥物代謝能力不強,使得藥物的生物轉化率較低且無法在肝臟內被有效代謝,從而導致藥物排泄速度較低、血藥濃度較高,極易引發藥物中毒[39]。由此可見,探討美羅培南用于新生兒感染時的安全性顯得尤為重要。
2018年9月21日,國家衛生健康委員會醫政醫管局發布的《碳青霉烯類抗菌藥物臨床應用專家共識》明確提出,新生兒使用美羅培南治療感染的推薦劑量為年齡<7 d,20 mg/kg,q12 h;7~28 d,20 mg/kg,q8 h。治療新生兒腦膜炎時,年齡<7 d,40 mg/kg,q12 h;7~28 d,40 mg/kg,q8 h[42]。而美羅培南藥品說明書并未提及新生兒的用法用量。本研究納入的25篇RCT中均未出現超劑量使用的現象,因此排除了因超劑量用藥而導致不良反應的混雜因素。本研究結果顯示,試驗組患兒的整體不良反應發生率和皮疹、胃腸道反應、血紅蛋白下降等不良反應發生率均顯著低于對照組。亞組分析結果顯示,美羅培南的安全性總體上優于頭孢他啶、替加環素、頭孢曲松等對照藥物,尤其是在用于治療新生兒化膿性腦膜炎、新生兒重癥多重耐藥菌感染、新生兒重癥細菌感染等疾病時,美羅培南均顯示出良好的安全性。發表偏倚分析結果顯示,以整體不良反應發生率為指標時,各研究散點大部分集中在倒漏斗圖的中上位置,提示本研究存在一定程度的發表偏倚;以具體不良反應發生率為指標時,各指標的倒漏斗圖基本對稱,各研究散點分布基本均勻對稱,提示本研究存在發表偏倚的可能性較小。筆者認為,部分結果存在發表偏倚可能與納入文獻的質量偏低有關。
綜上所述,美羅培南用于新生兒感染的安全性較好,特別是用于新生兒化膿性腦膜炎、新生兒重癥多重耐藥菌感染、新生兒重癥細菌感染時的安全性優于頭孢他啶、替加環素、頭孢曲松等抗菌藥物。本研究局限性包括:(1)多數文獻未提及分配方案的隱藏和盲法,難以根據提供的信息判斷是否存在其他重要偏倚,對結果的可信度造成一定的影響;(2)患兒的感染類型不一且嚴重程度不同,導致給藥劑量、給藥時間等給藥方案出現差異,存在一定的異質性;(3)納入文獻多為中文文獻,發表時間較為集中,且文獻質量不一,對研究結果有一定的影響;(4)受納入RCT數量的限制,無法對新生兒膿毒血癥合并化膿性腦膜炎等適應證進行進一步的亞組分析,故本研究結論有待更多大樣本、多中心的RCT進一步證實。
參考文獻
[ 1 ] 連雯雯,陳文倩,閻雨,等.美羅培南的藥動學/藥效學研究及治療藥物監測研究進展[J].中國醫院用藥評價與分析,2021,21(1):121-124,128.
[ 2 ] 吳小燕,文曉柯,李慧,等.美羅培南新發及嚴重不良反應綜述[J].中南藥學,2019,17(4):576-579.
[ 3 ] 過曉雯,周佳.兒科美羅培南臨床應用評價標準的建立與應用分析[J].中國現代應用藥學,2020,37(2):242-247.
[ 4 ] 張石革,藏靖,梁建華,等.碳青霉烯類抗生素的研究進展及其在抗感染中的應用評價[J].中國醫院用藥評價與分析,2004,4(2):71-75.
[ 5 ] 王艷蕊.美羅培南對新生兒重癥細菌感染的療效及其對炎癥因子水平改善的影響[J].抗感染藥學,2020,17(4):588-590.
[ 6 ] 閆孝永,江春容.醫院兒科用抗菌藥物不良反應報告206例分析 [J].中國藥業,2017,26(9):82-84.
[ 7 ] 許峰,黨紅星.關注兒科重癥細菌感染的優化抗菌治療策略[J].中華兒科雜志,2011,49(1):1-3.
[ 8 ] 閆樺,王晶,齊賽卿,等.美羅培南在新生兒重癥感染治療中的應用價值及安全性[J].兒科藥學雜志,2017,23(2):16-18.
[ 9 ] 席加水,馬燕,聶翠.美羅培南治療新生兒重癥細菌感染的臨床療效及安全性評價[J].山東醫藥,2011,51(51):35-36.
[10] 李秋實.美羅培南治療新生兒重癥多重耐藥菌感染臨床研究[J].中國藥業,2017,26(2):60-63.
[11] 吳朝波.美羅培南治療新生兒重癥細菌感染32例療效分析[J].中國實用醫藥,2011,6(15):41-42.
[12] 劉宇,米弘英,楊芬.美羅培南治療新生兒及嬰幼兒重癥感染療效評價[J].中國藥房,2011,22(26):2466-2468.
[13] ZENG X T,ZHANG Y G,KWONG J S W,et al. The methodological quality assessment tools for preclinical and clinical studies,systematic review and meta-analysis,and clinical practice guideline:a systematic review[J]. J Evid Based Med,2015,8(1):2-10.
[14] 丁玉玲,劉建軍.美羅培南治療新生兒重癥感染的效果研究[J].當代醫藥論叢,2018,16(14):130-132.
[15] 于新生.美羅培南治療新生兒重癥多重耐藥菌感染的臨床價值研究[J].中外醫療,2019,38(16):39-42.
[16] 吳敏.美羅培南治療新生兒化膿性腦膜炎的臨床研究[J].中國農村衛生,2019,11(8):37.
[17] 廖景文.美羅培南治療新生兒化膿性腦膜炎的臨床療效分析[J].中國繼續醫學教育,2020,12(34):140-144.
[18] 張定芬.美羅培南對新生兒重癥細菌感染的療效及安全性觀察[J].中國婦幼保健,2013,28(34):5642-5644.
[19] 張慧蕓,韓麗.美羅培南治療新生兒重癥細菌感染的療效及安全性評價[J].中國處方藥,2017,15(8):90.
[20] 張藝森.美羅培南結合替加環素治療新生兒重癥多重耐藥菌感染的療效觀察[J].北方藥學,2017,14(12):108- 109.
[21] 張鵬遠.美羅培南治療新生兒重癥多重耐藥菌感染臨床研究[J].藥品評價,2019,16(4):38-40,47.
[22] 曾淑英,黃郁波.美羅培南與頭孢他啶對新生兒重癥細菌感染的臨床療效與安全性比較[J].抗感染藥學,2019,16(7):1161-1163.
[23] 李麗.美羅培南治療新生兒化膿性腦膜炎臨床療效分析[J].北方藥學,2018,15(4):96-97.
[24] 李新紅,蘇惠文,班奕,等.美羅培南治療新生兒化膿性腦膜炎的療效及安全性評價[J].現代診斷與治療,2020,31(13):2046-2047.
[25] 林娟娟,牛迪.美羅培南治療新生兒重癥多重耐藥菌感染的臨床效果及安全性[J].中外醫學研究,2018,16(33):18-19.
[26] 柳俊伶.美羅培南在新生兒化膿性腦膜炎治療中的臨床分析[J].中國處方藥,2019,17(10):100-101.
[27] 段煉.分析美羅培南對新生兒化膿性腦膜炎的臨床治療價值[J].世界復合醫學,2019,5(3):64-67.
[28] 王衛星,付淑芳.美羅培南與頭孢他啶治療新生兒重癥細菌感染的療效對比[J].中國婦幼保健,2018,33(9):2029-2031.
[29] 簡于群,單志紅.美羅培南聯合替加環素治療新生兒重癥多重耐藥菌感染的臨床效果[J].臨床合理用藥雜志,2015,8(27):12-13.
[30] 耿美麗.美羅培南聯合頭孢曲松鈉治療新生兒化膿性腦膜炎71例療效評價[J].藥品評價,2021,18(5):304-307.
[31] 胡德飛.新生兒化膿性腦膜炎的早期診斷和治療方法探討[J].當代醫學,2018,24(24):142-143.
[32] 蔣曉莉.美羅培南聯合注射用頭孢曲松鈉治療57例新生兒化膿性腦膜炎的療效及安全性分析[J].黑龍江中醫藥,2020,49(4):110-111.
[33] 陳衛平,林莉,徐陽.美羅培南治療新生兒化膿性腦膜炎的臨床效果[J].當代醫學,2020,26(12):11-13.
[34] 韋紅艷,程琳,廖華玉,等.美羅培南治療新生兒膿毒血癥合并化膿性腦膜炎的療效觀察[J].中國處方藥,2019,17(5):77-78.
[35] 馬榮偉,王莉.美羅培南治療新生兒重癥細菌感染的臨床療效及安全性分析[J].中國藥物與臨床,2016,16(10):1481-1482.
[36] 魏小娣,樊婷.美羅培南治療新生兒化膿性腦膜炎臨床效果觀察[J/OL].中國醫學前沿雜志(電子版),2016,8(9):141-144[2020-08-30]. http:www.yixueqianyan.cn/CN/10.12037/YXQY.2016.09-25.
[37] 黃全發.美羅培南治療新生兒重癥多重耐藥菌感染的有效性[J]世界復合醫學,2020,6(9):168-170,183.
[38] 黃青,吳斌,朱然.美羅培南與頭孢他啶對新生兒重癥細菌感染患兒抗感染治療的臨床療效及安全性比較[J].抗感染藥學,2018,15(4):594-596.
[39] 仲兆金.碳青霉烯類抗生素在兒科的臨床應用[J].國外醫藥抗生素分冊,2009,30(2):76-81.
[40] 莫海玲. 4種碳青霉烯類抗生素的藥理學特點及臨床應用評價[J].中國醫院用藥評價與分析,2007,7(2):96-98.
[41] 李金妞.美羅培南對新生兒重癥細菌感染的療效及安全性觀察[J].臨床研究,2020,28(6):92-94.
[42] 國家衛生健康委員會醫政醫管局.關于印發碳青霉烯類抗菌藥物臨床應用專家共識等3個技術文件的通知:國衛辦醫函〔2018〕822號[EB/OL].(2018-09-21)[2020-08-
30]. http://www.nhc.gov.cn/cms-search/xxgk/getManu-
scriptXxgk.htm?id=95f65ca473b44746b24590e94468b8ff.
(收稿日期:2021-05-20 修回日期:2021-08-16)
(編輯:陳 宏)

