外周血APN、HbA1c、糖基化ApoA-I水平與冠心病患者PCI術后血運重建的關系
李 涵,黃宇鵬,金紅艷,倪自強,楊國康
冠心病的病理基礎是冠狀動脈粥樣硬化導致管腔狹窄,進而引起心肌缺血缺氧[1],因此經皮冠狀動脈介入治療(PCI)對冠心病患者冠狀動脈血運重建、恢復狹窄或閉塞段血流、改善預后具有重要意義[2-3]。不過既往臨床研究發現,PCI術后仍有10%~30%的患者血運重建失敗,需要再次血運重建[4]。如何減少PCI術后血運重建失敗成為臨床關注的重點。目前認為脂聯素(APN)、糖化血紅蛋白(HbA1c)、糖基化載脂蛋白A-I(ApoA-I)是反映機體糖脂代謝的敏感指標,而且有研究證實上述指標與冠狀動脈粥樣硬化密切相關,有可能影響冠心病患者PCI術后血運重建[5-6]。本研究旨在探討外周血APN、HbA1c、糖基化ApoA-I水平與冠心病患者PCI術后血運重建的關系,現報告如下。
1 對象與方法
1.1研究對象 選取2019年1月—2020年10月我院行PCI的冠心病患者132例。納入標準:符合冠心病診斷標準[7];PCI包括直接PCI、轉運PCI及溶栓后緊急PCI,均滿足相應的PCI指征[8]。排除標準:對造影劑、支架材料過敏者;伴凝血功能障礙者;靶血管直徑<2.25 mm者;嚴重鈣化病變預擴張不充分者;有PCI史者;合并嚴重肺、肝、腎、腦疾病及惡性腫瘤者。根據患者PCI術后冠狀動脈造影結果判斷血運重建情況,分為不完全血運重建35例(A組)和完全血運重建97例(B組)。不完全血運重建為冠狀動脈造影后發現患者冠狀動脈存在多支多處病變,即使植入支架也只能改善部分血管的血運情況,仍存在小分支血管閉塞,部分血管仍然狹窄,存在慢血流或無復流現象,缺血心肌組織的微循環依然不能全部恢復。
1.2研究方法 ①收集患者臨床資料,包括性別、年齡、吸煙史、基礎疾病、多支病變、左主干病變、分叉病變、PCI類型、植入支架數目、支架最大長度、支架最大直徑。②PCI術后第2日清晨抽取患者空腹外周血2管,每管5 ml,一管為紅色頭蓋真空管,3000 r/min離心10 min分離血漿,檢測血漿APN水平;一管為灰色頭蓋,加草酸鉀氟化鈉抗凝劑,用于檢測HbA1c、糖基化ApoA-I水平。應用日立公司生產的7600型全自動生化分析儀采用雙抗體夾心法檢測血漿APN水平,試劑盒購自羅氏診斷產品(上海)公司。應用美國伯樂公司生產的D-10型全自動HbA1c分析儀采用高壓液相法檢測HbA1c水平,配套試劑盒購自美國伯樂公司。采用蛋白免疫印跡法檢測糖基化ApoA-I水平,試劑盒購自美國Thermo Scientific公司,以β-actin為內參,計算糖基化ApoA-I相對灰度值。

2 結果
2.1臨床資料比較 A組中有吸煙史、伴高血壓病、伴糖尿病、伴高脂血癥、多支病變的比例明顯高于B組(P<0.05,P<0.01)。見表1。

表1 PCI術后不完全和完全血運重建的冠心病2組臨床資料比較
2.2外周血APN、HbA1c、糖基化ApoA-I水平比較 A組血漿APN水平低于B組(P<0.05),HbA1c、糖基化ApoA-I水平高于B組(P<0.01),見表2。
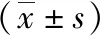
表2 PCI術后不完全和完全血運重建的冠心病2組外周血APN、HbA1c、糖基化ApoA-I水平比較
2.3外周血APN、HbA1c、糖基化ApoA-I水平對PCI術后血運重建的預測價值 ROC曲線分析顯示,糖基化ApoA-I水平預測PCI術后血運重建的曲線下面積(AUC)最大,靈敏度、特異度最高,其次為HbA1c和APN,見表3和圖1。

圖1 外周血APN、HbA1c、糖基化ApoA-I水平預測PCI術后血運重建的ROC曲線APN為脂聯素,HbA1c為糖化血紅蛋白,ApoA-I為載脂蛋白A-I,PCI為經皮冠狀動脈介入治療,ROC為受試者工作特征

表3 外周血APN、HbA1c、糖基化ApoA-I水平預測PCI術后血運重建的ROC曲線分析
2.4PCI術后血運重建失敗影響因素分析 以PCI術后血運重建情況為因變量,賦值:不完全血運重建=1,完全血運重建=0。自變量賦值:吸煙史,有=1,無=0;高血壓病,有=1,無=0;糖尿病,有=1,無=0;高脂血癥,有=1,無=0;多支病變,有=1,無=0;APN低水平(≤3.9 mg/L),是=1,否=0;HbA1c高水平(≥5.5%),是=1,否=0;糖基化ApoA-I高水平(≥0.7),是=1,否=0。多因素Logistic回歸分析結果顯示,糖尿病、APN低水平、HbA1c高水平、糖基化ApoA-I高水平是冠心病患者PCI術后血運重建失敗的危險因素(P<0.05,P<0.01)。見表4。

表4 PCI術后血運重建失敗的多因素Logistic回歸分析
3 討論
PCI已成為治療冠心病的重要方法,目前冠心病患者PCI治療率在90%以上[9]。不過由于血栓形成等多種原因,PCI術后仍有部分患者不能達到完全血運重建,出現冠狀動脈無血流或慢復流現象,心肌灌注不良,引起心肌再梗死,嚴重影響患者預后。本研究重點分析導致PCI術后血運重建失敗的影響因素,結果發現PCI術后血運重建與性別、年齡、左主干病變、分叉病變、PCI類型、植入支架數目、支架最大長度、支架最大直徑無明顯關聯。國外研究也認為,冠狀動脈本身病變特征及采取的支架治療器械不會影響PCI術后血運重建效果[10]。本研究發現吸煙史、高血壓病、糖尿病、高脂血癥、多支病變與PCI術后血運重建有一定關聯,與王丹陽和丁紹平[11]研究結果相符。吸煙、高血壓病、糖尿病、高脂血癥是冠狀動脈粥樣硬化的危險因素,故而有可能影響PCI術后血運重建的效果。不過本研究多因素Logistic回歸分析卻發現上述指標中僅有糖尿病為PCI術后血運重建失敗的獨立危險因素,這可能說明高血糖及糖脂代謝紊亂對PCI術后血運重建效果有重要影響。
本研究發現A組血漿APN水平低于B組,HbA1c、糖基化ApoA-I水平高于B組,差異有統計學意義。APN由脂肪細胞分泌,可增強胰島素敏感性,抑制肝糖原異生,是調節機體血糖穩定的重要因子[12]。既往文獻報道APN與動脈粥樣硬化密切相關,冠狀動脈狹窄程度越高,血漿APN水平越低[13]。本研究還發現,APN低水平可使PCI術后血運重建失敗的風險提高2.370倍,因此提高冠心病患者血漿APN水平有助于預防PCI術后血運重建失敗。目前公認HbA1c水平升高會增加冠狀動脈狹窄程度,與冠心病預后不良呈正相關[14]。本研究也發現HbA1c高水平是PCI術后血運重建失敗的危險因素,與王娟等[15]報道結果一致。ApoA-I是高密度脂蛋白的功能結構蛋白,可積極調節血脂代謝,不過其經過糖基化作用形成糖蛋白,在高糖環境下卻有不良影響[16]。一方面,糖基化ApoA-I影響正常的抗氧化、抗炎功能,損傷血管內皮功能,導致血栓形成;另一方面,糖基化ApoA-I促進了血管趨化因子、黏附因子分泌及粥樣斑塊生成,導致動脈粥樣硬化[17]。上述可以解釋糖基化ApoA-I高水平增加了冠心病患者PCI術后血運重建失敗的風險。
綜上,外周血APN、HbA1c、糖基化ApoA-I可作為冠心病患者PCI術后血運重建的預測指標,血運重建失敗與APN降低、HbA1c和糖基化ApoA-I升高有關。早期行外周血APN、HbA1c、糖基化ApoA-I檢測可有助于篩選出高危患者,密切監護并及時采取有效措施以避免不良心血管事件發生。

