腹腔鏡下卵巢巧克力囊腫剝除術中不同分離方案與開腹手術對卵巢巧克力囊腫患者激素水平的影響
徐向瑜,段鑫蕾,張翠林
(新野縣人民醫院 婦產科,河南 南陽 473500)
卵巢巧克力囊腫是一種主要發生于卵巢內的常見病,通過不斷增大,侵蝕周圍正常組織,損害卵巢[1]。目前采用開腹術、腹腔鏡下剝除術等方法治療。其中,開腹術無特殊的限定條件,適用于所有患者;而腹腔鏡下卵巢巧克力囊腫剝除術為微創手術,具有切口小、手術時間短等優勢,以鈍性分離法和注水分離法最為常用[2]。本研究選取82例卵巢巧克力囊腫患者進行研究,旨在探討腹腔鏡下卵巢巧克力囊腫剝除術中不同分離方案與開腹手術對卵巢功能、妊娠率的影響。
1 資料與方法
1.1 一般資料本研究經新野縣人民醫院倫理委員會批準。前瞻性選取2018年2月至2020年2月診治的82例卵巢巧克力囊腫患者作為研究對象。納入標準:符合卵巢巧克力囊腫診斷標準,經CT或B超等影像學檢查確診。排除標準:(1)存在卵巢手術史;(2)伴有多囊卵巢綜合征。兩組一般資料比較,差異無統計學意義(P>0.05)。見表1。
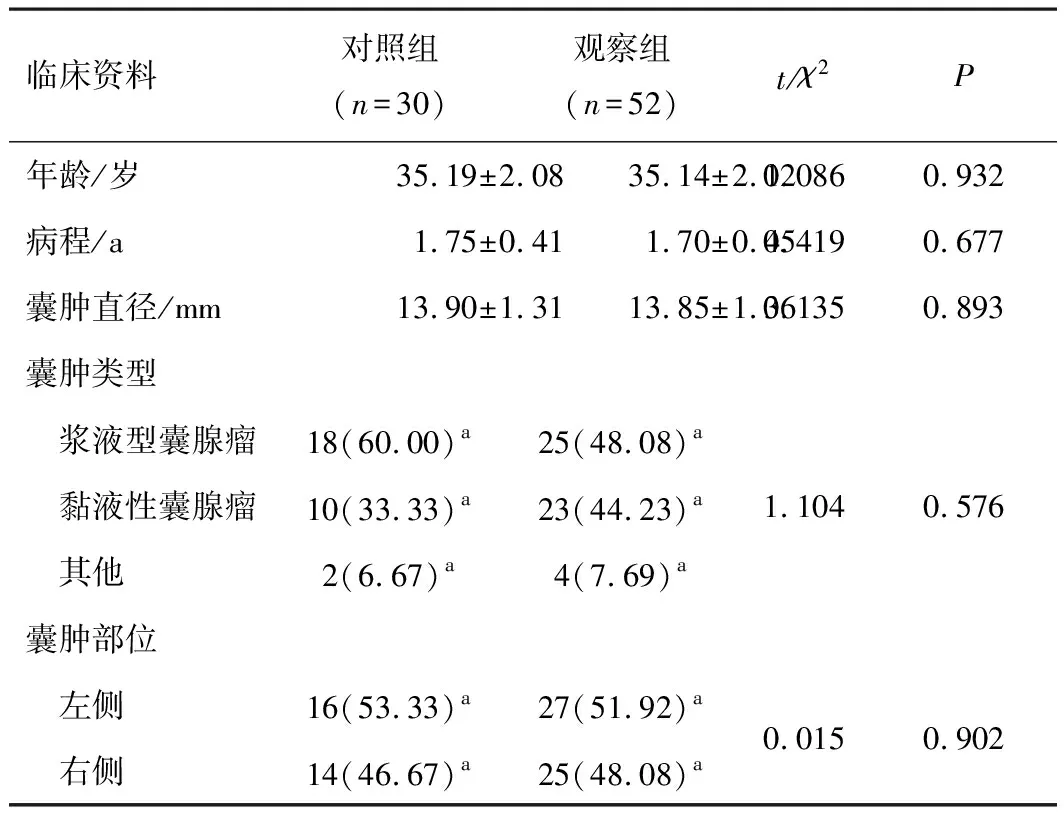
表1 兩組一般資料比較
1.2 手術方法
1.2.1術前處理 兩組受試者于治療前行常規檢查,待排除手術禁忌證后,擇期行手術治療。
1.2.2對照組 接受開腹手術治療。取平臥位,氣管插管,全身麻醉,于下腹做一橫向切口,切開皮下組織,打開腹部,采用冷刀切開卵巢,分離、剝除囊腫,縫合,進行抗感染治療。
1.2.3觀察組 接受腹腔鏡下卵巢巧克力囊腫剝除術治療。取平臥位,氣管插管全身麻醉后,建立氣腹,壓強為12~15 mmHg(1 mmHg=0.133 kPa),經臍孔置入腹腔鏡套管,經臍下腹或上腹穿刺置入手術器械套管。鈍性分離組在囊腫表面劃一小口,準確找到卵巢皮質與囊腫壁界限后,鈍性分離。注水分離組在找到卵巢皮質與囊腫壁界限后,采用1∶6稀釋垂體后葉素20~30 mL注入囊腫壁與卵巢皮質交界處,形成水墊后通過張力分離囊腫與皮質。最后切開包膜,銳性分離,剝離囊腫,縫合創面,包扎。
1.3 觀察指標(1)激素水平。分別于術前、術后3個月檢測患者卵泡刺激素(follicle stimulating hormone,FSH)、黃體生成素(luteinizing hormone,LH)、雌二醇(estradiol,E2)水平。抽取空腹靜脈血3 mL,離心處理,采用化學發光法檢測。(2)記錄兩組妊娠率、復發率以及并發癥(出血、氣栓、感染)發生情況。
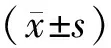
2 結果
2.1 激素水平比較治療前,3組血清FSH、LH、E2水平比較,差異無統計學意義(P>0.05);治療3個月后,注水分離組FSH、LH水平低于鈍性分離組與對照組,E2水平高于鈍性分離組與對照組(P<0.05)。見表2。
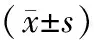
表2 兩組術前和術后3個月FSH、LH、E2比較
2.2 妊娠率、復發率及并發癥對照組妊娠率為26.67%(8/30),復發率為43.33%(13/30),發生3例出血、1例氣栓、2例感染,并發癥發生率為23.33%(7/30);鈍性分離組妊娠率為53.85%(14/26),復發率為26.92%(7/26),發生1例出血,并發癥發生率為3.85%(1/30);注水分離組妊娠率為76.92%(20/26),復發率為3.85%(1/26),未出現并發癥,并發癥發生率為0。注水分離組妊娠率高于鈍性分離組與對照組,復發率低于鈍性分離組與對照組,并發癥發生率低于對照組(P<0.05)。
3 討論
卵巢巧克力囊腫發病率在臨床上呈日益上升趨勢,多見于青年和中年女性。目前臨床上該病的發病機制尚未明確,僅認為其與經血逆流異位種植學說、體腔上皮化生學說、遺傳學說、免疫因素等具有一定相關性[3]。對該病通常采用期待療法、藥物及手術等方法治療。其中,第一種與第二種適合近絕經期女性,且癥狀相對較輕,而對于年輕女性及病灶組織較大,往往需要通過手術方法治療,譬如開腹手術、腹腔鏡下卵巢巧克力囊腫剝除術等。開腹手術雖然能夠切除病灶組織,但因受手術時間過長、切口較大等因素的影響,易在一定程度上增加感染發生率。另外,有研究表明,開腹手術會對卵巢功能造成影響[4]。腹腔鏡下卵巢巧克力囊腫剝除術是在腹腔鏡的協助下盡可能完整剝離囊壁,去除病灶,具有切口小、術中出血量少等優勢[5]。在研究結果中可看到,注水分離組與鈍性分離組住院時間、排氣時間短于對照組,充分體現了腹腔鏡下卵巢巧克力囊腫剝除術的優點。但有研究表示,腹腔鏡下卵巢巧克力囊腫剝除術中不同分離方案的療效也不同。另外,對卵巢儲備功能的影響也不同[6]。
目前,臨床上評估卵巢功能主要是依賴FSH、LH、E2指標。其中,FSH是由腺垂體嗜堿性細胞所分泌,在人體發育、生長、青春期性成熟以及生殖相關的生理過程中發揮重要調控作用[7]。LH為腺垂體分泌的糖蛋白,在促進女性排卵、黃體生成及月經周期調節過程中發揮重要作用[8]。E2是臨床觀察卵巢儲備功能的重要指標,由卵巢濾泡、黃體生成。當手術治療對卵巢功能造成損傷,則會表現出性激素分泌異常,譬如FSH、LH水平上升,E2水平下降[9]。分析為,卵巢儲備功能下降時,竇狀卵泡數量會顯著減少,卵泡發育速度減緩,導致雄激素水平下降,而雄激素的下降會在一定程度上影響下丘腦-垂體-卵巢軸行負反饋調節,通過刺激垂體,大量釋放FSH、LH[11]。鑒于上述信息,本文進行了深入研究,治療后,注水分離組FSH、LH水平低于鈍性分離組與對照組,而E2高于鈍性分離組與對照組,從中可看到注水分離組對卵巢儲備功能的影響更小,而另外兩組對卵巢儲備功能的影響大。其原因在于鈍性分離過程中,當無法準確找到卵巢皮質與囊壁的分界點時,會在實行剝除操作時剝離正常的卵巢組織,從而降低卵巢的儲備功能,而開腹手術對卵巢進行切開,同樣會降低卵巢的儲備功能[10-11]。另外,注水分離組妊娠率高于鈍性分離組與對照組,也反映了注水分離組的卵巢功能受損程度低,因卵巢功能不僅決定著超促排卵周期對后續超促排卵激素用量的敏感性,還決定卵泡獲得數量,而卵泡獲得數量的增加也會在一定程度上提高妊娠率[12]。故注水分離組的妊娠率更高,且復發率及并發癥發生率低于鈍性分離組與對照組,表明了注水分離的操作方法安全性更高,療效也更加理想。
綜上所述,腹腔鏡下卵巢巧克力囊腫剝除術對卵巢儲備功能影響較小,尤其是注水分離法,因對卵巢組織損傷小,故妊娠率更高。

