容積旋轉(zhuǎn)調(diào)強(qiáng)放射治療與9野靜態(tài)調(diào)強(qiáng)放射治療在侵犯顱內(nèi)鼻咽癌患者中的劑量學(xué)特點
劉小慧
福建醫(yī)科大學(xué)附屬第一醫(yī)院放療科 (福建福州 350005)
鼻咽癌是我國常見的惡性腫瘤,發(fā)病具有明顯的地域及種族差異,呈南高北低的分布趨勢[1]。由于該病發(fā)病具有隱匿性,部分以面麻、復(fù)視等癥狀就診的患者,往往提示腫瘤已侵犯至顱內(nèi),加之鼻咽與腦干、脊髓等重要器官毗鄰,因此,對于侵犯至顱內(nèi)的患者,其計劃設(shè)計難度較大。在對靶區(qū)有較好覆蓋的同時,如何最大限度地保護(hù)腦干、脊髓、視神經(jīng)等重要危及器官(organ at risk,OAR),一直是放射治療計劃設(shè)計的難題。目前,調(diào)強(qiáng)放射治療(intensity modulated radiation therapy,IMRT)已成為鼻咽癌標(biāo)準(zhǔn)的治療方式[2],在此基礎(chǔ)上發(fā)展起來的容積旋轉(zhuǎn)調(diào)強(qiáng)放射治療(volumetric modulated arc therapy,VMAT)與IMRT相比,可以達(dá)到近似或更優(yōu)的劑量學(xué)分布,且有更好的預(yù)后[3]。本研究基于侵犯顱內(nèi)的鼻咽癌患者,旨在探討兩種不同治療方式的劑量學(xué)特點,以期為此類患者選擇更優(yōu)的放射治療方式提供臨床依據(jù),現(xiàn)報道如下。
1 資料與方法
1.1 一般資料
選取2018年9月至2019年10月于我院就診的11例侵犯顱內(nèi)的鼻咽癌患者,其中男7例,女4例;中位年齡61歲;按2017年美國癌癥分期聯(lián)合委員會(American Joint Committee on Cancer,AJCC)第8版分期,所有患者均為T4分期,9.1%(1/11)的患者為N1分期,72.7%(8/11)的患者為N2分期,18.2%(2/11)的患者為N3分期,最終均為ⅣA期。本研究已獲得醫(yī)院醫(yī)學(xué)倫理委員會審核批準(zhǔn)。納入標(biāo)準(zhǔn):經(jīng)病理確診為鼻咽癌且無遠(yuǎn)處轉(zhuǎn)移;行MRI或PET-CT等影像學(xué)檢查確認(rèn)腫瘤侵及顱內(nèi)海綿竇、腦膜及顱神經(jīng)等;患者對本研究知情并自愿簽署知情同意書。排除標(biāo)準(zhǔn):既往有頭頸部放射治療史。
1.2 設(shè)備與條件
(1)CT模擬定位:SOMATOM Definition AS螺旋CT(日本)、LAP Dorado 3模擬激光定位系統(tǒng)(德國)。(2)體位固定:康利達(dá)KLD-PLVC-OC全碳纖維體架(中國)和博達(dá)神州熱塑型體膜(中國)。(3)放射治療前圖像掃描獲得:SOMATOM Definition AS螺旋CT(日本)。(4)圖像傳輸及治療計劃設(shè)計:計劃CT圖像通過局域網(wǎng)傳輸至RAYSTATION治療計劃系統(tǒng)。(5)治療儀器:瓦里安Trilogy醫(yī)用高能電子直線加速器(美國),裝配Varian Exact IGRT治療床。
1.3 技術(shù)路線
1.3.1模擬及體位固定
通常情況下,患者取仰臥位,將頭頸肩架、頭部置于合適角度的頭枕中,使頭頸部呈正常仰伸位,雙手自然放于體側(cè),使用頸肩熱塑膜固定體位,行CT平掃加增強(qiáng)掃描,掃描范圍從頭頂至氣管分叉處,掃描層厚為3 mm。
1.3.2靶區(qū)勾畫原則
使用RAYSTATION 4.7.5.4醫(yī)師工作站行靶區(qū)勾畫,靶區(qū)定義參考國際輻射單位與測量委員會(International Commission on Radiation Units and Measurements,ICRU)50、62 號文件。(1)腫瘤靶區(qū)(gross tumor volume,GTV),包括原發(fā)灶和轉(zhuǎn)移淋巴結(jié):原發(fā)灶GTVnx指臨床檢查和影像學(xué)所見的原發(fā)腫瘤;淋巴結(jié)區(qū)GTVnd指臨床和(或)影像學(xué)觀察到的腫大淋巴結(jié)區(qū)域。(2)臨床靶區(qū)(clinical target volume,CTV),包括CTV1和CTV2:其中原發(fā)腫瘤周圍極有可能受侵的鄰近區(qū)域或極有可能轉(zhuǎn)移的區(qū)域以CTV1表示,即高危區(qū);CTV2指根據(jù)腫瘤的生物學(xué)行為推斷出的可能出現(xiàn)轉(zhuǎn)移的淋巴結(jié)區(qū)域,為CTV1向前、上下、兩側(cè)各外擴(kuò)0.5~1.0 cm后外擴(kuò)0.3~0.5 cm(根據(jù)腫瘤累及情況及與脊髓、腦干等組織結(jié)構(gòu)的間距決定外擴(kuò)的適當(dāng)距離)及GTVnd和所在淋巴引流區(qū)及需要預(yù)防照射的陰性淋巴引流區(qū),即選擇照射區(qū)。(3)計劃靶區(qū)(planning target volume,PTV):靶區(qū)的PTV為各靶區(qū)分別外放3 mm,簡稱為PTVnx、PTVnd、PTV1和PTV2。
1.3.3OAR勾畫原則
OAR定義參考ICRU 62、83號報告,包括腦干、視神經(jīng)、視交叉、脊髓、顳葉、眼球、晶體、中耳、內(nèi)耳、下頜骨、顳頜關(guān)節(jié)等。脊髓、腦干分別外放3 mm,生成危及器官計劃靶區(qū)(planning organ at risk volume,PRV),用于計劃設(shè)計及評估。
1.3.4處方劑量及OAR限量
所有患者的處方劑量均采用同步加量的方式給予。PTVnx的靶區(qū)處方劑量為70.95 Gy、PTVnd的劑量為66 Gy、PTV1的劑量為59.4 Gy、PTV2的劑量為52.8 Gy,分割33次,5次/周。
1.3.5計劃設(shè)計及劑量限制
在RAYSTATION 4.7.5.4醫(yī)師工作站上對入組的11例患者分別進(jìn)行容積旋轉(zhuǎn)調(diào)強(qiáng)(雙弧)及9野靜態(tài)調(diào)強(qiáng)計劃設(shè)計,設(shè)計過程采用相同參數(shù),劑量限制參考美國腫瘤放射治療協(xié)作組(Radiation Therapy Oncology Group,RTOG)0225和0615標(biāo)準(zhǔn),具體見表1。

表1 正常組織的劑量限制
1.4 計劃對比評價指標(biāo)
(1)靶區(qū):適形性指數(shù)(conformity index,CI)、均勻性指數(shù)(heterogeneity index,HI),其中CI=(Vt,ref×Vt,ref)/(Vt×Vref),式中,Vt為總計劃靶區(qū)體積,Vt,ref為95%處方劑量等劑量線所包繞的靶區(qū)體積,Vref為95%處方劑量等劑量線所覆蓋的所有區(qū)域的體積,CI越接近于1表明靶區(qū)適形性越好;HI=(D2-D98)/D50,式中,Dx表示占其自身總體積的百分比x的吸收劑量,HI越小表明靶區(qū)劑量的均勻性越好。(2)OAR:腦干、脊髓、顳葉、視神經(jīng)、視交叉、晶體、腮腺、中耳、內(nèi)耳、顳頜關(guān)節(jié)、喉等。
1.5 統(tǒng)計學(xué)處理
采用SPSS 22.0統(tǒng)計軟件進(jìn)行數(shù)據(jù)處理,采用配對t檢驗比較兩種治療方式同一靶體積或同一OAR受照劑量均值之間的差異,P<0.05為差異有統(tǒng)計學(xué)意義。
2 結(jié)果
2.1 兩種計劃靶區(qū)實際體積比較
兩種計劃PTVnd、PTV2的體積比較,差異均無統(tǒng)計學(xué)意義(P>0.05);9F-IMRT組PTVnx、PTV1的體積均小于VMAT組,差異有統(tǒng)計學(xué)意義(P<0.05),見表2。

表2 兩種計劃靶區(qū)實際體積比較例)
2.2 兩種計劃靶區(qū)劑量學(xué)比較
兩種計劃PTVnx的D98、D50,PTVnd的D98,PTV1的Dmean,PTV2的D98、Dmean比較,差異均無統(tǒng)計學(xué)意義(P>0.05);9F-IMRT組PTVnx的D2、HI,PTVnd的D2,PTV1的D2,PTV2的D2均高于VMAT組,差異有統(tǒng)計學(xué)意義(P<0.05);9F-IMRT組PTVnx的CI,PTV1的D98均低于VMAT組,差異有統(tǒng)計學(xué)意義(P<0.05),見表3。

表3 兩種計劃靶區(qū)劑量學(xué)比較例)
2.3 兩種計劃正常組織受照劑量比較
兩種計劃脊髓PRV的Dmax,左視神經(jīng)的Dmax,視交叉的Dmax,左晶體的Dmax,左、右腮腺的Dmean,左、右中耳的Dmean,左、右內(nèi)耳的Dmean,左、右顳頜關(guān)節(jié)的Dmax,喉的Dmean比較,差異均無統(tǒng)計學(xué)意義(P>0.05);9F-IMRT組腦干PRV的D0.1cc,左、右顳葉的Dmax,右視神經(jīng)的Dmax均高于VMAT組,差異有統(tǒng)計學(xué)意義(P<0.05);9F-IMRT組右晶體的Dmax低于VMAT組,差異有統(tǒng)計學(xué)意義(P<0.05),見表4。
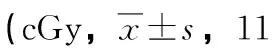
表4 兩種計劃正常組織受照劑量比較例)
3 討論
放射治療或以放射治療為主的綜合治療是鼻咽癌公認(rèn)的有效治療手段[4-5]。隨著計算機(jī)技術(shù)、影像學(xué)技術(shù)和加速器的發(fā)展,相較于IMRT,VMAT在靶區(qū)覆蓋及OAR保護(hù)方面更有優(yōu)勢[6]。既往有研究報道,在其他頭頸部腫瘤中,如膠質(zhì)母細(xì)胞瘤,VMAT與IMRT在靶區(qū)覆蓋方面無明顯差異[7]。Nagarajan等[8]對頭頸部腫瘤VMAT與IMRT計劃的劑量學(xué)比較研究提示,兩者在靶區(qū)覆蓋方面無明顯差異。本研究中所有患者均采用容積旋轉(zhuǎn)調(diào)強(qiáng)及9野靜態(tài)調(diào)強(qiáng)計劃設(shè)計,結(jié)果顯示,VMAT靶區(qū)的劑量分布優(yōu)于9F-IMRT,與Radhakrishnan等[6]報道的結(jié)果相似。
對于T4分期的鼻咽癌患者,由于腫瘤鄰近腦干、顳葉、視神經(jīng)、視交叉等重要結(jié)構(gòu),因此,在滿足處方劑量要求的同時,應(yīng)盡可能減少OAR的受照劑量。本研究中,入組患者PTVnx的體積無法達(dá)到處方劑量的95%,究其原因在于,腫瘤與腦干鄰近,在保證腦干盡可能達(dá)到限量要求的同時,靶區(qū)的體積即會有所“犧牲”。既往有研究報道,放射治療后腦干損傷與T分期有關(guān),分期越晚,發(fā)生腦干損傷的可能性越大[9]。進(jìn)一步研究顯示,這主要是因為T4分期的患者往往有更高的Dmax,而Dmax是腦干損傷的獨立影響因素。本研究結(jié)果顯示,9F-IMRT組腦干PRV的D0.1cc高于VMAT組,與Jia等[10]報道的結(jié)果相似;在危及器官評價方面,兩種計劃顳葉及視神經(jīng)均無法滿足限量,主要是因為侵及顱內(nèi)的T4分期鼻咽癌患者,其靶區(qū)位置毗鄰顳葉及視神經(jīng),兩者PRV與靶區(qū)PTV有重疊,所以顳葉及視神經(jīng)很難達(dá)到目標(biāo)劑量。
綜上所述,在侵犯顱內(nèi)的鼻咽癌患者中,VMAT靶區(qū)的劑量分布優(yōu)于9F-IMRT,腦干、顳葉、視神經(jīng)等危及器官的受照劑量低于9F-IMRT。但是,本研究入組樣本數(shù)少,對于VMAT是否可推及所有侵犯顱內(nèi)的鼻咽癌患者,需要更大規(guī)模的前瞻性研究。

