基于1H-NMR血清代謝組學的阿爾茨海默病腎虛精虧證生物學機制及地黃飲子的干預作用研究
帥月圓,韓 誠,2,曹建華,李少創,秦亞莉,2
(1.山西中醫藥大學中醫腦病學山西省重點實驗室,山西 晉中030619;2.山西中醫藥大學基礎醫學院,山西 晉中030619;3.山西大學中醫藥現代研究中心,山西 太原030006)
阿爾茨海默病(Aizheimer's disease,AD)是一種中樞神經系統退行性疾病,其主要特征為進行性認知功能障礙和記憶力減退以及行為改變[1]。據WHO報道,目前全球共有癡呆癥患者約5000萬,以AD患者為主[2]。該病早期難以察覺,確診時多已發展到中晚期,給患者的日常生活、工作及社交帶來嚴重影響。AD的具體發病機制目前尚未完全研究透徹,存在多種假說。早期診斷的困難、發病機制的不明確、治療效果的不顯著以及病程的不可逆都表明AD的危害程度,隨著我國老齡化進程的不斷發展,對于AD的早期防治越來越顯現出重要的醫學價值和社會意義。
AD在中醫學中歸屬于癡呆范疇,其病機為髓減腦消,神機失用,病性為本虛標實,本虛又以腎虛為關鍵。腎主骨生髓與腦相通,AD患者多年老體衰,腎精漸虧,腦髓失于充養而消減,髓海空虛則心無所慮,精明失聰,神無所依而出現癡呆的各種表現[3]。故中醫對于AD的治療多從腎虛精虧著手,地黃飲子作為經典補腎方劑常被用于AD腎虛精虧證的治療。研究表明,地黃飲子可以通過減輕膽堿能系統損害、抗氧化和減少自由基、抑制神經細胞凋亡發揮對AD的治療作用[4]。本研究運用經典補腎方劑地黃飲子對AD腎虛精虧證進行干預,分析其內源性代謝物的變化,探尋AD腎虛精虧證的生物學機制以及地黃飲子干預AD腎虛精虧證的作用機制。
1 材料與方法
1.1 實驗材料
1.1.1 實驗動物SPF級雄性SD大鼠60只,體質量(200±20)g,購于北京維通利華實驗動物技術有限公司[SCXK(京)2016-0011],動物飼養于山西中醫藥大學動物房,經適應性喂養1周后開始實驗。
1.1.2 藥物與試劑 地黃飲子購于北京同仁堂山西連鎖店;Aβ1-42購于杭州中肽生化有限公司(批號:AP0039);D-半乳糖購于北京索萊寶科技有限公司(批號:D8310-100 g);重水(D2O)購自美國蘭迪斯維爾Norell公司。
1.1.3 實驗儀器 腦立體定位儀(深圳瑞沃德生命科技有限公司,型號:68503);SorvallTMLegendTMXT/XF離心機(美國/Thermo Scientific);Morris水迷宮視頻跟蹤分析系統(上海吉量軟件科技有限公司,型號:JLBehvMwMM);Bruker 600 MHz AvanceⅢNMR Spectrometer(德國布魯克公司)。
1.2 實驗方法
1.2.1 地黃飲子水煎劑的制備 按地黃飲子各藥材(熟地黃、巴戟天、山茱萸、石斛、肉蓯蓉、炮附子、五味子、肉桂、茯苓、麥冬、石菖蒲、遠志、薄荷、生姜、大棗質量比12∶9∶9∶9∶9∶6∶6∶6∶6∶6∶6∶6∶3∶3∶3)配比稱取藥材。加入8倍量蒸餾水浸泡30 min,水煎提取25 min,收集水煎液,再用8倍體積水提取20 min,將2次煎煮藥液混合均勻并加熱濃縮,每劑中藥濃縮為含生藥量2 g/mL,4℃冰箱冷藏保存。
1.2.2 分組與給藥 大鼠適應性喂養1周后,按Rand函數隨機分為正常對照組、AD腎虛精虧證組、地黃飲子低劑量組(5.2 g/kg)、地黃飲子中劑量組(10.4g/kg)、地黃飲子高劑量組(20.8 g/kg),每組12只。證候造模第5周開始灌胃給藥,地黃飲子各劑量組給予相應濃度藥液,正常對照組和AD腎虛精虧證模型組灌胃等體積蒸餾水。1次/d,至造模結束為止。
1.2.3 AD腎虛精虧證模型的制備及驗證 采用房事不節法[5-6]和腹腔注射D-半乳糖溶液構建腎虛精虧證模型。除正常對照組外的4組大鼠每天下午與處于動情期的雌性大鼠同籠,次日上午取出雄鼠,下午再投入動情期雌性大鼠籠內,如此輪轉,連續8周。除正常對照組外的4組大鼠每天腹腔注射D-半乳糖(50 mg/kg),連續8周。第8周在腎虛精虧證模型的基礎上采用側腦室注射Aβ1-42制備AD大鼠模型。除正常組外的大鼠固定在腦立體定位儀上,以微量注射器將5 μL預先孵育好的Aβ1-42混懸液緩慢注射到大鼠腦部側腦室區域。注射1周后用Morris水迷宮檢測各組大鼠的學習記憶能力。Morris水迷宮實驗主要包括定位航行和空間探索兩部分。定位航行實驗總共5 d,記錄大鼠每次自入水直至尋找到目標象限平臺并爬上平臺的時間即逃避潛伏期,時長最大值為120 s。第6天進行空間探索實驗,記錄大鼠60 s內穿越平臺的次數以及在目標象限停留的時間。
1.2.4 樣品收集與制備 造模結束后麻醉開腹,腹主動脈取血,在4℃、3000 r/min離心10 min,取上清液后移至EP管中,于-80℃冰箱中保存。取血清樣品450 μL,加入350 μL D2O,斡旋振蕩混勻后低溫離心,取上清液600 μL置于5 mm核磁管中,在Bruker 600 MHz核磁儀上測定,設置主要參數:采樣數據點數(TD)為65 536,掃描次數(NS)為64次,掃描譜寬(SWH)為12 019.23 Hz,傅里葉變換為0.183 Hz,脈沖間隔D1為1s,延遲時間為5.0 s。血清樣品采用CPMG(Carr-Purcell-Meiboom-Grill)脈沖序列,以衰減蛋白質和脂蛋白的寬峰。
1.2.51H-NMR譜圖處理 譜圖處理采用MestReNova 8軟件進行分析。所有譜圖進行手動相位、基線調整。血清譜圖以肌酐的化學位移(δ3.04)為標準進行校正,以0.01對化學位移區間δ0.60~9.00進行分段積分,其中δ4.67~4.89(殘余水峰)不進行積分,并將積分數據進行歸一化,導入Excel中進行下一步多元統計分析。
1.3 統計學方法
將上述處理的積分數據輸入到SIMCA-P+13軟件進行多元統計分析,采用偏最小二乘判別分析(partial least squares discriminant analysis,PLSDA)進行組間比較和模型驗證;采用正交偏最小二乘法判別分析(orthogonal PLS-DA,OPLS-DA)的S-plot圖,尋找對分類貢獻較大的變量,選擇(variable importance in the projection,VIP)>1的變量作為潛在生物標記物的鑒別依據。采用Graphpad Prism 8.0統計,數據采用One-Way ANOVA進行方差分析,兩兩比較采用LSD法,以P<0.05為差異有統計學意義。
2 結果
2.1 行為學結果
定位航行實驗中,隨著大鼠訓練時間的推移,AD腎虛精虧證組逃避潛伏期較正常對照組明顯延長,提示模型大鼠的學習記憶能力存在缺陷;與AD腎虛精虧證組比較,地黃飲子各劑量組的逃避潛伏期均縮短,說明地黃飲子可以改善AD腎虛精虧證大鼠的學習記憶能力(圖1A)。空間探索實驗中,與正常對照組相比,AD腎虛精虧證組大鼠穿越平臺次數明顯減少(P<0.001),經地黃飲子中劑量和高劑量干預后,平臺穿越次數升高(P<0.01和P<0.05)(圖1B);目標象限停留時間AD腎虛精虧證組較正常對照組明顯縮短(P<0.01),經地黃飲子中劑量和高劑量干預后,目標象限停留時間延長(P<0.01和P<0.05)(圖1C)。
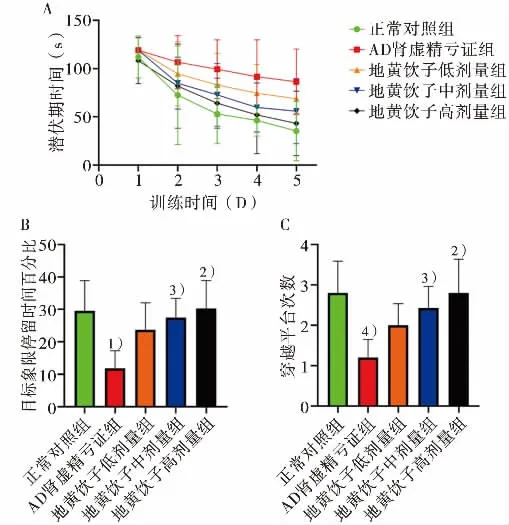
圖1 Morris水迷宮檢測結果
2.2 血清1H-NMR譜圖指認
參考有關文獻[7]及代謝物數據庫HMDB(http://www.hmdb.ca),結合本實驗1H-NMR譜圖對大鼠血清中的代謝產物進行指認,共指認出23種內源性代謝產物,具體結果見圖2和表1。
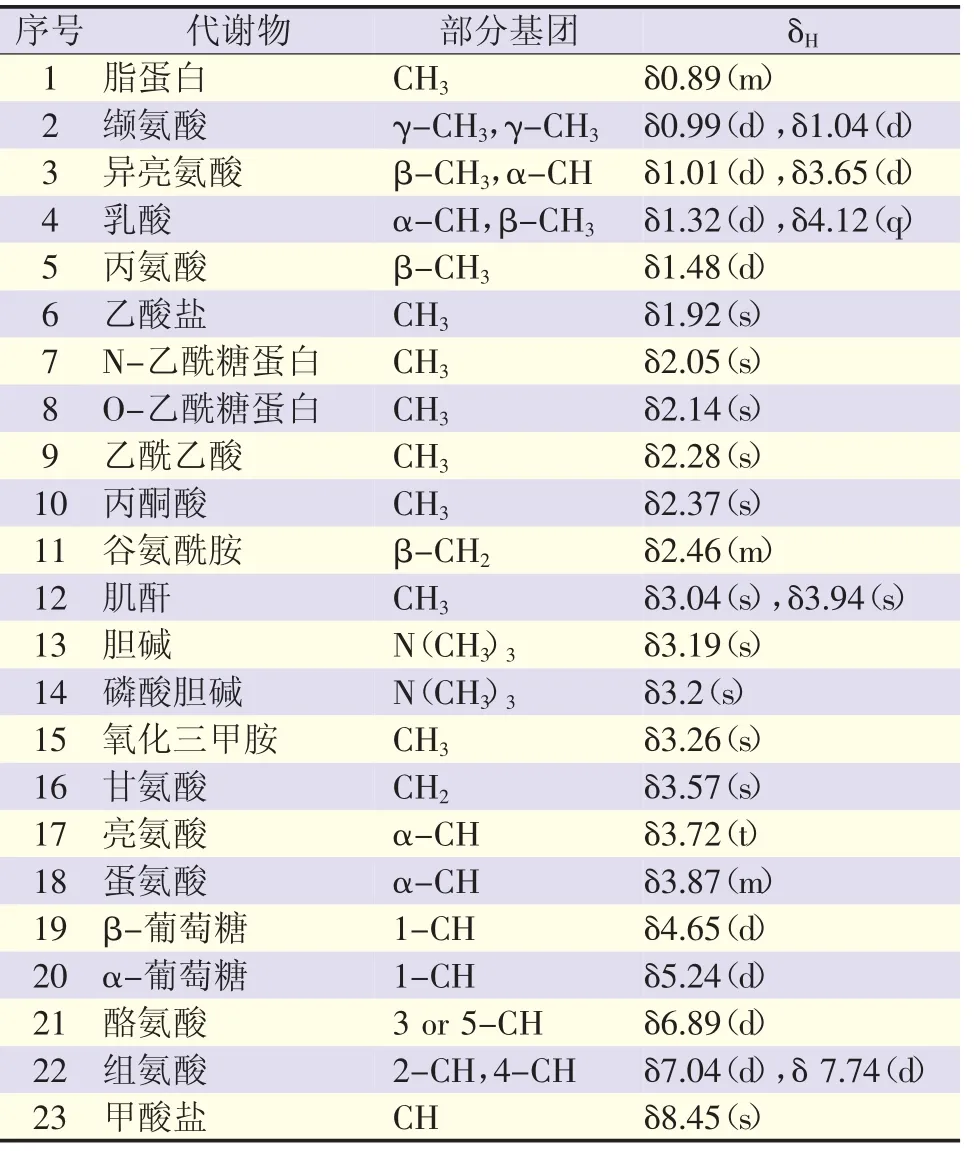
表1 大鼠血清樣本1H-NMR譜圖主要代謝物歸屬
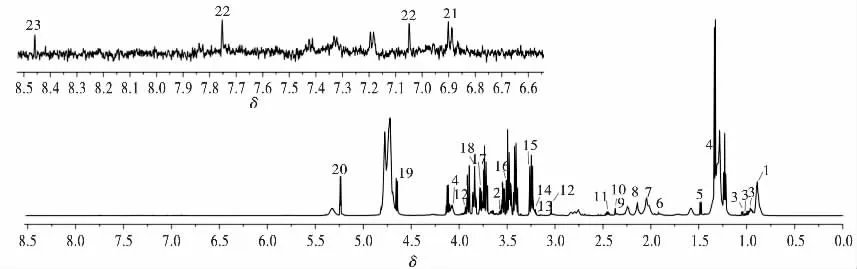
圖2 正常對照組大鼠血清樣本1H-NMR譜圖
2.3 多元統計分析
為進一步分析各組間內源性代謝物的差異,對復雜數據降維處理后進行多元統計分析。采用有監督的PLS-DA方法對各組血清樣本數據進行代謝輪廓分析,結果見圖3A。正常對照組與AD腎虛精虧證組的散點可以完全分開,說明AD腎虛精虧證組大鼠機體的代謝狀態存在明顯的改變。模型驗證結果顯示Q2回歸線與縱軸相交于零點以下,且左側Q2實驗值低于右邊的原始值,表明所建模型可靠性較高(圖3B)。
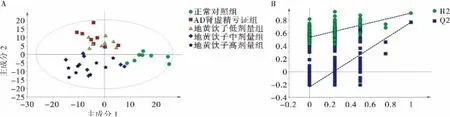
圖3 大鼠血清樣本PLS-DA散點圖(A)和相應的模型驗證圖(B)
2.4 血清差異代謝物的篩選
為進一步確定AD腎虛精虧證造模前后大鼠血清內源性代謝物的差異,采用OPLS-DA方法對樣品進行分析,得到OPLS-DA得分圖(圖4A)和相應的S-plot載荷圖(圖4B)。通過S-plot圖結合VIP值>1以及P<0.05尋找差異代謝物,共得到14個峰面積具有顯著性差異的內源性代謝物。由圖5可知,與正常對照組相比,AD腎虛精虧證組血清中纈氨酸、異亮氨酸、乳酸、丙氨酸、乙酰乙酸、亮氨酸、蛋氨酸含量升高,脂蛋白、N-乙酰糖蛋白、膽堿、甘氨酸、磷酸膽堿、β-葡萄糖、α-葡糖糖含量降低。地黃飲子可以有效調節以上差異代謝物接近正常對照組水平,其中地黃飲子低劑量可以升高脂蛋白的含量,降低異亮氨酸、乙酰乙酸的含量;地黃飲子中劑量可以升高脂蛋白、N-乙酰糖蛋白、磷酸膽堿的含量,降低乳酸、乙酰乙酸、丙氨酸、亮氨酸、蛋氨酸的含量;地黃飲子高劑量可以升高脂蛋白、N-乙酰糖蛋白、膽堿、磷酸膽堿、甘氨酸、β-葡萄糖、α-葡萄糖的含量,降低乳酸、丙氨酸、乙酰乙酸、亮氨酸的含量。以上3組中地黃飲子中劑量組、地黃飲子高劑量組的差異代謝物水平與正常對照組最為接近。

圖4 正常對照組與AD腎虛精虧證組血清樣本OPLS-DA得分圖(A)和相應的S-plot載荷圖(B)
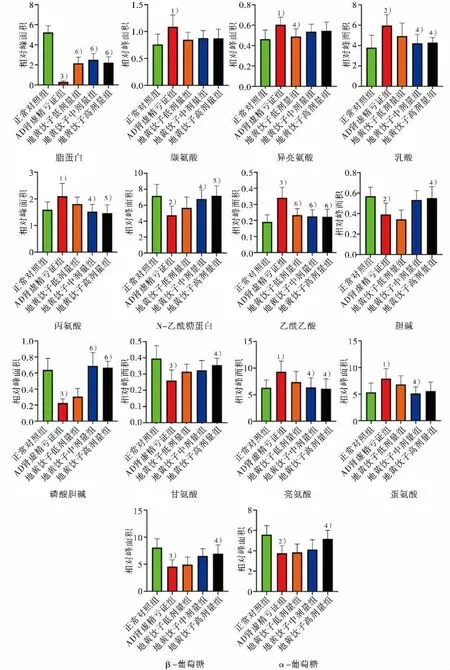
圖5 大鼠血清中差異代謝產物相對峰面積
3 討論
糖酵解是放能反應,它能供給生物體部分能量,尤其是在生理或病理條件下提供生命活動所需的能量。其關鍵代謝物質丙酮酸在乳酸脫氫酶的催化下最終還原為乳酸[8]。當酵解過度會引起乳酸積累過多而引起酸中毒。本研究中AD腎虛精虧組與正常對照組相比乳酸含量升高,提示AD腎虛精虧證狀態下機體存在嚴重的乳酸堆積;經地黃飲子干預后乳酸含量降低,表明地黃飲子可以改善機體的乳酸代謝水平。
乙酰乙酸是脂肪酸在肝臟中不完全氧化的產物,其作為酮體代謝中的一環,是某些器官的主要能源分子[9]。正常情況下,大腦的主要能源是葡萄糖,但在饑餓和患糖尿病時,大腦可有效利用酮體為其供能。長期饑餓時,腦所需能量75%來自乙酰乙酸。本研究中與酮體代謝相關的是乙酰乙酸,其含量的升高提示機體內通過脂肪酸氧化的產能降低[10]。
N-乙酰糖蛋白、α-葡萄糖、β-葡萄糖是機體糖代謝主要物質,在本研究中,AD腎虛精虧證組血清的N-乙酰糖蛋白、β-葡萄糖和α-葡萄糖的含量降低,提示機體內葡萄糖消耗增加,能量代謝障礙嚴重;經地黃飲子干預后三者的含量升高,表明地黃飲子可以通過糾正糖代謝紊亂來改善機體的能量代謝障礙。
纈氨酸、異亮氨酸、亮氨酸三者都為支鏈氨基酸(branched-chain amino acid,BCAA),并且都屬于必需氨基酸,支鏈氨基酸是唯一一類在肝外代謝的氨基酸,主要在骨骼肌,約占骨骸肌蛋白質必需氨基酸的35%,是體內主要供能的氨基酸[11]。研究表明機體BCAA含量的升高可能會通過影響血清素能系統從而增加AD風險[12]。在本研究中,AD腎虛精虧組血清中支鏈氨基酸以及肌肉組織蛋白的主要底物之一的蛋氨酸含量高于正常對照組,表明在腎虛精虧證狀態下機體能量消耗嚴重,能量供應無法滿足體內更旺盛的能量需求從而引起骨骼肌蛋白分解代謝水平的加強[13]。在地黃飲子干預后,亮氨酸和蛋氨酸的含量降低。
丙氨酸在肌肉組織中濃度最高,其作為氨的載體,經血液將氨運送到肝臟后生成丙酮酸,丙酮酸經糖異生途徑合成葡萄糖,為機體提供能源。本研究中AD腎虛精虧組丙氨酸與正常對照組相比呈升高狀態,經地黃飲子干預后含量降低,表明在腎虛狀態下機體的能量消耗巨大。
腎作為先天之本,其主要生理功能為主藏精、主水和主納氣。腎主水是指腎有主持和調節人體水液代謝的功能,其實現又依賴腎的蒸騰氣化作用。病理情況下,腎中精氣虧虛,氣化功能失常,脂質代謝作為機體水液代謝重要的一環同樣也會受到干擾[14]。脂蛋白運輸甘油三酯可用于能量代謝[15]。膽堿和膽堿磷酸是構成細胞膜的主要物質,血清中膽堿和膽堿磷酸的降低,提示細胞膜以及膜性結構如線粒體、內質網的脂質代謝受損[16]。本研究中AD腎虛精虧組中脂蛋白、膽堿和膽堿磷酸的含量呈降低狀態,經地黃飲子干預后又呈升高狀態,表明AD腎虛精虧證與脂質代謝紊亂關系密切。
當人步入老年時,腎精開始逐漸虧虛,腎精不足則髓海不充,于是腦的正常機能也隨之受到影響,輕則表現出記憶力衰退等癥狀,重則發病為AD,故腎虛精虧證是AD的發病基礎。在本研究中,纈氨酸、異亮氨酸、蛋氨酸、亮氨酸、丙氨酸、甘氨酸歸屬于氨基酸代謝,N-乙酰糖蛋白、β-葡萄糖、α-葡糖糖、乳酸歸屬于糖代謝,乙酰乙酸、脂蛋白、膽堿、磷酸膽堿歸屬于脂類代謝,而機體的主要能量來源正是來自糖、脂、蛋白質三類物質的氧化,故以糖、脂類、氨基酸代謝為主的能量代謝紊亂(不足)可能是導致AD腎虛精虧證發生的生物學機制。
腎虛往往提示人體各項臟腑功能減退或衰弱,從而導致體內的各項循環和代謝減慢。形體消瘦、腰酸膝軟和懈惰思臥是AD腎虛精虧證證候表現出的主要癥狀中的一類,本研究表明AD腎虛精虧證存在氨基酸代謝紊亂,本來主要存在于骨骼肌的支鏈氨基酸被大量釋放到血清中為機體供能,在內導致骨骼肌蛋白分解,在外則表現為形體消瘦。腰膝酸軟或與機體內乳酸代謝紊亂堆積于肌肉有關,而懈惰思臥則可能是機體能量供應不足的征兆。
綜上,AD腎虛精虧證組存在糖代謝、氨基酸代謝、脂質代謝三個方面的紊亂,三者均以能量代謝紊亂為主要特征,共同構成AD腎虛精虧證的證候生物學基礎;地黃飲子通過部分改善糖代謝、氨基酸代謝、脂質代謝的紊亂起到對AD腎虛精虧證的治療作用。

