高血壓病人心率與心律失常事件的關系探討
肖錦蓉,王心群,周明生
相關研究顯示,靜息心率與血壓密切相關,靜息心率增快與血壓水平呈正相關[1-2]。多項研究顯示,高心室率與心血管疾病發病率和死亡率顯著相關[3-5]。高心室率作為交感神經過度激活的標志,通過增加管壁剪切力對動脈產生直接的致動脈粥樣硬化作用[6-8],因此,過快的心室率是高血壓發生發展的獨立危險因素。本研究旨在觀察高血壓病人靜息心率與心律失常事件的關系。
1 資料與方法
1.1 研究對象 回顧性分析2018年1月—2019年10月在我院住院治療的318例高血壓病人,其中高血壓病史<5年145例,高血壓病史≥5年173例。納入標準:均符合高血壓診斷標準,未使用降壓藥物情況下,診室收縮壓(systolic blood pressure,SBP)≥140 mmHg(1 mmHg=0.133 kPa)和(或)舒張壓(diastolic blood pressure,DBP)≥90 mmHg[9];年齡18~80歲。排除標準:使用β受體阻滯劑或地爾硫卓等可能影響心率的藥物;有心律失常性心律失常病史;冠狀動脈CT或冠狀動脈造影檢查提示有冠心病;貧血病人;有甲狀腺功能亢進或甲狀腺功能減退病史;電解質紊亂導致的心律失常。本研究經過醫院倫理委員會批準,所有病人均簽署知情同意書。
1.2 觀察指標 統計所有病人臨床資料:包括既往病史、體質指數,均行24 h動態血壓、動態心電圖檢查及超聲心動圖檢查。記錄所有病人24 h SBP及DBP、夜間靜息心率(02:00~06:00,resting heart rate,RHR)、心率變異性(heart rate variability,HRV)指標[全部竇性心搏RR間期標準差(SDNN)、RR間期平均值標準差(SDANN)]、左室射血分數(LVEF),并統計竇性停搏、竇性心律失常、房室傳導阻滯等心律失常事件發生情況。測定所有病人立位及臥位腎素-血管緊張素-醛固酮系統(RAAS)指標[血漿腎素活性(plasma rennin activity,PRA)、血管緊張素(angiotensin,Ang)Ⅱ及醛固酮(aldosterone,ALD)]水平。采用化學免疫發光方法檢測,試劑盒購自上海鈺博生物科技有限公司。PRA檢測試劑盒(批號2018201),ALD檢測試劑盒(批號20171126),AngⅡ檢測試劑盒(批號20160728)。
2 結 果
2.1 高血壓病史≥5年與高血壓病史<5年病人臨床資料比較(見表1)
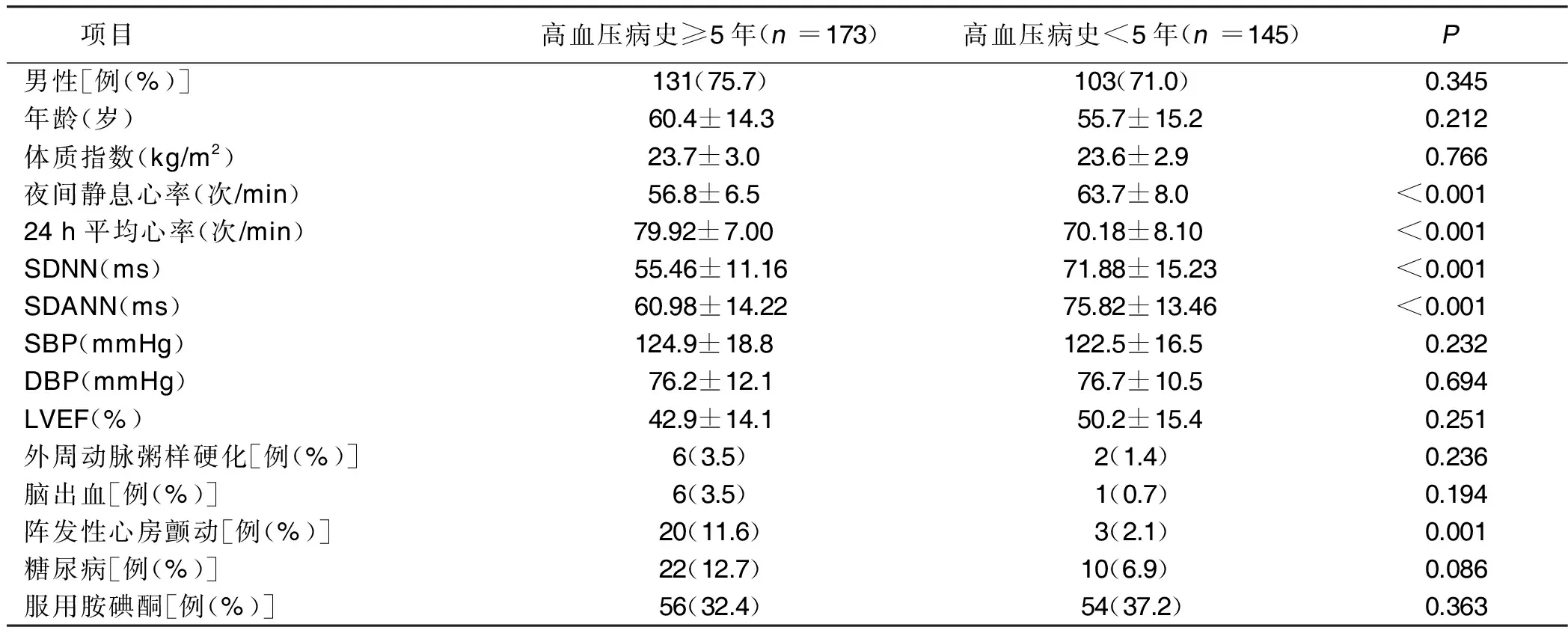
表1 高血壓病史≥5年與高血壓病史<5年病人臨床資料比較
2.2 高血壓病史≥5年與高血壓病史<5年病人心律失常事件發生率比較 所有高血壓病人發生心率過緩事件84例,發生率為26.4%,其中高血壓病史≥5年病人心律失常事件發生率為32.9%,明顯高于高血壓病史<5年病人的18.6%,差異有統計學意義(P<0.01)。高血壓病史≥5年病人竇性心律失常和竇性停搏發生率高于高血壓病史<5年病人,差異有統計學意義(P<0.05)。詳見表2。

表2 高血壓病史≥5年與高血壓病史<5年病人心律失常事件發生率比較 單位:例(%)
2.3 心律失常事件的影響因素分析 以出現心律失常事件為因變量,以年齡、性別、血壓水平(24 h SBP、24 h DBP)、高血壓病史、SDNN、SADNN、24 h平均心率、夜間靜息心率、陣發性心房顫動等為自變量進行多元線性回歸分析,分析高血壓病人中心律失常的影響因素。結果顯示:年齡>75歲、男性、24 h SBP>140 mmHg、24 h DBP>90 mmHg、高血壓病史≥5年、SDNN<50 ms、SADNN<50 ms、24 h平均心率>70次/min、夜間靜息心率<50次/min、陣發性心房顫動是高血壓病人發生心律失常事件的獨立危險因素。詳見表3。

表3 心律失常事件發生的影響因素Logistic回歸分析
2.4 心律失常組與非心律失常組RAAS指標比較 心律失常組立位或臥位血漿PRA、AngⅡ及ALD水平均高于非心律失常組,差異有統計學意義(P<0.01),提示心律失常組RAAS活性更高。詳見表4。
表4 心律失常組與非心律失常組RAAS指標比較(±s)
2.5 靜息心率與血漿PRA、AngⅡ、ALD水平的相關性分析 血漿PRA、AngⅡ、ALD水平均與靜息心率呈正相關。提示靜息心率水平可一定程度反映高血壓病人RAAS活性。詳見表5。
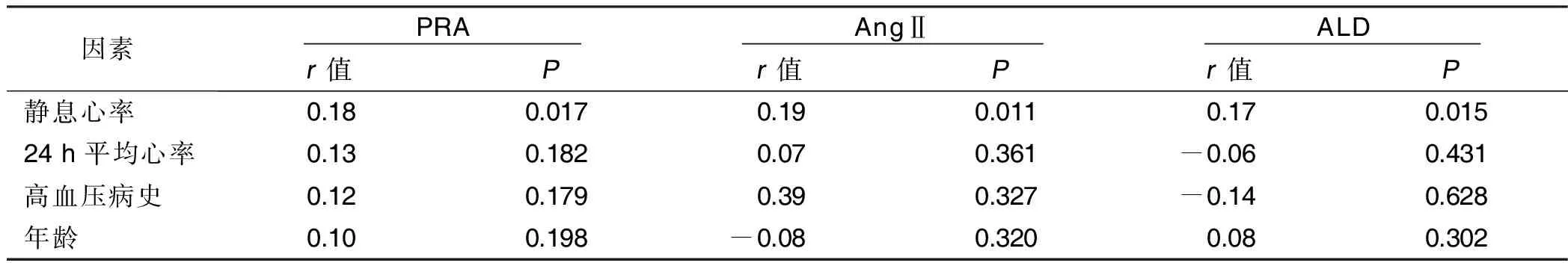
表5 靜息心率與RAAS指標的相關性分析
3 討 論
本研究結果顯示:高血壓病人病史越長,24 h平均心率越高,夜間靜息心率水平越低;高血壓病人病史越長,HRV指標如SDNN、SADNN降低;隨著高血壓病史延長,陣發性心房顫動發生率升高,心律失常事件發生率升高;年齡>75歲、男性、24 h SBP>140 mmHg、24 h DBP>90 mmHg、高血壓病史≥5年、SDNN<50 ms、SADNN<50 ms、24 h平均心率>70次/min、夜間靜息心率減慢<50次/min、陣發性心房顫動是高血壓病人發生心律失常事件的獨立危險因素。本研究中,高血壓病人心律失常事件發生率為26.4%,且高血壓病史越長,心律失常發生率越高,高血壓≥5年病人心律失常事件發生率為32.9%,遠高于普通人群中心律失常事件發生率[10]。由此可見,高血壓是心律失常疾病病人的高危人群。進一步研究發現,高血壓病史越長,24 h平均心率越高。相關研究顯示,心率升高與高血壓所致交感神經的過度激活有關[11-12],表明高血壓病史越長,交感神經興奮性越強。高血壓病史越長,夜間靜息心率水平越低,HRV指標降低。夜間靜息心率可一定程度反映迷走神經活動,夜間靜息心率降低反映迷走神經系統過度激活[13-14]。HRV降低提示自主神經系統功能失衡[15]。高血壓病人病史越長,交感神經和迷走神經過度激活,且存在自主神經系統調節功能障礙,與相關研究結果[16-17]一致。高血壓病史≥5年病人陣發性心房顫動和心律失常事件發生率升高,分析原因可能是由于高血壓發生發展導致自主神經系統的功能失調,作用于心臟傳導系統,最終導致心律失常事件發生。
自主神經系統對心臟傳導系統的調節主要通過釋放神經遞質與相應的受體結合后,調節竇房結、房室結、浦肯野纖維或心肌細胞膜離子通道的通透性,從而影響心臟傳導系統的自律性和傳導[18-19]。高血壓病人由于RAAS過度激活[20]、自主神經功能失調[21],引起心臟傳導系統離子通道發生重構,導致緩慢性心律失常。本研究結果顯示,心律失常病人RAAS相關指標PRA、AngⅡ及ALD升高,提示合并心律失常的高血壓病人體內RAAS活性更高。結合靜息心率與上述指標呈正相關,推測高血壓病人RAAS的過度激活可能是導致靜息心率升高的機制,作用于心臟傳導系統,最終發生心律失常事件。
本研究結果顯示,所有心律失常事件中,高血壓病史≥5年病人竇性心律失常和竇性停搏發生率較高。提示高血壓時間長,對竇房結影響較大,對房室結影響相對較小。結合以往研究,竇房結主要受交感神經支配,房室結主要由迷走神經支配,因此,高血壓病人交感神經過度激活可能顯著,對竇房結的抑制作用更強,高血壓病人竇性停搏發生率更高。
本研究存在一些不足之處:樣本量有限,相關結論需大樣本量研究證實;病人未按照高血壓分級進行分層,未對不同高血壓分級相應指標的影響進行分析。因此,本研究關注高血壓病史,以病程5年為節點進行分析,今后擴大樣本量對不同分級的高血壓相關指標進行分析。
綜上所述,高血壓病人心律失常事件發生率高于普通人群。高血壓病人病史越長,心律失常事件發生率越高,夜間靜息心率越低,且夜間靜息心率降低與心律失常事件相關。提示可通過夜間靜息心率評估高血壓病人心律失常事件的發生,盡早干預或調整藥物治療,這部分病人應避免使用β受體阻滯劑等影響心率的藥物。

