六方氮化硼納米片改進QuEChERS法凈化草莓中10種農藥殘留
趙燕芳,李慧娟,謝含儀,陳相峰
(齊魯工業大學(山東省科學院)山東省分析測試中心,山東濟南 250014)
草莓是一種小型水果,具有吸引人的顏色和獨特的風味,富含有益于人體健康的化合物,并且熱量值相對較低,因而成為最受人們歡迎的水果之一[1]。草莓可以以新鮮、冷凍或加工等形式存儲、食用,因為含有許多重要的膳食成分,包括礦物質、纖維,以及豐富的植物素(鞣花酸、花青素、槲皮素和兒茶素)和維生素(抗壞血酸和葉酸),所以被列為多酚和抗氧化能力的膳食來源之一[2]。為了提高草莓產量和質量,農藥在草莓生長過程中起著不可替代的作用;然而,不規范使用農藥會導致草莓農藥殘留甚至超標,嚴重影響環境安全、出口貿易以及消費者身體健康[3-4],因此,草莓中農藥殘留的檢測是一個非常重要的課題。
常用于農藥殘留檢測的技術包括氣相色譜法[5]、液相色譜法[6]、氣相色譜質譜法[7]和液相色譜質譜法[8]。樣品前處理是農藥殘留檢測的關鍵環節。為了避免復雜基質的干擾,樣品前處理的關鍵步驟是樣品提取液的凈化。由于植物樣品中含有大量的色素、氨基酸、生物堿等成分,因此在提取過程中這些物質會隨著目標有害物共提取出來[9]。該類共提取雜質會給檢測過程帶來諸多問題,如污染色譜柱、離子源以及干擾目標物的檢測結果,造成假陽性等問題。最常用的提取技術有固相萃取(SPE)法[10]、液-液萃取法[11]、滲透凝膠色譜[12]和QuEChERS(快速-簡單-廉價-高效-耐用-安全)法[13]等。傳統的固相萃取法的選擇性不強,無法建立綜合的多殘留分析方法。液-液萃取法基于相似相溶原理,不適于性質差異較大的多種殘留的凈化。常規的凝膠滲透色譜儀器昂貴,且耗時長,消耗有機試劑。使用固相萃取法和離線滲透凝膠色譜法時,存在工作效率低和操作繁瑣等問題,因此QuEChERS法以操作簡便和快速的特點,成為最常用的前處理方法之一。QuEChERS法通常采用N-丙基乙二胺(PSA)、十八烷基硅烷鍵合硅膠(C18)、石墨化碳黑等作為固相吸附提取液中的雜質,在去除色素及中弱極性干擾物時存在凈化效果不足問題,因此需要開發具有吸附多種雜質新型固定相,實現提取液的凈化。
六方氮化硼(hexagonal boron nitride, h-BN)納米材料以等數目的氮原子和硼原子通過sp2雜化方式結合成六元環,每個B、N原子提供一個p軌道形成共軛π鍵[14],具有良好的生物相容性和吸附性能。Jia等[15]制備了大比表面積(大于1 400 m2/g)的多孔h-BN納米材料,用于吸附水中的多種有機物,發現該材料能吸附其自身質量33倍的污染物。Wang等[16]將h-BN作為基質用于基質輔助激光解析離子化質譜法(MALDI-TOF)分析小分子,較傳統基質具有較小的背景干擾,提高了靈敏度。Furuhashi等[17]發現h-BN保留的磷酸化肽段的數量為C18和石墨化碳黑之和,可用來吸附化學性質較寬范圍的肽段。h-BN納米材料的獨特性質已經引起了國內外學者的廣泛關注,但是尚未見其用于樣品基質凈化的應用。
本文中首次利用一種大比表面積的二維h-BN納米片作為吸附固定相,采用分散固相萃取技術改進QuEChERS法,建立一種草莓樣品中多種農藥殘留的快速、簡便、有效前處理方法,進一步結合高效液相色譜串聯質譜法開發10種農藥殘留的分析方法。
1 實驗
1.1 儀器與試劑
主要儀器包括:高效液相色譜串聯質譜儀,Triple QuadTM 5500 AB SCIEX型,美國AB SCIEX有限公司;管式爐,OTF-1200X型,安徽合肥科晶材料科技有限公司;烘箱,DGX-9053B型,上海南榮實驗設備有限公司;恒溫水浴鍋,6HZ-A型,上海博迅實業有限公司醫療設備廠;離心機,MULTIFUGE XIR型,美國Thermo Scientific公司;真空干燥箱,DZF-6094型,上海一恒科學儀器有限公司。
主要試劑包括:甲醇(CH3OH,CAS 67-56-1)、乙腈(CH3CN,CAS 75-05-8),色譜純,美國新天地有限公司;氯化鈉(NaCl,CAS 7647-14-5),優級純,國藥集團化學試劑有限公司;無水硫酸鈉(Na2SO4,CAS 7487-88-9),分析純,國藥集團化學試劑有限公司;有機污染物相關化學品標準物質,純度大于95%(質量分數),德國Dr公司。單標標準溶液的儲備液質量濃度為10 mg/L。
1.2 儀器條件
色譜條件:色譜柱,Thermo Fisher Scientific C18型, 粒徑為2.6 μm, 2.1 mm×100 mm(內徑×長度); 流動相為甲酸銨(濃度為10 mmol/L)和乙腈,洗脫模式采用線性梯度洗脫。洗脫條件見表1,洗脫速率為0.3 mL/min,進樣體積為5 μL,色譜柱溫度為30 ℃,樣品盤溫度為10 ℃。

表1 高效液相色譜洗脫條件
質譜條件: 離子源為電噴霧(ESI)離子源,使用正離子掃描模式。電噴霧電壓為5 500 V,離子源溫度為500 ℃。氣簾氣壓力為138 kPa,碰撞氣壓力為50 kPa,霧化氣壓力為345 kPa,輔助氣壓力為345 kPa。入口電壓為10 V,碰撞室出口電壓為13 V。監測模式為多反應監測(MRM)。
1.3 h-BN納米片的制備
h-BN納米片制備方法依據文獻[18]并在其基礎上進行改進,步驟如下:在容積為50 mL的離心管中加入甲醇(10 mL)和水(10 mL)的混合液,然后分別加入物質的量分別為0.15、0.05 mol的尿素、硼酸,上述混合液在室溫下水浴振蕩1 h,然后在50 ℃烘箱中加熱12 h,將得到的白色固體轉移到石英舟中在管式爐中煅燒,氣氛為氮氣,煅燒溫度為900 ℃,保溫時間為2 h,得到的白色粉末用無水乙醇離心洗滌3次,在溫度為70 ℃時真空干燥2 h。
1.4 樣品前處理
1)草莓樣品處理。將草莓樣品洗干凈,取可食用部分置于攪碎機里攪碎,勻漿,裝入潔凈的離心管內,密封并標明標記。將試樣于-20 ℃冷凍保存。
2)標準溶液配制。稱取10 g勻漿后的空白草莓漿,置于50 mL離心管中,加入一定量的農藥殘留標準溶液,渦旋1 min,加入10 mL乙腈,渦旋1 min,再加入2 g氯化鈉和4 g無水硫酸鎂,離心分離,取上清液置于50 mL離心管中,加入4 mg h-BN納米片,渦旋1 min,在轉速為8 000 r/min時離心分離,上清液過孔徑為0.22 μm的濾膜后上機檢測。
3)加標回收率實驗。稱取10 g勻漿后的空白基質樣品,置于50 mL離心管中,加入一定量的農藥殘留標準溶液,渦旋1 min,加入10 mL乙腈,渦旋1 min,再加入2 g氯化鈉和4 g無水硫酸鎂,離心分離,取上清液置于50 mL離心管中,加入4 mg h-BN納米片,渦旋1 min,在轉速8 000 r/min下離心分離,上清液過孔徑為0.22 μm的濾膜后上機檢測。
2 結果與討論
2.1 h-BN納米片的表征
h-BN納米片的微觀形貌圖像及吸附-脫附等溫曲線見圖1。由圖1(a)、(b)可以看出,h-BN納米片具有二維的類似石墨烯的形貌; 由圖1(c)可以推算出h-BN納米片的比表面積很大,數值約為2 000 m2/g。h-BN納米片這種類石墨烯的結構及大的比表面積有助于對檢測樣品中雜質的吸附和對復雜基質凈化。

(a)掃描電子顯微鏡圖像

(b)透射電子顯微鏡圖像
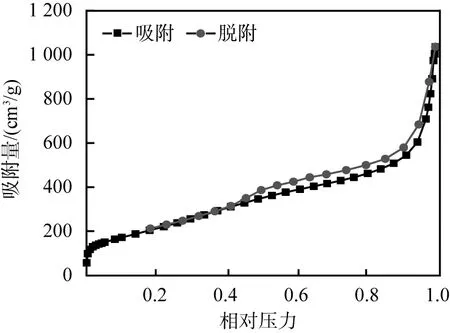
(c)吸附-脫附等溫曲線圖1 六方氮化硼納米片的微觀形貌圖像及 吸附-脫附等溫曲線
2.2 儀器條件的優化
2.2.1 色譜條件的優化
在液相色譜分析中,流動相的組成是一個重要因素,不僅影響目標物的色譜峰型和分離效果,也會影響檢測器的信號響應和檢測靈敏度。色譜優化過程以信號響應強度、峰型和干擾程度作為評價效果的依據。選用濃度為10 mmol/L的甲酸銨和乙腈作為流動相梯度洗脫,得到草莓樣品中10種農藥殘留化合物的保留時間色譜圖,如圖2所示。

圖2 草莓樣品中10種農藥殘留的保留時間色譜圖
2.2.2 質譜條件優化
優化三重四極桿質譜是一項艱巨的任務,原因是每個目標化合物都需要特定的實驗條件進行分析。為了找出保留時間和分析物峰之間的最佳分辨率,使用混合標準溶液在全掃描模式下進行初步實驗。串聯質譜探測器具有較高的選擇性和靈敏度,重點考慮的是母離子、子離子的選擇,以及最佳反應的碰撞能量的優化。質譜參數選擇首先對化合物進行全面掃描,然后選擇每個分析物的母離子,繼而優化碰撞能量電壓來生成產物離子。進一步優化每個化合物在MRM獲取過程中的特征離子躍遷和碰撞能量,進行定量分析。各化合物參考保留時間、監測離子對(同一化合物的母離子對應不同的子離子)、去簇電壓(DP)、碰撞能量電壓(CE)參考值見表2。
2.3 凈化條件優化
2.3.1 h-BN納米片用量
為了得到較大的回收率及可以重現的色譜峰強度,去除基質中的干擾物質是必要的。本文中提出用QuEChERS法凈化草莓樣品中基質干擾物,無水硫酸鎂用于去除基質中的水分,h-BN納米片用于去除其他干擾物質,如脂肪酸、色素和其他基質化合物。研究發現,h-BN納米片可以作為QuEChERS法中的替代材料,用于分散固相萃取基質中干擾物來凈化草莓樣品。圖3所示為h-BN納米片用量條件優化結果。從圖中可以看出:少量的h-BN納米片 (小于4 mg)不能獲得最大回收率,原因可能是吸附劑的用量較少,不能很好地凈化樣品基質;當h-BN納米片用量為4 mg時,回收率達到最大值,并且經過處理的最終樣品顏色透明;當h-BN納米片用量過多時,可能導致吸附大多數加標的農藥。本文中選用4 mg為h-BN納米片的最佳用量。
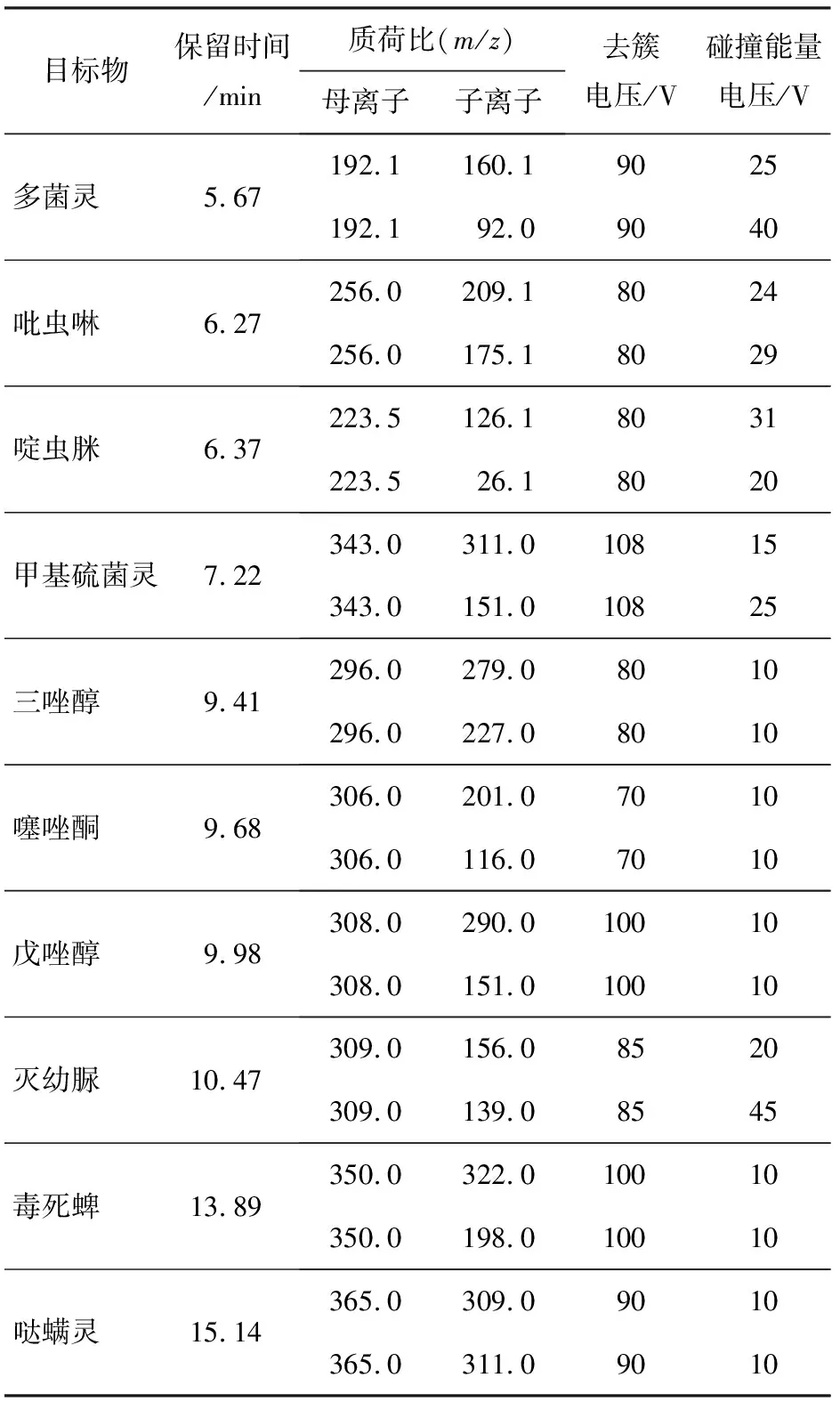
表2 草莓樣品中10種農藥殘留的保留時間、監測離子對、去簇電壓、碰撞電壓參數
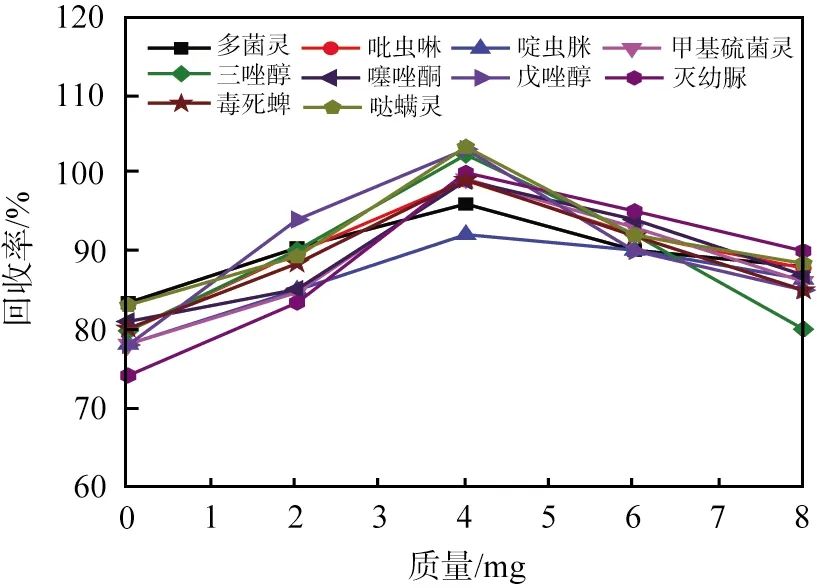
圖3 10種農藥殘留回收率與六方氮化硼納米片用量的關系
2.3.2 凈化時間
凈化時間也是影響凈化效果的一個重要因素。凈化時間為20~100 s時對不同目標物(質量比為100 mg/kg)回收率的影響見圖4。由圖可以看出:凈化初始時目標物的回收率較小,原因是凈化時間過短,不能使h-BN納米片充分凈化草莓樣品基質,干擾了目標物的測定。凈化時間為60 s時,凈化劑充分發揮了凈化作用,目標物回收率最大。隨著凈化時間繼續增加,目標物的回收率減小,原因可能是凈化時間過長,h-BN納米片對目標物有部分吸附。實驗最終選定60 s作為最佳凈化時間。
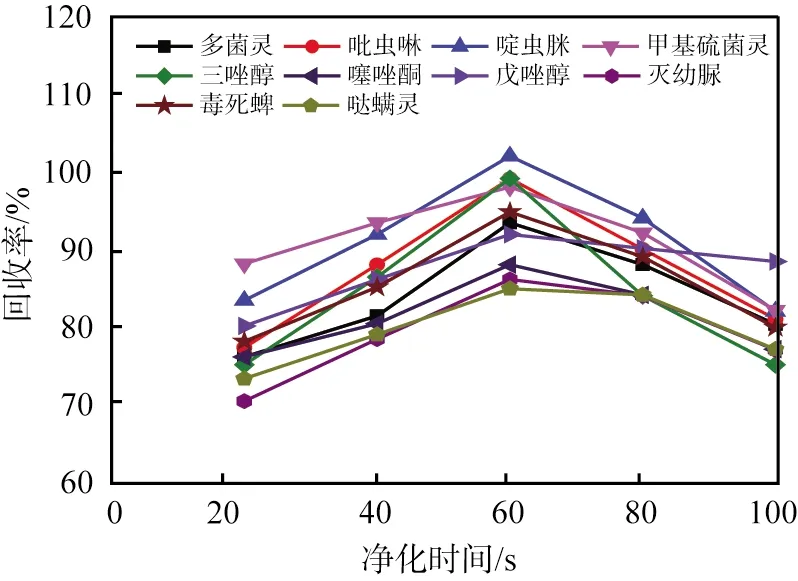
圖4 10種農藥殘留回收率與凈化時間的關系
2.4 方法建立
草莓中10種農藥殘留的分析結果見表3。從表中可以看出,在最優的實驗條件下,10種農殘質量比線性范圍均為0.1~500 mg/kg,相關系數r為0.999 2~0.999 8,方法檢出限(信噪比為3)為0.000 5~0.01 mg/kg,定量限(信噪比為10)為0.002~0.003 mg/kg。采用質量比為100 mg/kg的10種農藥殘留進行重復性實驗,日內相對標準偏差為2.56%~5.98%(n=5,n為測定次數),日間相對標準偏差為2.24%~5.32%(n=5),不同批次合成的h-BN納米片的重復性相對標準偏差為2.25%~6.25%(n=5)。上述結果表明,h-BN納米片可以改進QuEChERS法凈化草莓樣品中農藥殘留污染物。
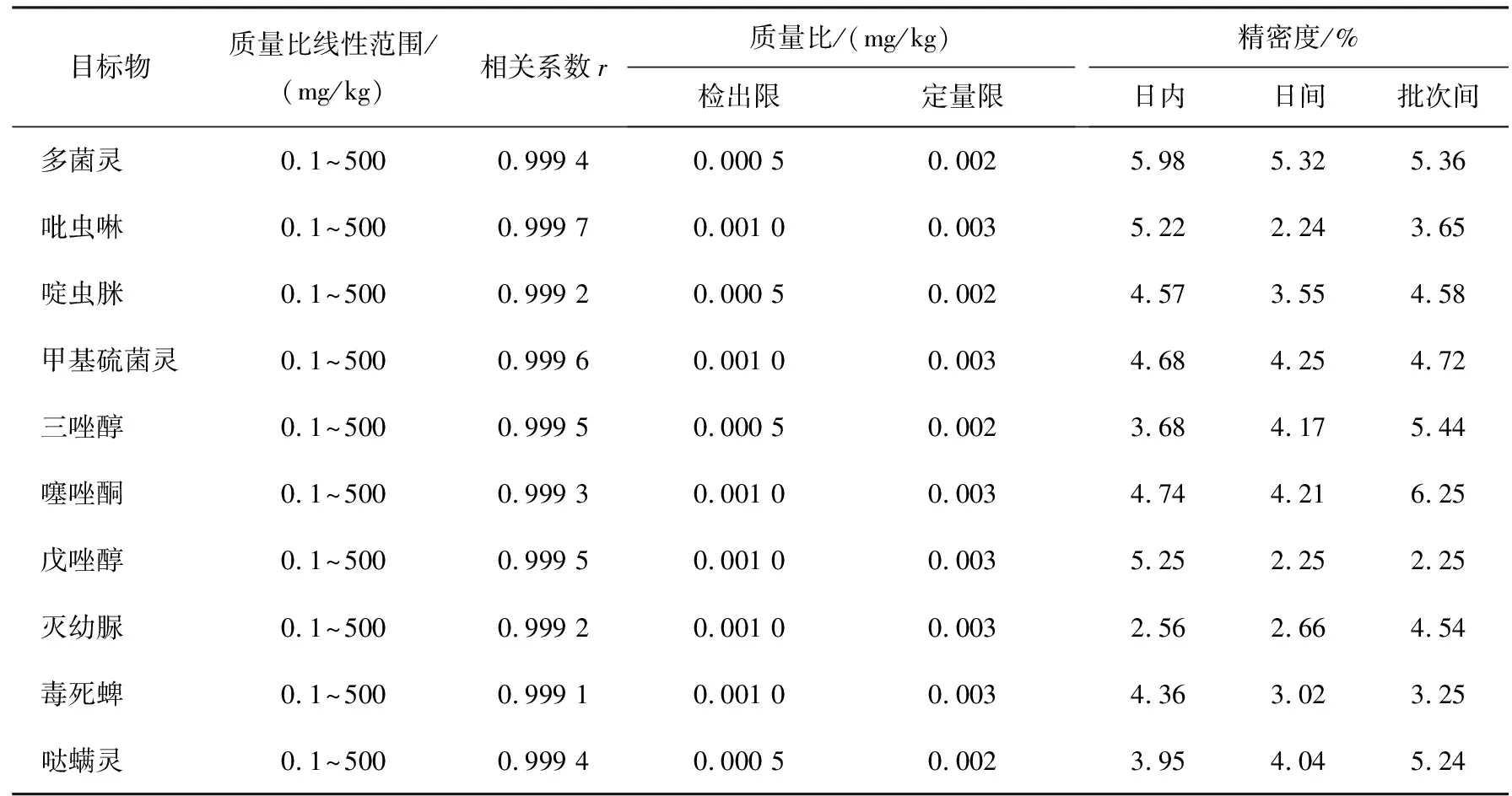
表3 草莓中10種農藥殘留的分析結果
2.5 樣品分析
將基于h-BN納米片改進的QuEChERS法用于草莓樣品中10種農藥殘留污染物的凈化,在草莓樣品中加入農藥殘留標準物質的量作為加標量(質量比分別為1、10、50 mg/kg),對于加標樣品也進行同樣的前處理。進一步結合高效液相色譜串聯質譜儀分析實際樣品中痕量農藥殘留污染物,結果見表4。由表可以看出,樣品的回收率為86.03%~106.3%,表明該方法結果穩定、可靠,可應用于草莓實際樣品中痕量農藥殘留的分析。
3 結論
本文中首次利用h-BN納米片改進的QuEChERS法,建立了一種快速、靈敏的草莓樣品中多種農藥殘留分析方法,得到以下主要結論:
1)h-BN納米片用于分散固相萃取法,可以有效凈化基質中農藥提取物。萃取后的凈化過程主要是去除基質中的干擾物質,而不是提取和分離分析物。
2)h-BN納米片可以快速、有效地吸附樣品中色素等干擾物,凈化基質,并結合高效液相色譜串聯質譜法可以分析樣品中痕量農藥殘留。
3)該方法的線性范圍、精密度、回收率均符合農藥分析的要求,結果證實了該方法的可行性,可用于草莓產品中農藥殘留的常規檢測和監測,為痕量農藥分析和樣品清理找到有效途徑,有望廣泛應用于各種水果中微量農藥的監測。
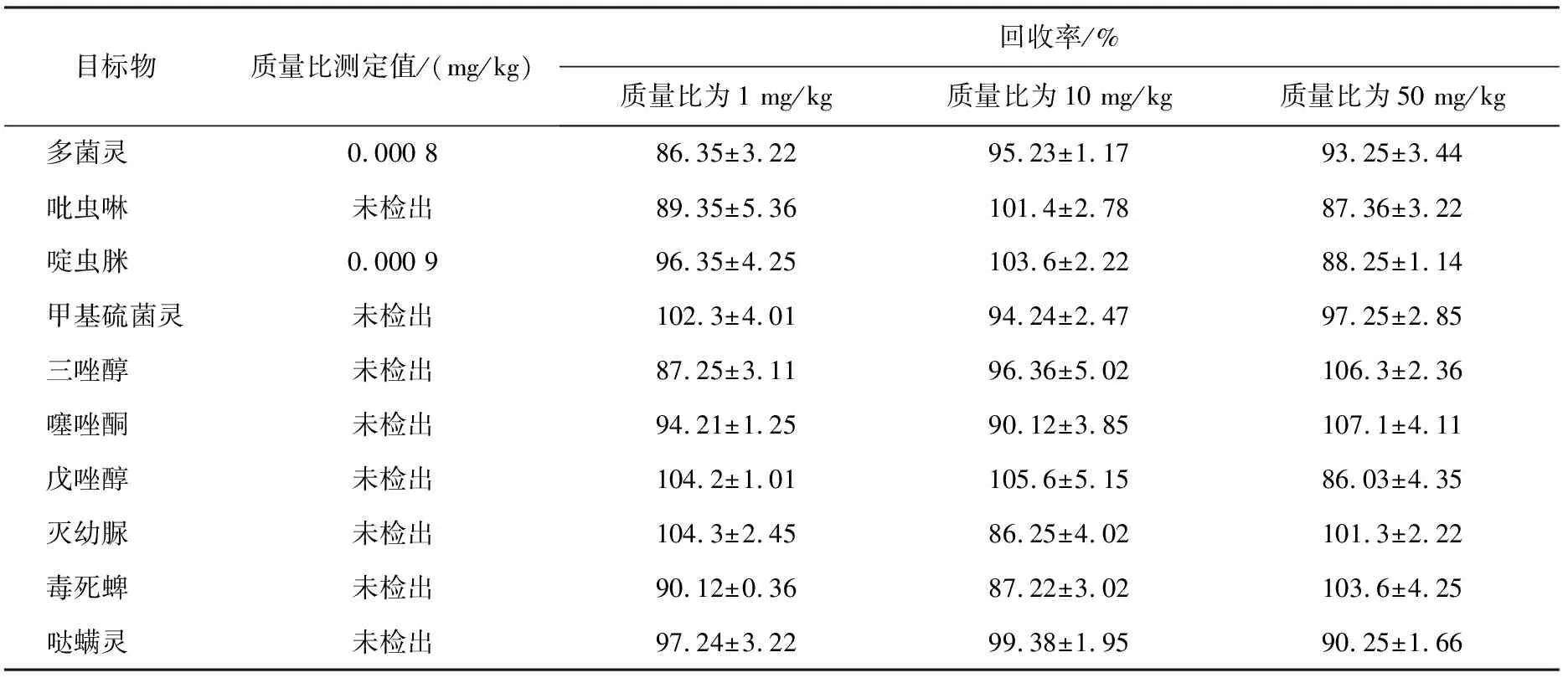
表4 草莓樣品中10種農藥殘留污染物不同加標量(質量比)回收率結果

