瑪納斯湖鹵水自然蒸發析鹽規律及硼、鋰富集規律研究
邊紹菊,許乃才,張永興,李 武
(1.青海師范大學化學化工學院,青海西寧810016;2.中國地質科學院鄭州礦產綜合利用研究所;3.中國科學院青海鹽湖研究所)
瑪納斯鹽湖[1]位于新疆維吾爾自治區準噶爾盆地西部塔城地區和布克賽爾蒙古自治縣和什托洛蓋鎮境內。阿勒泰-奎屯217國道及和什托洛蓋-克拉瑪依公路均從湖區西側經過,交通方便。湖盆深居準噶爾盆地腹地,古爾班通古特沙漠之中,多風沙,少降水,為溫帶大陸性干旱-半干旱氣候。
瑪納斯河水已不能入湖,主要靠大氣降水和地下水補給。晶間鹵水富含于石鹽和芒硝層中。瑪納斯湖鹵水主要是晶間鹵水,僅在雨季湖面才有少量湖表鹵水。晶間鹵水相對密度為1.241、pH為6.87、礦化度為328.44 g/L,鹽湖水化學類型為硫酸鹽型硫酸鎂亞型。瑪納斯湖石鹽生產始于20世紀50年代,曾建立和豐(瑪納斯)鹽場開采表層石鹽。后來利用溝渠生產再生鹽,并開始利用鹽田生產灘曬鹽,年產原鹽10余萬t。主要產品有原鹽、再生鹽、粉精鹽、加碘鹽等系列品種。自2005年開始新疆新雅泰化工有限公司以瑪納斯湖的晶間鹵水為原料,生產硫酸鉀和硫酸鉀鎂肥。
黃雪莉等[2]曾對瑪納斯湖水進行了25℃等溫蒸發及室溫蒸發實驗,實驗給出了瑪納斯湖鹵水蒸發析鹽規律,以及自然蒸發析出鉀鎂混鹽的結論,但未提到硼、鋰等資源的含量以及在蒸發過程中的分布和富集規律。
鹵水蒸發結晶順序與析鹽規律為鹵水開發的工藝設計提供最基礎和直接的依據,同時為了對鹵水資源進行全面的利用,對硼、鋰等元素的分布和富集規律的了解也是必不可少的。因此,對鹵水進行蒸發實驗獲得析鹽規律和硼、鋰等元素的分布規律是非常必要的[3-5]。
水鹽體系相圖是鹽湖鹵水資源加工利用過程的重要依據,是整個工藝設計與計算的基礎與理論依據。實際過程中很難找到完全適合于工藝生產的水鹽體系相圖數據,更多的是以相似的水鹽體系相圖為工藝生產設計和指導的依據,這樣往往會給實際生產控制過程帶來偏差,更有甚者會嚴重影響到生產的正常進行。解決的最佳辦法是針對每一種鹽湖鹵水開展鹵水蒸發結晶析鹽實驗[6-7],依據實驗結果確定生產工藝技術,然而盲目的蒸發實驗耗時耗力,很難通過一兩次實驗摸準分離節點。
ISLEC(Integrated of Solution Equilibrium Calculator)是一個基于相圖方法和Pitzer-Simonson-Clegg超自由能模型開發的鹵水-鹽礦平衡模擬模型[8-9],可應用于包含Ca-Na-K-Mg-Li-Cl-SO4-H2O多元體系多溫范圍的相平衡模擬計算。此模型雖然不像相圖一樣可視直觀,但能進行快速計算,以其計算的節點為依據進行實驗可以極大地縮短實驗時間。本文引用此軟件聯網版進行鹵水常溫蒸發模擬計算,并以模擬結果指導蒸發實驗的進行,得出瑪納斯湖水自然蒸發時的結晶路線和析鹽規律。
1 實驗
1.1 原料和分析方法
本文所用鹵水為2015年11月取于瑪納斯湖的晶間鹵水。化學組成見表1中L0,表中LH數據為文獻[2]報道的瑪納斯鹵水組成,從表中數據可知,L0鹵水除NaCl外,其他組成含量均高于文獻報道的組成,但各組成大概是文獻的3倍,并且組成類似。
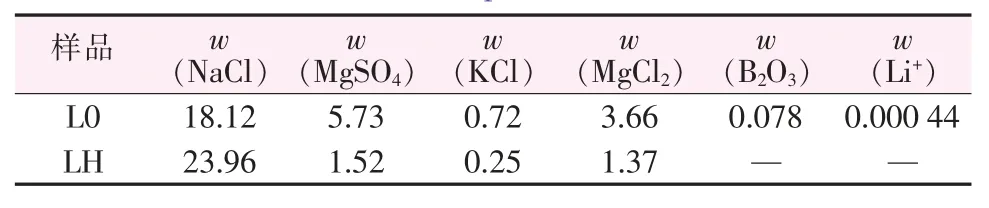
表1 瑪納斯湖鹵水組成Table 1 Chemical composition of Manasi brine %
所有樣品中常規離子包括K+、Mg2+、Ca2+、Cl-、SO42-、B2O3采用化學分析方法分析,Li+采用原子吸收光譜分析。K+采用四苯硼鈉-季銨鹽反滴定法;Mg2+、Ca2+采用EDTA容量法;Cl-采用汞量法;SO42-采用BaCl2沉淀質量法;B2O3采用甘露醇法;Na+采用電荷平衡法計算,未列于表中。
1.2 研究方法
本研究用水為瑪納斯湖晶間鹵水,起始鹵水標記為L0。文章中涉及的模擬計算采用ISLEC軟件聯網版進行。模擬采用體系為Na-K-Mg-Li-Cl-SO4-H2O。
自然蒸發于青海西寧室內進行,取9.000 kg瑪納斯湖鹵水(L0)置于塑料箱,室內自然蒸發,采取電風扇模擬自然風,其間室溫變化為17.5~21.5℃。根據ISLEC計算結果分階段分離取樣,固液分離采取真空泵抽濾,分離所得到的固液相均進行化學分析,同時送粉末進行XRD檢測確定物相組成,并對固相分析結果進行配礦。
1.3 瑪納斯湖鹵水ISLEC計算及蒸發實驗
1.3.1 ISLEC模擬計算瑪納斯湖鹵水20℃自然蒸發過程
以L0為起始鹵水進行計算,每一種新鹽飽和時作為分段節點,共計3段:L0到L1C(瀉利鹽飽和)為石鹽段;L1C到L2C(光鹵石飽和)為瀉利鹽段;L2C到L3C(水氯鎂石飽和)為鉀混鹽段。表2為模擬計算各階段液相組成,表3是模擬計算各階段析出鹽的組成。
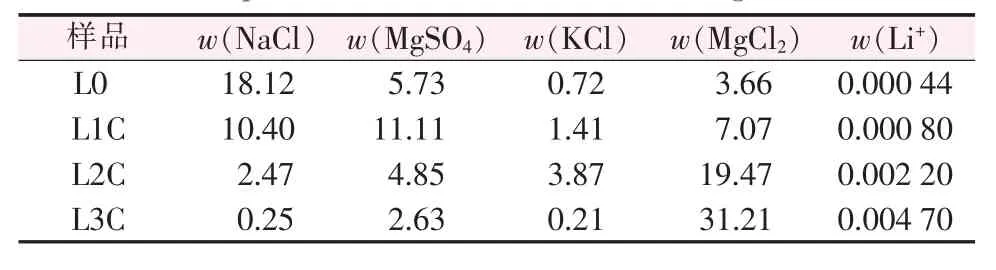
表2 ISLEC計算瑪納斯鹵水20℃蒸發過程液相組成Table 2 Chemical composition of Manasi brine during the evaporation at 20℃calculated through ISLEC %
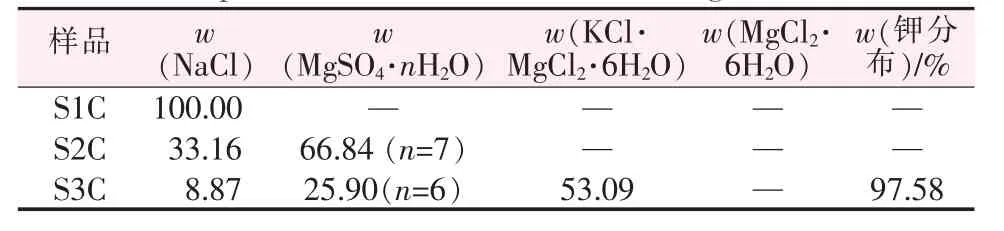
表3 ISLEC計算瑪納斯鹵水20℃蒸發過程析出鹽種類及含量Table 3 Chemical composition of the solids during the evaporation at 20℃calculated through ISLEC %
1.3.2 瑪納斯湖鹵水自然蒸發實驗
表4 列出了瑪納斯湖晶間鹵水室內自然蒸發實驗中每次分離液相的化學分析組成。表5為分離固相的化學分析組成及XRD物相鑒定結果,以鹽礦組成形式和夾帶母液的含量表示。
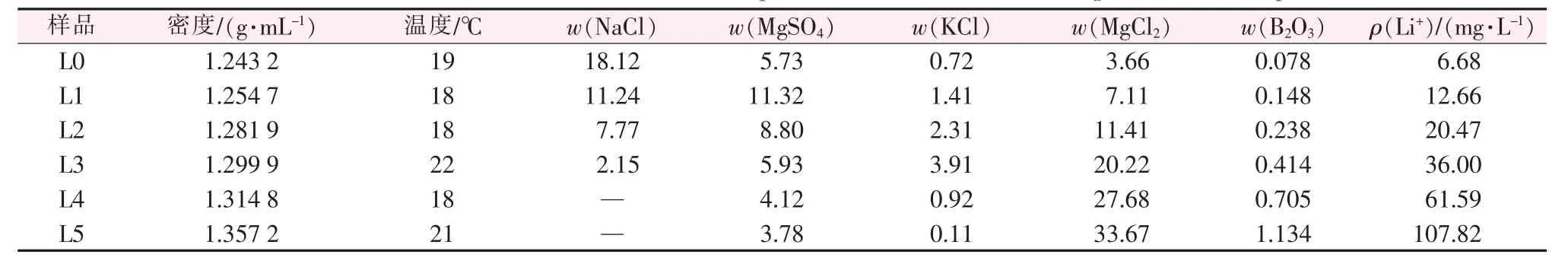
表4 瑪納斯湖鹵水自然蒸發液相組成Table 4 Chemical composition of Manasi brine during the natural evaporation %
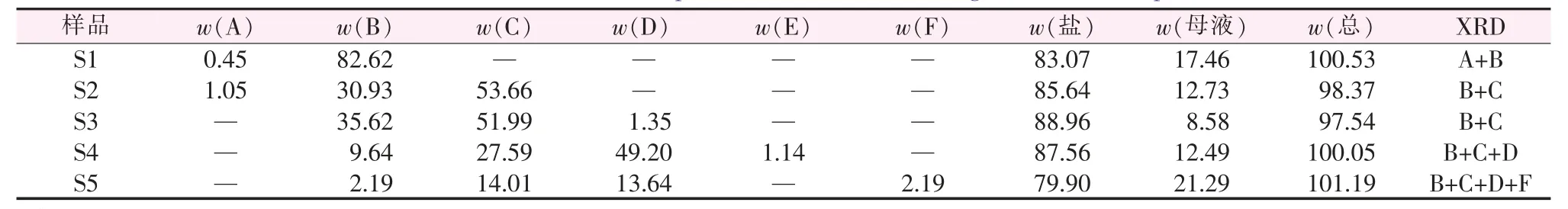
表5 瑪納斯鹵水自然蒸發固相組成Table 5 Chemical composition of the solids during the natural evaporation %
2 結果與討論
2.1 蒸發過程相圖分析及液相組成在相圖中的走向
瑪納斯湖水組成位于Na+,K+,Mg2+∥Cl-,SO42--H2O五元體系25℃介穩相圖(圖1)的瀉利鹽區(L0),屬于典型的硫酸鎂亞型鹵水。
從相圖1a中分析,此湖水在自然蒸發過程中氯化鈉飽和之后將會析出大量的瀉利鹽,液相組成將沿著AL0的延長方向移動,一直到達氯化鉀和瀉利鹽共飽線,交于B點;繼續蒸發,析出瀉利鹽和氯化鉀,液相組成沿著共飽線由B到達C;C點是瀉利鹽、氯化鉀和光鹵石的共飽和點。根據過程向量分析,此階段KCl溶解、瀉利鹽和光鹵石析出,直到氯化鉀溶解完全,液相組成在C保持不動;繼續蒸發,析出瀉利鹽與光鹵石,液相組成沿著共飽線由C到達D點;D點是瀉利鹽、光鹵石與水氯鎂石的共飽點,繼續蒸發析出瀉利鹽、光鹵石與水氯鎂石,直至溶液被蒸干。
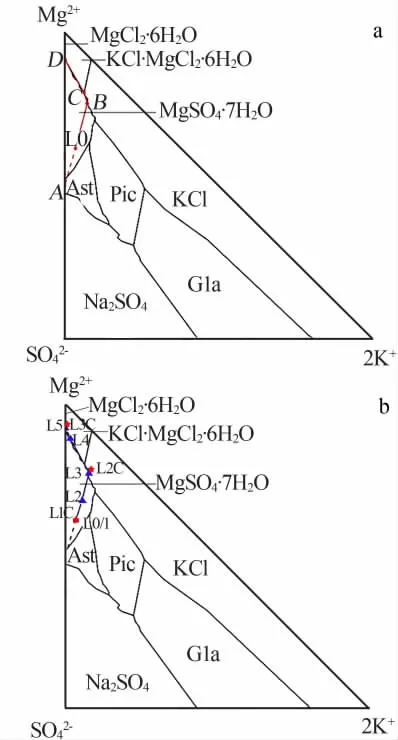
圖1 Na+,K+,Mg2+∥Cl-,SO42-·H2O五元體系25℃介穩相圖[10]預示的L0鹵水蒸發時的液相走勢(a)及ISLEC計算和實驗獲得的液相組成在相圖中的位置(b)Fig.1 Liquid phase trend of L0 brines in the evaporation process indicated by the metastable phase diagram[10]of Na+,K+,Mg2+∥Cl-,SO42-·H2O at 25℃(a)and the location of brine of ISLEC and experiment in the diagram(b)
將ISLEC模擬計算蒸發過程中液相的組成(L1C、L2C、L3C)及實際蒸發過程中液相組成(L0-L5)標注于Na+,K+,Mg2+∥Cl-,SO42--H2O五元體系25℃介穩相圖中(圖2b)。可以看出,模擬計算及室內自然蒸發實驗各階段的液相組成,基本與介穩相圖預示的路線一致。
2.2 蒸發過程結晶路線及析鹽規律
2.2.1 模擬蒸發過程結晶路線及析鹽規律
ISLEC程序模擬計算結果(表3)可知,瑪納斯湖水L0在20℃時自然蒸發的結晶路線:①NaCl;②NaCl+MgSO4·7H2O;③NaCl+MgSO4·6H2O+KCl·MgCl2·6H2O;④NaCl+MgSO4·4H2O+KCl·MgCl2·6H2O+MgCl2·6H2O。
第一階段為石鹽階段,析出固相為NaCl。第二階段為瀉利鹽階段,析出固相為NaCl+MgSO4·7H2O。第三階段為光鹵石階段,析出固相為NaCl+MgSO4·7H2O+KCl·MgCl2·6H2O,該階段析出光鹵石品位為53.09%(KCl品位為14.24%),鉀收率97.58%。由相圖分析可知,鉀鹽飽和后有一小段氯化鉀、瀉利鹽共析階段,但當光鹵石飽和后,又有一小段KCl回溶而光鹵石析出階段,而后才是光鹵石和瀉利鹽共析階段,如果這一小段氯化鉀階段不做分段分離,合并到光鹵石階段,最終固相中不出現氯化鉀。第四階段為水氯鎂石階段,光鹵石基本析出完畢,剩余鹵水為氯化鎂飽和的老鹵,繼續蒸發少量水即可析出大量水氯鎂石及少量氯化鈉、瀉利鹽和光鹵石。
2.2.2 實際蒸發過程結晶路線及析鹽規律
由表5可知,瑪納斯晶間鹵水在實際自然蒸發過程中的結晶路線:①CaSO4·2H2O+NaCl;②CaSO4·2H2O+NaCl+MgSO4·6H2O;③NaCl+MgSO4·6H2O+KCl(少量)+KCl·MgCl2·6H2O;④NaCl+MgSO4·6H2O+KCl·MgCl2·6H2O+MgCl2·6H2O。
自然蒸發實驗中析鹽種類和析鹽順序與介穩相圖預示和ISLEC模擬計算的基本一致。主要的差別在于鹵水實際蒸發過程中:1)石鹽及瀉利鹽階段有石膏存在;2)實際過程中瀉利鹽為六水瀉鹽;3)光鹵石階段混合有少量氯化鉀,這是由于實際過程KCl不能完全回溶所致。光鹵石段(S4+S5合并)獲得的光鹵石品位為36.72%,KCl品位為10.59%,品位比ISLEC計算的略低是由于實際實驗中鹽礦分離時夾帶了10%~20%的母液。
其結晶路線和析鹽順序與其他硫酸鹽型鹽湖鹵水如大柴旦夏季鹽湖鹵水的結晶路線是類似的[11]。同時,本文研究所得瑪納斯湖晶間鹵水自然蒸發的結晶路線與黃雪莉等[2]研究的結果有不一致的地方。黃雪莉等[2]給出的結晶路線中前期有白鈉鎂礬析出,且鉀是以鉀鎂鹽的形式析出,這主要是因為具體實驗條件和操作的差別導致。
2.3 蒸發過程中液相組成變化
圖2 為瑪納斯湖水蒸發過程中液相組成的變化趨勢,其中虛線為ISLEC計算結果,實線為實驗結果;綠色線條代表NaCl、紅色線條代表MgSO4、黑色線條代表KCl、藍色代表MgCl2。
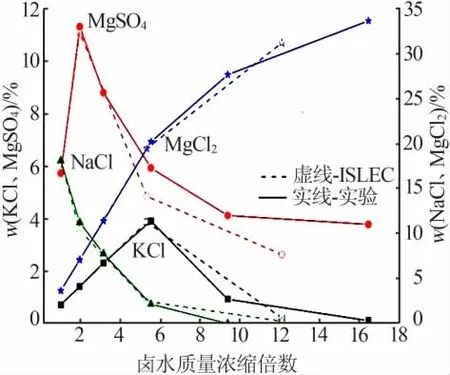
圖2 瑪納斯鹵水蒸發過程中液相組成變化趨勢Fig.2 Variation trend of liquid phase composition during evaporation of Manasi brine
由表2、表4和圖2可知,隨著蒸發的進行,已飽和的氯化鈉析出,溶液中的氯化鈉不斷減少。液相中的硫酸鎂隨著蒸發的進行不斷富集,當質量分數達到約11%時飽和,而后硫酸鎂以瀉利鹽的形式析出,溶液中硫酸鎂含量開始降低。液相中氯化鉀濃度也隨著蒸發的進行直線升高,硫酸鎂析出一定量后,液相中氯化鉀質量分數約3.9%時達到飽和,隨后隨著氯化鉀以光鹵石的形式析出后,液相中氯化鉀含量急劇下降。隨著蒸發的進行,液相中氯化鎂含量一直處于富集上升階段,在光鹵石析出之前氯化鎂的含量隨蒸發的進行直線升高;而隨著光鹵石的析出,溶液中氯化鎂的濃縮趨勢放緩,到水氯鎂石飽和時,溶液中氯化鎂質量分數可達到30%以上。由圖2可以看出,ISLEC計算及實驗得到的液相組成變化趨勢基本一致。
2.4 蒸發過程中硼、鋰的富集分布規律
瑪納斯湖晶間鹵水室內蒸發實驗的不同濃縮階段,液相中硼、鋰及鹵水質量濃縮倍數關系見表6。由表6看出,整個蒸發過程中,鹵水濃縮了約16倍,每一階段液相中B2O3及Li+的濃縮倍數基本與鹵水濃縮倍數一致,且固相中B2O3及Li+的含量屬母液夾帶范圍。這表明,在蒸發過程中B2O3和Li+并未析出,而是一直富集在鹵水中,當氯化鎂飽和時,B2O3可富集到約1%(質量分數),Li+約100 mg/L。這個結論與海水型硫酸鎂亞型鹵水蒸發過程中硼、鋰富集規律是一致的,高世揚等[11]指出,這一類型的鹵水中硼可富集到極限動態硼酸鹽溶解度(B2O3約5.3%)而不析出,而Li+在到達MgCl2、MgSO4及Li2SO4共飽和前也可以富集到約0.4%。
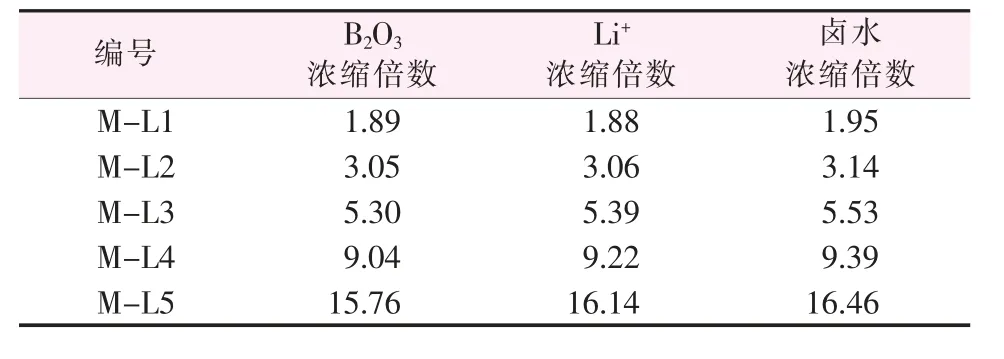
表6 鹵水及鹵水中B2O3、Li+的濃縮倍數Table 6 Concentrated times of brine and B2O3,Li+in brine
3 結論
1)通過對ISLEC模擬計算與實驗結果的比較可以看出,實驗中自然蒸發的結晶路線和節點與ISLEC模擬的結果基本一致,在實驗中只要按照ISLEC計算的節點分離可以得到與模擬一致的結果。這也印證 了ISLEC在Na+,K+,Mg2+∥Cl-,SO42--H2O體系自然蒸發模擬計算的準確性,可以用于預測其結晶路線和分離節點,指導室內實驗和鹽田實驗的進行。
2)瑪納斯湖水在自然蒸發過程中析鹽順序為:NaCl-MgSO4·6H2O-KCl·MgCl2·6H2O-MgCl2·6H2O。鉀鹽開始析出時,約需要蒸失水分54%,鉀鹽以光鹵石的形式析出,且在整個鉀鹽析出階段都伴隨著瀉利鹽的析出,得到品位較低且較難加工的鎂、鉀混鹽礦,建議采用冬季除硝后再進行鹽田攤曬,得到不含硫酸鹽的光鹵石礦。
3)瑪納斯湖水硼含量較低,原始鹵水中B2O3含量僅為0.078%(質量分數,下同),但其在蒸發過程中并不析出,可以一直富集在鹵水中,當大部分鉀析出完畢時,可富集到約1%,可以提取利用。原始瑪納斯湖水中Li+含量極低,質量濃度僅為6.68 mg/L,即使富集到老鹵階段也僅約100 mg/L,難以開發利用。

