CT與超聲彈性成像對肝炎肝硬化的診斷及Child-Pugh分級相關性的研究
李 斌 孟德莉 徐美芳
紹興文理學院附屬醫院放射科 (浙江 紹興, 312000)
肝硬化作為慢性乙型肝炎(CHB)患者常見的并發癥與病理結局,是導致患者死亡的主要因素之一[1]。肝組織病理學檢查仍為診斷肝炎肝硬化的“金標準”,但由于肝活檢的創傷性與局限性,易導致漏診,甚至出現出血、內臟受損等并發癥,難以作為常規監測手段。傳統的超聲、CT作為肝硬化常用的影像學檢查方法,可通過評估肝臟形態學及血流動力學進行診斷,具有的良好重復性與一致性[2]。超聲彈性成像是近年來新型非侵入性超聲檢查技術,被國際指南推薦用于肝硬化診斷,但其對于肝硬化程度及分期的敏感性仍缺乏足夠證據[3,4]。本研究通過回顧性分析肝炎肝硬化患者CT和超聲彈性成像資料,評價二者對肝炎肝硬化患者診斷價值,并分析其與Child-Pugh分級及肝功能的相關性。
1 資料與方法
1.1 一般資料 收集2018年1月至2020年6月在我院影像科接受檢查的CHB患者,共173例。其中男91例,女82例,年齡43~90歲,平均(56.9±5.1)歲;Child-Pugh分級:A級40例,B級64例,C級69例。
1.2 入組標準 ①患者均符合中華醫學會肝病學分會、感染病學分會制定的《慢性乙型肝炎防治指南(2015年版)》診斷標準[5],并經肝穿刺活檢確診,CT、超聲檢查資料齊全;②年齡18~80歲;③Child-Pugh分級為A~C級;④排除酒精性肝硬化或其他病毒性肝炎所致肝纖維化或肝硬化,排除合并嚴重心腦腎功能障礙者。本研究符合《赫爾辛基宣言》,患者或家屬對研究知情同意。
1.3 方法
1.3.1 CT檢查 入院后72 h內采用西門子SIMENS SOMATOM Definition AS 64排CT行腹部掃描,先平掃再行多期動態增強掃描,依次掃描肝頂至髂窩或恥骨聯合下緣。經前臂靜脈高壓注入碘海醇注射液(300 mg/ml)80~100 ml,注射速度2.5~3.5 ml/s。注射后依次行三期增強掃描,其中動脈期30 s、門脈期60 s、延遲期120 s。掃描參數:管電壓120 kV,管電流250 mA,螺距1.5,掃描層厚5 mm,層間距5 mm。
1.3.2 超聲彈性成像檢查 采用GE Vivid E9彩色多普勒超聲診斷儀行腹部檢查,探頭頻率5.0 MHz。取仰臥位,采用二維超聲從肝實質回聲、被膜光滑程度、邊緣形態、肝靜脈清晰程度等4個方面檢查肝臟多個切面圖像,在最大切面處切換為彈性成像模式,患者屏氣3~5 s后依靠心臟搏動進行成像,注意避開肝內管道結構。當顏色充滿取樣框的90%及以上且圖像穩定時凍結圖像,在成像區域中選取半徑為1 cm的區域進行參數分析,計算肝臟硬度值(LSM),單位為kPa。重復操作5次,取其平均值。
1.3.3 肝硬化CT分級標準 Ⅰ級:肝脾形態正常或輕度異常,門靜脈壓正常;Ⅱ級:肝臟體積輕微縮小,出現局部萎縮,脾臟輕度增大或可見2~3種門靜脈高壓征;Ⅲ級:肝臟形態明顯異常,體積明顯縮小,邊緣呈結節狀,或可見3~4種門靜脈高壓征且合并少量腹腔積液;Ⅳ級:肝臟體積顯著萎縮,實質密度不均,可見明顯結節,邊緣呈鋸齒狀,存在4種以上門靜脈高壓征且合并大量腹腔積液[6]。
1.4 統計學方法 應用SPSS 20.0軟件對數據進行統計分析,統計各種診斷方法的靈敏度、特異度、準確度。P<0.05為差異有統計學意義。
2 結果
2.1 不同檢查方法對肝硬化的診斷效果 以肝穿刺活檢病理診斷為金標準,超聲彈性成像、聯合診斷對肝硬化診斷的靈敏度、特異度及符合率均顯著高于CT,差異均有統計學意義(P<0.05);聯合診斷對肝硬化診斷的靈敏度、特異度及準確度顯著優于超聲彈性成像較,差異均有統計學意義(P<0.05)。見表1、2。
2.2 不同Child-Pugh分級患者LFI、肝硬化CT分級情況 隨著Child-Pugh分級的增加,LFI明顯增高,差異均有統計學意義(P<0.05)。Child-Pugh分級A級與B級患者肝硬化CT分級比較,差異無統計學意義(P>0.05),見表3。

表3 不同Child-Pugh分級患者LFI、肝硬化CT分級比較 (例)
2.3 病案舉例
2.3.1 病案1 患者男, 61歲,乙型肝炎肝硬化失代償期,肝功能異常。上腹部增強CT掃描顯示:肝臟外形縮小,表面呈波浪狀,肝裂增寬,肝葉比例失調,門脈主干增寬,脾臟增大,食管下段、胃底靜脈曲張,脾靜脈曲張,腹腔積液。超聲彈性成像示LSM為19.0 kPa,見圖1。
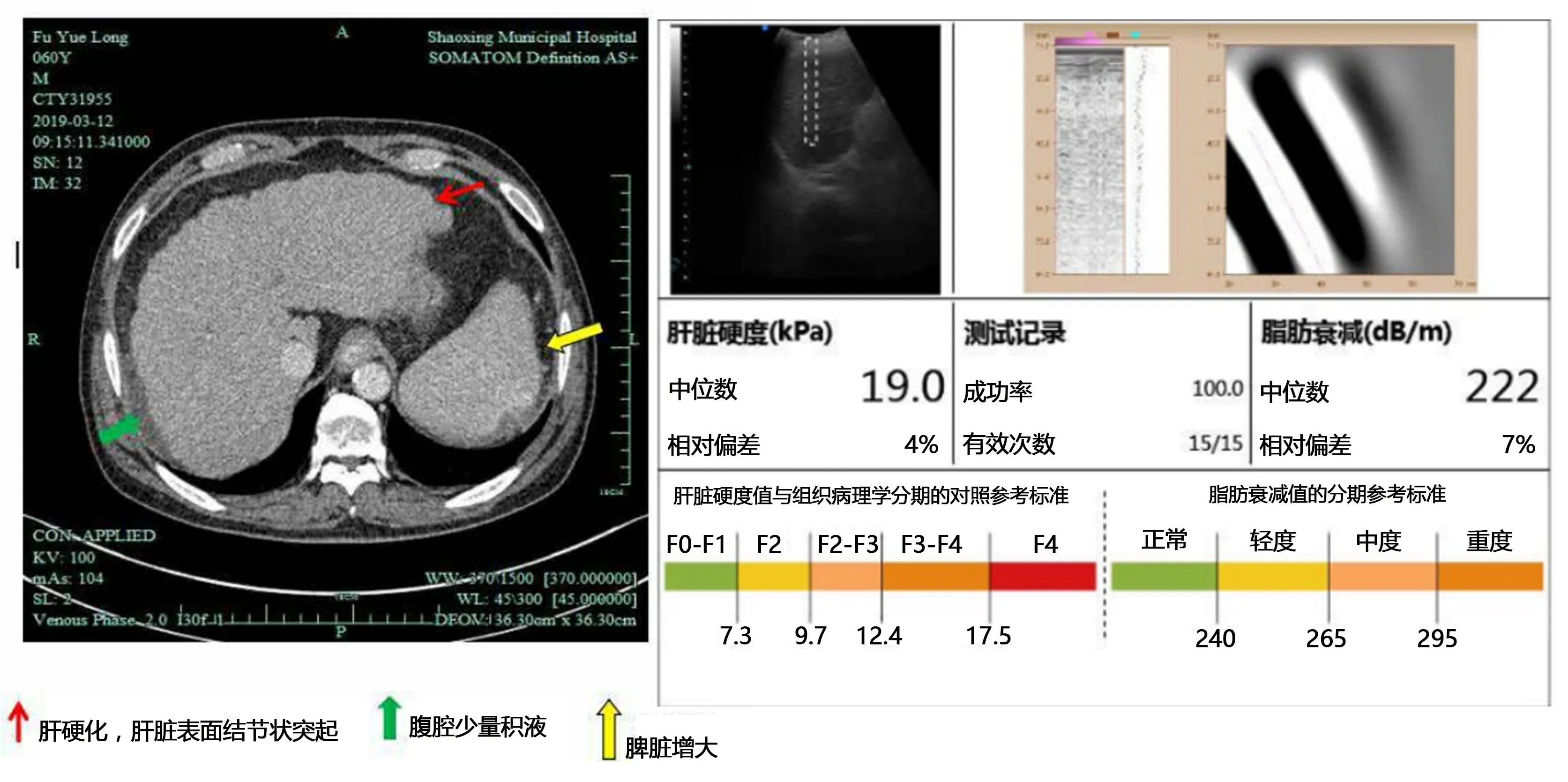
圖1 CT與超聲彈性成像對比圖(病案1)
2.3.2 病案2 患者男,42歲,輕度肝硬化,上腹部增強CT掃描顯示:肝臟外形略縮小,表面欠光整,肝裂增寬,脾臟輕度增大。超聲彈性成像示LSM為11.0 kPa,見圖2。
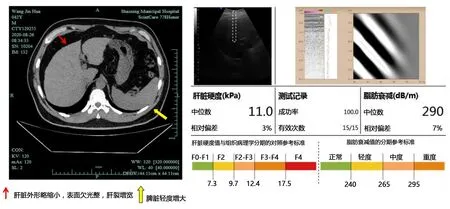
圖2 CT與超聲彈性成像對比圖(病案2)
3 討論
準確診斷評估肝硬化及其嚴重程度對控制病情進展、治療及預后具有重要臨床意義。Child-Pugh評分仍是目前臨床最常用的肝硬化患者肝功能失代償的評價體系,主要與血清白蛋白、總膽紅素、凝血酶原時間、腹水、肝性腦病5個指標直接相關,眾多研究已證實其在肝硬化預后中評估價值,但隨著臨床研究的不斷深入,其精準性的弊端也逐漸顯現,尤其是難以防止外源性因素和肝臟營養狀態的影響,導致相同Child-Pugh分級的肝硬化患者呈現較大的預后差異[7,8]。
近年來,隨著影像學技術的快速發展,無創性評估肝硬化,已成為肝硬化定性定量的診斷的常用手段[9]。CT對肝硬化的診斷主要依靠肝臟形態的變化,可清楚顯示肝大小和輪廓、肝裂增寬、肝實質密度不均、膽囊移位、膽囊壁增厚、膽囊窩增大等形態學改變,同時繼發門靜脈增粗、腹水、脾大、側支循環形成等門脈高壓征象,但肝硬化早期形態學改變缺乏特異性,可能導致誤診或漏診[10]。超聲彈性成像定量分析是一種新型非侵入性診斷措施,能根據不同組織彈性系統及外力壓迫產生的差異化反應,間接顯示傳統超聲技術未能探測到的腫瘤及擴散病灶,廣泛應用于甲狀腺癌、乳腺癌等疾病的診斷[11]。鄭穎等[12]研究認為,肝纖維化區域的超聲彈性成像分析圖像仍相對正常,而肝硬化后則表現為圖像分布不均,由此可見超聲彈性成像可反映肝纖維化到肝硬化的發展過程,對于肝硬化早期診斷具有明顯優勢。魏占芳等[13]研究發現,超聲彈性成像具有組織彌漫定量分析功能,能結合患者心血管搏動力壓縮組織成像,避免手動按壓誤差,且不受體重、腹水、肝組織萎縮、肋骨間隙狹窄等因素的影響,具有較高準確度。
本研究以肝穿刺活檢病理診斷為金標準,結果顯示超聲彈性成像對肝硬化診斷的靈敏度、特異度及符合率顯著高于CT,說明超聲彈性成像診斷肝硬化的能力顯著優于CT,聯合CT檢測診斷效能進一步提高。CT對肝硬化的診斷多局限于肝表面與比例,而超聲彈性成像可對肝臟質地進行精準評估。Hube等[14]一項多中心研究報道指出,常規CT對肝硬化的診斷敏感性為77.1%~84.3%、特異性僅52.9%~67.6%,且對征象的分析常依賴影像學醫師的經驗,存在較強主觀性。結果還提示LFI在肝硬化早期肝功能區分評估能力優于CT分級,LFI越大,Child- Pugh分級也越高,肝功能損傷越明顯,說明超聲彈性成像LFI值可作為評估肝硬化患者肝功能的重要指標。Xu等[15]采用COX風險比例模型進行生存分析顯示,肝硬化LFI評分越高,生存期越短,肝硬化LFI評分在介入治療前對肝功能與預后的預測、評估具有一定價值。
綜上所述,CT、超聲彈性成像對肝硬化診斷具有較高價值,各具優勢,二者聯合診斷可顯著提高早期肝硬化的定性診斷能力,且有助于評估肝硬化程度和分期,避免不必要的肝活檢。由于本研究的樣本量較少,今后我們將通過大樣本、多中心研究進一步深入論證。

