不同沉淀劑對酚抽法提取植物蛋白質效果比較分析
霍玉鑫,甘番露,王玉晶,張雪妍,王旭初,謝全亮

摘? 要:酚抽法已經逐漸成為植物蛋白質組研究中通用的蛋白質提取方法,但在各種改進酚抽法中,應用到的沉淀試劑各不相同,致使蛋白沉淀得率、純度和沉淀時間也各異,本研究以熱帶植物橡膠樹葉片、膠乳和海馬齒葉片為研究材料,在過飽和硫酸銨甲醇溶液、醋酸氨甲醇溶液和丙酮溶液沉淀劑下對比蛋白提取的效果,通過單向電泳檢測、膠圖質量分析、質譜鑒定、蛋白沉淀時間和得率比較,發現3種沉淀劑提取的蛋白樣品1-DE圖譜顯示的蛋白條帶數量均較多,但醋酸銨沉淀法提取蛋白圖譜有條紋不清晰現象。得出結論:丙酮沉淀法對橡膠樹葉片和膠乳蛋白質的提取率較高,硫酸銨沉淀法對海馬齒葉片蛋白質提取率較高。過飽和硫酸銨甲醇溶液和丙酮沉淀劑提取的蛋白質質量較高,所得蛋白圖譜背景清晰,質譜鑒定蛋白質信息量大。研究結果可優化提取高質量植物蛋白質的方法,并有望為頑拗類植物蛋白質組學研究提供參考。
關鍵詞:蛋白提取;橡膠樹;海馬齒;沉淀劑;聚丙烯凝膠電泳;質譜
中圖分類號:TQ936? ? ? 文獻標識碼:A
Comparative Analysis of the Effects of Different Precipitation Agents on Extraction of Plant Protein by Phenol Extract
HUO Yuxin1, GAN Panlu1, WANG Yujing1, ZHANG Xueyan1, WANG Xuchu1,2*, XIE Quanliang1,2*
1. Hainan Normal University / Key Laboratory of Tropical Island Ecology, Ministry of Education, College of Life Sciences, Haikou, Hainan 571158, China; 2. College of Life Science and Agricultural, Shihezi University, Shihezi, Xinjiang 832003, China
Abstract: The borax/PVPP/phenol (BPP) protocol is a widespread protein extraction method in plant proteome research. However, BPP extraction of plant protein, combined with different precipitation agents, the precipitation time, yield and purity of extracted protein is strikingly different. In this study, Sesuvium portulacastrum and Para-rubber tree leaves, and rubber latex were used as the research materials. The plant protein was extracted and analyzed with precipitating agents of supersaturated potassium ammonium sulfate alcohol solution, ammonium acetate methanol solution and acetone solution. Using the methods of SDS-PAGE, gel electrophoresis image quality, mass spectrum identification, settling duration and comparative analysis of protein yield, it was showed that the protein bands extracted by the ammonium acetate precipitation method were not evident. Hevea leaves and latex showed a higher yield of protein in acetone solution. S. portulacastrum leaves had a higher yield of protein in supersaturated potassium ammonium sulfate alcohol solution. The clear background of gel electrophoresis figures was found for the supersaturated potassium ammonium sulfate ethanol solution and acetone solution. The comprehensive protein sequence information identified by mass spectrometry had a higher quality of precipitated protein. The research results can optimize the method of extracting high-quality plant protein, and it will be expected to provide references for recalcitrant plant taxa proteomics research in the future.
Keywords: protein extraction; Hevea brasiliensis; Sesuvium portulacastrum; precipitant; polypropylene gel electrophoresis; mass spectrometry
DOI: 10.3969/j.issn.1000-2561.2021.10.035
從植物組織中制備高質量的蛋白質樣品用于蛋白質組學分析是一個巨大的挑戰,而蛋白質組學已經發展成為研究植物蛋白功能的重要技術手段[1-2],是一種檢測植物基因在轉錄后是否被翻譯和修飾等較新穎且有效的研究植物蛋白的方法,從而填補了從轉錄組到代謝組的中間空缺[3-5]。目前,蛋白組學的研究技術方法有很多,例如2-DE[6]、MALDI[7]、Label-free[8]和iTRAQ/TMT[9]等技術,被廣泛用于研究某種特定生理環境下動植物的全蛋白、差異表達水平以及互作分析等。但由于植物各種組織細胞中含有特定的物質能夠降低提取蛋白的質量及產率,所以無法提取固定得率的蛋白質,需要針對特定的材料采取特定的提取處理方法[10-11],從而提高提取植物蛋白質的質量,這也是決定蛋白質組學后續比較分析的關鍵因素。
由于植物組織的特殊特性,通常因堅固的細胞壁、蛋白酶、大的液泡、高濃度的有機酸和次級代謝產物(酚類化合物和色素)等物質,嚴重干擾蛋白質的提取、分離和鑒定,致使從植物各組織中分離蛋白質組分具有很大的挑戰性,也是影響植物蛋白組學研究最關鍵因素[12-14]。利用酚抽法可用于頑拗類植物組織中蛋白質提取[15],但提取蛋白的得率還需進一步提升。針對木本植物橡樹、松樹和楊樹的次生木質部總蛋白提取,發現使用優化的TCA-丙酮方法,提取蛋白質效果最佳[16]。在挪威針云杉和歐洲山毛櫸的葉和根中分離蛋白質,發現在包含7 mol/L尿素和2 mol/L硫脲的分離液劑下提取和分離蛋白質最佳[17],但提取方法中并未涉及沉淀劑的深入討論。在谷物種子中用不同緩沖液可以分離出種子內不同蛋白質用于蛋白質組學研究[18],其在沉淀劑選擇上并未改進。以三氯乙酸、丙酮沉淀和苯酚提取黃連木的雄性和雌性植物蛋白質比較研究,詳細描述了這3種提取方法的優缺點和應用,使研究者能為特定的物種、組織或細胞類型選擇合適的方法[19],但是在沉淀劑的選擇方面也未深入研究。在模式植物擬南芥中提取總蛋白時,可用常規溶解劑就能溶解一系列蛋白質,并實現其高效定量的回收,使用這種方法可用于試劑盒直接定量[20],但并非綠色植物都可以使用該方法。隨后,Flengsrud[21]在大麥葉、馬鈴薯葉和云杉針葉組織中提取蛋白質,克服了綠色植物中固有的蛋白質組學分析障礙,但在蛋白質的產率和純化方面還有待優化。綜上所述,在植物蛋白提取方法不斷更新過程中,蛋白得率和質量是影響蛋白組學深入研究的主要因素,針對這方面的困難應著眼于在提取不同植物組織蛋白質過程中,如何選取最佳沉淀劑,從而獲得純度較高的蛋白質。
在筆者前期的研究中,發現利用本實驗室改進酚抽法(Borax/PVPP/Phenol,BPP)提取橡膠樹以及海馬齒組織蛋白的得率以及質譜鑒定結果相差都非常大,難以進行后續蛋白質組學分析研究。因此,為了克服上述困難,我們選擇了巴西橡膠樹(Hevea brasiliensis)的葉片和膠乳(含多糖多酚類物質)以及高含鹽海岸植物海馬齒(Sesuvium portulacastrum L.)的葉片材料特殊性,提供了一種輔助蛋白質提取方法,首次針對這3種材料在BPP提取緩沖液結合過飽和硫酸銨甲醇溶液、醋酸銨溶液和丙酮溶液3種沉淀劑展開了蛋白提取方法的研究,在蛋白得率、凝膠圖譜和質譜鑒定等方面系統分析。通過實驗表明,針對不同植物材料選擇不同沉淀劑的方法,確實對植物蛋白質提取很有效,并且同時適用于聚丙烯凝膠電泳及質譜分析的2種蛋白組學分析手段。為采用BPP法提取不同植物蛋白時選擇合適的沉淀劑提供理論支持,也為今后植物蛋白質組學研究提供技術參考。
1? 材料與方法
1.1? 材料
以中國熱帶農業科學院實驗田內橡膠樹(‘熱研73-3-97)新鮮葉片(Hevea leaves,HL)、橡膠樹新鮮膠乳(latex,LA)以及番杏科多年生匍匐草本植物海馬齒新鮮葉片(Sesuvium leaves,SL)為實驗材料。橡膠樹切割先讓膠乳流25滴以上,流盡樹皮表面的雜質后開始取樣,取樣用的割刀需要高溫灼燒消毒滅菌后使用,以免引起H. brasiliensis死皮病。用植物蛋白質BPP法(Borax/PVPP/Phenol)提取蛋白。BPP蛋白提取緩沖液配置:100 mmol/L EDTA,100 mmol/L Tris, 50 mmol/L維生素C,50 mmol/L硼砂,1%(V/V)Triton X-100,1 g(W/V)PVPP,30%(W/V)蔗糖和2%(V/V)β-巰基乙醇,pH 8.0;蛋白裂解液:1%(V/V)IPG buffer,2 mol/L硫脲,2%(W/V)CHAPS,7 mol/L尿素,13 mmol/L DTT;標準Laemmli buffer:0.001%(W/V)溴酚藍,2%(W/V)SDS,5%(V/V)β-巰基乙醇,10%甘油,62.5 mmol/L Tris-HCl;膠條平衡液:0.002%(W/V)溴酚藍,2%(W/V)SDS,30%(V/V)甘油,50 mmol/L Tris-HCl,6 mol/L尿素;GAP凝膠染色液:0.125%(W/V)考馬斯亮藍G-250,5%(V/V)磷酸,10% (W/V)硫酸銨,10%(V/V)甲醇,30%(V/V)乙醇;凝膠脫色液:5%(V/V)乙酸,30%(V/V)乙醇;胰蛋白酶緩沖液;25 mmol/L碳酸氫銨,1 mmol/L氯化鈣,pH 8.5。
1.2? 方法
1.2.1? 植物蛋白的提取? 采集植物組織后,立即浸入液氮預冷研缽中速凍,并加入1% PVPP粉末防止氧化,充分研磨成干粉后,稱取3 g植物組織粉末,加入盛有10 mL預冷BPP提取緩沖液50 mL離心管中,室溫渦旋震蕩10 min。加入等體積Tris飽和酚,室溫渦旋震蕩10 min。用BPP提取緩沖液配平,4 ℃,16 000 ×g,離心15 min。吸取上清液于新的50 mL離心管中,再次加入等體積BPP提取緩沖液,4 ℃渦旋震蕩5 min。再次加入BPP提取緩沖液配平,4 ℃,16 000 ×g,離心15 min。取上清液1 mL,分裝入含有5 mL不同沉淀劑的10 mL離心管中,不同沉淀劑為:(1)預冷的過飽和硫酸銨甲醇溶液(supersaturated ammonium sulfate methanol,SAM)可使蛋白質溶解性變小產生物理沉淀,稱為蛋白質“鹽析”現象。(2)丙酮溶液(acetone solution, AS)通過有機溶劑丙酮溶液破壞蛋白質的水化層,降低介電常數,從而增強帶電蛋白質分子之間的相互作用,促進蛋白顆粒聚集沉淀。為避免蛋白變性,丙酮溶液需要低溫且操作時間盡量縮短;(3)預冷0.1 mm/L的乙酸銨溶液(ammonium acetate solution,AA)中性鹽減少蛋白質變性,但可破壞蛋白質的水化膜,暴露出憎水區域,使蛋白質聚集沉淀,憎水區的多少決定沉淀量。沉淀劑均為上清液體積的5倍即:蛋白提取上清液/沉淀劑= 1/5,置于?20 ℃過夜沉淀。
1.2.2? 蛋白定量? 采用Bradford方法蛋白定量,Bradford定量液:0.05 g CBB G-250,95%乙醇25 mL,50 mL 85%磷酸,超純水定容至500 mL,濾紙過濾使用。在測定樣品濃度前,先制作標準蛋白的標準曲線。樣品要置于冰上保持低溫,準備牛血清標準蛋白(bull serum albumin,BSA)作為標準樣品,裂解液lysis buffer(LB),紫外分光度儀器設定測樣品蛋白OD595,測定每個樣品至少重復3次。
1.2.3? SDS-PAGE凝膠電泳染色和圖像采集? 使用不連續膠聚丙烯酰胺凝膠電泳(SDS-PAGE)法根據分子量大小對蛋白質進行分離。分離膠濃度為12.5%,濃縮膠濃度為5%。25 μL蛋白質樣品上樣體積:20 μL(V樣品+VLB)+5 μL蛋白loading buffer,marker:10 μL,蛋白質量約為30 μg,與Laemmli buffer混勻后上樣。電泳在16 ℃恒溫水浴下進行,電泳程序設定:10 W、40 min,20 W、1.2 h。
凝膠染色:考馬斯亮藍G-250染色液按照標準化配方提前一天配制。漂洗后的凝膠轉入染色液中,搖床低速30 r/min染色過夜。
脫色:脫色液標準化配方現用現配。取出染色好的凝膠放入蒸餾水漂洗5 min,轉入脫色液中,按照標準化試劑配方中的方法進行脫色過程。
凝膠分析:脫色后的凝膠用ImageScanner Ⅲ掃描儀(GE Healthcare)進行掃描和圖像采集掃描凝膠,掃描時保證圖片分辨率,并保存。利用ImageMaster 5.0軟件分析蛋白電泳圖譜條帶數。
1.2.4? 凝膠膠內蛋白酶解? 選取目標差異蛋白,進行膠內酶解,胰蛋白酶液與含有蛋白的凝膠粒混合后,在37 ℃恒溫水浴,酶解15 h。酶解后收集酶解上清液直接用于質譜鑒定。
1.2.5? 質譜鑒定及蛋白數據庫搜索? 將上述酶解產物進行質譜鑒定,采用的是布魯克公司基質輔助激光解析電離飛行時間質譜儀(5800 MALDI- TOF Bruker),進行一級和二級質譜分析。所獲得的蛋白數據通過Mascot Distiller軟件分析肽的指紋圖譜(peptide mass fingerprinting,PMF)得出結果,再利用Matrix Science網站(http://www. matrixscience.com)進行蛋白肽段匹配和數據庫搜索鑒定。
2? 結果與分析
2.1? 橡膠樹葉片、膠乳和海馬齒葉片的總蛋白提取
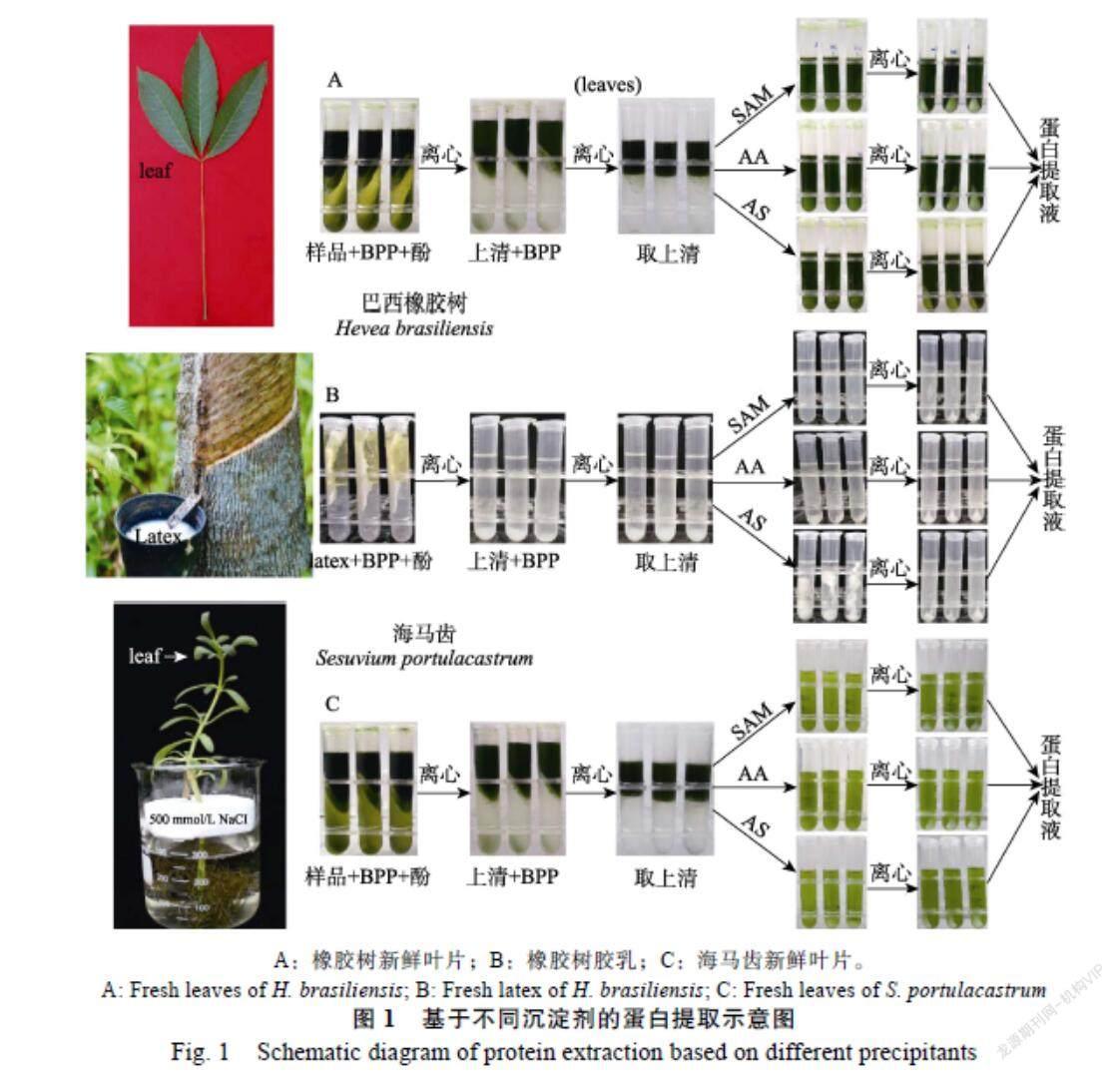
酚抽法是植物蛋白提取的常用方法,而BPP法是本實驗室在此法的基礎上進一步優化改良的一種高效蛋白提取方法,既適于從多糖多酚類及高鹽分含量的植物材料的蛋白質提取,還可用于頑拗植物獲得較高產量蛋白。利用BPP法可在橡膠樹新鮮葉片、新鮮膠乳和海馬齒新鮮葉片中提取到3~10 mg/g不等的總蛋白,針對這3種材料,我們設計3種蛋白質沉淀劑,蛋白質提取過程(圖1)。
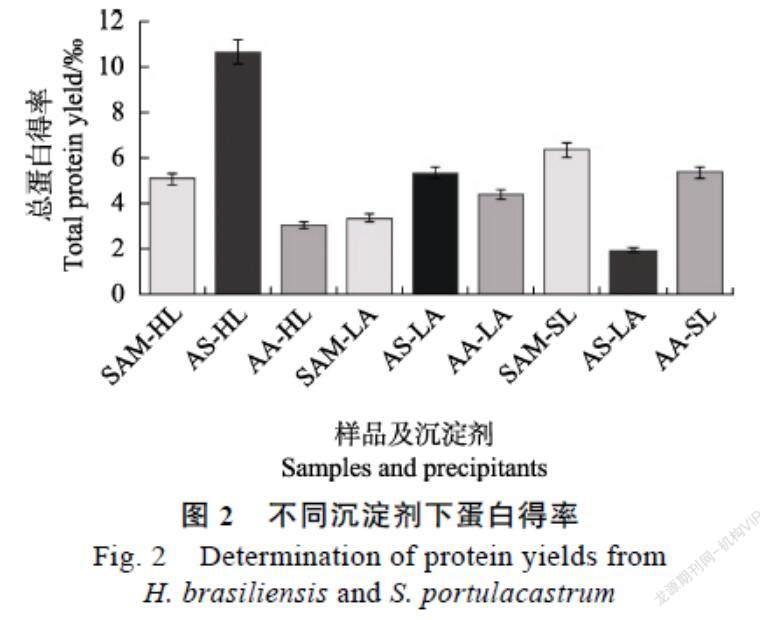
在不同沉淀劑下提取總蛋白得率結果顯示,每克材料的蛋白得率偏差比較大,其中HL在不同沉淀劑下的得率大小順序為:AS-HL(10.64± 0.06 mg/g)> SAM-HL(5.10±0.06 mg/g)>AA-HL(3.09±0.01 mg/g);LA的總蛋白得率在不同沉淀劑下的大小順序為:AS-LA(5.35±0.02 mg/g)> AA-LA(4.43±0.02 mg/g)>SAM-LA(3.386± 0.08 mg/g);SL總蛋白得率大小順序為:SAM-SL(6.385±0.06 mg/g)>AA-SL(5.371±0.04 mg/g)> AS-SL(1.959±0.04 mg/g)。比較結果顯示,HL總蛋白得率在AS得率最高;LA在AS沉淀時總蛋白得率最高,SL在SAM沉淀劑下蛋白得率最高(圖2)。
2.2? 聚丙烯酰氨凝膠電泳分析
從SDS-PAGE的結果可以看出,經過除雜后的蛋白條帶邊界輪廓清晰,凝膠圖背景干凈,分離效果好,并未出現條帶拖尾和彌散不均的現象(圖3)。
在高分子量(>100 kDa)區域和較低分子量(<20 kDa)區域均可監測到明顯的蛋白條帶。應用ImageMaster 5.0軟件對1-DE圖譜進行蛋白的條帶統計分析,不同沉淀劑下的結果檢測出不同數目的蛋白條帶(表1)。經過統計蛋白條帶結果顯示,SAM沉淀劑下的平均條帶較多(39±1.41),?其次,AS沉淀劑下的平均蛋白條帶(36±1.41),蛋白條帶最少的是AA的1-DE平均蛋白條帶較少(29±2.42)。而且橡膠樹葉片和海馬齒葉片組織的蛋白條帶具有相似的圖譜,在條帶數和個別條帶在豐度上出現一定的差異。
2.3? 蛋白膠內酶解及MALDI TOF質譜分析
挖取凝膠上各選取12個重復性好、分離性好、相對豐度較高且是已知具有代表性蛋白進行膠內酶解,其中包括二磷酸核酮糖羧化 (ribulose bisphosphate carboxylase,RubisCO)、小橡膠粒子(small rubber particle protein,SRPP)和橡膠延伸因子(rubber elongation factor,REF),利用本實驗室改進后報道的蛋白酶解方法進行膠內酶解,隨后進行MALDI TOF 5800質譜儀進行一級質譜和二級質譜鑒定,經鑒定獲得了較好的PFF和PMF質譜圖譜(圖4)。鑒定到的蛋白數據進行數據搜庫,由于熱帶植物海馬齒還未發表基因組及轉錄組數據專有的蛋白數據庫,因此將質譜鑒定結果通過Mascot Distiller軟件分析,隨后用Matrix Science在NCBInr中的(NCBI-National center for biotechnology information non-redundant database)綠色植物蛋白總庫,利用在線引擎(http://www.matrixscience.com/ search)進行搜索,經一級和二級質譜鑒定特定標記性蛋白,共鑒定了36個蛋白質,從所得的PMF一級質譜圖譜上看,主要肽段質譜離子峰集中范圍在800~ 2500 m/s之間,這說明在這個酶切片段更加有利于下一步二級質譜分析。并說明提取蛋白中含雜質少,無其他蛋白污染。這些特定蛋白的總肽段數在10~62左右,最高可達到62條(表2),并且Trypsin的自切峰強度較低,該方法中酶切充分,不易自切。由于熱帶典型海岸植物海馬齒沒有發表基因組及對應的蛋白數據庫,因此,質譜鑒定結果通過Mascot Distiller分析,鑒定后統計了蛋白理論等電點和分子量,蛋白實驗等電點和分子量,匹配肽段的數量,覆蓋率和得分等情況。
利用Matrix Science 搜索引擎對鑒定的蛋白及肽段搜庫匹配,36個蛋白點相關信息,統計可信蛋白理論等電點和蛋白分子量與實驗測定的蛋白等電點和蛋白分子量進行統計比較,結果顯示實驗測定值和理論值基本一致,有小部分蛋白的實驗等電點與分子量和理論值有偏差,例如A4-1,鑒定結果發現蛋白的分子量有偏差,經理論分析這些蛋白可能是某些蛋白的亞基結構,在生物學功能的蛋白組成中,通常都是由多個亞基組合而成,這些蛋白主要參與翻譯后修飾無機離子和氨基酸轉運代謝,分子伴侶和信號轉導等代謝通路的作用產生了蛋白結構變化。通過變性凝膠電泳將蛋白亞基結構分離,因此,鑒定蛋白的實驗等電點和分子量會出現一定范圍內的偏移現象。根據蛋白搜庫結果顯示,HL和SL在SAM沉淀劑下肽段匹配數和覆蓋率質量高于AA和AS沉淀劑的質量;LA蛋白提取在AA沉淀劑下的蛋白質量優于SAM和AS沉淀劑提取的蛋白質量。
3? 討論
幾十年來,已在許多植物物種中進行了大量的蛋白質組學研究,但是植物蛋白質提取的質量高低仍然是影響蛋白質組學研究最重要因素[19]。
聚丙烯凝膠電泳一直是一種最廣泛用于分離總蛋白的工具提取物以及從各種途徑獲得的蛋白質級分預分餾程序[12]。為了獲得高質量高純度的植物蛋白質,我們基于BPP緩沖液結合3種沉淀劑,提取了橡膠樹和海馬齒等組織的蛋白質,相比較兩者的蛋白得率和質量差異較大,但是蛋白質圖譜與前期橡膠樹和海馬齒蛋白圖譜非常不同。與前期研究中的凝膠圖譜相比[22-24],我們的凝膠圖譜更清晰,并且包含更多的蛋白條帶。在鑒定代表性蛋白質中,相同蛋白質包含不同的蛋白質同工型,在凝膠圖譜上也具有不同的實驗Mr和pI值,分析原因可能是由于修飾蛋白質變形后所致。
在過去的植物蛋白提取方法的研究中,針對提取緩沖液的改進優化研究較多,例如在植物葉片[13, 15-17, 20, 25-26]、種子[18, 21, 27]、根[28]以及花器官[12, 19]等,但是著眼于研究植物蛋白提取過程中沉淀劑的選擇方面涉及內容較少。我們比較3種沉淀劑的蛋白得率和質譜鑒定結果發現,HL和SL在SAM沉淀劑提取蛋白質量優于其他2種沉淀劑;LA的蛋白提取在AA的蛋白質量優于其它兩個沉淀劑提取的蛋白質質量。而通過硫酸銨和醋酸銨比例的優化,可以限制蛋白變性并能提高蛋白質提取的質量[22],這一結果與前人研究結果保持一致,但該方法并未在高鹽生植物蛋白提取中應用。聚丙烯酰胺凝膠電泳可比較3種沉淀劑提取蛋白質的質量[29-30],雖然3種沉淀劑的蛋白質圖譜在較高和較低的Mr區域均可觀察到了明顯的蛋白條帶,且大部分相似,但是標記性蛋白條帶的清晰度和灰度有明顯的差異。李肖芳等[31]利用3種方法對鹽生植物鹽角草的蛋白提取,其中丙酮沉淀和三氯乙酸沉淀提取的蛋白雜質較多,在蛋白凝膠圖中有嚴重拖尾或橫向紋理現象。而本研究的凝膠圖譜結果可見更清晰的蛋白條帶,說明選取合適的蛋白沉淀劑可以獲得更高純度的蛋白質。從總體上看,BPP方法可以收集到低濃度的蛋白質,并且獲得的蛋白質可以成功用于蛋白質組學分析。本研究結果也說明,BPP方法結合不同沉淀劑可獲得更多多糖多酚植物和高鹽鹽生植物高質量的蛋白質,保證能夠提取低濃度溶液中的蛋白質。迄今為止,這3種沉淀劑之間蛋白得率及提取蛋白質量進行比較研究還尚未報道,本研究是首次提出BPP方法結合不同沉淀劑進行蛋白提取分析的研究。
綜上所述,BPP方法結合3種沉淀劑的使用,具有被廣泛應用的潛力,還可用于低蛋白濃度溶液的植物蛋白質組學分析。學者可根據研究材料選擇最適沉淀劑提取蛋白,這對于不同植物提取高純度和高質量的蛋白質極其重要,也為植物蛋白組學獲取高質量蛋白提供一定的理論基礎。
參考文獻
[1] Thiellement H, Bahrman N, Damerval C, et al. Proteomics for genetic and physiological studies in plants[J]. Electrophoresis, 1999, 20: 2013-2026.
[2] Wang X. Protein and proteome atlas for plants under stresses: New highlights and ways for integrated omics in post-geno?m?ics era[J]. International Journal of Molecule Sciences, 2019, 20(20): 5222.
[3] Parkhey S, Chandrakar V, Naithani S C, et al. Efficient extraction of proteins from recalcitrant plant tissue for subsequent analysis by two-dimensional gel electrophoresis[J]. Journal of Separation Science, 2015, 38: 3622-3628.
[4] Gallardo K, Job C, Groot S P, et al. Proteomic analysis of Arabidopsis seed germination and priming[J]. Plant Physiology, 2001, 126: 835-848.
[5] Hoa le T P, Nomura M, Kajiwara H, et al. Proteomic analysis on symbiotic differentiation of mitochondria in soybean nodules[J]. Plant Cell Physiology, 2020, 45: 300-308.
[6] Rabilloud T. How to use 2D gel electrophoresis in plant proteomics[J]. Methods Molecule Biology, 2014, 1072: 43-50.
[7] Yang H, Liu N, Liu S. Determination of peptide and protein disulfide linkages by MALDI mass spectrometry[J]. Topics in Current Chemistry, 2013, 331: 79-116.
[8] Nahnsen S, Bielow C, Reinert K, et al. Tools for label-free peptide quantification[J]. Molecular and Cellular Proteomics, 2013, 12: 549-556.
[9] Merrill A E, Coon J J. Quantifying proteomes and their post-translational modifications by stable isotope label-based mass spectrometry[J]. Current Opinion in Chemical Biology, 2013, 17: 779-786.
[10] Righetti P G, Boschetti E. Low-abundance plant protein enrichment with peptide libraries to enlarge proteome coverage and related applications[J]. Plant Science, 2020, 290: 110302.
[11] Potin F, Lubbers S, Husson F, et al. Hemp (Cannabis sativa L.) protein extraction conditions affect extraction yield and protein quality[J]. Journal of Food Science, 2019, 84(12): 3682-3690.
[12] Wang W, Tai F, Chen S. Optimizing protein extraction from plant tissues for enhanced proteomics analysis[J]. Journal of Separation Science, 2008, 31(11): 2032-2039.
[13] Chapman B, Castellana N, Apffel A, et al. Plant proteogenomics: from protein extraction to improved gene predictions[J]. Methods in Molecular Biology, 2013, 1002: 267-294.
[14] Rode C, Winkelmann T, Braun H P, et al. DIGE analysis of plant tissue proteomes using a phenolic protein extraction method[J]. Methods in Molecular Biology, 2012, 854: 335-342.
[15] Wang W, Vignani R, Scali M, et al. A universal and rapid protocol for protein extraction from recalcitrant plant tissues for proteomic analysis[J]. Electrophoresis, 2006, 27(13): 2782-2786.
[16] Plomion C, Lalanne C. Protein extraction from woody plants[J]. Methods in Molecular Biology, 2007, 355: 37-41.
[17] V?lcu C M, Schlink K. Efficient extraction of proteins from woody plant samples for two-dimensional electrophoresis[J]. Proteomics, 2006, 6(14): 4166-4175.
[18] Branlard G, Bancel E. Protein extraction from cereal seeds[J]. Methods in Molecular Biology, 2007, 355:15-25.
[19] Wu X, Gong F, Wang W. Protein extraction from plant tissues for 2DE and its application in proteomic analysis[J]. Proteomics, 2014, 14(6): 645-658.
[20] Conlon H E, Salter M G. Plant protein extraction[J]. Methods in Molecular Biology, 2007, 362: 379-383.
[21] Flengsrud R. Protein extraction from green plant tissue[J]. Methods in Molecular Biology, 2008, 425: 149-152.
[22] Wang X C, Shi M J, Lu X L, et al. A method for protein extraction from different subcellular fractions of laticifer latex in Hevea brasiliensis compatible with 2-DE and MS[J]. Proteome Science, 2010, 8(1): 35.
[23] Wang D Y, Wang H Y, Han B, et al. Sodium instead of potassium and chloride is an important macronutrient to improve leaf succulence and shoot development for halophyte Sesuvium portulacastrum[J]. Plant Physiology and Biochemistry, 2012, 51(1): 53-62.
[24] Yi X, Sun Y, Yang Q, et al. Quantitative proteomics of Sesuvium portulacastrum leaves revealed that ion transportation by V-ATPase and sugar accumulation in chloroplast played crucial roles in halophyte salt tolerance[J]. Journal of Proteomics, 2014, 99: 84-100.
[25] Wang W, Scali M, Vignani R, et al. Protein extraction for two-dimensional electrophoresis from olive leaf, a plant tissue containing high levels of interfering compounds[J]. Electrophoresis, 2003, 24(14): 2369-2375.
[26] Jin X, Zhu L, Tao C, et al. An improved protein extraction method applied to cotton leaves is compatible with 2-DE and LC-MS[J]. BMC Genomics, 2019, 20(1): 285.
[27] Delgado E, Valverde-Quiroz L, Lopez D, et al. Characterization of soluble glandless cottonseed meal proteins based on electrophoresis, functional properties, and microscopic structure[J]. Journal of Food Science, 2019, 84(10): 2820-2830.
[28] Akyüz A, Ersus S. Optimization of enzyme assisted extraction of protein from the sugar beet (Beta vulgaris L.) leaves for alternative plant protein concentrate production[J]. Food Chemistry, 2021, 335: 127673.
[29] Wang X C, Chang L L, Wang B C, et al. Comparative proteomics of Thellungiella halophila leaves from plants subjected to salinity reveals the importance of chloroplastic starch and soluble sugars in halophyte salt tolerance[J]. Molecular and Cellular Proteomics, 2013, 12: 2174-2195.
[30] Aiello D, Siciliano C, Mazzotti F, et al. Protein extraction, enrichment and MALDI MS and MS/MS analysis from bitter orange leaves (Citrus aurantium)[J]. Molecules, 2020, 25(7): 1485.
[31] 李肖芳, 韓和平, 王旭初, 等. 適用于鹽生植物的雙向電泳樣品制備方法[J]. 生態學報, 2006, 26(6): 1848-1853.
責任編輯:崔麗虹

