下調AQP-4 對腦缺血再灌注損傷模型大鼠的干預效果及作用機制研究
惠超杰李文輝曹立新慕莉蓉
(1.青海大學附屬醫院神經外科,西寧 810001; 2.青海大學附屬醫院干部保健科,西寧 810001)
大腦是人體對缺氧最為敏感的器官,腦組織缺血的情況下會導致大腦局部組織及其功能的損害,損害的程度大多數和缺血時間的長短以及殘存血流量的多少有著一定的關聯[1]。 短期的不完全缺血只會引起可逆性的損害,長時間的完全缺血或嚴重性缺血會引起梗死,組織學病變下最明顯的組織學變化是腦水腫以及細胞的壞死[2]。 腦缺血在一定時間后恢復血供,其功能不但不會出現恢復,反而會出現更加嚴重的腦功能障礙,該癥狀被稱之為腦缺血-再灌注損傷[3]。 腦缺血-再灌注損傷是一個包括花生四烯酸代謝障礙在內的一種多因素參與的較為復雜的病理過程,其中包括了缺血期的原發性損傷和再灌注期的繼發性損傷[4]。 本研究中建立大鼠腦缺血再灌注損傷模型,靶向調控AQP-4,旨在探究下調AQP-4 對腦缺血再灌注損傷模型大鼠的干預效果及作用機制。
1 材料和方法
1.1 實驗動物
選取40 只清潔級SD 健康雄性大鼠購自廣州賽業百沐生物科技有限公司[SCXK(粵)2020-0055],大鼠飼養在青海省大學附屬醫院[SYXK(粵)2020-0242],體重210~243 g,平均(226.5±13.2)g。 在12 h 光照,濕度45%~55%,溫度25℃環境下喂養大鼠一周。 本研究通過我院倫理委員會批準((2020)年倫審(45)號),且遵守3R 原則進行。
1.2 主要試劑與儀器
兔抗大鼠AQP-4 抗體(Hyclone 公司;貨號:PAB28892);大鼠抗大鼠IL-1β、IL-6、TNF-α 抗體( Selleck 公司; 貨號: ATA31401; FNab04283;ATA38860);大鼠抗兔BMP4、P-Smad 抗體(Gibco公司;貨號:FNab00919;H00004091-B01P);Na+、Pdp 試劑盒(南京建成生物工程研究所;貨號:CKE10708;FT-P91045 T)。
1.3 實驗方法
1.3.1 造模及分組干預
隨機選取10 只大鼠作為本文研究正常組,不做任何處理。 其余30 只大鼠建立腦缺血再灌注損傷模型:對大鼠進行麻醉干預后固定,頸中皮膚剪開,將頸內、外動脈、左側頸總動脈暴露于手術視野之中并分離,結扎頸外動脈、翼腭窩。 使用線栓對頸總動脈遠端切口至頸內動脈2 cm 處進行穿線,對腦組織中動脈近端血流進行阻塞,2 h 后去除線栓并再灌注1 d。 將30 只腦缺血再灌注損傷大鼠隨機分為模型組、上調AQP-4 組、下調AQP-4 組各10 只,上調 AQP-4 組大鼠尾部靜脈注射30 mg/kg agoAQP-4,下調AQP-4 組大鼠尾部靜脈注射30 mg/kg antagoAQP-4,正常組、模型組大鼠尾部靜脈注射等量生理鹽水。
1.3.2 大鼠腦組織含水量測定
選取相同時間點各組各1 只大鼠,處死后提取完整腦部,分批處死,切除前端的嗅球以及后部的小腦和腦干,隨后沿大腦的正中線切開,提取左側的半腦組織,使用電子分析天平對半腦組織進行稱量濕重,稱重后記錄,隨后防止紅外線干燥箱內進行烘干,直至恒重,干重后再次進行測量記錄并進行計算,計算公式為:腦組織含水量=(濕重-干重)/濕重×100%。
1.3.3 大鼠學習記憶能力檢測
提前準備高50 cm、直徑150 cm 的圓形水池,在水池內標注4 個點位,標注好之后注入半池溫水,水溫為25℃。 隨后在水池中央內放入高30 cm、直徑10 cm 的平臺。 分別于已標記的4 處點位在造模成功后1 周后將大鼠置于水中,統計各組大鼠自如水點游至預置平臺時間,將120 s 內未游至平臺的大鼠引至平臺之上,將潛伏期記為120 s,大鼠在平臺上停留30 s 之后,再將其放置其他不同入水點進行重新測試。 所有大鼠均連續測試4 d,在第5 天時將平臺撤除,將大鼠從入水點放至水中,記錄60 s 以內大鼠穿越平臺的次數。
1.3.4 制作標本和HE 染色
標本制作:取各組大鼠尾部靜脈血2 mL,離心處理15 min 后分離上清液,放置-80℃環境下保存待測。 各組大鼠麻醉處死,提取大鼠海馬區組織,固定浸泡至4%甲醛中,于24 h 后行常規石蠟包埋以及連續切片。
HE 染色:將切片烤干后,進行包埋脫蠟處理,處理后順序置入不同濃度的乙醇中個復水3 min。隨后使用蘇木精染色15 min 后進行清洗,清洗3 次后使用鹽酸乙醇分化處理30 s,充分清洗后使用1%伊紅進行染色,使用乙醇進行脫水處理后進行脫蠟處理,封片后使用顯微鏡進行觀察。
1.3.5 各組大鼠TNF-α、IL-1β 水平檢測
使用散射比濁法檢測TNF-α、IL-1β 水平:根據待檢驗TNF-α、IL-1β 中提取的血清樣品在凝固的過程中發生變化的散射光確定檢測,在光探檢測器為九十度直角的單色光源中向血清樣本加凝血激活劑,在樣品凝塊的過程中,散射光的強度會慢慢增加,當血清樣本完全凝固后,光探測器會發生變化,會送到檢測器上處理并且描出凝固曲線后檢測TNF-α、IL-1β 的變化。
1.3.6 Na+、P-dp 含量檢測
大鼠處死后取腦組織,去掉嗅球、小腦和地位腦干,在冰上將大腦組織按照1 ∶9的生理鹽水制成10%的組織均漿進行離心處理,離心后提取上清液隨后使用試劑盒測定,測定時嚴格按照試劑盒說明書進行。
1.3.7 AQP-4、BMP4、P-Smad 表達檢測
使用Western blot 法檢測AQP-4、BMP4、P-Smad表達:首先使用PBS 緩沖液對標本進行沖洗,隨后裂解30 min,裂解后測定其蛋白濃度。 取20 μg 蛋白質進行電泳,電泳的同時加入蛋白緩沖液,10 min后把電轉膜放置到濃度為10%的牛奶中進行浸泡,常溫環境下封閉2 h。 封閉后結合一抗孵育1 d,第2 天取出后使用TBST 液進行沖洗,隨后結合二抗。1 h 后進行清洗、顯色,對蛋白AQP-4、BMP4、PSmad 表達進行檢測。
1.4 統計學方法
使用SPSS 20.0 軟件分析。 計量資料使用平均數±標準差(±s)進行描述,兩組間比較進行獨立樣本t檢驗;計數資料以%表示,兩組間比較進行χ2檢驗,多組對比行聯合假設檢驗(F檢驗)檢驗,以P<0.05 表示差異具有統計學意義。
2 結果
2.1 大鼠學習記憶能力比較
如表1 所示,與正常組比較,其他三組大鼠各時間點逃避潛伏期較長、穿越平臺次數較低(P<0.05);與模型組和上調AQP-4 組相比,下調AQP-4組大鼠各時間點逃避潛伏期較短、穿越平臺次數高(P<0.05)。
表1 各組大鼠學習記憶能力比較(±s,n=10)Table 1 Comparison of learning and memory abilities of rats in each group
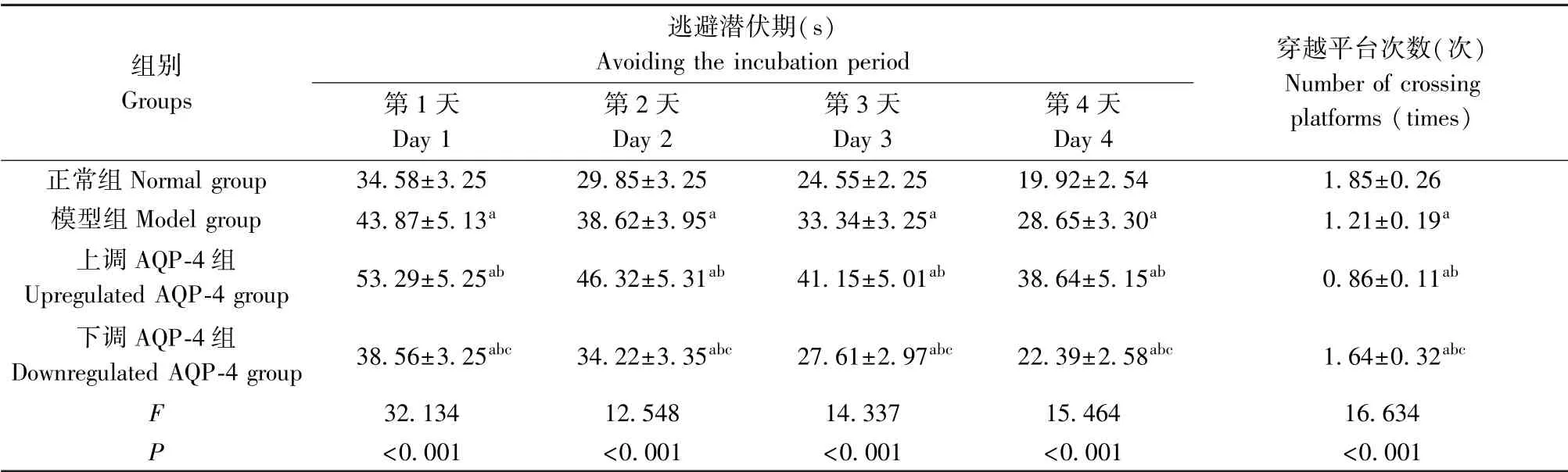
表1 各組大鼠學習記憶能力比較(±s,n=10)Table 1 Comparison of learning and memory abilities of rats in each group
注:與正常組相比,aP<0.05;與模型組相比,bP<0.05;與上調AQP-4 組相比,cP<0.05。Note. Compared with normal group, aP<0.05. Compared with model group, bP<0.05. Compared with the upregulated AQP-4 group, cP<0.05.
組別Groups逃避潛伏期(s)Avoiding the incubation period第1 天Day 1第2 天Day 2第3 天Day 3第4 天Day 4穿越平臺次數(次)Number of crossing platforms (times)正常組Normal group 34.58±3.25 29.85±3.25 24.55±2.25 19.92±2.54 1.85±0.26模型組Model group 43.87±5.13a 38.62±3.95a 33.34±3.25a 28.65±3.30a 1.21±0.19a上調AQP-4 組Upregulated AQP-4 group 53.29±5.25ab 46.32±5.31ab 41.15±5.01ab 38.64±5.15ab 0.86±0.11ab下調AQP-4 組Downregulated AQP-4 group 38.56±3.25abc 34.22±3.35abc 27.61±2.97abc 22.39±2.58abc 1.64±0.32abc F 32.134 12.548 14.337 15.464 16.634 P<0.001 <0.001 <0.001 <0.001 <0.001
2.2 各組大鼠腦組織病理HE 染色圖
如圖1 所示,正常組大鼠腦組織細胞排列規則,結構完好,細胞核較為清晰。 模型組與上調AQP-4組腦組織細胞排列順序錯亂,細胞核出現破裂情況,并且伴隨著水腫的存在,炎癥細胞入侵。 下調AQP-4 組大鼠腦子細胞排列較為規則,細胞核破裂情況、水腫、炎癥入侵情況較輕。
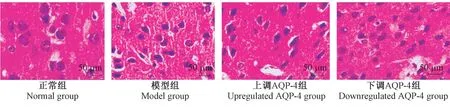
圖1 各組大鼠腦組織病理HE 染色圖Figure 1 HE staining of the pathological brain tissue of rats in each group
2.3 各組大鼠神經功能和腦組織含水量對比
如表2 所示,與正常組相比,模型組、上調AQP-4 組、下調AQP-4 組神經功能評分上升,腦組織含水量增多(P<0.05);與模型組和上調AQP-4 組相比,下調AQP-4 組神經功能評分下降,腦組織含水量減少(P<0.05)。
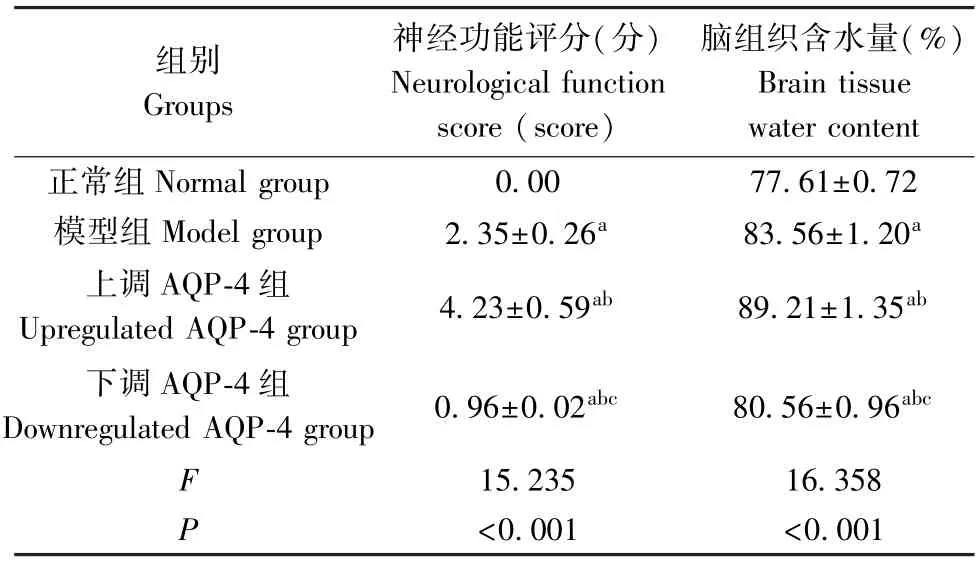
表2 各組大鼠神經功能評分和腦組織含水量對比( x-±s,n=10)Table 2 Comparison of nerve function score and brain tissue water content of rats in each group
2.4 各組大鼠TNF-α、IL-1β 水平比較
如表3 所示,與正常組比較,其他三組大鼠TNF-α、IL-1β 水平升高(P<0.05);與模型組和上調AQP-4 組相比,下調AQP-4 組大鼠TNF-α、IL-1β 水平下降(P<0.05)。
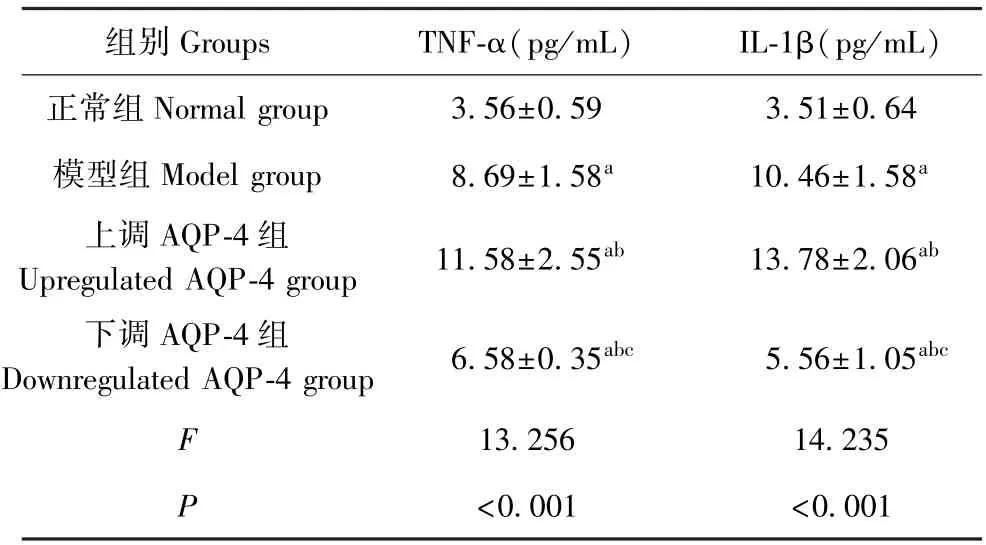
表3 各組大鼠TNF-α、IL-1β 水平比較( x-±s,n=10)Table 3 Comparison of TNF-α and IL-1β levels in each group
2.5 各組大鼠AQP-4、BMP4、P-Smad 表達比較
如表4、圖2 所示,與正常組比較,其他三組大鼠AQP-4 表達上升、BMP4、P-Smad 表達下降(P<0.05);與模型組和上調AQP-4 組相比,下調AQP-4組大鼠AQP-4 表達下降、BMP4、P-Smad 表達上升(P<0.05)。

圖2 AQP-4、BMP4、P-Smad 表達Western blot 蛋白圖Note. A, Normal group. B, Model group. C, Upregulated AQP-4 group. D, Downregulated AQP-4 group.Figure 2 Western blot protein expression ofAQP-4, BMP4 and P-Smad
表4 各組大鼠AQP-4、BMP4、P-Smad 表達比較(±s,n=10)Table 4 Comparison of expressions of AQP-4, BMP4 and P-Smad in each group
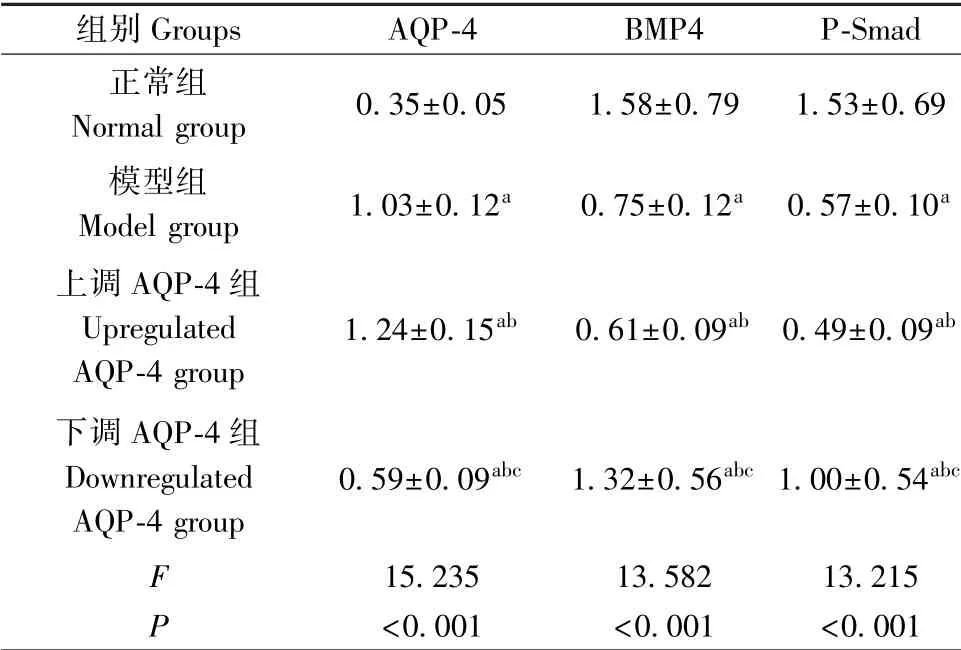
表4 各組大鼠AQP-4、BMP4、P-Smad 表達比較(±s,n=10)Table 4 Comparison of expressions of AQP-4, BMP4 and P-Smad in each group
注:與正常組相比,aP<0.05;與模型組相比,bP<0.05;與上調AQP-4組相比,cP<0.05。Note.Compared with normal group, aP<0.05. Compared with model group, bP < 0.05. Compared with the upregulated AQP-4 group,cP<0.05.
組別Groups AQP-4 BMP4 P-Smad正常組Normal group 0.35±0.05 1.58±0.79 1.53±0.69模型組Model group 1.03±0.12a 0.75±0.12a 0.57±0.10a上調AQP-4 組Upregulated AQP-4 group 1.24±0.15ab 0.61±0.09ab 0.49±0.09ab下調AQP-4 組Downregulated AQP-4 group 0.59±0.09abc 1.32±0.56abc 1.00±0.54abc F 15.235 13.582 13.215 P<0.001 <0.001 <0.001
2.6 各組大鼠Na+、P-dp 含量比較
如表5 所示,與正常組比較,其他三組大鼠Na+、P-dp 含量上升(P<0.05);與模型組和上調AQP-4 組相比,下調AQP-4 組大鼠Na+、P-dp 含量下降(P<0.05)。
表5 各組大鼠Na+、P-dp 含量比較(±s,,n=10)Table 5 Comparison of Na+ and P-dp contents in each group

表5 各組大鼠Na+、P-dp 含量比較(±s,,n=10)Table 5 Comparison of Na+ and P-dp contents in each group
注:與正常組相比,aP<0.05;與模型組相比,bP<0.05;與上調AQP-4組相比,cP<0.05。Note. Compared with normal group, aP<0.05. Compared with model group, bP < 0.05. Compared with the upregulated AQP-4 group, cP<0.05
組別Groups Na+(mg/g) P-dp(U/g)正常組Normal group 0.25±0.05 7.51±2.23模型組Model group 1.02±0.12a 12.52±3.59a上調AQP-4 組Upregulated AQP-4 group 1.13±0.15ab 13.54±3.79ab下調AQP-4 組ownregulated AQP-4 group 0.41±0.09abc 8.21±2.21abc F 14.859 20.135 P<0.001 <0.001 D
3 討論
腦出血是目前人類死亡率較高的疾病之一,但該病的發病嚴重機制尚未明確[5]。 當腦缺血-再灌注發生時,不僅會造成腦水腫,還會對機體神經功能造成嚴重的損傷[6]。 截止到目前,臨床眾多學者仍并未將腦缺血再灌注損傷發病機制研究透徹,所以臨床的治療不太理想。 有學者指出,AQP-4 的分布于腦內水分子的運轉有一定的關聯,其對于維護大腦中的水平衡起到了一定的作用。 腦缺血再灌注損傷中AQP-4 呈現異常的表達[7]。 但是目前關于調控AQP-4 表達對腦缺血再灌注損傷干預效果的研究還鮮有報道。
AQP-4 作為一種水通道蛋白,廣泛的存在于中樞神經系統中,其能夠構成膠質細胞和腦脊液以及血管之間的水調節和運輸的重要結構基礎[8]。 臨床研究顯示,AQP-4 的表達與腦脊液的分泌、重吸收、電解質等生理過程密切相關[9]。 大量學者在研究中提到,水通道蛋白是一類存在于所有生命細胞屏障中膜轉移通道的蛋白質,它們能夠容許水分子在細胞和它的周圍環境間運動,其主要分布在腦組織內面向毛細血管內皮細胞、軟腦膜等細胞膜的足突上[10-11]。 本文研究中顯示,腦缺血再灌注損傷大鼠AQP-4 表達異常升高,對其進行下調能夠對大腦提供保護作用,改善腦缺血再灌注損傷大鼠認知功能、神經功能,使學習記憶能力得到提升,由此可見,對大鼠AQP-4 表達進行下調對大腦有著較好的保護作用。
大量臨床研究顯示,腦缺血再灌注損傷與炎癥因子有著一定的關聯,TNF-α、IL-1β 是臨床最常用的檢測因子,對其進行檢測能夠對較為直觀的觀測出腦缺血再灌注損傷的發生和發展[12]。 有臨床研究顯示,腦缺血再灌注損傷時炎癥因子異常表達,對其進行有效的干預能夠對其進行調控,說明炎癥因子和腦缺血再灌注損傷有著密切的關聯[13]。 本文研究中發現腦缺血再灌注損傷大鼠TNF-α、IL-1β水平較高,說明腦缺血再灌注損傷常常伴隨著炎癥反應的發生,與上述表達一致。 本文研究中還發現,下調AQP-4 表達的腦缺血再灌注損傷大鼠TNFα、IL-1β 水平下降,說明下調AQP-4 表達能夠減輕腦缺血再灌注損傷大鼠腦組織的炎癥反應程度,進而達到保護腦組織的作用。
大量研究表明,BMP4/Smad 通路在細胞凋亡、分化等過程中均有所參與,BMP4、Smad 為BMP4/Smad 通路的最主要配體[14]。 目前臨床對BMP4/Smad 通路和AQP-4 表達的相關性尚未有報道。 本文研究中發現,腦缺血再灌注損傷大鼠BMP4、Smad表達較低,下調AQP-4 表達的腦缺血再灌注損傷大鼠BMP4、Smad 表達上調,說明腦缺血再灌注損傷伴隨著腦組織神經細胞凋亡,對AQP-4 表達進行下調,能夠通過BMP4/Smad 通路抑制腦缺血再灌注損傷大鼠腦組組織的自噬和凋亡,對腦組織進行保護。
綜上所述,對腦缺血再灌注損傷模型大鼠進行下調AQP-4 表達,能夠改善大鼠的學習記憶能力、神經功能,減輕腦缺血在灌注損傷大鼠的炎癥反應,出現上述情況的原因可能與調控BMP4/Smad通路有關,為腦缺血再灌注損傷的臨床治療提供了新的研究方向和理論依據。

