酰化黃酮苷類化合物研究進展
鐘朝敏,徐念智,李 兵
(廣西中醫藥大學藥學院,南寧 530200)
黃酮類化合物有多種生物活性,在食品、保健品和化妝品等行業均有廣泛的應用前景。有研究表明黃酮糖苷類化合物經酰化修飾后,其脂溶性和水溶性有明顯提高,通過改變理化性質還能提高其生物利用率[1]。該類化合物具有低毒、高活性等優點。目前,利用特異性酰化來修飾黃酮苷類化合物以提高其穩定性和生物活性越來越引起研究者的興趣。結合現有文獻,本研究總結了酰基化黃酮苷類化合物的國內外研究進展,從酰化結構種類和生物活性方面展開討論,以期為該類化合物的深入研究提供理論基礎和研究思路。
1 酰化黃酮苷類化合物類型及結構特點
酰基化是修飾藥物結構及功能的有力手段,大量研究報道了黃酮類化合物主要是采用酶催化的方法實現酰基化修飾[2]。該類化合物的表面裝飾主要以乙酰基、對香豆基、沒食子酰基等修飾呈現,其中對香豆基的酰基化修飾是最重要的形式[3]。有研究表明[4],花青素酰基化后結構更穩定,與多酚聚集一起可呈現出更藍的花色,促進脂肪及類脂代謝的同時,還增強了抗菌和抗氧化等生物活性。從Afendi等[5]總結的黃酮類物質信息庫發現,酰基化黃酮類化合物主要存在于黃酮苷、黃酮醇類和花青素中,母核結構類型如圖1 所示。本研究主要對乙酰基、咖啡酰基、香豆酰基、沒食子酰基等幾類酰化單元進行歸納。
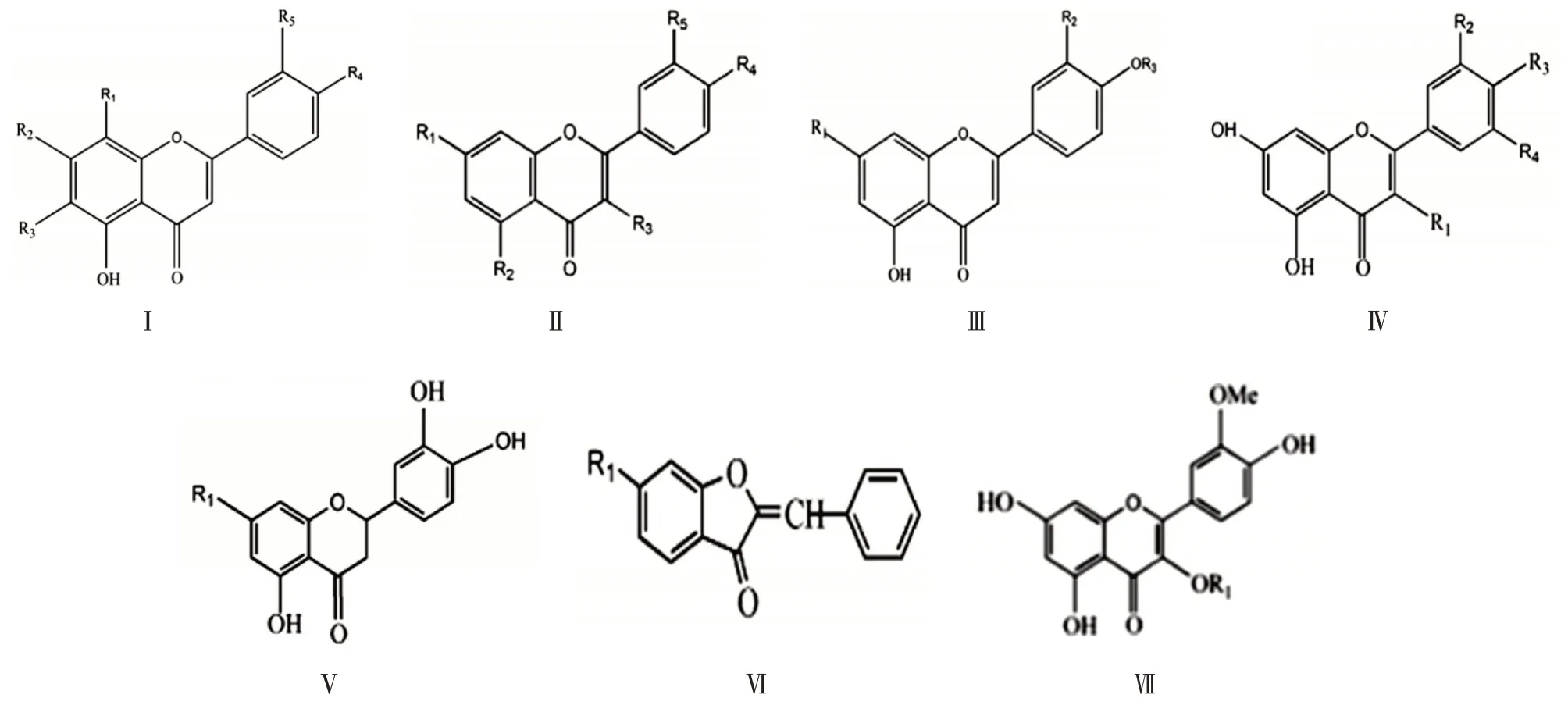
圖1 酰基化黃酮苷母核類型
1.1 乙酰基黃酮苷
Lee 等[6]首次從春黃菊地上部分的甲醇提取物中分離出2 種新的乙酰化黃酮醇二糖苷。雷軍等[7]從點地梅95%乙醇提取物的正丁醇萃取部分分離出4 種乙酰基黃酮醇苷,糖基結構均為吡喃鼠李糖苷。還有大量研究報道了從不同植物中分離得到該類成分,如地稔、狗脊、桑葉等,乙酰基黃酮苷的來源及化學式[6-19]見表1。
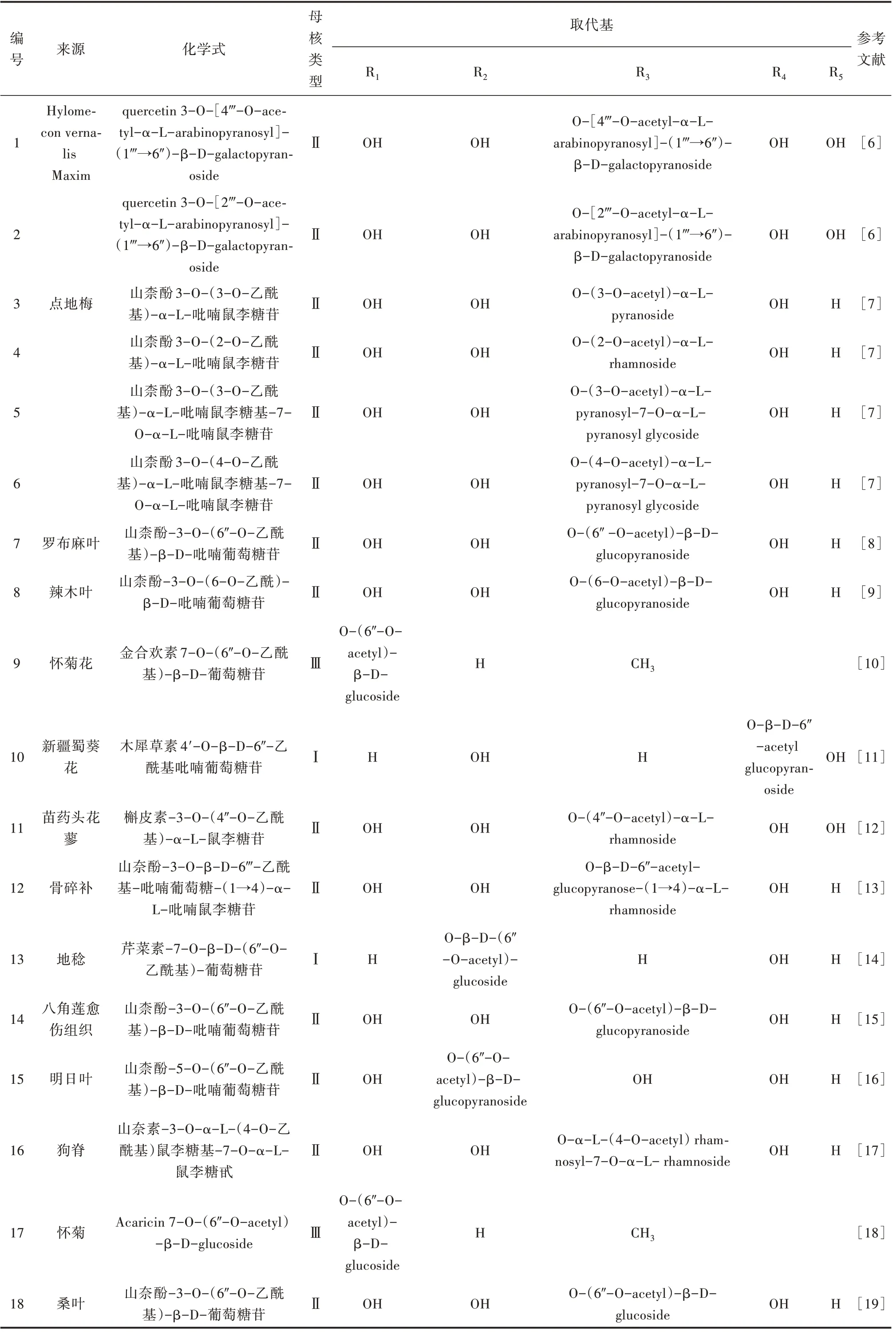
表1 乙酰基類黃酮苷來源及化學式
1.2 咖啡酰基黃酮苷
張潔等[20]、潘爭紅等[21]從裸花紫珠中發現了3種以木犀草素為母核的酰基化黃酮苷。Xi 等[22]從鼠曲草乙酸乙酯部分分離出3 種新的咖啡酰基黃酮醇苷,除母核不一樣外,其糖基、酰基的基團和連接均相同。部分學者還從綠蘿葉、牡荊葉、粘毛蓼、盒果藤等植物中發現此類黃酮苷,咖啡酰基類黃酮苷來源及化學式[20-29]見表2。
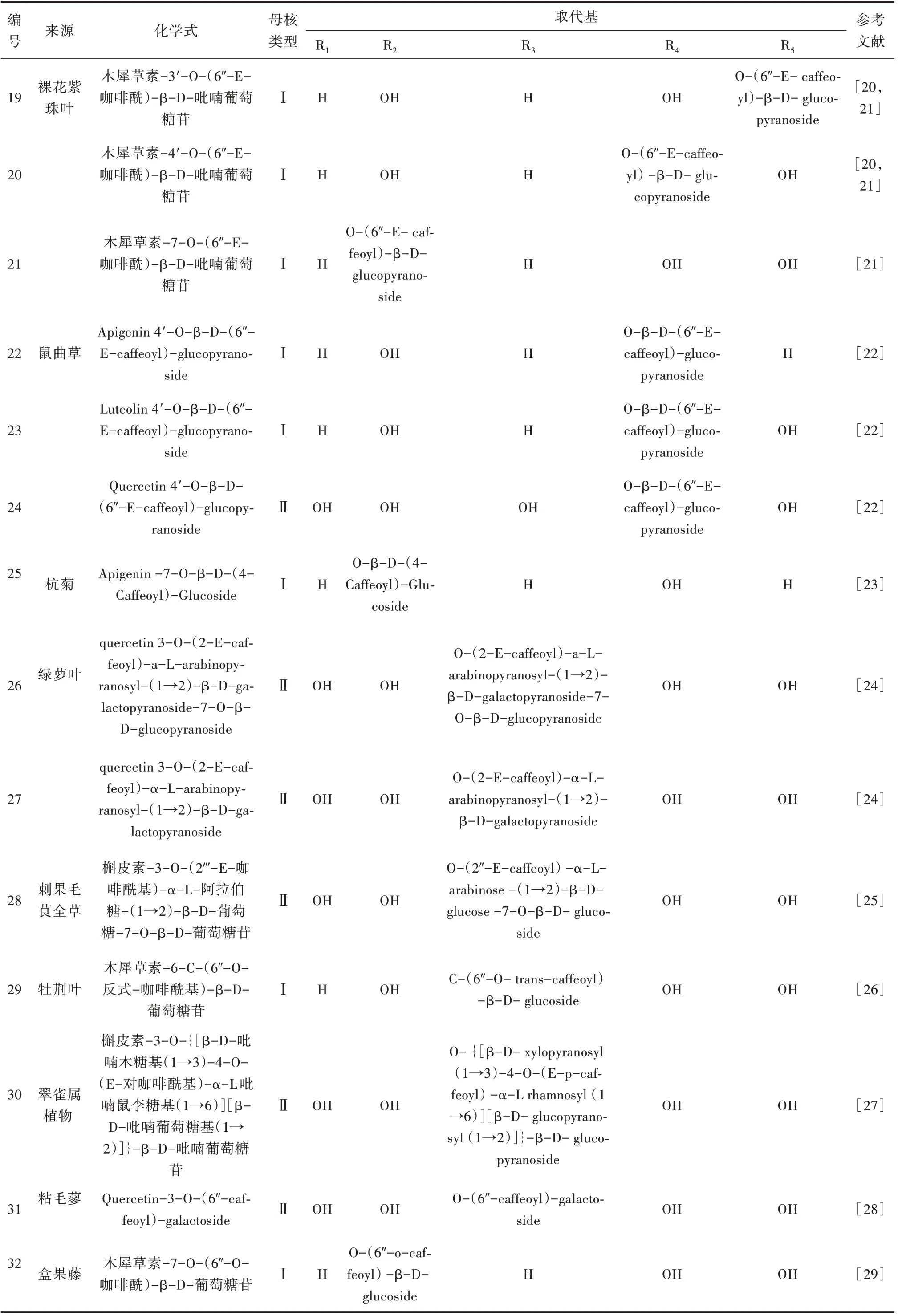
表2 咖啡酰基類黃酮苷來源及化學式
1.3 香豆酰基黃酮苷
李向日等[30]從零陵香的70%乙醇提取物中發現一種新的酰化黃酮四糖苷成分,命名零陵香黃酮A。Tian 等[31]、Lu 等[32]從FBT 中分離出3 種新的酰基糖苷黃酮化合物,包括2 種槲皮素酰基糖苷和1 種山奈酚酰基糖苷,分別命名為茶黃素苷E、茶黃素苷F、茶氨酸氨基糖苷A。大量研究發現,該類成分還存在于蜀葵花、地錦草、月季花等植物中,香豆酰基類黃酮苷來源及化學式[30-53]見表3。

表3 香豆酰基類黃酮苷來源及化學式
1.4 阿魏酰基黃酮苷
潘爭紅等[21]從裸花紫珠葉的95%乙醇提取物中分離出一種木犀草素-7-0-(6″-E-阿魏酰)-β-D-吡喃葡萄糖苷。吳碧靈等[25]從刺果毛茛全草的乙醇提取物分離得到槲皮素-3-O-(2?-E-阿魏酰基)-β-D-槐糖-7-O-β-D-葡萄糖苷。師帥等[54]從金蓮花體積分數為60%的乙醇溶液提取物中分離得到一個apigenin-8-C-(2″-O-feruloyl)-β-D-glucoside。阿魏酰基黃酮苷相應的植物來源及化學式[21,25,36,38,43,51,54-56]見表4。

表4 阿魏酰基類黃酮苷來源及化學式
1.5 沒食子酰基黃酮苷
李夢云[57]首次從水蓼全草中分離出一種酰基化黃酮苷,結構鑒定為槲皮素-3-O-(2″-O-沒食子酰基)葡萄糖苷。石娟等[58]從鹿銜草的全草中發現一種沒食子酰黃酮苷(2″-O-沒食子酰基金絲桃苷)。沒食子酰基黃酮苷相應的植物來源及化學式[12,38,40,46,57-64]見表5。
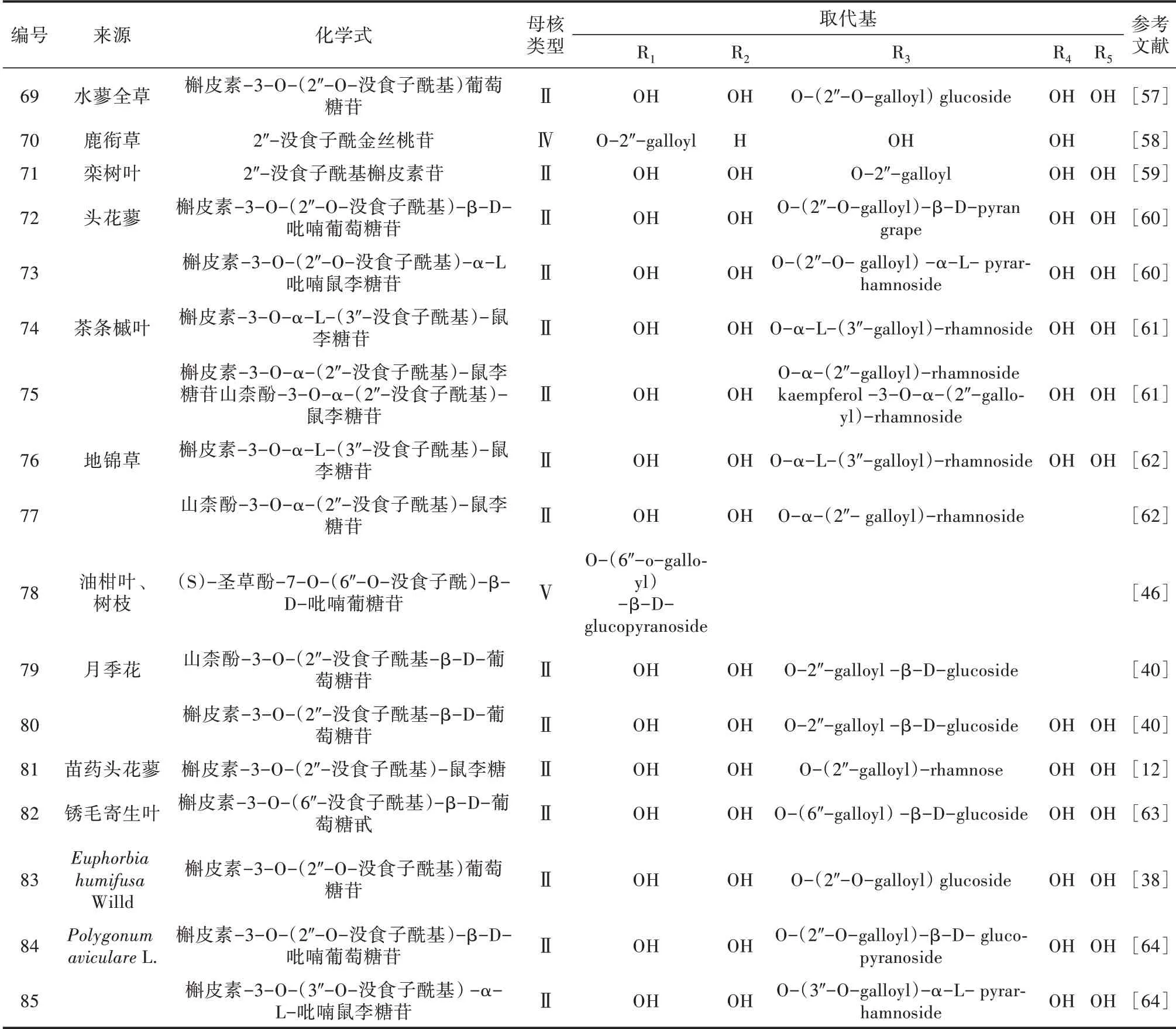
表5 沒食子酰基類黃酮苷來源及化學式
1.6 其他類型的酰基黃酮苷
陳月紅[65]從金盞銀盤中鑒定出一種丙酰基橙酮苷,其結構為Z-6-O-(6″-丙酰基-β-D-吡喃葡萄糖基)-6,7,3′,4′-四羥基橙酮。楊小鳳等[66]從欒樹種子中分出2 種新的酰基化黃酮五糖苷,分別命名為欒樹酮A、欒樹酮B。還有許多科研者研究報道了該類化合物,相應產物來源及化學結構[9,55,65-74]見表6。

表6 其他酰基類黃酮苷來源及化學式
2 酰化黃酮苷的生物活性
2.1 抗病毒活性
黃酮類化合物是天然產物中抗病毒的典型代表,大量的研究表明該類化合物具有廣泛的抗病毒活性,主要涉及抗HIV、抗流感病毒、抗HBV、抗HCMV 等。酰化黃酮苷類化合物在抗突變、抗增殖、抑制癌細胞入侵等方面具有較好的效果,近年來受到人 們 的 普 遍 關 注。Tian 等[75]在CamellikaempferosideA 存在或不存在的情況下,以MTT 測定MCF-7和丙二醛-甲基溴-231 細胞的活性,結果表明,CamellikaempferosideA 對惡性細胞MCF-7 和MDAMB-231 細胞的生長有相似的抑制作用。田瑛[76]首次發現從地錦草抗HBV 活性部位得到的2 種酰基化黃酮單糖苷具抗HBV 活性,通過研究活性部位中酰基化黃酮苷與體外抗HBV 活性的影響,發現黃酮類化合物結構中的糖基數量及母核結構與其抗HBV活性有密切關系,表現為黃酮單糖苷>黃酮二糖苷,芹菜素>木犀草素>槲皮素;而經酰基化黃酮糖苷有較好的體外抗HBV 活性,表現為沒食子酰基>阿魏酰基>香豆酰基。

續表3
2.2 抗氧化活性
植物中的黃酮類化合物,可有效清除機體內氧自由基,防止細胞退化和衰老,是一種廣泛存在的抗氧化劑,也是黃酮類化合物重要的生物活性。有學者研究了黃酮類化合物的體外抗氧化功能,發現其對自由基、超氧陰離子、過氧化氫等有害物質均有較好的清除效果[77]。陳月紅[65]對金盞銀盤中得到的丙酰基橙酮苷進行抗氧化活性方面的研究,發現其在濃度為0.025~0.100 mg/mL 時對OH-的清除率較高,且清除率與濃度呈正相關。酚羥基是黃酮類化合物清除自由基的主要活性基團,研究發現,在一定程度上增加酚羥基的數目,抗氧化活性也會相應增強,分子中的羥基數目、位置與活性有直接關系。Manir 等[78]通過1,1-二苯基-2-苦基肼(DPPH)自由基測量,比較4 種槲皮素酰基糖苷Camelliaquecetiside A-D的抗氧化性能,發現Camelliaquecetiside A清除DPPH 自由基的能力最強,IC50=(19.8±0.1)μmol/L。李夢云[57]對水蓼中分離出的槲皮素-3-O-(2″-O-沒食子酰基)葡萄糖苷進行清除DPPH 自由基測試,發現其抗氧化能力強于陽性對照的維生素C,說明水蓼可以作為一種較好的天然抗氧化劑。
2.3 抗炎活性
有研究報道,黃酮類化合物發揮抗炎作用的主要場所在巨噬細胞,該類化合物通過抑制核轉錄因子κB(nuclearfactorκB,NF-κB)信號通路和下調促炎標記物的表達來抑制巨噬細胞的炎性反應[79]。張靜[72]利用LPS 誘導的BV-2 小膠質細胞活化模型,對從夏至草中分離得到的山奈酚和槲皮素酰化黃酮苷進行體外抗炎活性篩選,使用NO 試劑盒檢測一氧化氮(NO)的含量,發現山奈酚戊二酰基糖苷能不同程度地抑制脂多糖誘導的BV-2 細胞釋放NO。
2.4 抗菌活性
李夢云[57]通過對水蓼中分離出的槲皮素-3-O-(2″-O-沒食子酰基)葡萄糖苷進行抑菌活性測試,發現其對金黃色葡萄球菌最小抑菌濃度最小,為31.2 μg/mL,表明抑菌效果最好,當槲皮素上3-OH基團被糖苷取代后抑菌活性有所下降且對不同的細菌影響效果不同,進一步證明了水蓼具有抑菌活性的物質基礎。Gatto 等[80]的研究發現,3-O-acylquercetines 在100 mg/mL 時具有較廣的抗菌譜,對選定的革蘭氏陽性菌株(金黃色葡萄球菌、伊凡諾氏利斯特氏菌等),革蘭氏陰性菌株(大腸桿菌、福氏志賀氏菌、鼠傷寒沙門氏菌等)和酵母菌(白色念珠菌、光滑念珠菌)均有顯著抑制作用,且其抑菌效果和親脂性都比槲皮素好,因此可更好地應用在皮膚或黏膜上的抑菌治療。2005 年,趙海譽[81]發現北葶藶子中的芐基芥子油有廣譜抗菌作用,且對酵母菌等20 種真菌及數10 種其他菌株都表現出抗菌效應。
2.5 抗補體活性
補體系統是先天免疫的重要組成部分,在調節獲得性免疫中也起著重要作用,二酰基化黃酮苷對補體系統有顯著的抑制效果。2012 年,Xi 等[22]基于邁耶斯的改進方法,從補體的經典途徑出發,研究鼠曲草中的咖啡酰基黃酮化合物對補體的抑制作用,發現黃酮類化合物主要以劑量依賴的方式表現出補體調節特性。黃酮醇-糖-咖啡酰構型的4 種酰化黃酮醇苷均顯示出很強的活性,其中木犀草素4′-Oβ-D-(6″-E-咖啡酰)-吡喃葡萄糖苷具有最高的抗補體活性,其IC50為(0.045±0.005)mg/mL。這是首次對木犀草素抗補體活性進行報道,同時也初步證明了該植物是一種有效的補體抑制劑。孫連娜等[82]公布了酰化黃酮苷化合物及其在制備補體抑制劑藥物上的發明,該發明經體外試驗證實了鼠曲草中4 種酰化黃酮苷在對補體系統的經典途徑激活所引發的細胞溶血均有抑制作用,且各單體化合物的活性比鼠曲草總提取物的活性強,表明酰化黃酮苷是一類很好的補體抑制劑,且其有效濃度低,可作為活性成分用來制備新型的抗補體藥物。
2.6 其他生物活性
隨著分離提取及純化技術的提升,酰基化黃酮的生物活性研究得以更加深入,除以上歸納的作用,該化合物還有很多種生物活性,如抑制乙醇脫氫酶活性、預防骨骼肌萎縮、抑菌、降血糖血脂和減肥等。HMG-CoA 還原酶是肝細胞合成膽固醇過程中的限速酶,催化生成甲羥戊酸(MVA),抑制HMG-CoA 還原酶從而阻礙膽固醇的合成。Lu 等[83]通過分子對接模擬分析了AGFs 及其代謝產物對α-葡萄糖苷酶和HMG-CoA 還原酶的抑制能力,結果表明,AGFs的抑制活性顯著受到酰基結構、糖基數目和構象的影響,并發現從茯磚茶中分離的酰基化合物對α-葡萄糖苷酶和HMG-CoA 還原酶具有很強的抑制活性,其中Camelliquercetiside F 抑制HMG-CoA 還原酶活性最高,與含酰基的代謝物相比,不含酰基的代謝物一般抑制能力較低,分析原因可能是酰基結構參與穩定疏水力的形成,提高了生物活性化合物的生物活性。2020 年,Hsieh 等[84]研究發現Teaghrelins與ghrelin 一樣,都是通過下調Atrogin-1andMu RF-1泛素E3 連接酶的表達量以減緩地塞米松引起的肌管直徑減小,表明其對骨骼肌萎縮有保護作用。
3 小結與展望
近年來,黃酮類化合物廣泛地應用于醫藥、食品等行業中,然而,由于該類化合物分子結構導致其溶解性差,生物利用率受到限制。因此,在不同植物來源的黃酮類化合物的基礎上,對該類化合物進行酰基化修飾,不僅可以改變其溶解性,促進脂肪及類脂代謝,提高其生物利用度,而且還能增加該類化合物的抗菌及抗氧化等生物活性。隨著酰基化黃酮苷的進一步研究,未來將會有更多的成分及功效被發現。通過查閱并分析國內外的相關文獻,發現酰化黃酮苷類化合物在天然植物中廣泛分布,目前該類產物的植物來源已有大量報道,但在分離提取以及生物活性方面的研究報道仍較少,期待今后有更多相關領域的研究。

