4種天然物質抗氧化能力的研究
張雯雯,張艷妮,楊麗榮,張宏博,段艷,郭文瑞
(1.內蒙古農業大學 食品科學與工程學院,內蒙古 呼和浩特 010000;2.內蒙古自治區食品檢驗檢測中心,內蒙古 呼和浩特 010000;3.內蒙古農業大學 獸醫學院,內蒙古 呼和浩特 010000)
肉品因富含脂肪、蛋白質等營養物質,易發生氧化,嚴重影響其色澤、質構、風味及營養價值,進而造成經濟損失。近些年來,市場上抗氧化劑的使用越來越多,但經研究證明,常用的合成抗氧化劑可誘發腸胃病,甚至是導致癌癥,天然抗氧化物相對安全性較高,因此深受廣大消費者的青睞[1]。目前,常用的天然抗氧化劑有多酚、維生素、多糖、皂苷四大類,其中多酚類抗氧化物研究較多,主要因其苯環上連接的多羥基結構經相關反應后發揮抗氧化作用,如茶多酚、單寧等[2]。常用的維生素類抗氧化劑如維生素E(vitamin E,VE)、維生素C(vitamin C,VC),通過與其他物質的相互作用及相關基因調控脂類代謝[3]。蝦青素是一種類胡蘿卜素,存在于各種海洋生物中,它是一種生物抗氧化劑,比維生素E和其他類胡蘿卜素具有更強的自由基清除活性[4]。皂苷是苷元為三萜或螺旋甾烷類化合物的一類糖苷,皂苷主要通過清除自由基、減少細胞損傷、調節氧化應激等機制達到抗氧化的效果[5]。多糖是超過10個單糖組成的聚合糖高分子碳水化合物,多糖的抗氧化作用主要體現在提高機體抗氧化酶活性、清除體內自由基、抑制脂質過氧化、保護生物膜等方面[3-6]。
目前,天然抗氧化物的研究已經比較深入,越來越多研究者通過研究抗氧化物的抗氧化能力,以期將其聯合使用,從而使其各有效成分通過多靶點、多環節綜合發揮其功效。經陳雪[7]研究,在對DPPH自由基的清除能力測定中,南瓜多糖和人參皂苷復配物要強于單一組。本試驗選擇具有多酚結構的單寧、人參皂苷、枸杞多糖、蝦青素等4種天然抗氧化物在不同濃度下對DPPH、ABTS+、羥基、超氧陰離子等自由基清除能力、金屬離子螯合能力、總還原能力、脂質抗氧化能力的影響,為天然抗氧化劑的復配應用提供理論依據。
1 材料與方法
1.1 材料與試劑
單寧提取物(純度99%)、人參皂苷提取物(純度80%)、枸杞多糖提取物(純度50%)、蝦青素提取物(純度10%):西安瑞林生物科技有限公司;1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-picrylhydrazyl,DPPH)、2,2-偶氮二(2-甲基丙基醚)二鹽酸鹽[2,2'-azobis(2-methylpropionamidine)dihydrochloride,AAPH]、2,2’-聯氮-雙-3-乙基苯并噻唑啉-6-磺酸[2,2'-azino-bis(3-ethylbenzothiazoline-6-sulfonic acid),ABTS]、羅恩試劑、硫酸亞鐵、30%過氧化氫(均為分析純):天津市風船化學試劑科技有限公司;三羥甲基氨基甲烷鹽酸鹽(Tris-HCl)、VC、鄰二氮菲(均為分析純):國藥集團化學試劑有限公司;2-硫代巴比妥酸(分析純):上海科豐實業有限公司;鄰苯三酚(分析純):天津市福晨化學試劑廠。
1.2 儀器與設備
SYNERGY H 1酶標儀(96孔板):雷康恒泰(北京)商貿有限公司;DHP-9802電熱恒溫水浴鍋:北京長安科學儀器廠;AL204萬分之一電子天平:梅特勒-托利多儀器有限公司;JC-HW-2渦旋振蕩器:北京優晟聯合科技有限公司。
1.3 方法
1.3.1 樣品制備
單寧、人參皂苷、枸杞多糖、蝦青素分別配制濃度為 5 mg/mL 的溶液,并分別稀釋為 0.2、0.4、0.6、0.8、1.0 mg/mL,作為待測樣品備用。
1.3.2 DPPH自由基清除能力的測定
參考Kop等[8]的研究方法,取4 g DPPH用無水乙醇定容至100 mL容量瓶內,配制濃度為0.04 mg/mL的DPPH溶液避光放置備用;取0.1 mL樣品加入到新配制的3.9 mL DPPH溶液中,混勻,在37℃水浴條件下反應60 min,在517 nm處測吸光度,計算公式如下。
DPPH 自由基清除率/%=[1-(A1-A2)/A3]×100
式中:A1為3.9 mL DPPH+0.1 mL樣品的吸光度;A2為3.9 mL乙醇+0.1 mL樣品的吸光度;A3為3.9 mL DPPH+0.1 mL乙醇的吸光度。
1.3.3 ABTS+自由基清除能力的測定
參考孫玉姣等[9]的研究方法,取同等體積的7.4 mmol/L ABTS溶液和2.6 mmol/L K2S2O8溶液,置于100 mL棕色廣口瓶中,混合均勻,于室溫(20℃)靜置12 h~16 h,再用無水乙醇稀釋45倍作ABTS工作液(OD734nm=0.7±0.02)備用。取 0.2 mL 樣品,加入到 0.8 mL ABTS溶液中,振蕩10 s,充分混合后避光靜置6 min,在734 nm處測吸光度為A1,以0.2 mL乙醇代替樣品為空白組,測得吸光度A0,計算公式如下。
ABTS+自由基清除率/%=(1-A1/A0)×100
1.3.4 羥基自由基清除能力的測定
參考王賀等[10]的方法,取樣品2 mL,加入1 mL 0.75 mmol/L鄰二氮菲溶液、2 mL 0.2 mol/L磷酸鹽緩沖鹽溶液(phosphate buffered saline,PBS)(pH7.4),混勻再加入1 mL 0.75 mmol/L硫酸亞鐵溶液、1 mL 0.01%過氧化氫溶液,混勻后在37℃水浴1 h,在536 nm處測吸光度,對照組用蒸餾水代替過氧化氫溶液,空白組用蒸餾水代替樣品,計算公式如下。
羥基自由基清除率/%=(As-Ac)/(Ab-Ac)
式中:As為試驗樣品的吸光度;Ac為對照組的吸光度;Ab為空白組的吸光度。
1.3.5 超氧陰離子自由基清除能力的測定
參考王雅等[11]的研究方法,取2 mL樣品、4 mL 0.05 mol/L Tris-HCl溶液(pH8.2),在25℃水浴加熱20 min;取出后加入60 μL 25 mmol/L鄰苯三酚溶液,充分混勻在25℃水浴加熱5 min;取出后加入200 μL 10 mmol/L鹽酸溶液,終止反應,在325 nm處測吸光度。
超氧陰離子自由基清除率/%=[1-(A1-A2)/A3]×100
式中:A1為60 μL鄰苯三酚+2 mL樣品的吸光度;A2為 60 μL 蒸餾水+2 mL 樣品的吸光度;A3為 60 μL鄰苯三酚+2 mL蒸餾水的吸光度。
1.3.6 金屬離子螯合能力
參考齊佳慧等[12]的研究方法,取0.5mL樣品、0.1mL 10g/LVC溶液、0.1mL4g/L硫酸亞鐵溶液、1mL0.2mol/L氫氧化鈉溶液,混勻后,在37℃水浴靜置20 min;取出后,加入0.2 mL 10%三氯乙酸溶液,靜置10 min,再取0.2 mL上清液,加0.5 mL 1 g/L鄰二氮菲溶液,充分混勻,靜置10 min,在510 nm處測吸光度。用0.5 mL蒸餾水做空白對照,計算公式如下。
金屬離子螯合能力/%=(1-As/Ac)×100
式中:As為樣品的吸光度;Ac為空白樣的吸光度。
1.3.7 總還原能力
參考齊佳慧等[12]的研究方法,將15.2 mL 0.1 mol/L氫氧化鈉溶液和0.68g磷酸二氫鉀混勻后定容至100mL,配制成0.2 mol/L pH6.6的磷酸緩沖鹽溶液。取0.5 mL不同濃度樣品,加入1 mL PBS緩沖液、1 mL 1%鐵氰化鉀溶液,混勻后,在50℃水浴加熱20 min;取出后加入1 mL 10%三氯乙酸溶液充分混勻,終止反應;取1 mL上清液、1 mL蒸餾水、1 mL 0.15%三氯化鐵溶液,混勻后,靜置20 min;在700 nm處測量吸光度,蒸餾水做空白試驗。
總還原能力=A1-A0
式中:A1為樣品的吸光度;A0為空白樣的吸光度。
1.3.8 脂質抗氧化能力
參考孫玉姣等[9]的研究方法,取0.4 mL 10%蛋黃勻漿液,加入0.2 mL樣品,再加入0.2 mL 40 mmol/L AAPH,混勻,37℃溫浴1 h,再加入1 mL 10%三氯乙酸溶液,1 mL 0.67%β-硫代巴比妥酸(2-thiobarbituric acid,TBA)溶液,100μL2mol/L鹽酸,2mL 0.1 mol/L PBS(pH7.4),混勻,95℃水浴 30 min,立即放入冰水浴,冷卻,5 000 r/min離心15 min,取上清液,于532 nm處測吸光度,用蒸餾水做空白試驗。
脂質抗氧化能力/%=(1-A1/A0)×100
式中:A1為樣品的吸光度;A0為空白樣的吸光度。
1.4 數據分析
數據采用spss18.0進行平均值、標準差及主成分分析,采用Excel作圖。
2 結果與分析
2.1 DPPH自由基清除能力
4種天然抗氧化劑DPPH自由基清除能力的變化見圖1。
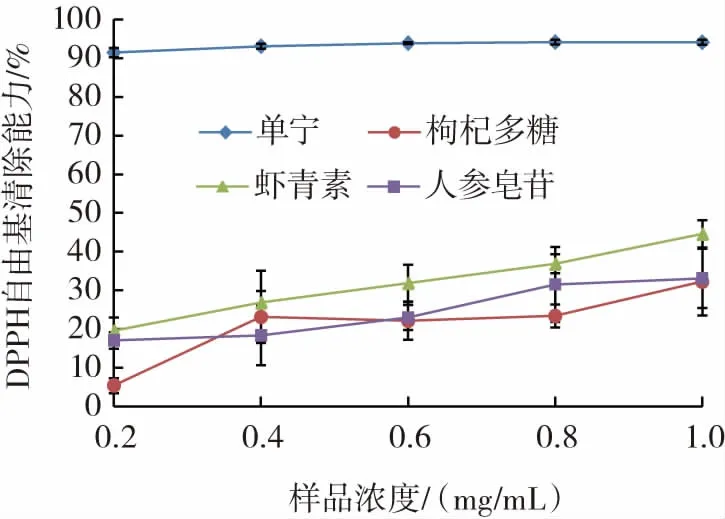
圖1 4種天然抗氧化劑DPPH自由基清除能力的變化Fig.1 Changes in DPPH free radical scavenging ability of four natural antioxidants
DPPH自由基是一種很穩定的以氮為中心的自由基,可表示對羥基、烷基及過氧化自由基抑制作用[13]。如圖1所示,單寧濃度在0.2 mg/mL~1.0 mg/mL時,對DPPH自由基清除能力在90%以上且隨著濃度的增加變化不大,較高于其它3種抗氧化物,可能是由于單寧為多酚類物質,可以更快地從酚或酚陰離子轉移電子到DPPH自由基,形成較強的氫鍵[14]。蝦青素、人參皂苷的DPPH自由基清除能力均隨濃度增高呈上升趨勢,枸杞多糖與人參皂苷在0.4 mg/mL~1.0 mg/mL濃度時,DPPH自由基清除能力差異不明顯,清除能力均在18%~34%之間。結果表明,4種天然抗氧化劑皆對DPPH自由基有清除作用,在0.2 mg/mL~1.0 mg/mL時,單寧清除能力較高。
2.2 ABTS+自由基清除能力
ABTS+自由基清除試驗是測定化合物抗氧化能力的重要方法[15]。4種天然抗氧化劑ABTS+自由基清除能力的變化如圖2所示,

圖2 4種天然抗氧化劑ABTS+自由基清除能力的變化Fig.2 Changes in the ABTS+free radical scavenging ability of four natural antioxidants
單寧濃度在0.2 mg/mL~1.0 mg/mL時,對ABTS+自由基清除能力在81%~86%,變化不明顯,0.6 mg/mL~1.0 mg/mL時人參皂苷的ABTS+自由基清除能力與單寧相近,濃度在 0.2 mg/mL~1.0 mg/mL,單寧的 ABTS+自由基清除能力高于蝦青素組。劉曉培[16]的研究表明單寧純化物具有較強的ABTS+自由基清除能力。人參皂苷及枸杞多糖的ABTS+自由基清除能力隨著濃度的增加呈上升趨勢,單寧濃度在0.2 mg/mL~0.8 mg/mL時,對ABTS+自由基清除能力隨著濃度的增長而上升,蝦青素與枸杞多糖的ABTS+自由基清除能力無明顯差異。結果表明,在0.2 mg/mL~1.0 mg/mL之間4種天然抗氧化劑的ABTS+自由基清除能力為單寧優于其他3種。
2.3 羥基自由基清除能力
4種天然抗氧化劑羥基自由基清除能力的變化見圖3。
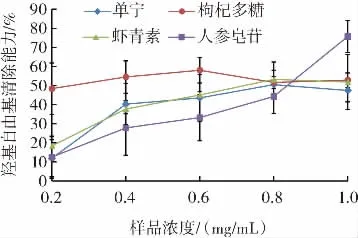
圖3 4種天然抗氧化劑羥基自由基清除能力的變化Fig.3 Changes in the scavenging ability of four natural antioxidant hydroxyl radicals
羥基自由基是活性氧中最活潑的氧自由基[17],也是毒性最大的自由基,是造成生物體損傷的主要因素[18]。如圖3所示,在0.2 mg/mL~0.6 mg/mL之間的枸杞多糖清除羥基自由基的能力較高于蝦青素和人參皂苷,而蝦青素、單寧的羥基自由基清除能力無明顯差異,根據張麗等[19]研究,枸杞多糖具有較強的羥基自由基清除能力。在濃度為0.8 mg/mL時,4種抗氧化物差異不明顯。在樣品濃度為1.0 mg/mL時,人參皂苷的羥基自由基清除能力為75.70%,大于其他3種。根據張馨妍等[20]的研究結果顯示在西洋參總皂苷提取出的6種人參皂苷皆有較強的羥基自由基清除能力。結果表明,0.2 mg/mL~0.6 mg/mL的枸杞多糖及1.0 mg/mL的人參皂苷具有較好的清除羥基自由基的能力。
2.4 超氧陰離子自由基清除能力
4種天然抗氧化劑超氧陰離子自由基清除能力的變化見圖4。
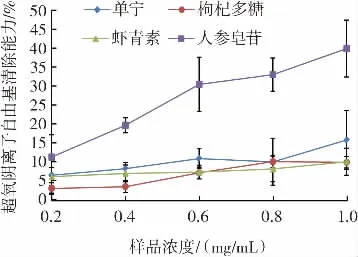
圖4 4種天然抗氧化劑超氧陰離子自由基清除能力的變化Fig.4 Changes in superoxide radical scavenging ability of four natural antioxidants
超氧陰離子自由基是機體內壽命最長的自由基,通常作為自由基鏈式反應的引發劑,產生活性更強的自由基[21]。如圖4所示,濃度在0.4 mg/mL~1.0 mg/mL,人參皂苷對超氧自由基的清除能力高于單寧、枸杞多糖和蝦青素,且濃度增大清除能力呈增長趨勢,即有一定的計量效應。黃文靜等[22]、楊炳偉[23]的研究表明皂苷類對超氧陰離子自由基具有較強的清除能力。單寧、蝦青素以及枸杞多糖的超氧陰離子自由基清除能力無明顯差異。結果表明,在0.2 mg/mL~1.0 mg/mL間人參皂苷對超氧陰離子自由基的清除能力較強。
2.5 總還原能力
4種天然抗氧化劑總還原能力的變化見圖5。
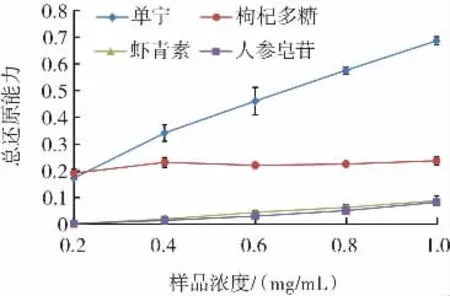
圖5 4種天然抗氧化劑總還原能力的變化Fig.5 Changes in total reducing power of four natural antioxidants
如圖5所示,單寧的總還原能力與其濃度呈正比,具有一定的劑量依賴性,在0.4 mg/mL~1.0 mg/mL,單寧的總還原能力高于枸杞多糖、人參皂苷、蝦青素,根據Zargar等[24]研究,提取于金合歡、尤金妮亞、菩提樹、銀合歡、番石榴等植物樹葉的單寧具有較強的還原性。而枸杞多糖的總還原能力又高于人參皂苷和蝦青素,人參皂苷和蝦青素的總還原能力無明顯差異。結果表明,在0.2 mg/mL~1.0 mg/mL 4種天然抗氧化物的總還原能力:單寧優于枸杞多糖及人參皂苷、蝦青素。
2.6 金屬離子螯合能力
4種天然抗氧化劑金屬離子螯合能力的變化見圖6。
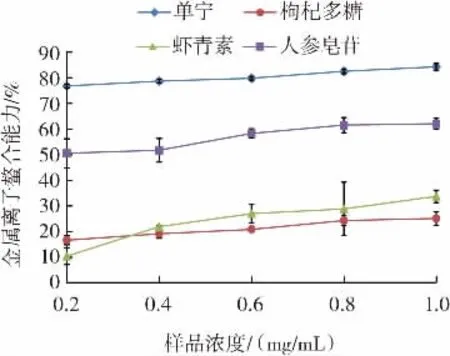
圖6 4種天然抗氧化劑金屬離子螯合能力的變化Fig.6 Changes in metal ion chelating ability of four natural antioxidants
金屬離子在有機體內具有多樣的配位作用和重要的催化作用,當金屬離子與有機配體形成穩定的螯合物后,螯合物可以發揮獨特的生理生化功能[25]。單寧是一種水溶性的多羥基物質,對金屬具有較強的螯合作用[26]。如圖6所示,通過對4種天然抗氧化劑金屬離子螯合能力分析,隨濃度升高4種抗氧化劑螯合金屬離子能力均呈上升趨勢。濃度在0.2 mg/mL~1.0 mg/mL時,單寧金屬離子螯合能力在76%~85%之間,高于枸杞多糖、人參皂苷、蝦青素。人參皂苷金屬離子螯合能力在50%~62%,高于蝦青素和枸杞多糖。蝦青素的螯合能力與枸杞多糖無明顯差異。結果表明,在0.2 mg/mL~1.0 mg/mL間4種天然抗氧化物的金屬離子鏊合能力:單寧優于人參皂苷、蝦青素及枸杞多糖。
2.7 脂質抗氧化能力
4種天然抗氧化劑脂質抗氧化劑能力的變化見圖7。

圖7 4種天然抗氧化劑脂質抗氧化能力的變化Fig.7 Changes in lipid antioxidant capacity of four natural antioxidants
自由基引發脂質過氧化并產生丙二醛,丙二醛可與硫代巴比妥酸縮合形成粉紅色復合物,該復合物在532 nm處有最大吸收峰,當體系加入抗氧化劑后將使該復合物顏色減弱,進而采用分光光度計測定該抗氧化劑的活性[27]。如圖7所示,4種抗氧化物皆隨其濃度增高脂質抗氧化能力呈上升趨勢,濃度在0.2 mg/mL~1.0 mg/mL,單寧脂質抗氧化能力較強且具有良好的量效關系,優于枸杞多糖、人參皂苷及蝦青素。結果表明,在0.2 mg/mL~1.0 mg/mL 4種天然抗氧化物的脂質抗氧化能力:單寧>枸杞多糖>人參皂苷>蝦青素。
2.8 4種天然抗氧化物抗氧化作用主成分分析
為探究4種天然抗氧化物的DPPH自由基、ABTS+自由基、超氧陰離子自由基、羥基自由基、總還原能力、金屬離子螯合能力對抗氧化性貢獻差異及其影響作用大小,得到4種天然抗氧化劑主成分特征值、貢獻率和累積貢獻率,如表1所示。成分得分系數反映抗氧化各指標對主成分影響的相對大小和方向,數值反映原變量對因子影響的大小,正負代表變化方向的差別。4種天然抗氧化物成分得分系數矩陣見表2。

表1 4種天然抗氧化主成分特征值及貢獻率Table 1 Characteristic values and contribution rates of the four natural antioxidant main components
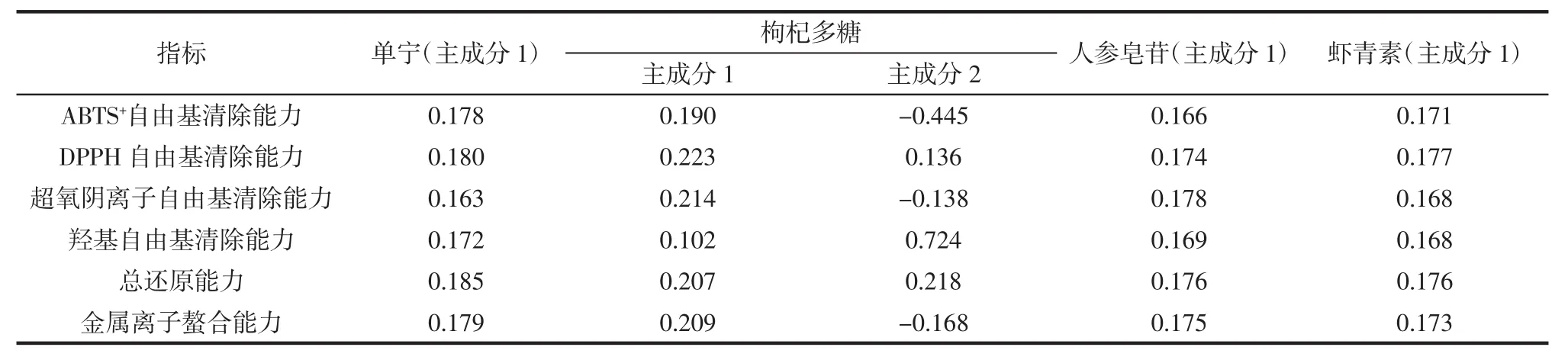
表2 4種天然抗氧化物成分得分系數矩陣Table 2 Matrix of score coefficients of four natural antioxidants
主成分分析(principal component analysis,PCA)目的在于利用原變量間相關性較強的特點,用較少的指標盡可能多地反映原數據信息,且所含信息互不重復,具有更優越的性能[28]。主成分分析中貢獻率越大,說明主成分所包含的原始變量信息越強。單寧的特征值在1以上的一個成分為主成分,貢獻率為89.285%。枸杞多糖特征值在1以上的兩個成分為主成分,累計貢獻率是92.886%,人參皂苷特征值在1以上的1個成分為主成分,貢獻率為92.508%;蝦青素特征值在1以上的1個成分為主成分,貢獻率為93.912%,皆能較好地代表原始數據所反映的信息,符合主成分分析要求。
由表2可知,單寧抗氧化性主成分1其因子得分系數在0.16以上,其中DPPH自由基清除能力,ABTS+自由基清除能力,總還原能力,金屬離子螯合能力相對較高。枸杞多糖主成分1各因子的得分系數最高的是DPPH自由基,主成分2影響最高的因子是羥基自由基。人參皂苷及蝦青素都只有一個主成分,且各指標相關程度很高,說明這一個主成分可以很好地反映抗氧化能力測定結果。人參皂苷抗氧化性影響最高的是超氧自由基清除能力。蝦青素的抗氧化性各因子得分系數最高的是DPPH自由基清除能力。主成分分析結果與不同濃度下各天然物質的各抗氧化指標研究結果一致。
3 結論
經不同物質在不同濃度下抗氧化活性分析,單寧的ABTS+、DPPH自由基清除能力最強。枸杞多糖及1.0 mg/mL的人參皂苷具有良好的清除羥基自由基的能力。人參皂苷對超氧陰離子自由基的清除能力較強。單寧的總還原能力較強,枸杞多糖次之。單寧螯合金屬離子能力較強,人參皂苷次之。4種天然抗氧化劑對脂質抗氧化能力由強到弱為單寧、枸杞多糖、人參皂苷、蝦青素。經主成分分析,單寧的DPPH自由基清除能力較好。蝦青素的DPPH自由基清除能力較好,人參皂苷的超氧陰離子自由基清除能力較好,枸杞多糖的羥基自由基清除能力及總還原能力較好。

