稻田養殖紅螯螯蝦個體大小與腸道菌群相關性研究
楊慧贊,呂 敏,楊彥豪,盧天和,童 潼,梁俊杰,楊秋月,張 琴,黃 崢,王 瑞
(1.廣西壯族自治區水產科學研究院,廣西水產遺傳育種與健康養殖重點實驗室,南寧 530021;2.廣西民族大學海洋與生物技術學院,南寧 530006)
腸道微生物是最多樣的微生物群,其對宿主的消化平衡、免疫防御和生理機能調節至關重要。水生動物體表和體內均存在有大量微生物,消化道作為營養物質消化吸收的場所,定殖了數量巨大、種類繁多的微生物,參與宿主多種生物進程。水生動物腸道微生物的穩定受水質、水溫、天氣、飼養模式和物種等多種因素影響。近幾年,“組學”技術的發展,信息技術、數據分析軟件包和存儲系統的進步,有效促進了水產養殖動物腸道微生物研究。紅螯螯蝦()屬十足目(Decapoda)擬螯蝦科(Parastacidae)紅螯螯蝦屬(),原產澳大利亞,因其具有體型大、繁殖力強、生長快,能耐受廣泛的環境條件等特點,逐漸成為各國淡水龍蝦的研究熱門品種。通過對紅螯螯蝦腸道微生物進行研究,獲得與其營養代謝、能量獲取、生長性能等相關影響因子,可有效促進紅螯螯蝦養殖技術的進步。
目前有關紅螯螯蝦的研究主要集中于生物學、生理學、水產養殖和生產等相關研究,還未見其腸道微生物的研究報道。紅螯螯蝦腸道菌群組成及養殖環境對其腸道菌群的影響還屬未知。本研究通過對稻田養殖不同大小的紅螯螯蝦腸道細菌16S rDNA基因V3~V4區進行高通量測序,獲得紅螯螯蝦腸道菌群組成特點。通過紅螯螯蝦腸道菌群組成特點分析,探討紅螯螯蝦個體大小與其腸道菌群組成的相關性,以期獲得與紅螯螯蝦生長相關的菌群結構,為優化紅螯螯蝦養殖條件、益生菌篩選和病害防控等提供數據支撐。
1 材料與方法
1.1 試驗材料
紅螯螯蝦采自廣西南寧蘇圩鎮紅螯螯蝦稻田生態養殖示范基地,稻田水溫26.5 ℃,所有樣品為同一塊稻田、同批次苗種、同時放養。樣品分為大個體組[RB:(4.5±10.8) g,(10.2±0.5) cm]和小個體組[RS:(27.7±7.7) g,(7.6±0.7) cm],每個組設3個重復,無菌采集紅螯螯蝦后腸,將5尾的后腸及其內容物混合為1個重復。
1.2 細菌基因DNA提取及高通量測序
紅螯螯蝦樣品按照HiPure Stool DNA Kit(Magen生物,中國)說明書方法提取總DNA。采用PCR擴增核糖體RNA基因的16S rDNA V3-V4區序列。反應條件為:94 ℃ 2 min;98 ℃ 10 s,62 ℃ 30 s,68 ℃ 30 s,30個循環;68 ℃延伸5 min。使用引物為:341F(CCTACGGGNGGCWGCAG)和806R(GGACTACHVGGGTATCTAAT)。反應體系為 50 μL:10 × KOD Buffer 5 μL、2 mmol/L dNTPs 5 μL、Forward Primer(10 μmol/L)和Reverse Primer(10 μmol/L)各1.5 μL、KOD Polymerase 1 μL、MgSO(25 mmol/L) 3 μL、Template DNA 100 ng、補超純水至50 μL。PCR產物經2%瓊脂糖凝膠電泳檢測后,按照AxyPrep DNA Gel Extraction Kit(Axygen Biosciences,美國)說明書方法進行回收,采用ABI StepOnePlus Real-Time PCR System進行定量后在Illumina平臺進行PE250測序(廣州基迪奧生物科技有限公司)。
1.3 高通量測序結果生物信息學分析
紅螯螯蝦腸道細菌高通量測序結果借助基迪奧公司在線實時交互式數據分析平臺Omicsmart(http://www.omicsmart.com)分析。主要分析步驟包括:原始測序序列的拼接和質控;采用USEARCH軟件的UPARSE算法進行OTU聚類分析,相似度大于97%的序列聚為一類,計算獲得每個OTU在各個樣品中的Tags絕對豐度和相對信息;采用RDP Classifier的Na?ve Bayesian assignment算法,與greengene數據庫進行物種注釋(設定置信度的閾值為0.8~1)對代表性OTU進行物種注釋;Alpha多樣性分析,并采用Welch’s T檢驗分析樣本差異顯著性;在生物學分類的門和屬水平進行細菌群落結構和相對豐度分析;LEFse指示物種分析,獲得組間菌群差異,找出主要特異菌群;Tax4Fun開展KEGG預測及KO豐度統計,預測菌群功能;使用R語言工具、Excel軟件進行相關數據圖形化。
2 結果與分析
2.1 樣本16S rDNA基因高通量測序結果
通過樣本16S rDNA基因高通量測序,RB組共獲得352768條有效序列,聚類獲得615個OTUs;RS組共獲得351744條有效序列,聚類獲得602個OTUs;RB組和RS組共有OTUs數量為345個,RB組特有OTUs為270個,RS組特有OTUs為257個。
2.2 菌群Alpha多樣性分析
紅螯螯蝦腸道細菌群落Alpha多樣性指數見表1。Alpha多樣性結果分析顯示,RB組的Chao指數、Ace指數、香農指數和辛普森指數均高于RS組,但差異不顯著(>0.05),表明RB組菌群物種豐富度、菌群多樣性和均勻度差異不顯著,這可能是由于樣品處于相同環境并攝食相同餌料造成。RB組和RS組的覆蓋率分別為99.74%和99.72%,表明測序深度已經基本覆蓋到樣品中所有的物種,所得數據基本能反映樣品真實物種組成情況。

表1 RB和RS Alpha多樣性指數Tab.1 Alpha-diversity index of the samples in RB and RS group
2.3 樣品菌群門水平組成差異分析
稻田養殖紅螯螯蝦腸道細菌群落門水平組成如圖1所示,RB組和RS組的優勢菌門相同,均為變形菌門(Proteobacteria)、軟壁菌門(Tenericutes)、厚壁菌門(Firmicutes)、梭菌門(Fusobacteria)、擬桿菌門(Bacteroidetes)等,但各個優勢菌門在RB組和RS組的組成比例存在差異,如變形菌門菌群在RB組所占比例為42.62%,而在RS組為51.78%;軟壁菌門菌群在RB組所占比例為41.15%,而在RS組為35.71%;RB組浮霉菌門(Planctomycetes)和藍藻(Cyanobacteria)菌群所占比例分別是RS組的3.6倍和5.5倍。
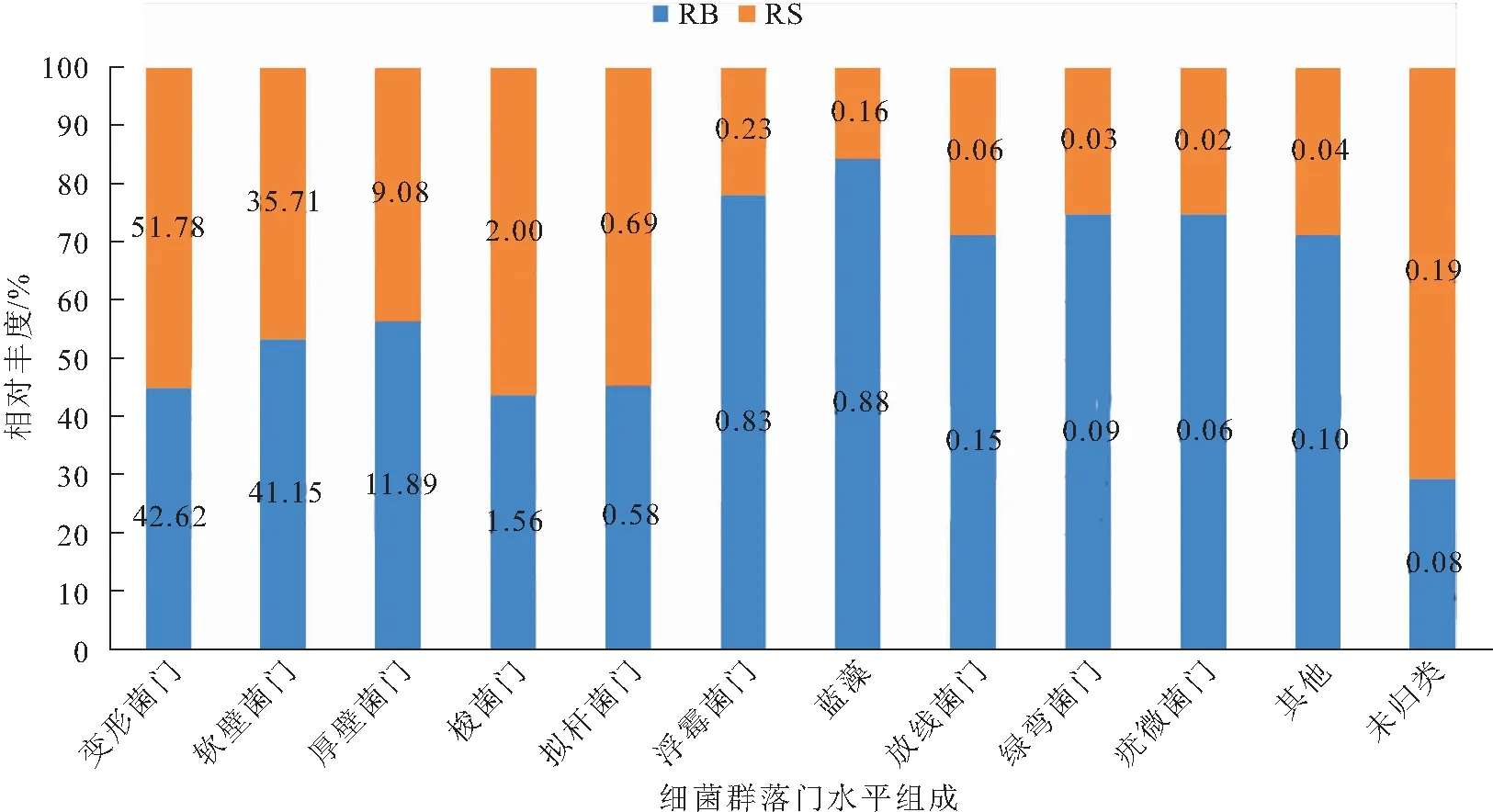
圖1 RB組和RS組腸道菌群門水平相對豐度Fig.1 Relative abundance of intestinal microflora of RB and RS on phylum level
2.4 樣品菌群屬水平組成差異分析
稻田養殖紅螯螯蝦腸道細菌群落屬水平組成如圖2所示,RB組和RS組排名前10的優勢菌屬分別為、檸檬酸桿菌屬()、梭菌屬()、、弧菌屬()、乳球菌屬()、、布拉格菌屬()、棍狀厭氧菌屬()、氣單胞菌屬()。其中梭菌屬、、弧菌屬菌群比例RB組分別為RS組的2.42、8.14和6.00倍,而乳球菌屬和布拉格菌屬菌群比例RS組分別為RB組的15.45和21.13倍。
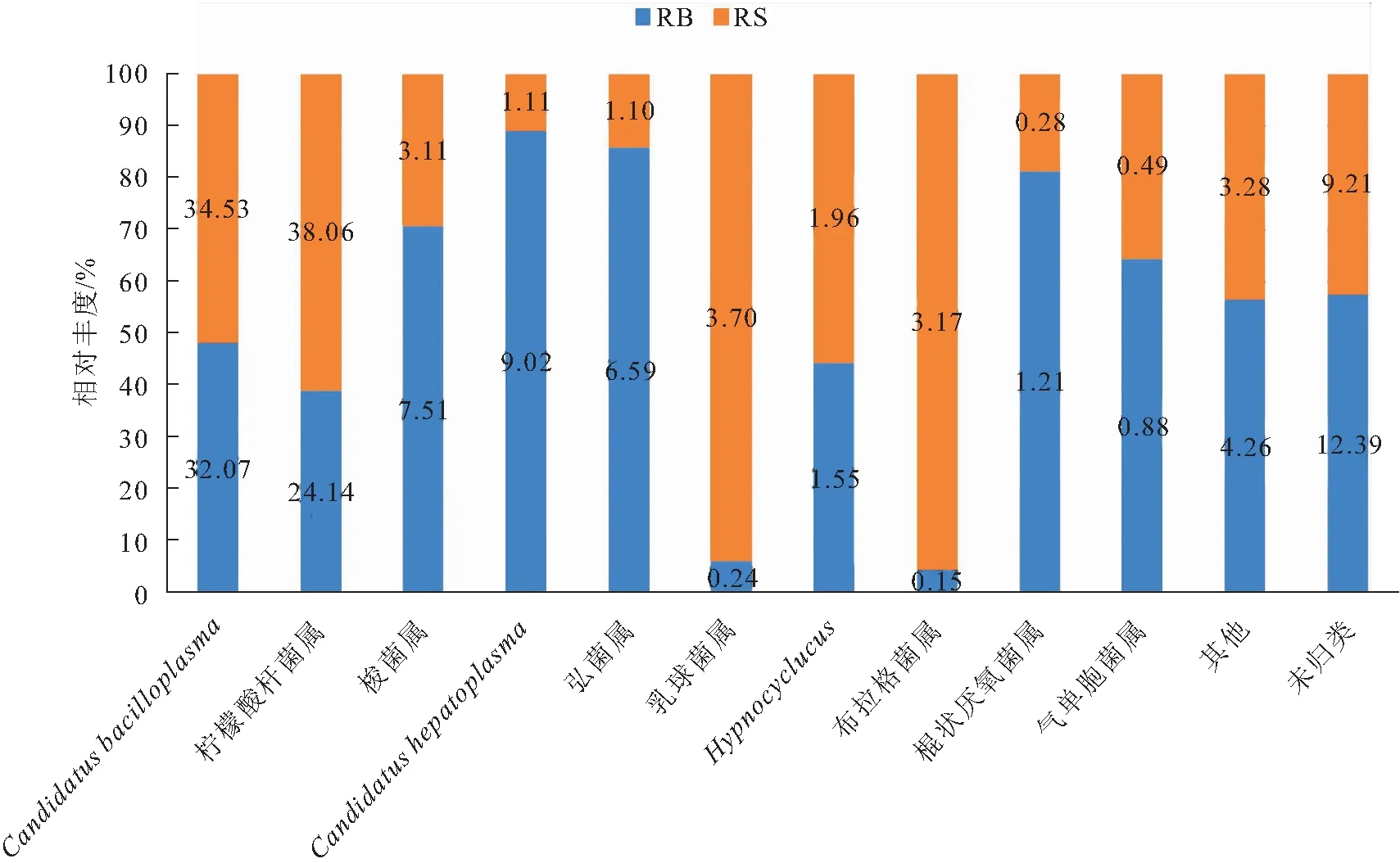
圖2 RB組和RS組腸道菌群屬水平相對豐度
2.5 樣品菌群指示物種分析
通過LEFse分析RB和RS組間菌群差異,獲得組間特異的主要菌群作為樣品菌群的指示物種,分析結果如圖3所示,RB組的特異菌群為乳酸菌科的乳桿菌屬()和片球菌屬()、蒼白桿菌屬()、軍團桿菌屬()及變形桿菌目(Gammaproteobacteria Incertae Sedis)等菌群;RS組的特異菌群為擬桿菌目(Bacteroidales)、紅小梨形菌屬()、布拉格菌屬()和不動桿菌屬()菌群。
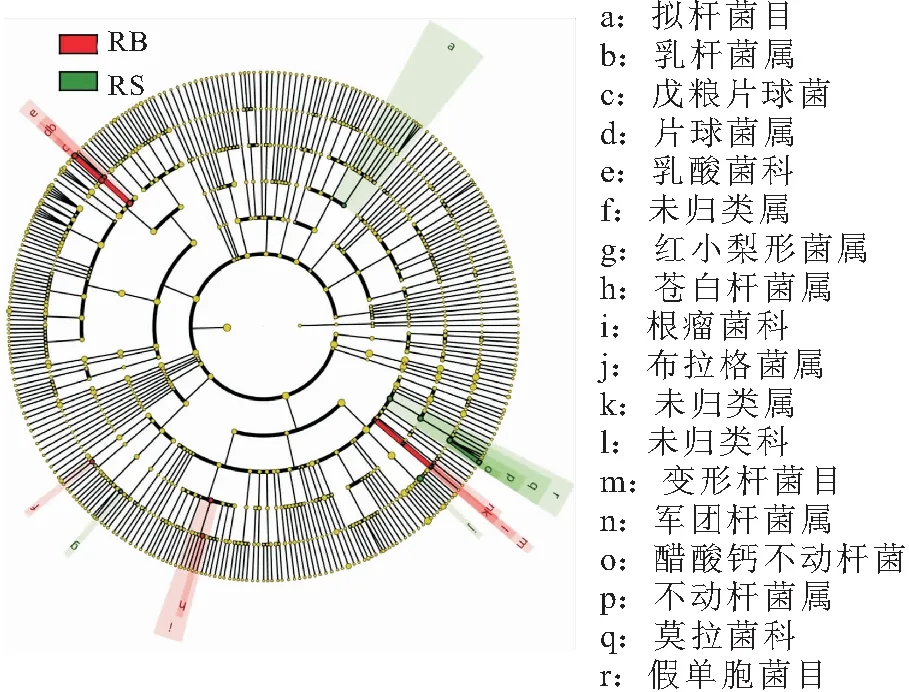
圖3 RB組和RS組腸道菌群指示物種聚類圖Fig.3 Cluster diagram of indicator species of intestinal microflora of RB and RS
2.6 樣品菌群功能分析
通過Tax4Fun對16S序列的SILVA注釋進行KEGG功能預測,獲得樣本中KO、pathway等功能的相對豐度,結果如圖4所示。
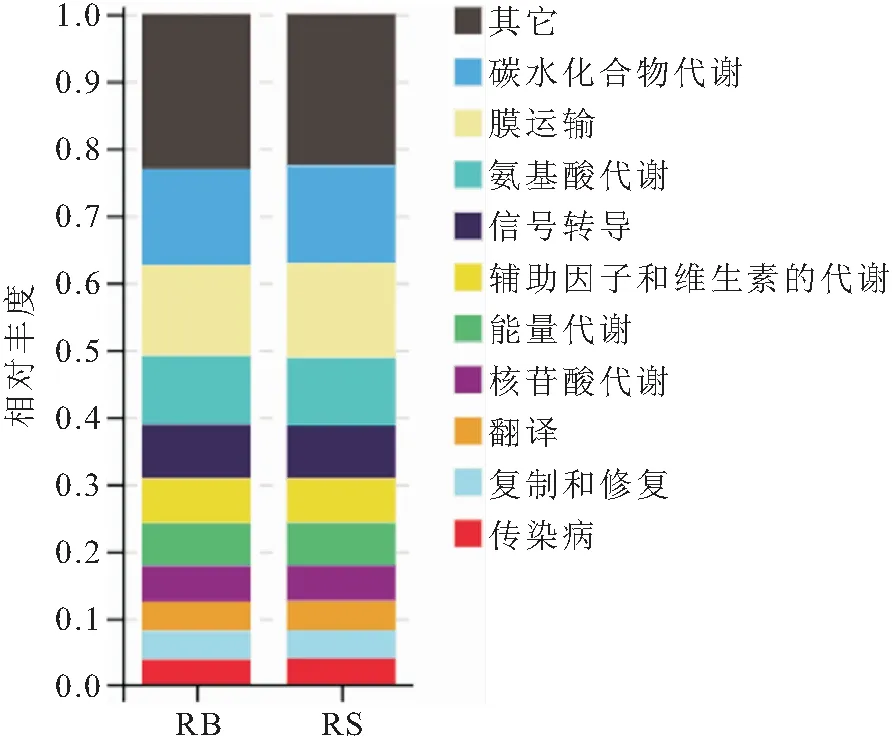
圖4 RB組和RS組腸道菌群功能堆疊圖Fig.4 Functional stacking diagram of intestinal microflora in RB and RS
RB組和RS組腸道菌群功能通過Welch’s T檢驗,獲得豐度均值顯著差異的功能聚類,結果如圖5所示。除甘油磷脂代謝RS組豐度高于RB組,纈氨酸亮氨酸和異亮氨酸降解、檸檬烯和蒎烯降解、香葉醇降解、D-谷氨酰胺與D-谷氨酸代謝等功能RB組豐度均高于RS組。因此,RS組在脂代謝方面強于RB組,RB組在氨基酸代謝、聚酮類代謝、外源生物降解和代謝、消化系統和免疫系統等方面強于RS組。
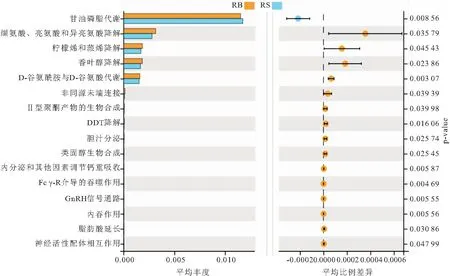
圖5 RB組和RS組腸道菌群功能差異Fig.5 Functional differences of intestinal microflora between RB and RS groups
3 討論
水生生物腸道菌群通常以變形菌門、厚壁菌門和擬桿菌門為主。本研究通過16S rDNA的高通量測序研究了稻田養殖紅螯螯蝦RB與RS腸道菌群多樣性,研究顯示RB組獨有OTUs、RB和RS組共有OTUs和RS組獨有OTUs數量各占總OTUs數量的31%、40%和29%,表明RB和RS組腸道細菌種類具有一定的共性,也存在較大的差異,與其他淡水螯蝦,如馬龍螯蝦()、克氏原螯蝦腸道菌群研究結果相似。除變形菌門、梭菌門和擬桿菌門豐度與紅螯螯蝦個體大小呈負相關外,其他優勢菌群豐度均與紅螯螯蝦個體大小呈正相關。投喂益生菌可顯著改善腸道菌群結構,提高馬龍螯蝦腸道軟壁菌門和浮霉菌門等有益菌群,促進先天免疫相關的代謝功能和基因表達。RB組軟壁菌門和浮霉菌門豐度均高于RS組,與紅螯螯蝦個體大小呈正相關,表明這兩種菌群對螯蝦的生長可能具有促進作用。研究顯示,除個體差異因素外,品種、飼料和養殖環境是影響腸道菌群結構的重要因素。本研究菌群Alpha多樣性結果顯示RB組和RS組的菌群豐富度、多樣性和均勻度均差異不顯著,可能是由于樣品的品種、飼養環境、飼料投喂完全相同所致。另外,紅螯螯蝦腸道藍藻豐度也與個體大小呈正相關,從側面表明大個體具有更強的攝食能力。
梭菌屬能夠利用包括纖維素、單糖和木聚糖等糖類為宿主提供營養。從人類糞便樣本中分離的梭菌能夠在結腸中積累Treg細胞,從而抑制腸道炎癥。梭狀芽孢桿菌在健康克氏原螯蝦腸道中起炎癥抑制的作用,而在鎘引起的不健康腸道中會加重炎癥相關疾病。本研究中RB組梭菌屬豐度為RS組的2.42倍,表明梭菌屬在健康紅螯螯蝦腸道可能起積極作用。弧菌屬包含很多種水產養殖條件致病菌,可引起細菌性傳染疾病暴發,是蝦類養殖的巨大威脅。但也有大量研究數據表明,蝦類疾病的發生是蝦及菌群相互作用的平衡被打破的結果,而不是完全由單一病原造成的結果。有研究顯示弧菌屬為克氏原螯蝦腸道菌群的優勢菌群,但也有研究顯示克氏原螯蝦腸道菌群并不含有弧菌屬,表明弧菌屬并不是克氏原螯蝦腸道的固有菌群,其豐度可能受環境的影響。本研究結果顯示,弧菌屬在健康紅螯螯蝦腸道中具有較高的豐度。乳球菌屬、乳桿菌屬和片球菌屬分別屬乳酸菌目的鏈球菌科、乳桿菌科。乳酸菌是腸道微生物的組成部分,通常被認為是益生菌,在促生長、宿主免疫調節和抗病性等方面發揮有益的作用。乳酸菌及其代謝產物可促進蝦的存活、生長和免疫反應,增強蝦對病原體的抵抗力。乳球菌和乳桿菌體外均具有抗弧菌活性,南美白對蝦()口服后可在其腸道定殖抗弧菌感染。乳桿菌可調節宿主TOR依賴的營養傳感機制及蛻皮激素和胰島素激素信號促進生長。片球菌可提高蝦的增重率、存活率、飼料轉化率和血淋巴總抗氧化水平。本研究RB組腸道弧菌屬豐度為RS組的6.00倍,而RS組腸道乳球菌屬豐度為RB組的15.45倍,推測可能是RS組腸道較高的乳球菌屬豐度對弧菌屬產生了抑制作用。但菌群指示物種分析結果顯示RB組特異具有乳桿菌屬和片球菌屬菌群,因此乳桿菌屬和片球菌屬可能在促進紅螯螯蝦生長方面起重要作用。
腸道微生物參與消化過程中物質循環和能量流動,其代謝產物在維持宿主生理穩態方面起關鍵作用。因此,腸道菌群及其代謝功能的信息是了解動物健康狀況的有效途徑。雖然不同個體的腸道菌群存在差異,但與代謝途徑相關的基因在個體中是穩定的,這些微生物基因主要參與碳水化合物代謝和氨基酸合成等代謝途徑。RB組和RS組腸道菌群雖然存在差異,但其菌群的功能均主要富集為碳水化合物代謝、膜運輸、氨基酸代謝、信號轉導等。RB組和RS組腸道菌群功能聚類差異分析顯示,RS組在脂代謝方面強于RB組,RB組在氨基酸代謝、聚酮類代謝、外源生物降解和代謝、消化系統和免疫系統等方面強于RS組。這些菌群功能的差異,可能是影響紅螯螯蝦生長的重要因素。
本研究通過比較分析稻田養殖紅螯螯蝦個體大小與腸道菌群間的關系,發現個體大小與腸道菌群的結構組成和豐度、菌群的代謝功能有關,說明在相同的養殖環境和飼養方法條件下,紅螯螯蝦腸道微生物可影響紅螯螯蝦的生長性能。此外,根據本研究結果推測同屬乳酸菌目的乳球菌屬和乳桿菌屬在紅螯螯蝦腸道的功能存在差異,乳球菌屬可抑制腸道弧菌屬的豐度,而乳桿菌在促進紅螯螯蝦生長方面起重要作用,為不同功能益生菌的開發提供參考。

