K8[Cd(H2O)CuW11O39]/PANI/ZnS三元復合材料的合成、表征及光催化性能
欒成鈺,單秋杰,司徒嘉俊,陳 林,陳 偉
(齊齊哈爾大學化學與化學工程學院,黑龍江齊齊哈爾 161006)
隨著化工產(chǎn)業(yè)迅速發(fā)展,工業(yè)污水污染嚴重、毒性高等問題嚴重困擾著我們,尋找綠色、安全的治理方法成為諸多學者的研究方向。光催化作為一種新型綠色無污染、高效的催化方法受到社會的廣泛關(guān)注[1]。多金屬氧酸鹽因為獨特的Keggin 結(jié)構(gòu),可負載多種化合物,提高其催化性能和重復使用性能[2],成為研究熱點。ZnS 具有禁帶寬度較寬[3]、光生載流子產(chǎn)率高以及導帶電勢低等優(yōu)點[4],在治理環(huán)境污染、光解水產(chǎn)氫、人工光合作用等領(lǐng)域發(fā)展前景較好[5]。聚苯胺是亞苯基化合物,其優(yōu)良的光學性質(zhì)在光催化領(lǐng)域受到青睞,可以通過摻雜特殊的原子和離子調(diào)節(jié)表面屬性[6]。
本文從如何提高光催化性能方向入手,將具有優(yōu)異光學性能的雜多酸、聚苯胺、ZnS 進行復合,成功制備復合催化劑K8[Cd(H2O)CuW11O39]/PANI/ZnS,并對其進行廢水降解實驗,探究光催化性能。
1 實驗
1.1 試劑與儀器
試劑:硫酸鎘(CdSO4)、硫酸銅(CuSO4)、鎢酸鈉(Na2WO4)、冰乙酸、無水乙醇、苯胺、鹽酸(HCl)、氯化鉀(KCl)、硫化鋅(ZnS)、過硫酸銨[(NH)4S2O8]、龍膽紫(GV)(均為分析純)。
儀器:Spectrum-One 型紅外光譜儀、LambdaTu-1901 型紫外光譜儀(美國Perkin-Elmer 公司),X-射線粉末衍射儀(德國布魯克AXS 公司),S-4300 型掃描電子顯微鏡(日本日立公司),化學吸附儀(美國康塔儀器公司)。
1.2 催化劑的制備
1.2.1 K8[Cd(H2O)CuW11O39]的制備
將18.15 g Na2WO4放于250 mL 燒杯中,加入100 mL 去離子水,將二者混合并充分攪拌,逐滴滴入冰乙酸至pH 為6,將溶液加熱至80 ℃。配制1 mol/L CuSO4溶液,用量筒量取10 mL 緩慢滴加到燒杯中,80 ℃恒溫20 min 后,用量筒量取10 mL 1 mol/L CdSO4溶液緩慢滴加進燒杯中并不斷攪拌,緩慢加入冰乙酸調(diào)節(jié)pH 至3.8,80 ℃恒溫2 h,冷卻至室溫。稱取12.25 g KCl 并加入30 mL 乙醇溶解,將溶解后的溶液加入燒杯中,攪拌40 min,放入0~2 ℃冰箱冷卻過夜,抽濾、烘干,得K8[Cd(H2O)CuW11O39](簡稱CdW11Cu)。
1.2.2 PANI/ZnS 的制備
配制50 mL 含有5 mmol (NH)4S2O8的鹽酸水溶液(0.1 mol/L),加入0.2 g ZnS 納米粉末,超聲分散混合物40 min。向混合溶液中滴加含有0.5 mL 苯胺的鹽酸水溶液(50 mL,0.1 mol/L)。用冰水浴將反應(yīng)溫度控制在0~5 ℃,劇烈攪拌5 h。待反應(yīng)完全后抽濾,濾餅依次用0.1 mol/L 鹽酸和去離子水洗滌,放入干燥箱中干燥2 h后即得PANI/ZnS。
1.2.3 K8[Cd(H2O)CuW11O39]/PANI/ZnS 的制備
將0.2 g PANI/ZnS 溶于20 mL 水中,超聲分散0.5 h,用0.1 mol/L 鹽酸調(diào)節(jié)pH 至3,然后加入30 mL 0.1 mol/L 的CdW11Cu 溶液[V(乙醇)∶V(水)=1∶1]。將混合溶液加熱至60 ℃恒溫5 h,降至室溫,洗滌、抽濾、60 ℃真空干燥2 h,得K8[Cd(H2O)CuW11O39]/PANI/ZnS(簡稱CdW11Cu/PANI/ZnS)。
1.3 光催化實驗
配制一定質(zhì)量濃度的龍膽紫溶液置于100 mL 燒杯中,緩慢滴加冰乙酸調(diào)節(jié)pH,稱取適量CdW11Cu/PANI/ZnS 加入其中,將溶液放置于陰暗處攪拌30 min,取樣離心5 min,將分光光度計的波長調(diào)節(jié)至龍膽紫最大吸收波長581 nm 處,將盛有上層清液的比色皿放入分光光度計中,測得初始吸光度為A0,在30 W 紫外光照射下反應(yīng)150 min,間隔10 min 取樣,離心5 min后測試吸光度為At,按下式計算脫色率:

2 結(jié)果與討論
2.1 表征
2.1.1 紅外光譜
由圖1a 可知,表示Keggin 雜多酸的特征峰分別在443、887、802、949 cm-1(Cu-Oa、W-Ob-W、W-Oc-W、W-Od)處出現(xiàn)。由圖1b 可知,509 cm-1左右出現(xiàn)了Zn—S 伸縮振動特征峰;1 579、1 495、1 302、1 129 cm-1處出現(xiàn)了PANI 特征吸收峰,分別對應(yīng)苯環(huán)和醌式結(jié)構(gòu)的拉伸振動以及苯環(huán)CC、醌環(huán)C—N、苯環(huán)C—H 的伸縮振動吸收[7]。因為ZnS 使PANI 的表面電子云密度降低,原子間作用力下降,PANI/ZnS 的特征吸收峰出現(xiàn)紅移現(xiàn)象[8]。由圖1c 可知,CdW11Cu/PANI/ZnS 的吸收峰與CdW11Cu 和PANI/ZnS 的吸收峰相似,表明CdW11Cu 與PANI/ZnS 成功復合,且合成的三元復合材料的Keggin 型骨架沒有遭到破壞。

圖1 樣品的紅外光譜圖
2.1.2 紫外光譜
由圖2 可以看出,CdW11Cu/PANI/ZnS 的譜圖與CdW11Cu 相似,都在195、256 nm 左右出現(xiàn)雜多酸的CdW11Cu 中Od→W 和Ob,Oc→W 荷移躍遷 產(chǎn) 生 吸 收峰[9],表明合成的復合催化劑中存在雜多酸特殊的Keggin 結(jié)構(gòu)。圖2b 中,在423、530 nm 處呈現(xiàn)的吸收峰是PANI 鏈中苯環(huán)π-π*和πb-πq*的特征吸收峰[10],表明材料復合成功。復合催化劑的能隙為2.77 eV,ZnS 的能隙為3.70 eV,說明復合催化劑在可見光區(qū),低能隙電子躍遷所需能量較少,證明CdW11Cu/PANI/ZnS具有良好的光催化性能。
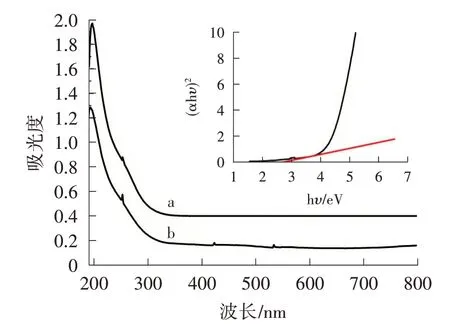
圖2 樣品的紫外光譜圖
2.1.3 X-射線粉末衍射
由圖3c 可以看出,在2θ=26.90°處出現(xiàn)的特征衍射峰屬于PANI,在2θ=47.65°、56.60°處出現(xiàn)ZnS 的特征衍射峰,且在10°~30°范圍內(nèi)的吸收帶變寬,表明通過摻雜,PANI 以翠綠亞胺鹽的形式包覆在ZnS 表面[11]。圖3a 中,在2θ=6.10°、9.60°、18.10°和29.10°處出現(xiàn)雜多酸CdW11Cu 的Keggin 特征衍射峰,與ZnS 的衍射峰比較,CdW11Cu/PANI/ZnS 的衍射峰強度明顯下降,說明晶粒縮小[12],表明CdW11Cu/PANI/ZnS 是一種晶態(tài)復合材料。
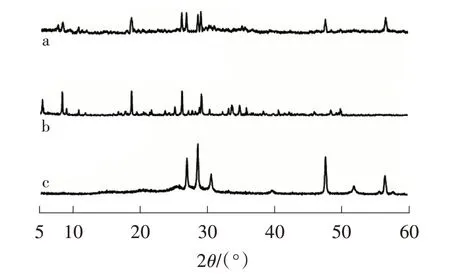
圖3 樣品的X-射線粉末衍射譜圖
2.1.4 N2吸附-脫附
樣品的吸附-脫附曲線及孔徑分布曲線見圖4。

圖4 樣品的吸附-脫附曲線及孔徑分布曲線
由圖4 可知,CdW11Cu/PANI/ZnS 的N2吸附-解吸等溫線為Ⅳ型等溫線[13],由于CdW11Cu/PANI/ZnS 的納米雜化體堆積,材料顆粒間存在介孔,且復合催化劑的孔徑為2.0~50.0 nm[14],因此是介孔材料。復合催化劑的比表面積為21.70 m2/g,孔體積為0.083 cm3/g,說明比表面積大,能夠更好地與廢水中的染料分子接觸,增強吸附能力。
2.1.5 SEM
由圖5可知,由于靜電力作用,CdW11Cu/PANI/ZnS復合催化劑呈現(xiàn)珊瑚樹枝狀納米纖維交織堆疊成的不規(guī)則三維多孔結(jié)構(gòu),該結(jié)構(gòu)增加了其與廢水中染料分子的有效接觸,能為光催化過程供應(yīng)更多的活化位點[15],提高光催化性能。

圖5 樣品的SEM 圖和掃描電子顯微鏡照片
2.1.6 EDS
由圖6 和表1 可看出,樣品測得的元素與合成的CdW11Cu/PANI/ZnS 理論上基本一致,并且不含有其他雜質(zhì)元素,說明合成的材料是CdW11Cu/PANI/ZnS。
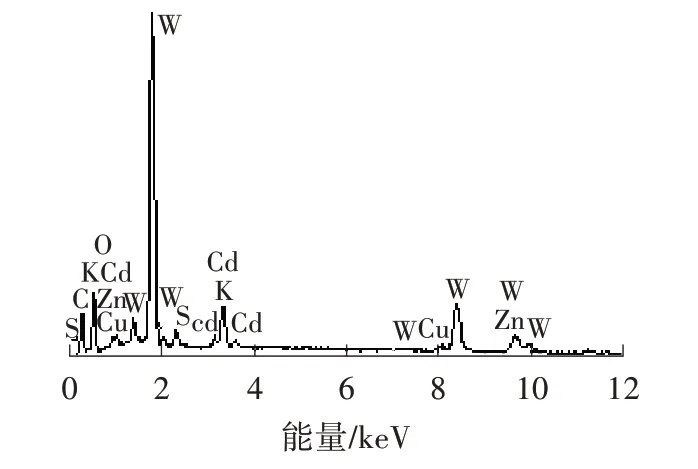
圖6 樣品的EDS 能譜圖

表1 樣品的元素百分比
2.1.7 XPS
由圖7 可以看出,電子結(jié)合能為36.80、283.51、403.76、178.76、530.10、412.53、934.21、1 023.74 eV 處分別出現(xiàn)了W4f、C1s、N1s、S2p、O1s、Cd3d、Cu2p 和Zn2p 的特征峰[16]。其中C 和N 元素的出現(xiàn)說明存在PANI;Cd和Cu元素的出現(xiàn)說明存在雜多酸CdW11Cu;Zn 和S 元素的出現(xiàn)說明存在ZnS。由此可以判斷,實驗成功制備了CdW11Cu/PANI/ZnS。
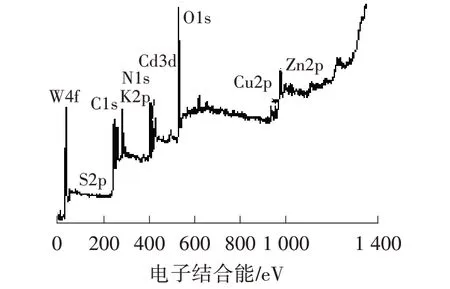
圖7 樣品的XPS 譜圖
2.2 龍膽紫溶液脫色率的影響因素
2.2.1 CdW11Cu/PANI/ZnS 降解龍膽紫溶液的吸附-脫附實驗
量取100 mL 10 mg/L 龍膽紫溶液,調(diào)節(jié)pH 為2,將10 mg CdW11Cu/PANI/ZnS 加入其中,置于黑暗處攪拌,每隔5 min 取1 次樣,測定581 nm 處的吸光度。由圖8 可看出,龍膽紫溶液的脫色率在加入CdW11Cu/PANI/ZnS 于暗處攪拌30 min 后不再發(fā)生變化。因此,為消除CdW11Cu/PANI/ZnS 對龍膽紫吸附-脫附實驗的影響,提前將龍膽紫溶液與CdW11Cu/PANI/ZnS 置于暗處攪拌30 min,此時測試的龍膽紫溶液吸光度為反應(yīng)初始值。
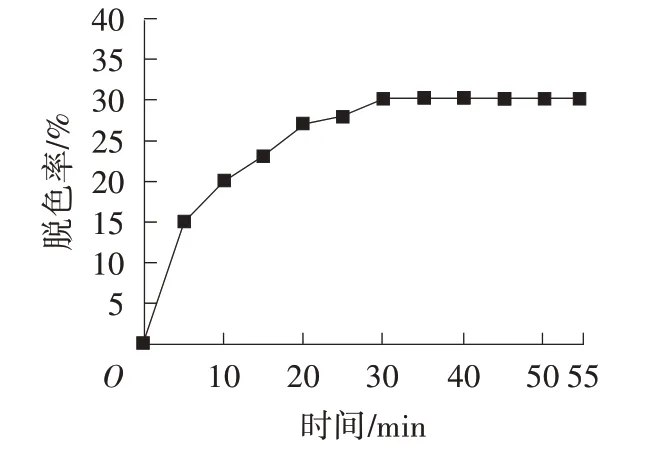
圖8 CdW11Cu/PANI/ZnS 避光吸附-脫附曲線
2.2.2 初始pH
由圖9 可知,當溶液初始pH 為2 時,溶液的脫色率最高(71.34%)。當溶液初始pH 逐漸升高時,溶液脫色效果逐漸下降。這是因為CdW11Cu/PANI/ZnS 本身顯酸性,酸性條件會促進還原反應(yīng)的發(fā)生,有利于破壞龍膽紫染料中的顯色基團萘環(huán)和偶氮雙鍵。因此龍膽紫溶液的初始pH 選擇2。
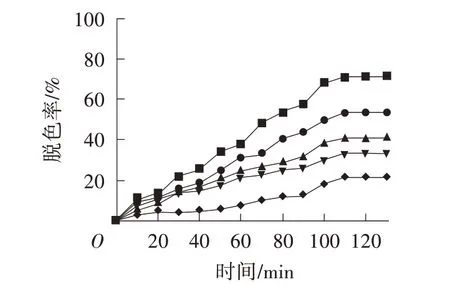
圖9 龍膽紫溶液初始pH 對脫色率的影響
2.2.3 龍膽紫初始質(zhì)量濃度
由圖10 可知,初始質(zhì)量濃度為5 mg/L 時溶液脫色率最高(88.45%)。隨著龍膽紫溶液初始質(zhì)量濃度增加,脫色率逐漸下降。這是因為CdW11Cu/PANI/ZnS參與降解反應(yīng)時生成的自由基有限,隨著溶液質(zhì)量濃度提高,染料分子附著在催化劑表面,使催化劑的物理吸附達到飽和,溶液中紫外光的透過率減少,為反應(yīng)提供的光照強度減弱,能夠被光照激發(fā)的活化因子減少,催化效果變差。因此龍膽紫溶液的初始質(zhì)量濃度選擇5 mg/L。
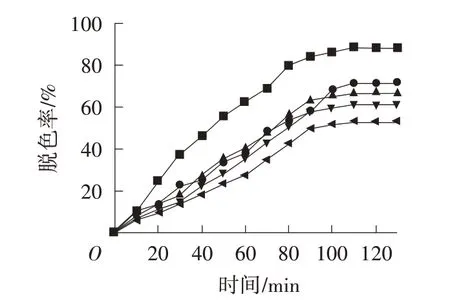
圖10 龍膽紫溶液初始質(zhì)量濃度對脫色率的影響
2.2.4 催化劑用量
由圖11 可知,催化劑用量為10 mg 時,溶液脫色率最高(92.15%)。

圖11 催化劑用量對脫色率的影響
隨著催化劑用量逐漸減少,脫色效果逐漸降低。這是因為當催化劑用量減少時,染料與催化劑的接觸概率減小,參與反應(yīng)的活化位點減少,染料脫色效果不明顯。當催化劑用量大于10 mg 時,過多的催化劑分子阻擋紫外光的透射,紫外光的透過率逐漸下降,阻礙復合催化劑對紫外光的利用,溶液脫色效果不明顯。因此催化劑用量選擇10 mg。
2.2.5 不同催化劑
由圖12 可以看出,CdW11Cu/PANI/ZnS 光催化降解龍膽紫的效果最好,脫色率最高能夠達到92.15%(PANI/ZnS、CdW11Cu、ZnS 的脫色率分別為25.24%、40.12%、12.34%),因此,CdW11Cu/PANI/ZnS 是一種高效降解染料的催化劑。
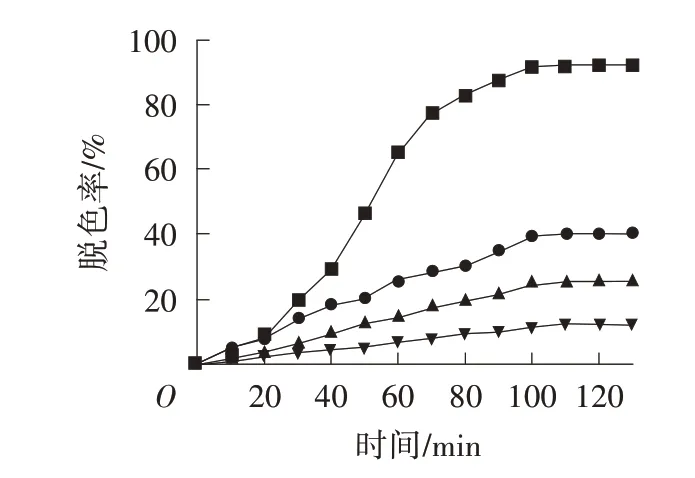
圖12 不同催化劑對脫色率的影響
2.3 催化劑的重復使用性
由圖13 可看出,重復實驗1 次后,催化劑對龍膽紫的脫色率為82.32%,重復實驗2 次后的脫色率為70.14%。隨著使用次數(shù)增加,脫色率逐漸下降,原因可能是催化劑表面附著的龍膽紫染料分子過多降低了催化劑純度,影響了光催化活性。重復實驗2 次后,催化劑對染料仍具有良好的降解作用,表明催化劑具有杰出的穩(wěn)定性和回收利用價值。
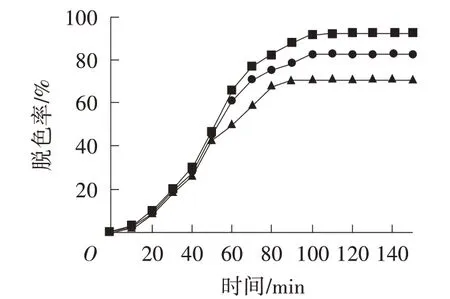
圖13 催化劑重復實驗3 次對脫色率的影響
3 結(jié)論
使用靜電自組裝法,將CdW11Cu 與PANI/ZnS 進行負載,合成了CdW11Cu/PANI/ZnS,并采用IR、UV、XRD、N2吸附-脫附、SEM、XPS 等手段進行表征。利用該復合催化劑降解龍膽紫染料,確定了優(yōu)化應(yīng)用工藝條件:龍膽紫溶液初始pH 2,初始質(zhì)量濃度5 mg/L,催化劑用量10 mg,此時溶液脫色率最高(92.15%)。在該條件下,CdW11Cu/PANI/ZnS 的催化性能高于CdW11Cu 和PANI/ZnS。重復實驗表明,該催化劑具有良好的穩(wěn)定性和重復使用性。

