拉莫三嗪治療顱腦損傷后癲癇血藥濃度與OCT1基因多態性的關系
周子健,陳紅德
(1.廣東省工傷康復醫院藥劑科,廣東廣州 510440;2.廣州市白云區石井人民醫院內科,廣東廣州 510430)
癲癇是一種慢性腦功能障礙性疾病,發病率較高,全球患者近7 000萬,給患者的日常生活和工作造成明顯消極影響[1]。癲癇是由大腦神經元異常放電導致,而顱腦損傷即容易造成大腦神經元異常從而導致癲癇[2]。拉莫三嗪(LTG)作為癲癇治療的一線藥物,在不同患者間的臨床療效存在較大差異,當藥物含量低于血藥治療窗時可能會引起治療無效,若高于血藥治療窗則有可能引起心血管、中樞神經等系統的不良反應[3-4],威脅患者的健康,因此對LTG血藥濃度及其影響因素的研究即成為癲癇臨床治療的研究重點。而有機陽離子轉運蛋白(OCT)作為一種內攝轉運蛋白,有研究發現有機陽離子轉運蛋白1(OCT1)介導的轉運過程與LTG的胞內濃度密切相關[5]。故本研究對LTG治療顱腦損傷后癲癇患者體內血藥濃度與OCT1基因多態性的關系進行了探討,旨在為LTG的臨床應用與癲癇治提供參考,現報道如下。
1 資料與方法
1.1 一般資料 選取2017年1月至2019年12月廣東省工傷康復醫院收治的80例顱腦損傷后癲癇患者為研究對象進行回顧性分析,根據治療效果的不同分為有效組(41例,顯效+有效)和無效組(39例)。有效組患者中男性19例,女性22例;年齡22~37歲,平均年齡(28.43±3.87)歲;體質量45~59 kg,平均體質量(52.67±5.34)kg;病程5~42個月,平均病程(21.43±2.88)個月。無效組患者中男性18例,女性21例;年齡23~35歲,平均年齡(28.19±3.25)歲;體質量44~60 kg,平均體質量(52.38±5.17)kg;病程7~41個月,平均病程(21.68±3.04)個月。兩組患者一般資料比較,差異無統計學意義(P>0.05),組間具有可比性。研究經廣東省工傷康復醫院醫學倫理委員會同意。診斷標準:參照《神經外科與癲癇(第2版)》[6]中顱腦損傷后癲癇的診斷標準,并經計算機斷層掃描及專科醫師診斷,確診為顱腦損傷后癲癇。納入標準:①符合上述診斷標準;②年齡≥18歲;③患者治療前均行OCT1 rs628031型基因檢測。排除標準 :①服用了可能影響LTG代謝的藥物(如避孕藥等)者;②已知對所使用藥物過敏者;③妊娠或哺乳期婦女;④合并有心肝腎等其他系統嚴重疾病者;⑤患者依從性差,不能遵從醫囑;⑥隨訪失訪者。
1.2 治療方法 ①基因檢測方法:抽取患者治療前外周靜脈血300 μL,并在國家生物技術信息中心數據庫中檢索人OCT1 rs628031序列,使用Primer 3.0進行引物設計,使用DNA純化試劑盒(北京康為世紀生物科技有限公司,批號:CW0524)提取患者DNA并純化,OCT1 rs628031基因型通過聚合酶鏈式反應擴增表達,以HYK-PSTAR-IIA型基因測序儀(深圳華因康基因科技有限公司,國械注準20143222171,型號:HYK-PSTAR-IIA)進行測序,完成后以GeneMapper 4.1進行分析。②給藥方法:患者均使用LTG(三金集團湖南三金制藥有限責任公司,國藥準字H20143194,規格:50 mg/片)單藥治療,劑量隨患者個體差異進行調整,持續6個月。
1.3 觀察指標 ①臨床療效統計。結束治療后隨訪1年對患者療效進行評估,療效標準參考《神經外科與癲癇(第2版)》[6],具體標準為:顯效:治療結束后1年癲癇發作次數減少量≥85%;有效:治療結束后1年50%≤癲癇發作次數減少量<85%;無效:治療結束后1年癲癇發作次數減少量<50%。同時依據治療效果將患者分為有效組(顯效+有效)和無效組。②觀察并比較兩組患者OCT1基因多態性。③比較不同OCT1 rs628031基因型患者LTG劑量、LTG穩態血藥濃度、LTG標準劑量血藥濃度差異。血藥濃度檢測方法為:抽取癲癇患者單用LTG治療至穩態谷濃度的清晨空腹外周靜脈血2 mL,2 500 r/min離心15 min分離血清后使用乙二胺四乙酸抗凝后分離血漿,-80 ℃存儲待檢,使用反相高效液相色譜法測定LTG血藥濃度。LTG標準劑量血藥濃度=LTG穩態血藥濃度/患者每日每千克體質量服藥劑量。
1.4 統計學分析 采用SPSS 18.0軟件進行數據處理,計數資料以[例(%)]表示,采用χ2檢驗;計量資料以()表示,兩組間比較采用t檢驗,多組間比較行方差分析。以P<0.05為差異有統計學意義。
2 結果
2.1 臨床療效統計 結束治療后隨訪1年,顯效患者占比13.75%,有效患者占比37.50%,無效患者占比48.75%,依據治療效果將患者分為無效組(39例)和有效組(41例)。
2.2 兩組患者OCT1 rs628031基因多態性比較 無效組患者OCT1 rs628031 GG、AG基因型占比顯著高于有效組,AA基因型占比顯著低于有效組,差異有統計學意義(P<0.05),見表1。

表1 兩組患者OCT1 rs628031基因多態性比較 [例(%)]
2.3 OCT1基因多態性與LTG劑量的相關性分析 OCT1 rs628031 GG、AG基因型攜帶者LTG劑量顯著低于OCT1 rs628031 AA基因型攜帶者,差異有統計學意義(P<0.05),見表2。
表2 OCT1基因多態性與LTG劑量的相關性分析( )
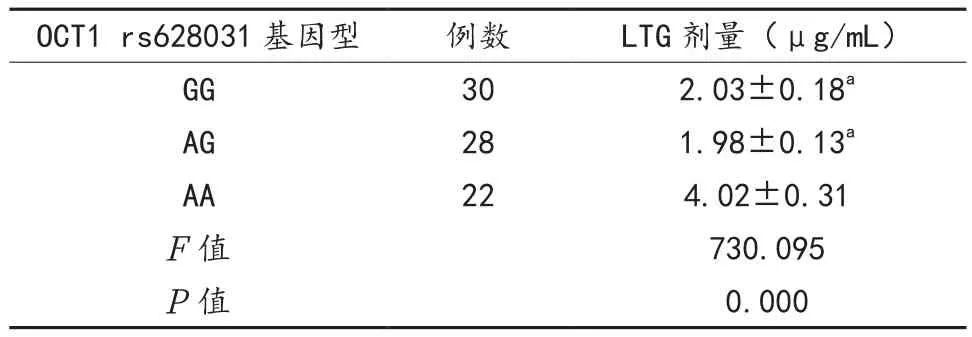
表2 OCT1基因多態性與LTG劑量的相關性分析( )
注:與AA型基因比較,aP<0.05。OCT1 rs628031:OCT1為有機陽離子轉運體1,rs628031為其基因多態性類別;GG、AG、AA為OCT1 rs628031基因的3個具體分型。
OCT1 rs628031基因型 例數 LTG劑量(μg/mL)GG 30 2.03±0.18a AG 28 1.98±0.13a AA 22 4.02±0.31 F值 730.095 P值 0.000
2.4 OCT1基因多態性與LTG穩態血藥濃度、標準劑量血藥濃度的相關性分析 不同OCT1 rs628031基因型攜帶者的穩態血藥濃度比較,差異無統計學意義(P>0.05),OCT1 rs628031 GG、AG基因型攜帶者LTG標準劑量血藥濃度顯著低于OCT1 rs628031 AA基因型攜帶者,差異有統計學意義(P<0.05),見表3。
表3 OCT1基因多態性與LTG穩態血藥濃度、標準劑量血藥濃度的相關性分析( )
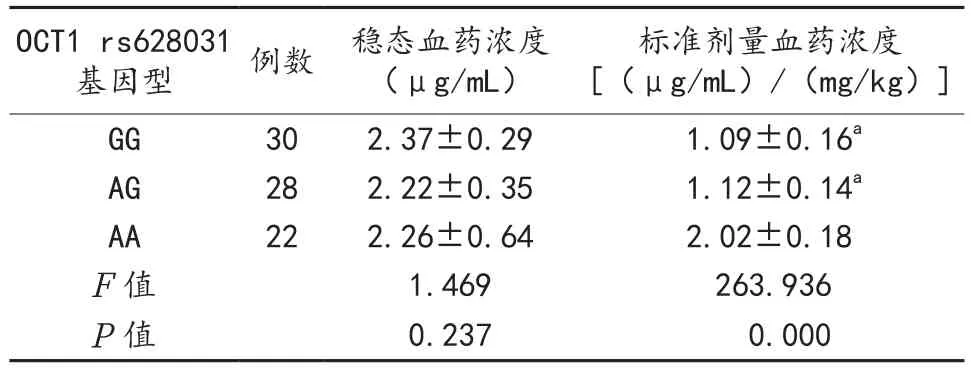
表3 OCT1基因多態性與LTG穩態血藥濃度、標準劑量血藥濃度的相關性分析( )
注:與AA型基因比較,aP<0.05。OCT1 rs628031:OCT1為有機陽離子轉運體1,rs628031為其基因多態性類別;GG、AG、AA為OCT1 rs628031基因的3個具體分型。
標準劑量血藥濃度[(μg/mL)/(mg/kg)]GG 30 2.37±0.29 1.09±0.16a AG 28 2.22±0.35 1.12±0.14a AA 22 2.26±0.64 2.02±0.18 F值 1.469 263.936 P值 0.237 0.000 OCT1 rs628031基因型 例數 穩態血藥濃度(μg/mL)
3 討論
顱腦損傷是在暴力擊打、碰撞等外力間接或直接作用于頭部后產生的顱腦組織損傷,若患者在受傷后昏迷≥6 h或發生再度昏迷的情況,則被視為重癥顱腦損傷,此類患者便極易在手術后出現創傷性癲癇并發癥[7-9]。顱腦損傷合并癲癇對患者的健康甚至生命安全都有極大威脅,尤其晚期患者的預后較差,死亡率較高[10]。因此在患者圍手術期使用抗癲癇藥物已成為臨床治療時的重要手段,LTG為應用最廣泛的藥物之一。
LTG作為一種廣譜抗癲癇藥物,近年來在全面性或部分性癲癇的臨床治療中應用時,取得了相對較好的治療效果,但治療過程中也發現一定問題,其中臨床最為關注的問題之一即LTG在不同患者體內的穩態血藥濃度有顯著差別[11-12],主要是因為血藥濃度的差異和LTG的治療效果與安全性有密切聯系。因此眾多臨床醫師開始對其差異加以關注并對引起這種差異的原因進行了持續研究,以期優化LTG的應用以增強療效和用藥安全性。既往研究發現藥物代謝轉運蛋白的基因多態性對抗癲癇藥物的生物利用度、藥代動力學等方面有明顯影響[13],譬如乳腺癌耐藥蛋白、p-糖蛋白、多藥耐藥相關蛋白-2等轉運蛋白,當其發生異常時,就會對LTG的血藥濃度造成影響,導致患者間療效產生差別[14]。
本研究在OCT1基因多態性與LTG療效、劑量相關性的觀察中發現OCT1 rs628031 GG、AG、AA基因型攜帶者之間的LTG療效和劑量水平有明顯差異;在OCT1基因多態性與LTG穩態血藥濃度、標準劑量血藥濃度相關性的觀察中,發現OCT1 rs628031 GG、AG、AA基因型攜帶者之間的穩態血藥濃度差異不大,但LTG劑量、LTG標準劑量血藥濃度有明顯差異。提示OCT1 rs628031基因多態性與LTG療效及標準劑量血藥濃度關系密切。由于有機陽離子通道轉運體能夠轉運內源性、外源性物質,與非帶電化合物和陽離子藥物的聚集與排泄密切相關[15],也有研究提出腦血管內皮細胞內部LTG有可能是OCT1底物[16]。因此OCT1的基因多態性亦有可能與LTG的療效、藥代動力學等存在聯系。但目前臨床關于OCT1的基因多態性的研究較少,對于OCT1的基因多態性與LTG治療顱腦損傷后癲癇間的關系仍不清晰,因此在后續的研究中仍期待開展更多的研究,以探討OCT1的基因多態性影響LTG治療效果的可能機制,以期尋找到LTG濃度、療效等的影響因素,從而更好地對顱腦損傷后癲癇患者進行臨床治療。
綜上,本研究發現顱腦損傷后癲癇患者在使用LTG治療時,藥物療效、劑量和標準劑量血藥濃度在OCT1不同基因類型攜帶者之間差異有統計學意義。

