Ⅲ期直腸癌術后放化療聯合恩沃利單抗的療效分析
武輝宇
大慶市人民醫院腫瘤三科,黑龍江大慶 163000
結直腸癌(colorectal cancer,RC)是全球發病率和死亡率最高的癌癥之一,全直腸系膜切除術(to‐tal mesorectal excision,TME)是可切除原發性腫瘤的主要治療方法,可將局部復發的風險從30%降低到約10%,而基于卡培他濱聯合奧沙利鉑的化療(或放化療)是Dukes' C(TNM Ⅲ 期)結腸腫瘤術后的標準治療方法。盡管治療方法有了顯著改善,但它導致的死亡率和發病率仍相當高,故探尋新型治療方法成為目前直腸癌的研究方向[1-3]。程序性死亡配體1(programmed death-ligand 1,PD-L1)蛋白是細胞膜上一種重要的跨模型免疫球蛋白,在腫瘤微環境的形成和腫瘤免疫逃逸等方面起著至關重要的作用,阻斷PD1/PD-L1 信號通路可解除對淋巴細胞的抑制作用[4-5],恩沃利單抗是我國自主研發的全球第一個PD-L1 單域抗體FC 融合蛋白,可特異結合人PD-L1 蛋白,阻斷PD1/PD-L1 信號通路,解除對T 細胞的抑制作用,進而調動免疫系統的抗腫瘤活性。基于此,本研究選取2018 年12 月—2021 年12 月在大慶市人民醫院腫瘤放射科接受直腸癌根治手術治療的80 例Ⅲ期直腸癌患者為研究對象,探究直腸癌根治術后放化療聯合恩沃利單抗的臨床效果,現報道如下。
1 資料與方法
1.1 一般資料
選取在本院腫瘤放射科接受直腸癌根治手術治療的80 例患者為研究對象,采用平行、對照、隨機方法將患者分為對照組和觀察組,每組40 例。對照組 男22 例,女18 例;年 齡35~74 歲,平 均(51.12±4.23)歲;高分化腺癌9 例,中分化腺癌10例,低分化腺癌21 例。觀察組男20 例,女20 例;年齡31~74 歲,平均(50.85±4.11)歲;高分化腺癌12例,中分化腺癌10 例,低分化腺癌18 例。兩組患者在性別、年齡、癌癥分化程度上比較,差異無統計學意義(P>0.05),具有可比性。所有研究過程均獲得患者本人及其家屬認可,簽署知情同意書,并獲得本院醫學倫理委員會批準。
1.2 納入與排除標準
納入標準:①Ⅲ期直腸癌術后的患者經病理性及影像學確診為腫瘤下緣距肛緣11 cm 以內中下段直腸腺癌,影像學顯示未發生遠處轉移,其分期參考2017 年美國癌癥聯合委員會(American Joint Committee on Cancer,AJCC)第八版直腸癌TNM 分期標準[6];②患者KPS 評分≥60 分,預計生存期超過3 個月;③患者接受本研究藥物治療前未接受過其他抗腫瘤藥物治療,且治療前無嚴重肝腎功能異常、血象異常、消化異常、心肺功能異常等現象出現;④患者對本次研究藥物均無過敏反應。
排除標準:①合并有其他腫瘤性疾病的患者;②依從性較差,無法完成整個治療過程和隨訪復查過程的患者。
1.3 方法
所有患者均接受全直腸系膜切除術,對照組患者術后行三維適形調強放療以及奧沙利鉑聯合卡培他濱化療治療。其中放療方法:取患者俯臥位,在CT 引導完成定位,并將定位圖像傳送至三維計劃治療系統,勾畫臨床靶區(clinical target volumes,CTV)和計劃靶區(planing target volume,PTV),CTV包括直,腸周圍系膜區,骶前區、吻合口、骼內血管淋巴結區引流區、坐骨直腸窩等,CTV 外擴0.5~1 cm為PTV,勾畫靶區并評價危及正常組織受量,包括小腸、膀胱、雙側股骨頭等,均采用6MV 的X 線給予患者放射治療,95%PTV,總劑量為50 Gy,2 Gy/次,1次/d,5 次/周,共25 次,危及正常組織劑量的限定,小腸:V20<20%,V40<30%,V50<10%,膀胱:V40<50%,股骨頭:V50<5%[7-8]。化療方案:奧沙利鉑(國藥準字H20 143263;規格:50 mg)劑量為 130 mg/m2,靜脈持續輸注2 h,每3 周1 個療程,同時給予卡培他濱(國藥準字H20 073024;規格:0.5 g)的治療,劑量為1 000 mg/m2,2 次/d,治療2 周后停藥1 周,共治療8 個療程,共計6 個月。
觀察組患者在對照組的基礎上聯合恩沃利單抗[國藥準字S20 210046;規格:(200 mg∶1.0 mL)/瓶]治療,400 mg/次,1 次/4 周,皮下注射,共治療6 個療程,共計6 個月。
1.4 觀察指標
1.4.1 近期療效評價 依據世界衛生組織(World Health Organization,WHO)關于實體瘤療效評價標準進行近期療效評估,完全緩解(complete response,CR):所有靶病灶完全消失,至少維持4 周;部分緩解(partial response,PR):所有目標病灶長徑總和小于50%以上;疾病穩定(stable disease,SD):介于PR與PD 之間;疾病進展(progression disease,PD):出現一個或多個新病灶,或目標病灶長徑總和增大25% 以上,以客觀緩解率(objective response rate,ORR)和疾病控制率(disease control rate,DCR)評估療效。ORR=CR%+PR%;DCR=CR%+PR%+SD%。
1.4.2 不良反應評價 參照常用藥物毒性標準(com‐mon toxicity criteria,CTC)和放射腫瘤協會(rtog therapy oncology group,RTOG)的不良反應標準評價兩組患者治療后出現的不良反應。分為0~Ⅳ級,Ⅲ級以上為嚴重不良反應。不良反應發生率=不良反應發生例數/總例數×100.00%。
1.4.3 遠期療效 依據患者納入本研究的時間,對所有患者進行隨訪,隨訪日期截至2022 年1 月1 日,計算總生存時間(overall survival,OS),即直腸癌術后當天至末次隨訪或死亡的時間,統計局部區域復發時間,即直腸癌手術后至腫瘤盆腔淋巴結轉移或盆腔內復發的時間,以及遠處轉移時間,即直腸癌手術后至盆腔以外淋巴結或臟器出現腫瘤轉移病灶的時間。
1.5 統計方法
采用SPSS 22.0 統計學軟件對數據進行處理,計量資料符合正態分布,以()表示,組間差異比較采用t檢驗;計數資料以頻數和百分比(%)表示,組間差異比較采用χ2檢驗,應用Kaplan-Meier 方法分析患者生存情況,采用Cox 比例風險模型分析患者預后影響因素,P<0.05 為差異有統計學意義。
2 結果
2.1 兩組患者近期療效對比
治療6 個月后,對照組CR4 例,PR16 例,SD10例,PD10 例,ORR、DCR 分別為50.0%、75.0%,觀察組CR8 例,PR15 例,SD12 例,PD5 例,ORR、DCR 分別為57.5%、87.5%均高于對照組,但差異無統計學意義(χ2=0.453、2.051,P>0.05)。
2.2 兩組患者不良反應對比
治療6 個月后,兩組患者均發生不同程度的不良反應,兩組患者在胃腸道、放射損傷、肝腎功能損害、血液系統損害、神經系統損害等方面發生率對比,差異無統計學意義(P>0.05),見表1。
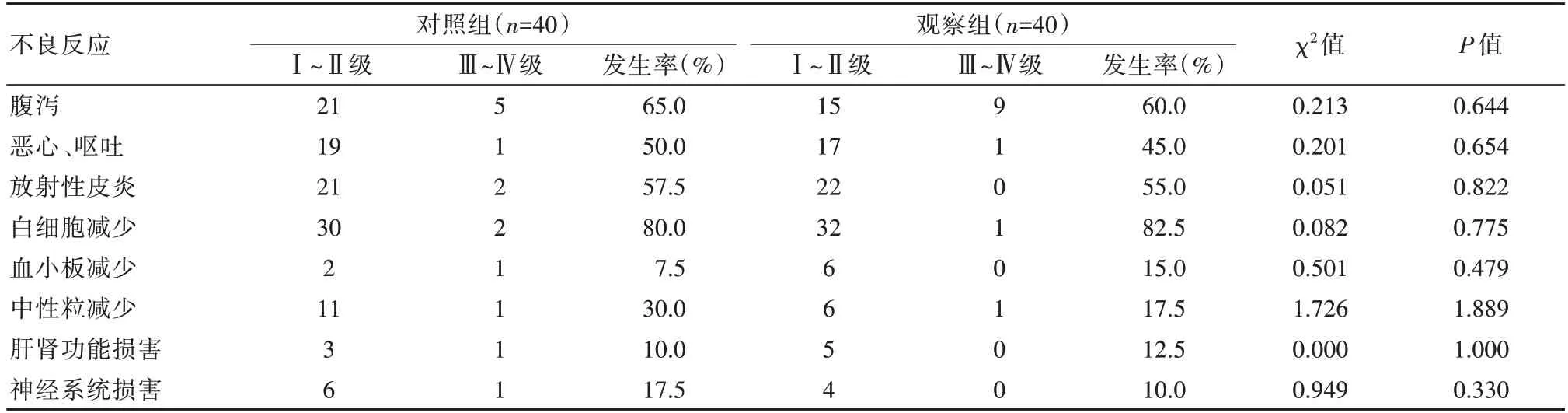
表1 兩組患者不良反應發生情況比較
2.3 兩組患者遠期療效對比
隨訪時間截至2022 年1 月1 日,對照組總生存時間為(29.87±1.59)個月,95%置信區間為26.759~32.981,觀察組總生存時間為(33.14±0.88)個月,95%置信區間為31.412~34.867,兩組患者OS 比較,差異有統計學意義(t=11.380,P<0.05);對照組3 年局部復發率、遠處轉移率分別為20.0%(8/40)、15.0%(6/40),顯著高于觀察組的2.5%(1/40)、0.0%(0/40),差異有統計學意義(χ2=4.507、4.505,P<0.05),對照組總生存率為72.5%(29/40),顯著低于觀察組的90.0%(36/40),差異有統計學意義(χ2=4.021,P<0.05)。見圖1。
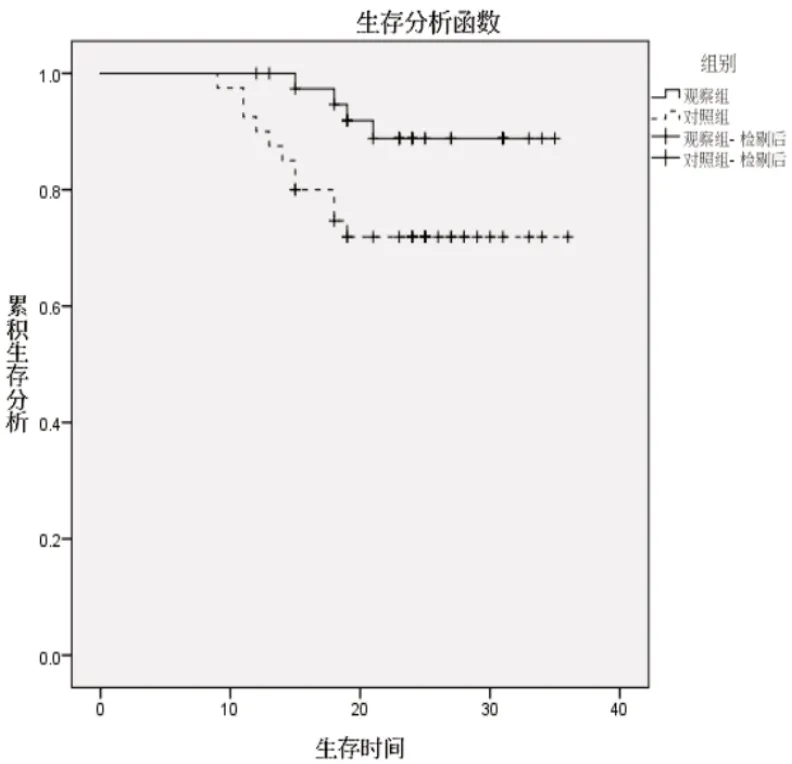
圖1 對照組和觀察組的OS
2.4 預后影響因素分析
分別對患者年齡、性別、癌癥分化程度及淋巴結轉移數目進行Cox 分析,結果顯示淋巴結轉移數目是Ⅲ期直腸癌術后患者3 年OS 獨立預后影響因素(P<0.05),而年齡、性別、癌癥分化程度不是影響3 年OS 的獨立影響因素(P>0.05),見表2。
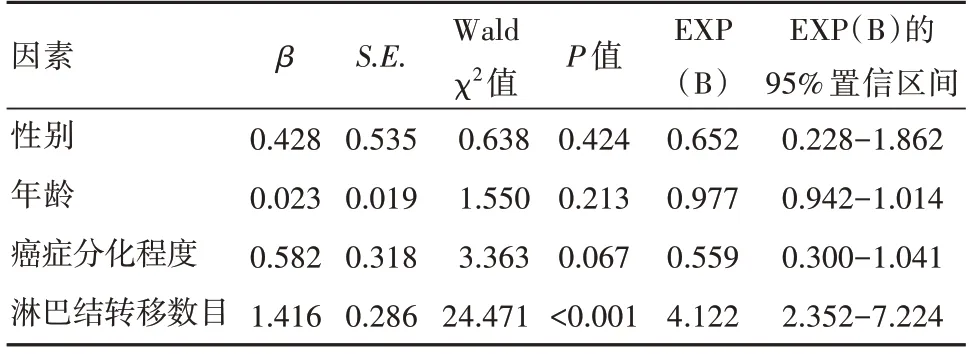
表2 影響Ⅲ期直腸癌術后患者3 年OS 的Cox 分析
3 討論
免疫療法被認為是一種有前途的抗癌治療方法,并已進行了數年的研究。盡管一些研究表明直腸癌患者對免疫療法很敏感,但在臨床實踐中只取得了很小的好處[9-10]。目前通過抑制免疫檢查點途徑取得的成功,如PD-L1 途徑,是免疫治療的一個突破。PD-1 是一種抑制分子,通過與其配體PDL1 的特異性作用抑制T 細胞的增殖和活化,限制效應T 細胞功能。PD-L1 組織分布廣泛,可以向免疫細胞提供抑制信號,從而抑制免疫反應。大多數腫瘤細胞可以上調 PD-L1 的表達,因此,這種機制可能有利于降低T 細胞對癌癥的細胞毒性并逃避抗癌免疫反應[11-13]。在非小細胞肺癌中,PD-1/PD-L1抑制劑已被推薦作為晚期 PD-L1 高表達的一線治療藥物。有文獻報道,有15%的直腸癌患者存在錯配修復功能的缺陷,而此類患者中腫瘤 PD-L1 表達水平非常低(<3%),單獨使用免疫檢查點抑制劑無效[14-16]。但一些研究表明,放化療治療后直腸癌中PD-L1 表達升高,這表明免疫檢查點抑制劑與CRT 聯合使用可能會提高晚期直腸癌的反應率[17]。本研究對Ⅲ期直腸癌患者術后放化療同時進行恩沃利單抗治療,結果顯示,觀察組ORR、DCR 均高于對照組但差異無統計學意義(P>0.05),這表明恩沃利單抗的近期療效優勢并不顯著,兩組患者均發生不同程度的不良反應,但差異無統計學意義(P>0.05),可見聯合沃麗恩單抗治療不增加患者放化療治療毒副作用,在蔡鵬[18]的研究中顯示,Ⅱ+Ⅲ期直腸癌根治術后卡培他濱或聯合奧沙利鉑同期放化療可將總生存率提高為77.8%,本研究結果顯示Ⅲ期直腸癌根治術后放化療聯合恩沃利單抗總生存率可達到90.0%,其觀察組總生存時間顯著長于對照組,對照組3 年局部復發率、遠處轉移率顯著高于觀察組(P<0.05)。這說明恩沃利單抗的遠期療效非常顯著,可明顯改善患者生存狀況,通過Cox分析顯示淋巴結轉移數目是影響患者OS 的風險因素(P<0.05),進一步說明Ⅲ期直腸癌患者術后放化療聯合應用恩沃利單抗優勢顯著。
綜上所述,Ⅲ期直腸癌根治術后放化療聯合恩沃利單抗取得較好的近期療效,顯著降低遠處轉移率和局部復發率,提高患者總生存期,且不增加遠期毒副反應發生率。

