嵌合抗原受體T細胞治療復發難治彌漫大B細胞淋巴瘤進展
李 青,鄧 琦
(天津市第一中心醫院 血液科,天津 300190)
彌漫大B細胞淋巴瘤(diffuse large B-cell lymphoma, DLBCL)是成人中最常見的非霍奇金淋巴瘤,在初診患者中占 35%~40%[1]。目前R-CHOP方案為標準一線治療方案,治療后約60%的患者可達完全緩解并實現長生存。但10%~15%的DLBCL患者原發耐藥,20%~25%會出現疾病復發[2], 中位總生存僅6個月[3],這部分難治復發DLBCL(R/R DLBCL)患者即使應用二線或多線治療能夠達到疾病緩解甚至進行自體造血干細胞移植,但多數仍會出現疾病再次復發進展,為治療的難點。嵌合抗原受體T細胞(chimeric antigen receptor T cell, CAR-T)的出現改變了R/R DLBCL的治療模式,本文就近年CAR-T細胞在R/R DLBCL患者中的治療進展做一綜述。
CAR-T細胞是通過基因修飾的方法在T細胞表面嵌合特定的抗原受體,也就是CAR結構,它能特異性結合腫瘤抗原,引起T細胞的擴增、活化,并釋放大量細胞因子[4],突出特點是高度特異性、非MHC限制性及強烈而持久的殺瘤效應。目前大多數CAR由單鏈可變區結構(single chain variable fragment,scFv)、跨膜區域和胞內信號轉導區組成(圖1)。一代CAR-T細胞內僅含一個活化結構域,缺乏共刺激信號,因此其在特異性識別腫瘤細胞相關抗原后的殺傷作用十分有限[5],二代CAR-T胞內含有一個活化結構域和一個共刺激區域,比如:CD28或4-1BB[6-7],增強了CAR-T的擴增和殺傷作用,三代CAR-T胞內部分則由活化結構域和多重共刺激區域組成,如:CD27,CD28,4-1BB和OX40等,這些結構域的增加不但能夠增加CAR-T細胞特異性識別及結合等能力,更能夠顯著擴大由胞外區傳遞的細胞信號,引起下級細胞殺傷作用的級聯增大。但因此引起細胞因子過度釋放,導致殺傷腫瘤細胞的同時造成正常器官的損害。最新的第四代或更新一代CAR-T技術將細胞因子的胞內段也放入嵌合受體上,能夠自分泌細胞因子招募更多的免疫細胞,進一步促進T細胞擴增和細胞因子的釋放,從而增強CAR-T的療效[8]。現階段獲批或臨床試驗應用比較廣泛的是第二代CAR-T。
1 目前獲批上市治療R/R DLBCL的CAR-T細胞產品進展(表1)
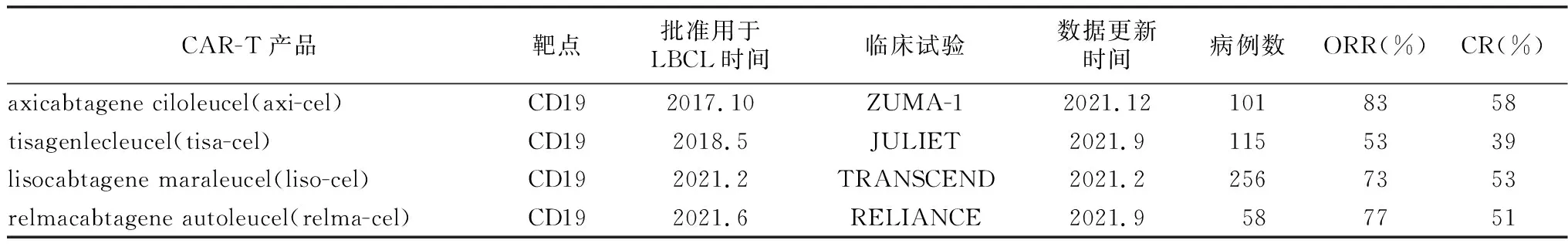
表1 目前上市的CART產品進展概況
1.1axicabtagene ciloleucel(axi-cel) 是包含CD28共刺激結構域的第2代CAR-T細胞,靶向腫瘤細胞的CD19抗原。2017年10月公布ZUMA-1研究結果,axi-cel治療R/R DLBCL客觀反應率(objective response rates,ORR)66%,完全緩解率(complete response rates,CRR)47%,美國食品藥品管理局(Food and Drug Administration,FDA)批準axi-cel用于治療二線及以上全身治療無效的R/R DLBCL[9-10],2018年6月年歐洲藥物管理局(European Medicines Agency EMA)批準上市。近期文獻報道了ZUMA-1兩年的隨訪結果并與挽救性化療進行對比[11],101例R/R DLBCL患者應用axi-cel,中位隨訪27.1個月, ORR 83%, CRR 58%,2年生存率為54%。亞組分析顯示,65歲以上的老年患者ORR和CRR分別為92%和75%,2年總生存(overall survival,OS)率為54%。同時與此前的SCHOLAR-1中挽救化療的患者進行對比,挽救化療ORR和CRR分別為34%和12%,2年生存率僅為20%[3]。2021年12月召開的第63屆美國血液學年會公布ZUMA-1的4~5年隨訪數據, 101例患者中位隨訪51.1個月,4年OS率為44%,1年無事件生存(event-free survival,EFS)率為43%,24個月EFS率為38%,且數據提示在第1年和第2年持續EFS的患者OS更長。不良反應方面:未見新的嚴重不良事件發生,且無axi-cel相關繼發性惡性腫瘤和具有復制能力的逆轉錄病毒確診病例[12]。上述隨訪結果肯定了axi-cel的長期療效。
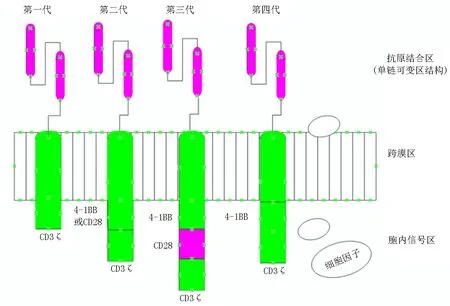
圖1 CART結構示意圖
1.2tisagenlecleucel(tisa-cel) 為靶向CD19的包含4-1BB共刺激結構域的第2代CAR-T細胞產品,依據JULIET研究結果[13],2018年5月美國FDA 批準tisa-cel用于治療R/R DLBCL、轉化性濾泡性淋巴瘤(TFL)和高級別B細胞淋巴瘤。柳葉刀2021年發布了JULIET研究的II期長期隨訪結果,115例未進行移植或移植后復發的R/R大B細胞淋巴瘤(R/R LBCL)患者,接受單劑tisa-cel,中位隨訪40.3個月,ORR為53%,CRR為39%,細胞因子釋放綜合征(cytokine release syndrome,CRS)發生率為57%,無治療相關死亡[14]。由于缺乏隨機對照研究,有學者將tisa-cel的JULET研究與axi-cel的ZUMA-1研究匹配調整后進行了比較,認為axi-cel有更高的緩解率,但1-2級CRS發生率更高,而3級以上CRS和神經毒性的發生率兩者無差別[15]。
1.3lisocabtagene maraleucel(liso-cel) 同樣是包含4-1BB共刺激結構域的第2代CAR-T細胞產品,liso-cel與tisa-cel不同之處是由純化的CD8+和 CD4+T 細胞以 1∶1 組成,根據 TRANSCEND研究結果[16],2021年2月美國FDA批準liso-cel用于治療R/R LBCL。本研究中269例患者,包含3%繼發中樞神經系統受累的患者,ORR和CRR分別為73%和53%,CRS發生率42%。在R/R DLBCL患者中,與挽救化療比較[17],匹配分析均顯示liso-cel組較挽救化療組具有優勢,ORR分別為71%對26%,CRR分別為49%對7%,OS為20.5個月對6個月。在與axi-cel的對比中,兩者的治療有效率相似,但liso-cel的嚴重不良事件的發生率更低[18]。
1.4relmacabtagene autoleucel(relma-cel;阿基侖賽注射液) 同樣為靶向CD19的第2代CAR-T。一項中國復發難治非霍奇金淋巴瘤患者的多中心、開放標簽、單臂Ⅱ期研究中(RELIANCE的研究),58 例患者接受了relma-cel治療,中位年齡為56歲。截至2020年12月31日,ORR為77.6%,CRR為51.7%。中位隨訪時間為17.9個月,12個月OS率76.8%[19]。2021年6月,中國國家藥品監督管理局(NMPA)批準relma-cel用于治療既往接受二線或以上系統性治療后R/R DLBCL成人患者(包括DLBCL非特指型、原發縱膈大B細胞淋巴瘤、高級別B細胞淋巴瘤和濾泡淋巴瘤轉化的DLBCL)。
2 CAR-T治療R/R DLBCL臨床試驗進展
迄今為止上市的CAR-T均靶向CD19抗原,治療失敗或耐藥的主要原因一方面是腫瘤的抗原逃逸,多表現為CD19陰性復發,也就是腫瘤細胞表面不表達CD19抗原;另一方面為腫瘤微環境中存在的多種抑制分子及自身免疫抑制機制,可能降低CAR-T擴增及殺傷活性。因此目前研究方向主要涵蓋更換抗原位點或改善腫瘤微環境兩方面。全球多項臨床試驗開展新靶點、多靶點的CAR-T以及多種聯合治療方案,以進一步提高療效、減少疾病復發。
2.1CD19/CD22 CAR-T CD19/CD22 雙靶點CAR-T可以克服CD19 CAR-T的抗原逃逸現象,2021年中國學者的一項CD19/CD22雙靶點CAR-T治療復發難治侵襲性B細胞淋巴瘤的研究中[20],16例入組的患者中,ORR為87.5%,CRR為62.5%,2年OS率 77.3%,無進展生存(PFS)率40.2%。4級以上CRS發生率6%。另有關于CD19/CD22 雙靶點CAR-T或CD19 CAR-T和CD22 CAR-T序慣輸注治療B細胞淋巴瘤的零星報道[21]。
2.2CD19/CD20 CAR-T 一項關于CD19/CD20串聯雙特異CAR-T的研究顯示,應用4-1BB-CD3ζ LV20.19 CAR T治療22例患者,82%患者有效,CRR達64%,為CD19弱表達或陰性的R/R DLBCL患者提供了治療選擇[22],我國學者關于優化的串聯CD19/CD20 CAR-T治療B細胞淋巴瘤的試驗結果2020年10月發布于BLOOD雜志[23],28例患者ORR和CRR分別為79%和71%,12個月PFS率為64%,CRS發生率為50%,3級以上CRS占14%。針對R/R DLBCL的Ⅱ期試驗[24],21例患者ORR和CRR分別為81%和52.4%,3~4級CRS和CAR-T相關性腦病綜合征(CRES)發生率為28.5%和9.5%。另一項應用LV20.19 CAR-T治療B細胞淋巴瘤的試驗結果顯示22例患者ORR為82%,CRR 64%,3~4級CRS的發生率為5%[22]。
2.3其他新靶點CAR-T CD79b CAR-T、Igβ-CAR T 在B細胞淋巴瘤的基礎實驗及動物實驗中有效[25]。另有我國學者設計的CD70 CAR-T應用于CD19陰性的復發難治B細胞淋巴瘤中,相關臨床試驗招募中[26]。
2.4CAR-T的聯合療法 CD19 CAR-T 在治療成人及兒童 B-ALL 中的完全緩解率高達90%[27], 但在ZUMA和JULIET研究中表明,CD19 CAR-T在R/R B細胞淋巴瘤中CRR僅50%左右[9, 28]。因此如何進一步提高CAR-T在R/R DLBCL患者當中的療效成為研究的熱點,除了新靶點、多靶點CAR-T外,近年出現了CAR-T的聯合治療。
“免疫檢查點療法”是通過阻斷被癌細胞激活的免疫抑制通路以提高T細胞抗腫瘤免疫應答的治療方法。程序性死亡分子及其配體(PD-1/PD-L1) 抑制劑是常見的免疫檢查點療法。在腫瘤特異性抗原刺激下,CAR-T細胞PD-1的表達會顯著上調,造成其抗腫瘤免疫反應的削弱[29]。Chong等[30]報道了1例R/R DLBCL 予以CAR-T治療,26天后因疾病進展予以PD-1抑制劑治療,獲得較好臨床反應。并且觀察到應用PD-1抑制劑后,CD19CAR-T的增殖活性有了大幅度提高。為了探索PD-1/PDL-1阻斷劑與CAR-T聯合治療R/R DLBCL的療效、最佳方案及合適劑量,目前有多項臨床試驗正在進行(NCT02706405、NCT02926833和NCT03310619)。
已有基礎實驗及動物實驗表明,Bruton’s tyrosinekinase抑制劑(BTK抑制劑)能夠增強CAR-T的抗腫瘤療效[31-32],Fraietta等[33]報道,BTK抑制劑在慢性淋巴細胞白血病患者中能夠促進CAR-T的植入及擴增,從而增強療效, Liu等[34]報道在套細胞淋巴瘤和濾泡淋巴瘤中觀察到相似的現象。目前BTK抑制劑聯合CAR-T在R/R DLBCL中的療效尚無報道,相關臨床試驗招募中((NCT04257578)。
關于CAR-T與放療的聯合包括放療作為CAR-T輸注前的橋接治療以及作為CAR-T治療后的挽救治療兩種方式。有學者報道,在R/R DLBCL中,放療作為axi-cel之前的橋接治療,ORR 81.8%,重度CRS的發生率為27%[35]。Imber等[36]用放療作為CAR-T后挽救治療,14例患者治療反應率達100%,中位總生存為10個月。目前放療與CAR-T聯合治療的最佳方案尚無定論。
3 CAR-T成本效益
與成品藥物不同,由于CAR-T的制備需要采集患者外周血T細胞,為患者“量身定做”特異性CAR-T,因此時間成本及經濟成本高,甚至限制了其臨床應用,特別是在發展中國家。有學者對現有產品tisa-cel在R/R DLBCL中的應用進行了成本效益分析[37], 相對于傳統化療來說,雖然CAR-T的治療費用高,但質量調整生命年(quality-adjusted life year, QALY)增加, 成本效益較挽救化療具有明顯優勢。日本學者的研究得出了同樣的結論[38]。近年來,關于CAR-T能否產品化的研究一直在進行,“通用型CAR-T”或“Off-the-Shelf”能夠讓CAR-T的治療更加經濟、方便和快捷,避免了每例患者進行采集-制備的繁瑣過程,但免疫排斥和供者CAR-T在患者體內的迅速耗竭一直是研究中的難點[39-40],也是目前國內外研究的熱點。
4 CAR-T治療的不良反應
隨著CAR-T技術的逐漸成熟,目前CAR-T治療的淋巴瘤患者最長隨訪時間已達5年以上,因此CAR-T治療的不良反應逐步被認識,處理手段日趨完善。包括CRS、免疫效應細胞相關神經毒性綜合征(immune effector cell-associated neurotoxicity,syndrome,ICANS)、脫靶效應以及B細胞功能障礙、感染等。
CRS是CAR-T治療過程中最常見的不良反應,本質是CAR-T識別靶細胞后自身被激活產生大量炎癥因子,引起的全身炎癥反應,包括發熱、乏力、肌肉酸痛等非特異癥狀及各個器官系統不同程度的損害。目前已有的分級系統包括最早的Penn標準、常用的LEE標準以及最新的由美國移植與細胞治療學會(the American Society for Transplantation and Cellular Therapy,ASTCT)定義的分級系統[41-43]。針對JULIET研究中的CRS分析顯示,對于同樣的患者,Penn分級評價的患者CRS級別較Lee標準和ASTCT標準更高[44],而針對3個分級標準的比較顯示目前指南對細胞因子抗體和糖皮質激素的不同建議可能導致過度或延誤治療[45]。
目前ICANS的具體發病機制仍未完全闡明,患者的臨床表現有明顯異質性,包括頭痛、躁狂、昏迷、癲癇、語言障礙、書寫障礙等等,ASTCT 提出了 ICANS 共識分級標準[41]。單中心的分析表明,在R/R DLBCL中,ICANS的發生率與患者的CR率和OS無關,同時發現高水平的D0纖維蛋白原提示發生ICANS的風險增加[46]。
CAR-T治療后由于B細胞缺乏或功能缺陷,感染風險增加,一項研究分析了60例DLBCL患者應用CAR-T治療1年,細菌、病毒和真菌的累計發生率分別為57.2%, 44.7%, 4%。多因素分析顯示主要危險因素為糖皮質激素的應用和感染史[47]。
5 小結和展望
CAR-T治療開啟了細胞免疫靶向治療的新時代,改變了難治/復發腫瘤的治療現狀,目前CAR-T已經成為經二線治療無效的R/R DLBCL患者的首選推薦方案,上述進展顯示CAR-T較挽救化療治療有效率明顯提高,能否將CAR-T治療作為首次復發患者的二線治療方案,甚至能否作為一線清除微小殘留病方案值得進一步探究[48],特別是對于化療耐藥的患者,CAR-T治療能否代替自體造血干細胞移植,目前已有隨機研究正在進行[49]。未來的研究方向包括一方面進一步篩選更加精準的抗原組合靶向淋巴瘤細胞,另一方面針對腫瘤微環境選取更加合適的聯合治療手段。

