生物質與煙煤混合燃燒特性及動力學分析研究
劉 浪,曾靖淞,焦慶瑞,楊 劍,任 山,唐石云,劉潤學,蒲玉寶
(1.貴州理工學院,貴州 貴陽 550003;2.重慶大學,重慶 400044)
引言
中國作為農業大國,每年會產生大量的農業廢物,如農作物秸稈等生物質,這些生物質通過吸收和釋放CO2的循環過程以可持續的方式生長,避免了CO2在大氣中的沉積[1]。對生物質進行資源化利用,可以減少對化石能源的使用,降低溫室氣體CO2的排放。然而,生物質的使用受到了季節變換、能量密度低和焦油量較大等因素的制約,將生物質和煤共同利用可以實現生物質高效利用[2]。
近年來,研究者對煤和生物質的共同利用進行了大量研究[3-4],如燃燒、熱解和氣化等,其中,煤和生物質的共同燃燒是最有前途的選擇之一。將含有大量固定碳的煤和大量揮發分的生物質共同燃燒,可以在低成本的前提下改善煤的轉化效率,降低SOx、NOx和CO2的排放;此外,生物質的灰分含有大量堿金屬和堿土金屬等,對煤粉的燃燒可起到催化作用,同時脫揮發分過程釋放的大量H 原子和O 原子會在較低的溫度下加速點火;煤和生物質共同燃燒可以減少或完全消除生物質單獨燃燒過程存在的灰沉積、結垢等問題。因此,將煤和生物質共同利用,不僅可以緩解環境問題帶來的壓力,還可以帶來一些技術和經濟收益。
熱分析技術(TGA),如熱重法(TG)和差示掃描量熱法(DSC)被廣泛應用于考察等溫和非等溫模式下煤和生物質燃燒的動力學行為和熱力學特征[5-6]。為了更好地了解共燃反應機理,學者們引用了不同的動力學模型對共燃反應進行分析[4,7]。F.H.GUO 等[4]使用Coats-Redfern(CR)法分析了生物質顆粒與煙煤、褐煤的混合燃燒動力學行為,發現混合燃燒被分為了揮發分逸出/燃燒和焦的燃燒兩個階段,第一階段的燃燒可以用一階模型來描述,而第二階段的燃燒則是由代表擴散控制的模型來描述。W.TONG 等[7]利用CR、Flynn-Wall-Ozawa(FWO)和Kissinger-Akahira-Sunose(KAS)法等研究了無煙煤與生物質焦的混合燃燒特性和動力學行為,結果表明CR 法與FWO、KAS 法計算出的活化能存在顯著差異,其中生物質焦質量分數為40%時CR法最適用。
然而,現下對共燃燒反應機理的研究多聚焦于使用某一種或同類型的動力學模型對燃燒動力學進行分析,鮮有研究針對燃燒反應整個過程不同動力學模型的適用性。因此,為了提供煙煤和生物質共燃燒的理論基礎和科學依據,本文通過熱分析方法對煤和生物質共燃燒的動力學參數和熱力學行為進行研究,選用模型擬合法CR 和無模型法FWO、KAS 分析共燃燒動力學,在此基礎上分析煤和生物質共燃燒的反應機理,并確定不同動力學模型適用的反應階段。
1 實 驗
1.1 原料
原料煤選用重慶煙煤(Bituminous Coal,BC),生物質選擇我國最常見的農作物麥稈(Wheat Straw,WS)。煤與生物質的工業分析和元素分析見表1。

表1 煤和生物質的工業分析和元素分析
煤和生物質采用機械混合,混合時間定為10 min,以防止樣品混合不均勻所引起的實驗誤差。混合樣品分別標記為BC-10%WS、BC-20%WS 和BC-40%WS,其中,樣品中數字代表混合樣品中WS 的混合比例(質量分數),如BC-10%WS 表示WS 質量分數為10%。
灰分樣品的制備參照ASTM E1755—01,在馬弗爐中將混合樣品燒制成灰。將約1 g 樣品置于剛玉坩堝中,以10 K/min 的速率加熱至250 ℃并保持30 min,然后在30 min 內將溫度升高至預設溫度并保持4 h。在這種控制溫度下產生灰分的程序是為了避免因火焰燃燒而造成無機元素的揮發[8]。溫度降至室溫后取出樣品稱量,直至燃燒后所得灰分質量不再變化后,將灰分樣品研磨至粒度75 μm 以下。
利用X 射線熒光光譜儀(XRF,賽默飛世爾ARL Perform′X)分析混合樣品的灰成分,結果如表2 所示。由表2 可以發現,隨著生物質混合比例的增加,灰分中酸性氧化物(SiO2、Al2O3)含量有所下降,與原料煤相比,當混合樣品中生物質質量分數為40%時,灰分中SiO2質量分數降低了4.48 個百分點,Al2O3質量分數降低了7.48 個百分點,與此同時,CaO、K2O、Na2O和MgO 含量均有一定的增加。對比煤和生物質灰分發現,煤灰分中酸性氧化物質量分數超過了75.00%,而生物質灰分中的酸性氧化物質量分數低于50.00%,且生物質灰分中含有大量的堿性氧化物。

表2 混合樣品灰分中各化學成分含量(質量分數)%
1.2 熱重實驗
在瑞士梅特勒熱重分析儀(TGA/DSC1/1600LF)進行燃燒反應實驗;待測樣品先在100 ℃干燥24 h 后,再進行熱重實驗,防止樣品中水分的存在影響實驗結果。每次稱取5 mg±0.2 mg 的樣品放入剛玉坩堝,分別以10 K/min、20 K/min 和30 K/min 的升溫速率在空氣氣氛下將樣品從室溫加熱至1000 ℃,空氣流量為50 mL/min;全程通N2作為保護氣,流量為50 mL/min。
1.3 燃燒反應特性
生物質的混合比例和升溫速率會影響混合樣品的燃燒反應性能。為定量分析混合樣品的燃燒反應特性,需引入一系列燃燒反應特性參數。Ti為著火溫度(單位K),反映了燃燒著火性能,Ti越低,樣品的著火性能越好,更易在溫度低的情況下開始燃燒;Tf為通過TG-DTG 方法定義的燃料燃燼溫度(單位K),體現燃料燃燼的難易程度,Tf越低,燃料的燃燼性能越好。(dx/dt)max和(dx/dt)mean分別對應最大燃燒速率和平均燃燒速率。為綜合描述燃燒反應性能,基于阿倫尼烏茲方程和上述參數提出了綜合燃燒特性指數(S),是反映著火和燃燼的綜合指數,其值越大,意味著燃燒反應性能越好。S 值由式(1)計算得到:
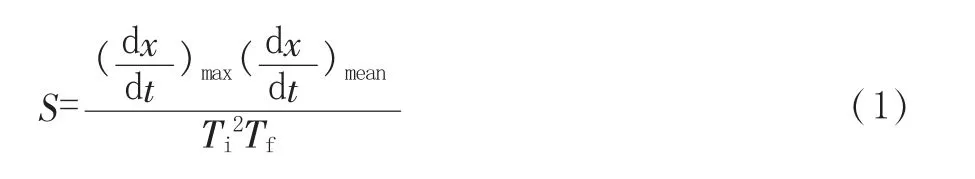
1.4 動力學分析
煤是一種成分復雜的燃料,其中有機和無機組分對燃燒過程的影響各不相同。目前為止,煤的具體燃燒機理尚不清晰,為了解煤燃燒過程機理,研究者們針對煤的非等溫燃燒過程提出了基于模型和無模型的兩種動力學方法,利用不同動力學方法對TGA 和DTG 結果進行公式計算,所得動力學參數可以用于煤的非等溫燃燒機理分析[9-11]。上述兩種方法都是基于煤燃燒的轉化率與時間的關系[見式(2)]所得:

式中:x 為燃燒轉化率,%;t 為燃燒反應時間,min;f(x)為假想的燃燒機理函數;K(T)為反應速率常數,是與溫度T 相關的函數,可以用Arrhenius 公式[式(3)]來表達:

式中:E 為反應活化能,kJ/mol;k0為指前因子;R 為摩爾氣體常量,值為8.314 J/(mol·K);T 為熱力學溫度,K。
轉化率x 可以基于初始質量m0、最終質量m∞和瞬時質量mt間關系計算得到,具體關系式見式(4):

對于非等溫熱重分析,當加熱速率β=dT/dt 為常數時,可將式(2)轉化為式(5):
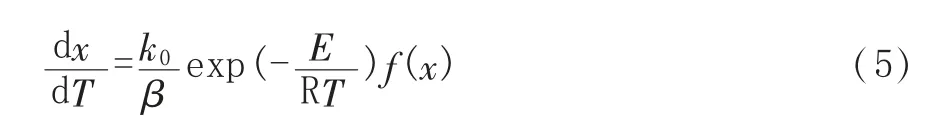
將式(5)通過積分整理可得式(6):
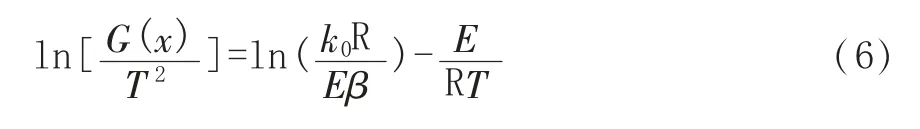
式中:G(x)為常見的機理函數,見表3。
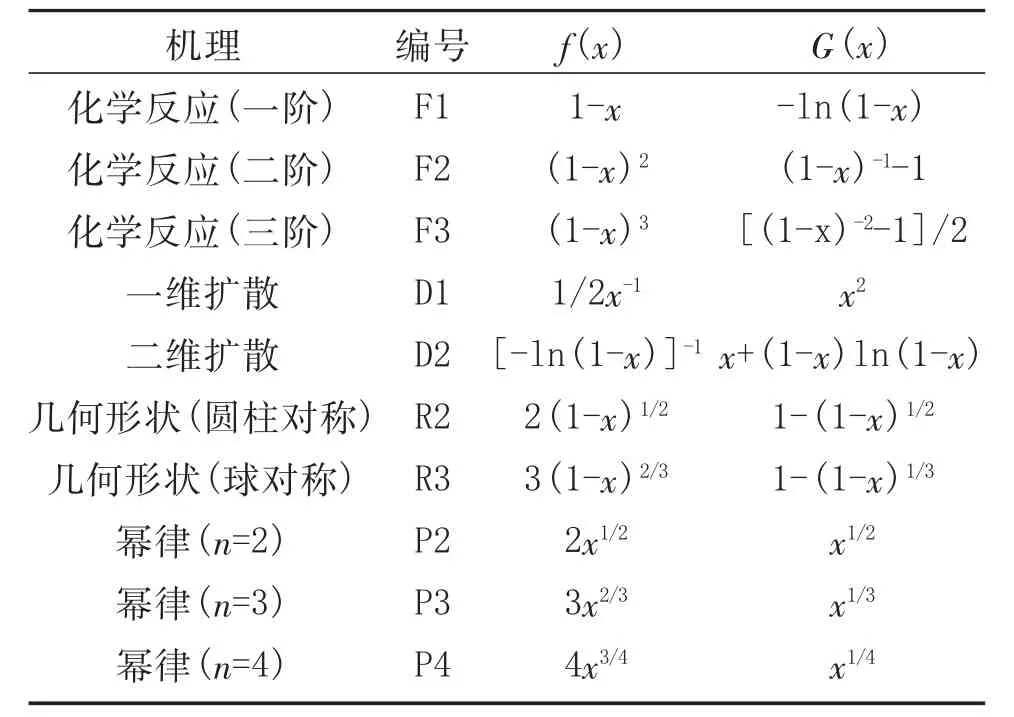
表3 常見機理函數
通過式(6),可以計算基于不同燃燒動力學方法的動力學參數。使用CR 法[12-13]分析煤燃燒動力學行為時,可將式(6)通過變量分離和積分后得到式(7):
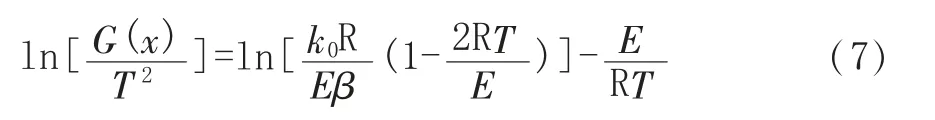
在大多數燃燒反應中,2RT/E 遠小于1,因此ln[k0R(1-2RT/E)/Eβ]可當作常數[14],利用等轉化率法,根據式(6)中的ln[G(x)/T2]與-1/T 的線性關系,擬合散點后,所得擬合直線的斜率(E/R)和截距可用于計算燃燒反應的活化能E 和指前因子k0。
無模型動力學方法是在不選擇反應級數的前提下對阿倫尼烏茲參數進行計算[15-16],這一方法需遵從等轉化率法,即在一定轉化率下,反應速率僅與反應溫度有關。將式(7)積分整理后可得式(8):

將式(5)使用doyle 近似法[17]整理后,可得FWO法[18-19],見式(9):

式(9)僅當E/RT 值處于20~60 時才有效[19],斜率(E/R)可通過lnβ 在不同升溫速率下的固定轉化率對應-1/T 的線性關系求得。
KAS 法處理方法與FWO 法相似,見式(10):
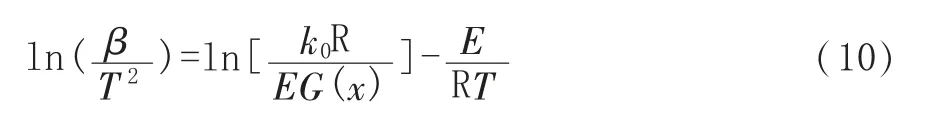
式(10)左邊與-1/T 在固定轉化率下為線性關系,燃燒反應活化能可通過直線斜率計算得到。值得注意的是,KAS 法僅當E/RT 居于20~50 時才能生效。
2 結果與討論
2.1 混合燃燒特性分析
煤和生物質的混合燃燒分別在10 K/min、20 K/min 和30 K/min 的升溫速率下進行,樣品的TG 和DTG曲線如圖1 所示。
由圖1 可知,煤和生物質混合燃燒的TG 和DTG曲線可分為3 個階段:Stage1 階段燃燒轉化率和速率不受溫度升高影響;Stage2 階段溫度的升高為煤的分解與反應提供了必要的熱力學條件,揮發組分和氣體產物的釋放使得TG-DTG 曲線發生明顯變化,而添加了生物質后,Stage2 階段可分為Phase1 和Phase2 兩個階段,分別對應揮發分和焦炭的燃燒;Stage3 階段混合樣品燃燒完全,僅剩灰分成分,樣品質量不再發生變化。煤和生物質的協同作用主要體現在Stage2 階段。圖1 中TG 曲線隨著WS 混合比例的增加向低溫區偏移,說明生物質的添加可以改善相同反應溫度下煤燃燒轉化率。導致這一結果的原因主要有:(1)生物質中揮發分可在較低溫度下燃燒,從而改善燃燒著火點;(2)揮發分的燃燒過程中伴隨著富氫氣體和熱量的釋放,促進了Phase2 階段焦炭的燃燒;(3)生物質灰中富含堿金屬和堿土金屬等對煤燃燒有催化作用的礦物成分,這些成分的存在使得煤燃燒性能得到了一定的提升。
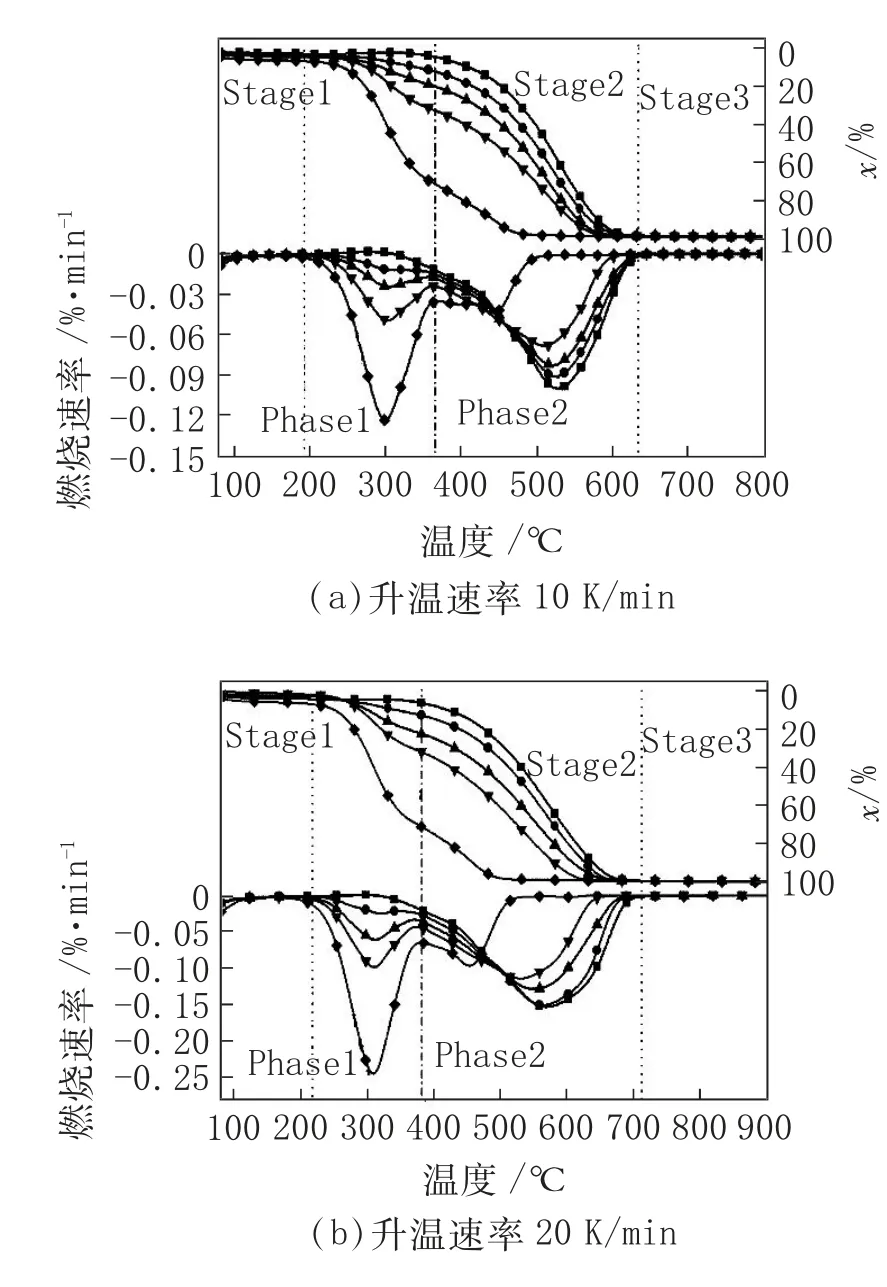
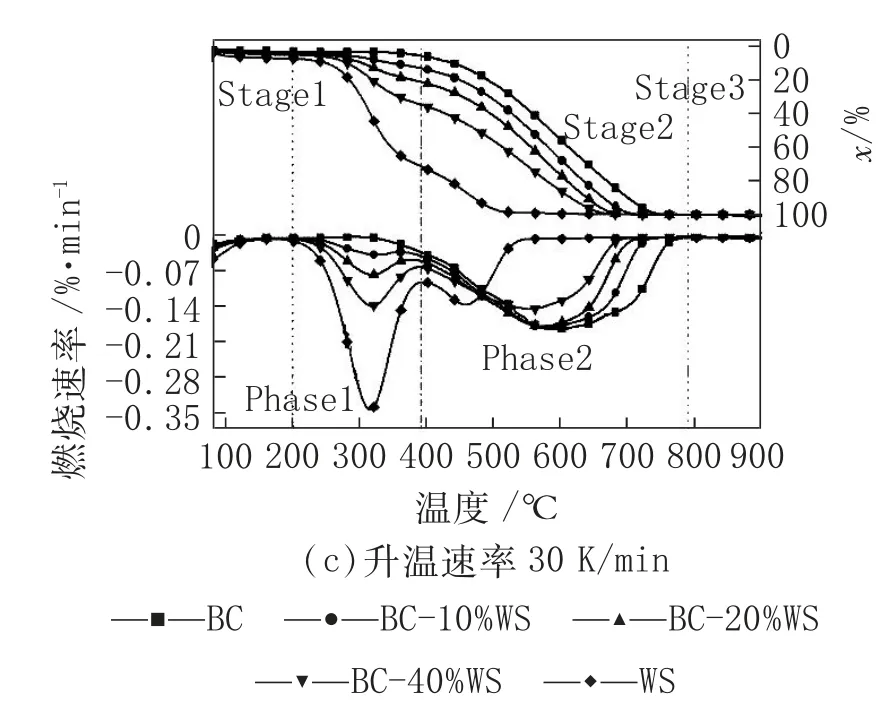
圖1 煤和生物質混合燃燒的TG-DTG 曲線
煤和生物質混合燃燒特性參數見表4。
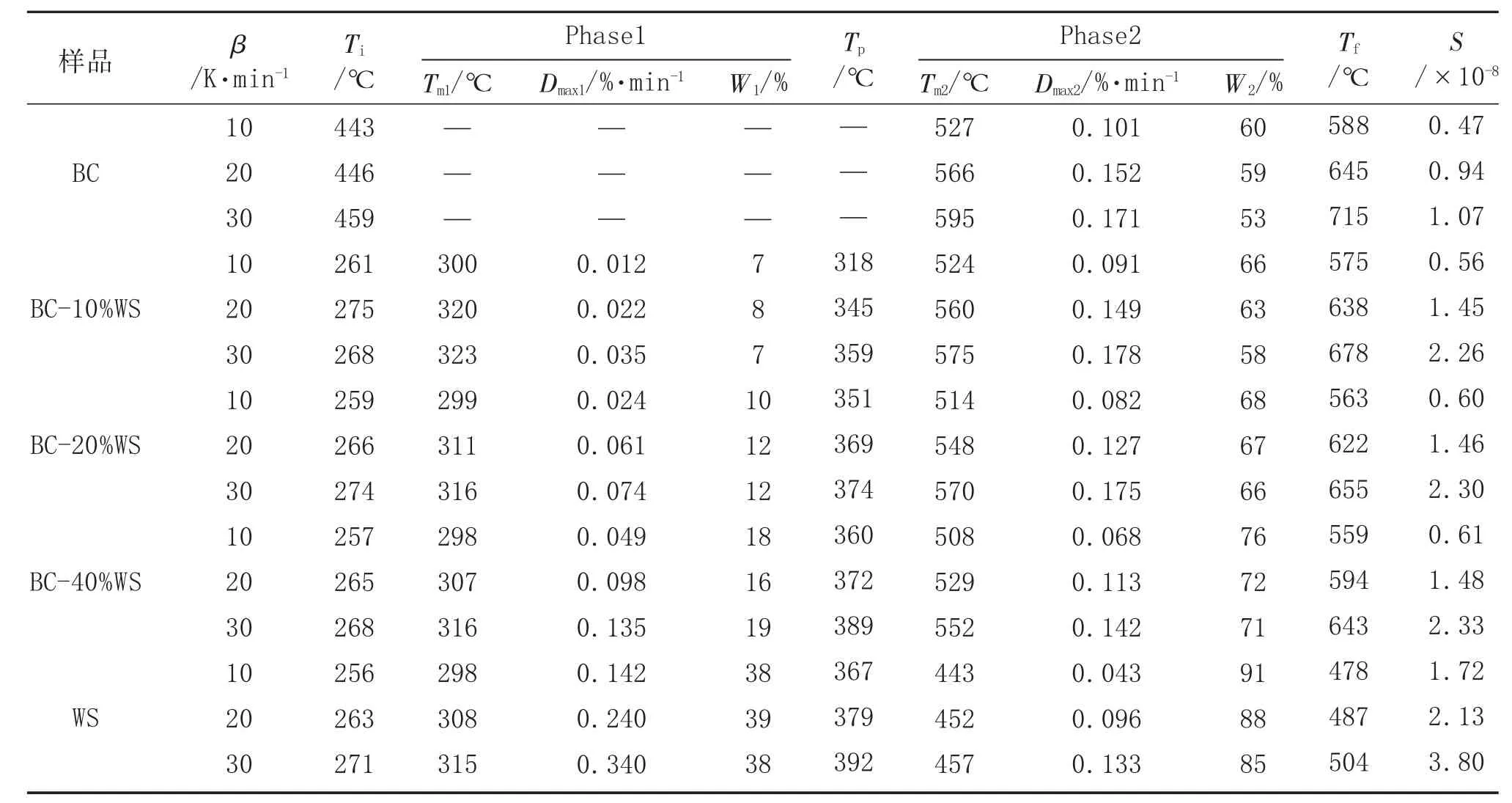
表4 煤和生物質混合燃燒特性參數
由表4 可知,添加了生物質后,樣品著火溫度迅速下降,這是生物質中揮發分燃燒所致,與圖1 結果一致。以升溫速率10 K/min 為例,當生物質質量分數由10%增加到40%時,樣品著火溫度由261 ℃下降到257 ℃,燃燼溫度由575 ℃下降到559 ℃,Phase1 階段最大燃燒轉化速率由0.012%/min 增加到0.049%/min,Phase2 階段最大燃燒轉化速率由0.091%/min 下降到0.068%/min,與圖1 結果一致。燃燼溫度的下降得益于揮發分、生物質灰分組分對焦炭的助燃和生物質自身優異的燃燒特性。煙煤中添加了生物質后,混合樣品燃燒溫度區間擴大,且隨著生物質混合比例的增大,燃燒溫度區間由261 ℃~575 ℃降低到257 ℃~559 ℃,說明增加生物質混合比例可以顯著改善混合樣品的燃燒性能。
為了深入分析增加生物質混合比例對生物質/煤燃燒性能的影響,對混合樣品燃燒的S 值進行計算,結果(見表4)表明,添加了生物質后,混合樣品的S 值顯著增加,隨著生物質質量分數由10%增加到40%,其S 值由0.56×10-8增加到0.61×10-8,進一步印證了生物質對混合樣品燃燒性能的積極影響。
2.2 相互作用分析
通過2.1 節的分析可以發現,生物質的添加可以明顯改善煤燃燒性能。而隨著燃燒反應的進行,煤、煤揮發分、生物質和生物質揮發分之間可能存在著相互作用,僅通過2.1 節的分析尚不能夠清晰地了解添加生物質后,煤、生物質及揮發分間的相互作用對混合樣品燃燒性能的影響。因此,為了更加清晰地了解混合樣品燃燒過程中的相互作用,引入理論燃燒轉化率公式[見式(11)],計算混合樣品的理論燃燒轉化率。

式中:xBC和xWS分別為煤(BC)和生物質(WS)的實際燃燒轉化率,%,由式(4)得到;f1和f2分別為煤(BC)和生物質(WS)在混合物中的質量分數,%。
升溫速率10 K/min 下,混合樣品的實驗和理論計算TG 曲線及兩者偏差見圖2。由圖2 可以發現,實驗TG 曲線與理論計算TG 曲線間存在明顯的差值,實驗TG 曲線呈現出向左偏移趨勢,偏差為負值,這可能是由于生物質的添加可以在低溫區為煤的燃燒提供更多的熱量,從而促進煤燃燒過程中的吸熱反應,使得煤燃燒更加完全。此外,還有研究認為煤和生物質的燃燒由熱效應控制[20],而添加了生物質以后,一方面揮發分在低溫區燃燒釋放熱量有利于促進煤的燃燒,另一方面生物質焦的多孔性也可以對煤的燃燒產生一定的促進作用。
當溫度低于300 ℃時,混合樣品的實驗與理論計算TG 曲線基本重合,無明顯差別,說明較低反應溫度下,煤和生物質間無相互作用或相互作用較弱。隨著溫度進一步升高,實驗和理論值間偏差開始迅速增加,在520 ℃左右達到最大值,此時BC-10%WS、BC-20%WS 和BC-40%WS 偏差值分別為-5.18%、-10.37%和-8.34%,這一時間段內生物質中揮發分燃燒釋放的含氫氣體和熱量使得生物質對煤燃燒產生了積極的協同作用,促進了煤的燃燒;當溫度居于520 ℃~620 ℃時,生物質灰分中存在的堿金屬和堿土金屬對焦炭燃燒有著促進作用,但是外部焦炭燃燒殘余的灰分開始覆蓋在剩余焦炭表面,不利于燃燒反應進行,因此在這一溫度段內的積極協同作用逐漸減弱。此外,由圖2(b)可知,生物質與煤的相互作用不隨WS 混合比例的增加而成比例增加,3 個混合樣品相互作用程度順序為BC-20%WS>BC-40%WS>BC-10%WS。
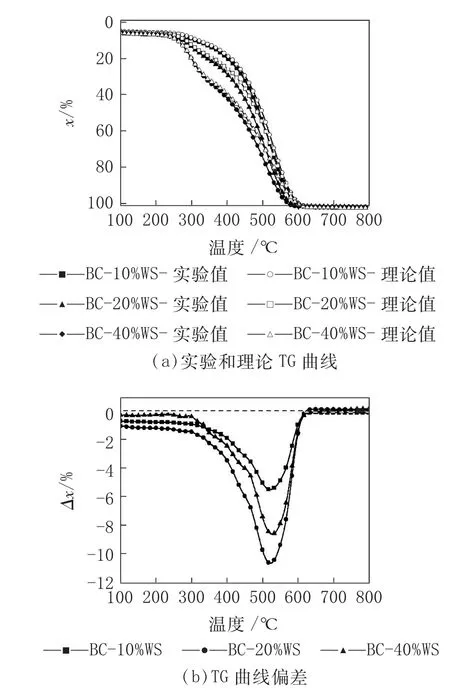
圖2 混合樣品在10 K/min 升溫速率下的實驗和理論TG 曲線及兩者偏差
綜上所述,混合樣品燃燒過程中,生物質揮發分燃燒所釋放的含氫氣體和熱量會迅速傳遞給煤,從而促進煤的燃燒,并且生物質中灰分也對煤的燃燒存在著不可以忽視的促進作用。
2.3 燃燒動力學分析
動力學參數通過動力學方法CR、FWO 和KAS 計算得到,活化能和指前因子可由擬合直線的斜率和截距得到。以升溫速率10 K/min 為例,使用CR 法,計算不同機理函數下的活化能和擬合相關系數(R2),結果見表5。
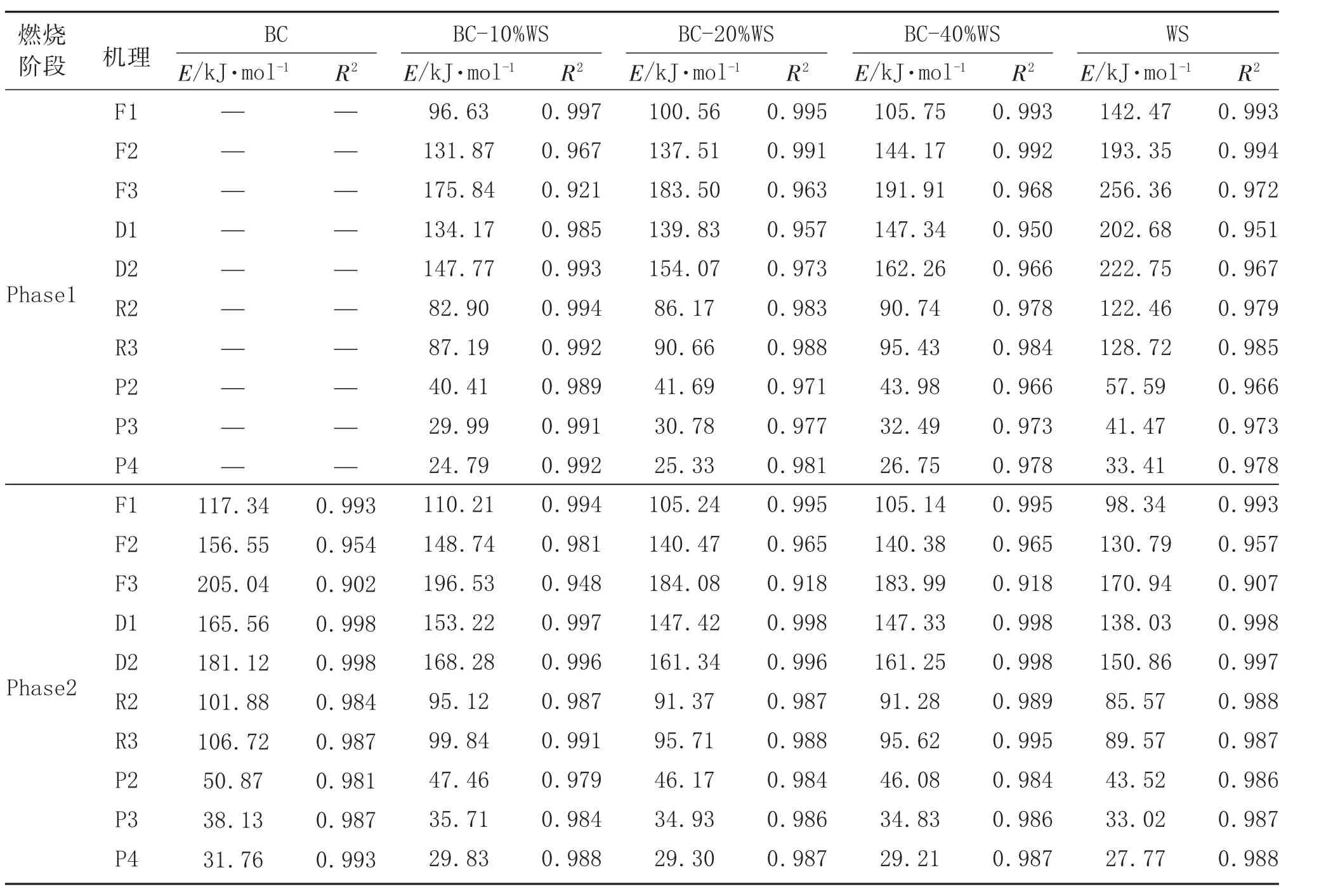
表5 升溫速率為10 K/min 時不同機理函數下的燃燒動力學參數
當反應溫度較低時,雖然生物質中揮發分的逸出有利于改善煤的著火溫度,但是隨著生物質混合比例的增加,參與反應的固定碳減少,因此混合樣品Phase1 階段的燃燒反應活化能呈上升趨勢。到Phase2 階段,隨著生物質混合比例的增加,活化能呈下降趨勢,這主要是因為:(1)隨著生物質混合比例的增加,混合樣品揮發分含量增加,Phase1 階段揮發分的大量逸出改善了煤的燃燒反應活性,這一結果也影響到了后續中高反應溫度下(Phase2 階段)焦的燃燒反應活性;(2)生物質中揮發分的大量逸出也使得生物質焦具有更好的孔隙率、碳結構無序性和更多的表面含氧官能團,這些結構特性也改善了后期燃燒反應活性;(3)生物質灰分中含有大量對前期揮發分逸出和后期焦燃燒反應有催化作用的堿金屬和堿土金屬。
對比各種機理函數的擬合相關系數可以發現,Phase1 階段F1 具有最好的擬合度,說明這一階段化學反應為燃燒反應控制環節,這時燃燒溫度較低,主要發生揮發分的燃燒反應,符合F1 假設的燃燒機理;而隨著燃燒溫度的升高,內部煤焦開始發生燃燒反應,煤焦的燃燒反應性由其表面活性位點的多少主導,因此這一階段傳質成為了燃燒反應的限制性環節,從表5 可以看到,Phase2 階段D1 和D2 具有較高的相關系數,這與煤燃燒反應的進行相一致。
以升溫速率10 K/min 為例,使用CR 法、FWO 法和KAS 法計算各混合樣品的平均活化能,結果見圖3。
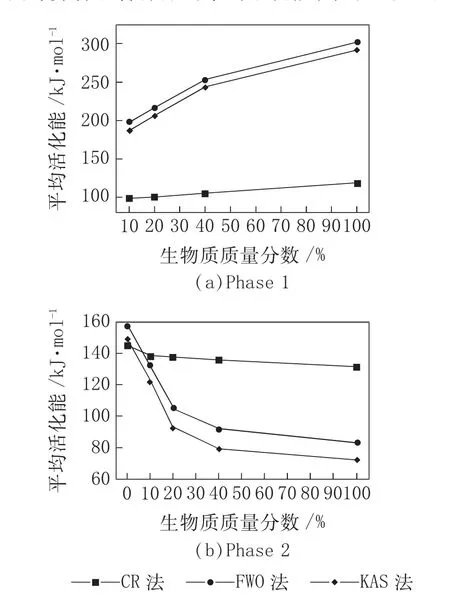
圖3 CR 法、FWO 法和KAS 法計算所得各混合樣品的平均活化能
從圖3 可以看出,使用3 種模型計算所得平均活化能隨著生物質混合比例升高的變化趨勢一致,但是使用CR 法計算的平均活化能值與FWO 法和KAS 法的有明顯差異,這主要是因為使用FWO 法和KAS 法計算活化能需要至少3 個升溫速率,而CR 法采用的是單升溫速率法計算平均活化能。圖3 中CR 法的平均活化能是由表5 中具有最高相關系數的機理函數所得,而FWO 法和KAS 法則是在不假設機理函數的前提下計算活化能,有學者認為后兩種通過多個升溫速率計算活化能的模型可以獲得較為準確的動力學參數[21-22]。但是FWO 和KAS 模型依然有其適用范圍,其中FWO 模型需要E/RT 值居于20~60 時才具有可靠性,KAS 模型則需要E/RT 值居于20~50 時才具有可靠性。
不同生物質混合比例下,E/RT 值隨著轉化率的變化趨勢見圖4。由圖4 可以看出,對于FWO 模型,Phase1 階段,除了WS,其他樣品皆有E/RT 值不在有效范圍內;相比于FWO 模型,KAS 模型的有效范圍更小,因此不在有效范圍內的E/RT 值略多于FWO 模型;燃燒反應居于Phase2 階段時,所有樣品均有坐落在有效范圍外的E/RT 值,這說明使用FWO 和KAS 模型計算得到的動力學參數并不完全可靠。從圖4 還可以發現,Phase1 和Phase2 階段坐落在有效范圍內的E/RT 值隨著生物質混合比例的增加而增多,說明FWO和KAS 模型的可靠性都隨著生物質混合比例的增加而增加。因此相比于FWO 和KAS 模型,假設了機理函數的CR 模型在獲得較高擬合相關系數的情況下,可能更具有可靠性。


圖4 E/RT 值隨轉化率變化趨勢圖
2.4 燃燒機理
煤和生物質共燃燒反應的主要燃燒階段由揮發分和焦炭的燃燒組成,通過一系列的吸附和脫附反應完成混合樣品的燃燒,主要分成3 個部分(見圖5):首先溫度較低時,脫揮發反應開始,揮發分逸出與空氣中氧氣作用,生成CO2;然后,隨著燃燒溫度的升高,揮發分燃燒完成,內部焦炭開始與氧氣反應,燃燒剩余灰分覆蓋在焦炭表面,且隨著反應的進行,灰層厚度會逐漸增加;最后混合樣品燃燒完全,僅剩下灰分成分,燃燒反應結束。在這一過程中,初始階段發生的揮發分燃燒主要受揮發分和氧氣的化學反應過程控制,傳質影響較小;隨著反應的進行,揮發分燃燒反應結束,焦炭的燃燒主導燃燒反應,此時一方面受到焦炭結構特性的影響,另一方面受到灰層覆蓋的影響,傳質作用開始起主導作用,這一階段,焦炭內部無定形碳結構逐漸被消耗,微晶結構朝著石墨化方向進行,內部結構趨于有序化,不利于燃燒反應的進行。而添加了生物質后,前期揮發分的析出為焦炭提供一定的H 和O 原子,從而改善了其第二部分焦炭的燃燒反應;其次生物質混合比例增加,部分煤灰被生物質灰分所替代,而生物質灰分中富含堿金屬和堿土金屬,這些礦物組分在燃燒反應過程中可以作為媒介,將氧氣傳遞到焦炭表面,從而改善焦炭燃燒反應性。綜上所述,添加生物質可以顯著改善煤燃燒反應性能,動力學模型CR 在使用合適的機理函數時,其可靠性大于無機理函數的FWO 和KAS 模型。

圖5 混合樣品燃燒機理示意圖
3 結論
3.1 生物質揮發分易燃燒,因此添加生物質可以大幅降低混合樣品的著火溫度,而揮發分燃燒所釋放的富氫氣體和熱量也改善了高溫下焦炭的燃燒反應性,此外生物質灰分中的堿金屬和堿土金屬對混合樣品的燃燒反應也有積極作用,因此隨著生物質混合比例的增加,混合樣品的綜合燃燒特性指數顯著增加。
3.2 煤和生物質混合燃燒過程中存在協同作用,其中BC-20%WS 的協同作用最好。
3.3 揮發分燃燒(Phase1)階段,燃燒反應活化能隨著生物質混合比例增加而增加,而焦炭燃燒(Phase2)階段則呈現出相反趨勢。相比較于無機理函數的FWO和KAS 動力學模型,采用適宜機理函數的CR 模型更適用于描述混合樣品的燃燒反應動力學。

