超高效液相色譜串聯質譜同時檢測人血清5種甾體激素方法學及生物參考區間的建立
陸優麗,楊雙雙,張美微,歐美賢,董春霞,沈薇薇,姜鳳麗,李水軍
(上海藥物Ⅰ期臨床暨藥物一致性評價工程技術研究中心 上海市臨床質譜研究所上海市徐匯區中心醫院 復旦大學附屬中山醫院徐匯醫院,上海 200031)
甾體激素又稱類固醇激素,是一類親脂性、低相對分子質量的化合物,其結構以環戊烷多氫菲母核為基礎。甾體激素在人體內可通過酶的作用相互轉化,在調節免疫、維持機體發展及生長發育等人體正常的生理生化活動中起著重要作用[1-2]。甾體激素根據功能的不同主要分為腎上腺皮質激素和性激素兩大類,其中性激素又分為雄激素、雌激素和孕激素。睪酮(testosterone,T)、雙氫睪酮(dihydrotestosterone,DHT)、雄烯二酮(androstenedione,AD)、脫氫表雄酮(dehydroepiandrosterone,DHEA)是人體內主要的雄激素,雄激素濃度的異常變化與疾病的發生密切相關:前列腺癌的形成最初依賴于T、DHT、AD、DHEA,并由雄激素受體信號軸介導,因此雄激素剝奪療法是局限性晚期或轉移性前列腺癌的主要臨床治療方法,雄激素水平的準確測定也是判斷雄激素是否缺乏的重要依據;性激素與肥胖有關,雄激素缺乏會導致肌肉質量、體積和力量的下降,是身體脂肪增加的主要原因,可導致性功能的下降[3-5]。《腎上腺皮質癌診治專家共識》[6]指出,雄激素的水平(如高濃度的DHEA)或分泌方式(如同時分泌雄激素和皮質醇)可能提示惡性病變,可用于臨床相關疾病的輔助診斷。有研究結果表明,多囊卵巢綜合征的發病與雄激素過多有關[7],同時檢測多種雄激素水平較檢測單項激素水平具有更高的診斷特異性[8]。17α羥孕酮(17alphahydroxyprogesterone,17OHP)可用于排除非典型腎上腺增生引起的雄激素升高,亦是鑒別診斷多囊卵巢綜合征的必要檢測指標之一[5],同時檢測T、DHT、AD、DHEA和17OHP是輔助和鑒別診斷多囊卵巢綜合征快速而有效的方法。
目前,仍有較多實驗室采用免疫學方法進行甾體激素的檢測[9-10],而免疫學方法因特異性差,容易受到人體內多種激素的交叉干擾,易出現假陽性或假陰性結果[11]。液相色譜串聯質譜(liquid chromatography-tandem mass spectrometry,LC-MS/MS)因檢測靈敏度高、特異性好,在小分子生物標志物的檢測中具有突出優勢,更被認為是甾體激素檢測的“金標準”[12-13]。《多囊卵巢綜合征中國診療指南》[14]建議聯合檢測多種甾體激素,以達到較好的特異性和準確性。然而,我國同時檢測T、DHT、AD、DHEA、17OHP這5種甾體激素的研究報道較少。劉琪等[15]運用液液萃取法建立了一種可同時檢測18種類固醇激素的LC-MS/MS方法,但未對干擾物進行驗證;曹正等[7]建立了同時檢測T、DHT、AD、DHEA和17OHP的方法,但未進行干擾物和基質效應的性能驗證;且這2項研究均未進行基于中國人群的生物參考區間的研究[7,15]。本研究旨在建立可同時檢測人血清中T、DHT、AD、DHEA和17OHP的超高效液相色譜串聯質譜(ultra high performance liquid chromatography-tandem mass spectrometry,UPLC-MS/MS)方法,并進行全面的性能驗證;同時,通過檢測上海地區表觀健康成年人血清中5種甾體激素的水平,建立適用于上海地區的血清T、DHT、AD、DHEA和17OHP的參考區間。
1 材料和方法
1.1 研究對象
根據美國臨床實驗室標準化學會(the Clinical and Laboratory Standards Institute,CLSI)C28-A3C文件[16]要求,從體檢人群中篩選符合要求的研究對象,共納入368名表觀健康者,其中男120名、女248名,年齡16~100歲。本研究獲得上海市徐匯區中心醫院倫理委員會批準。納入標準:無5種甾體激素異常相關疾病,無糖尿病、高血壓、腫瘤、冠心病、多囊卵巢綜合癥、月經不調、骨質疏松癥等相關病史及癥狀;體檢結果正常,血常規、尿常規、血清學檢查和肝功能、腎功能、血糖、血脂、腫瘤標志物等檢測結果均正常。排除標準:近期妊娠、哺乳期、大量飲酒、近期或長期獻血、輸血、接受手術者以及溶血、脂血等質量不合格樣本。
1.2 血清樣本采集與保存
采集所有研究對象晨起空腹前臂靜脈全血,1 200×g離心10 min,分離血清,保存于2 mL離心管中,-70 ℃冷凍保存待測。
1.3 試劑與標準品
分析物T(純度為99.54%)、DHT(純度為99.80%)、AD(純度為99.44%)、DHEA(純度為99.87%)、17OHP(純度為96.40%)、T-d3、DHT-d3、AD-13C3、DHEA-d5、17OHP-d8(純度均>97.00%)及內標的標準品均購自美國Cerilliant公司。甲酸、甲醇、乙腈(色譜級,美國TEDIA公司) ;氨水(色譜純試劑,中國國藥集團化學試劑有限公司);30%脂肪乳注射液(C14~C24,無錫費森尤斯卡比華瑞制藥有限公司);實驗用水為本實驗室采用Millipore純水系統(美國Millipore 公司) 自制。
1.4 主要儀器與耗材
API 4000串聯質譜儀(美國AB Sciex公司);LC-30AD高效液相色譜系統(日本島津公司);色譜柱為Poroshell 120 EC-C18(2.1×100 mm,2.7 μm,美國Agilent公司);Vortex Genie2 渦旋混合器( 美國Scientific Industries公司) ;Mikro22R冷凍高速離心機(德國Hettich公司) ;移液器( 德國Eppendorf公司);固相微萃取小柱為SOLAμ HRP(2 mg/mL 96 well plate,美國Thermo Fisher Scientific公司)。
1.5 溶液配制
因無法得到人空白血清基質,故用活性炭吸附過的小牛血清替代人血清作為空白基質,用于標準曲線的配制和稀釋實驗中的稀釋液,質控樣本和回收率、基質效應等的考察使用含本底的混合人血清樣本。
1.5.1 標準曲線及質控添加液的配制 用50%甲醇將(T、AD、17OHP)/DHT/DHEA儲備液配制成混合工作液,并按比例稀釋,制成標準曲線添加液和低、中、高濃度的質控添加液。詳細分析物濃度見表1。
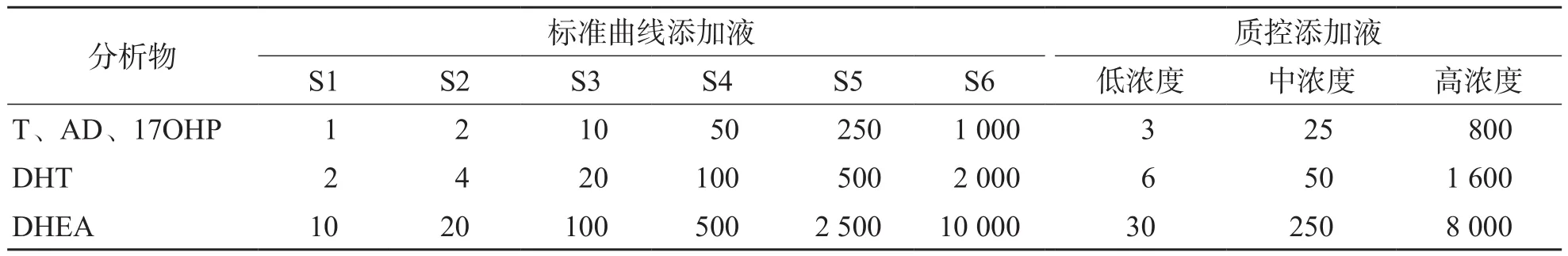
表1 標準曲線添加液和質控添加液配制濃度 ng/mL
1.5.2 標準曲線樣品和質控品的配制 準確吸取500 μL活性炭吸附過的小牛血清,加入5 μL標準曲線添加液中,得到標準曲線樣品;準確吸取500 μL混合人血清,加入5 μL質控品添加液中,得到質控品。
1.5.3 內標工作液的配制 將T-d3、AD-13C3、17OHP-d8、DHT-d3和DHEA-d5儲備液用50%甲醇稀釋,配制成濃度為10、20、20、40、100 ng/mL的內標工作液,待用。
1.6 樣本前處理
將待測人血清樣品和配制的標準曲線樣品、質控品和內標工作液取出,室溫平衡,檢測前混勻。取500 μL人血清樣品(另補充5 μL 50%甲醇)、505 μL標準曲線樣品和質控品,分別加入10 μL內標工作液,渦旋震蕩5 min混勻,再加入500 μL甲醇沉淀,震蕩5 min,22 136×g離心10 min,棄上清,分別加入500 μL 2%氨水和3.5 mL 2%氨水-10%甲醇,混勻,上樣至固相萃取小柱。固相萃取小柱操作步驟:(1)700 μL甲醇活化;(2)700 μL 10%甲醇-2%氨水平衡;(3)上樣;(4)700 μL 40%甲醇清洗2次;(5)50 μL甲醇洗脫2次(每步操作壓力均控制在30 psi以內)。將洗脫下來的溶液轉移至進樣管中,加入20 μL水混勻后進行分析,進樣體積為30 μL。
1.7 液相色譜條件
采用Poroshell 120 EC-C18色譜柱(2.1 mm×100 mm,2.7 μm)。流動相A為0.05%甲酸-30%乙腈水溶液,流動相B為0.05%甲酸-90%乙腈溶液。梯度洗脫程序:0.00 min(0%B),0.1~7.00 min(35%B),7.01~9.00 min(100%B),9.01~12.00 min(0%B)。流速為0.3 mL /min,持續12 min,進樣體積為30 μL。自動進樣器溫度為4 ℃。
1.8 質譜條件
用電噴霧離子源在正離子掃描模式下進行多反應監測模式分析,掃描間隔為5 ms。霧化氣(Gas1)60 psi,輔助氣(Gas2)70 psi,氣簾氣(CUR)30 psi,碰撞氣(CAD)12 psi,離子源溫度為550 ℃。分析物的具體質譜參數見表2。
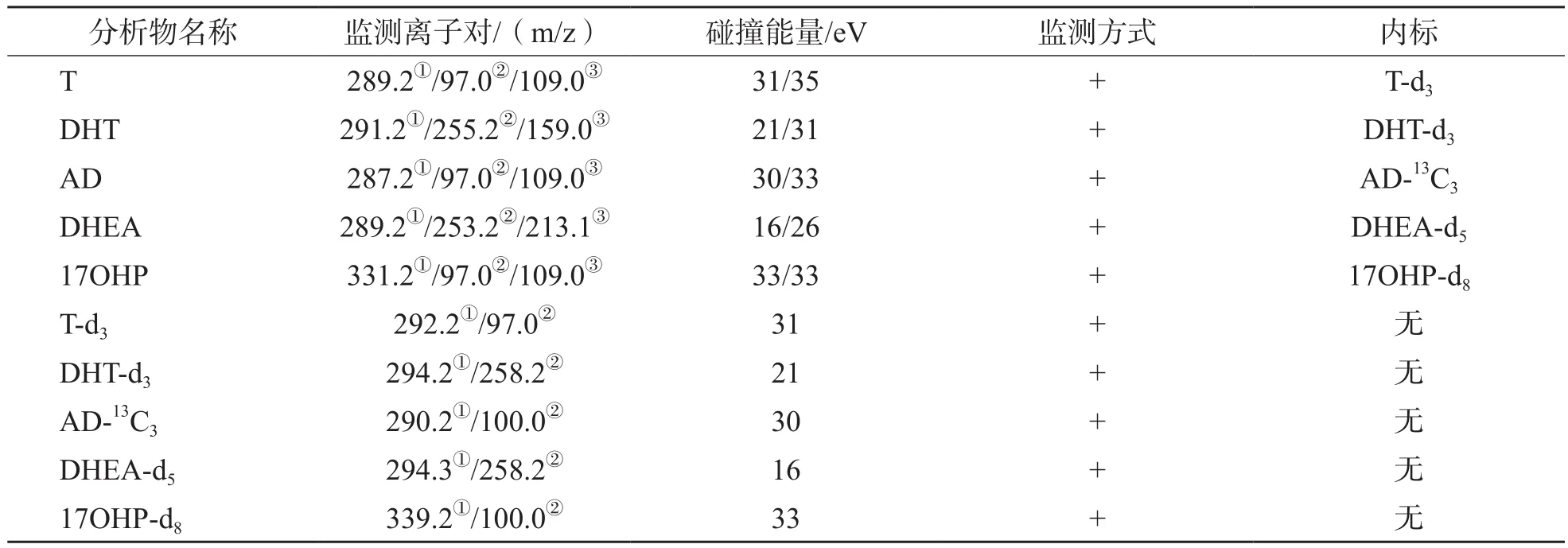
表2 分析物質譜參數
1.9 方法學驗證
1.9.1 殘留評價 在標準曲線最高濃度點樣品進樣完成后,進1針空白樣品,考察是否存在殘留。以分析物保留時間處的峰面積不超過最低定量檢測限(lower limit of quantification,LLOQ)的20.0%,內標保留時間處的峰面積不超過內標峰面積的5.0%為進樣無殘留。
1.9.2 準確度與精密度 準確吸取505 μL低、中、高濃度質控品和用于配制該質控品的混合人血清,按預處理方法各進行6次平行實驗,測定質控品各個分析物的濃度,計算批內準確度和精密度。連續制備3批質控品,考察批間準確度和精密度。計算公式:準確度=(實際測定值-本底值)/理論添加值×100%,精密度[以(變異系數(coefficient of variation,CV)表示]=標準偏差/測定濃度平均值×100%。
1.9.3 稀釋實驗 在混合的人血清基質中加入工作液配成最高定量檢測限(upper limit of quantification,ULOQ)和5倍的ULOQ樣本,用活性炭吸附過的小牛血清作為稀釋液分別稀釋2倍和10倍,至ULOQ濃度的1/2,按預處理方法處理后進樣分析,考察6份稀釋樣本的準確度和精密度。
1.9.4 基質效應和提取回收率 取5份不同來源的人血清各500 μL,加入10 μL內標工作液,按預處理方法處理,100 μL甲醇洗脫后加15 μL 50%甲醇水溶液和5 μL蒸餾水,混勻,進樣(A1/IS1)。取同樣來源的人血清500 μL,分別加入5 μL低、中、高3種濃度的質控添加液,再加入10 μL內標工作液,按預處理方法處理,100 μL甲醇洗脫后加15 μL 50%甲醇水溶液和5 μL蒸餾水,混勻,進樣(A2/IS2)。取同樣來源的人血清500 μL,不加內標,按預處理方法處理,100 μL甲醇洗脫后分別添加5 μL低、中、高3種濃度的質控添加液、10 μL內標工作液和5 μL蒸餾水,混勻,進樣(A3/IS3)。另取100 μL甲醇,分別加入5 μL低、中、高3種濃度的質控添加液、10 μL內標工作液和5 μL蒸餾水,混勻,進樣(A4/IS4)。以上樣品重復測定3次,分別得出分析物和內標的峰面積。計算公式:分析物基質效應=(A3峰面積-A1峰面積)/A4峰面積,內標校正的基質效應=分析物基質效應×IS4峰面積/IS3峰面積,分析物提取回收率(%)=(A2峰面積-A1峰面積)/(A3峰面積-A1峰面積)×100%,內標提取回收率(%)=IS2峰面積 / IS3峰面積×100%。
1.9.5 選擇性 盡管LC-MS/MS技術在特異性和選擇性方面優于其他檢測技術,但甾體激素種類豐富,血清中其他內源性結構類似物可能會對分析產生潛在干擾;此外,溶血和脂血也可能影響檢測結果。因此,本研究評估了UPLCMS/MS對結構類似的甾體激素、溶血、脂血等的抗干擾能力。
(1)干擾物。將可能干擾甾體激素檢測結果的分析物加入混合人血清中,并配置低值和高值質控品,測定待測物濃度,與未添加干擾物的質控品比較,計算結果的偏差。干擾物(血清濃度,根據參考區間上限或上限的10倍濃度確定加入量)包括孕酮(100 ng/mL)、雌二醇(4 ng/mL)、雌酮(2 ng/mL)、孕烯醇酮(30 ng/mL)、17羥基孕烯醇酮(100 ng/mL)、皮質醇(100 ng/mL)、可的松(100 ng/mL)。
(2)溶血。收集3份不同來源的全血樣本,各取2 mL血清,分別加入40 μL(2%)對應的血細胞,通過超聲處理使血細胞完全破碎后,各取510 μL,按前處理方法處理后測定其濃度,將結果與對應的無溶血的血清樣本濃度進行比較,計算偏差。
(3)脂血。收集3份不同來源的全血樣本,各取2 mL血清,分別加入10、20、40 μL(0.5%、1.0%、2.0%)的脂肪乳,振蕩混勻,得到高三酰甘油血清樣本,測定其三酰甘油濃度依次為4.58、6.65、10.79 mmol/L,各取510 μL,按前處理方法處理后,測定其中的甾體激素濃度,考察高三酰甘油對激素測定是否有干擾。
1.9.6 穩定性 收集6名體檢人員(男、女各3名)的血清樣本,每份樣本分裝成3份,分別考察其室溫(25 ℃)放置4、24 h;-25~-15 ℃放置30、100 d,以及-90~-70 ℃放置30、100 d的穩定性。
1.10 參考區間的建立
采用UPLC-MS/MS檢測368名表觀健康者的血清T、DHT、AD、DHEA和17OHP水平,并建立參考區間。采用UPLC-MS/MS檢測368名表觀健康者血清T、DHT、AD、DHEA和17OHP水平,并建立參考區間。按性別和年齡(16~20歲、21~30歲、31~40歲、51~60歲、>61歲)分別分組。
1.11 統計學方法
采用SPSS 24.0軟件進行統計分析。采用Dixon法剔除離群值。正態性檢驗采用Q-Q圖結合Kolmogorov-Smirnov檢驗。呈正態分布的計量資料用±s表示,組間比較采用方差分析,采用±1.96s方式建立參考區間。呈非正態分布的計量資料以中位數(M)[四分位數(P25~P75)]表示,組間比較采用Kruskal-Walli檢驗,采用百分位數法(P2.5~P97.5)建立參考區間。以P<0.05為差異有統計學意義。
2 結果
2.1 分離條件的摸索與優化
甾體激素在人體內含量低,人血清經蛋白沉淀后再用固相萃取柱純化濃縮,可以有效減小基質對分析測定的干擾,提高激素的檢測靈敏度。使用Poroshell 120 EC-C18色譜柱,用含甲酸的流動相進行梯度洗脫,可以較好地分離T、DHT、AD、DHEA和17OHP,峰形好,且靈敏度高。優化后的分析物及對應內標的色譜圖見圖1。
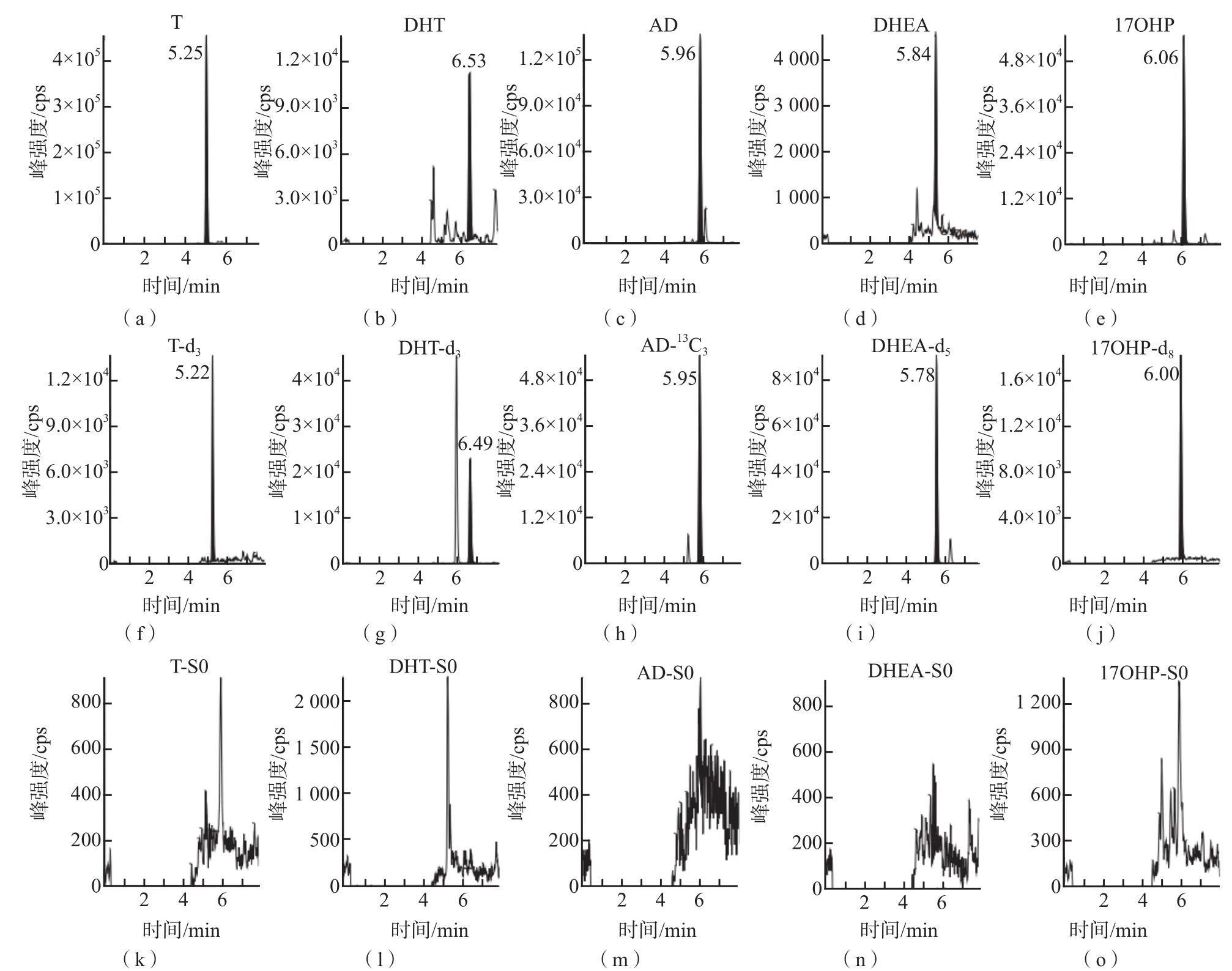
圖1 人血清樣本中T、DHT、AD、DHEA及17OHP及其對應內標、空白替代基質典型色譜圖
2.2 標準曲線和最低定量限
以標準曲線樣品分析物的濃度為X軸,分析物峰面積與對應內標峰面積的比值為Y軸,用最小二乘法1/x權重進行線性回歸,得到T、DHT、AD、DHEA、17OHP的回歸方程分別為:Y=0.004 89X+0.029(r2=0.999 6)、Y=1.67X+0.007(r2=0.999 5)、Y=2.05X+0.005(r2=0.999 8)、Y=0.28X+0.011(r2=0.999 8)、Y=2.51X+0.015(r2=0.999 9),線性關系良好。T、DHT、AD、DHEA和17OHP的最低定量限分別為0.01、0.02、0.01、0.10和0.01 ng/mL。
2.3 殘留評價
計算結果顯示,5種甾體激素各分析物保留時間處峰面積均不超過最低定量限LLOQ的20%,且內標保留時間處的峰面積不超過內標峰面積的5%,表明進樣無明顯殘留。
2.4 準確度、精密度和稀釋實驗
5種甾體激素3個批次的準確度和精密度測定低、中、高濃度質控樣品的批內平均準確度均為96.6%~105.6%,CV均<8%;批間準確度為95.0%~105.2%,批間CV均<6%。稀釋實驗結果表明,5倍ULOQ以內的樣本稀釋10倍后,采用本方法檢測,準確度為86.16%~103.60%,CV<5%,本方法的可報告范圍可覆蓋5 000倍。見表3。
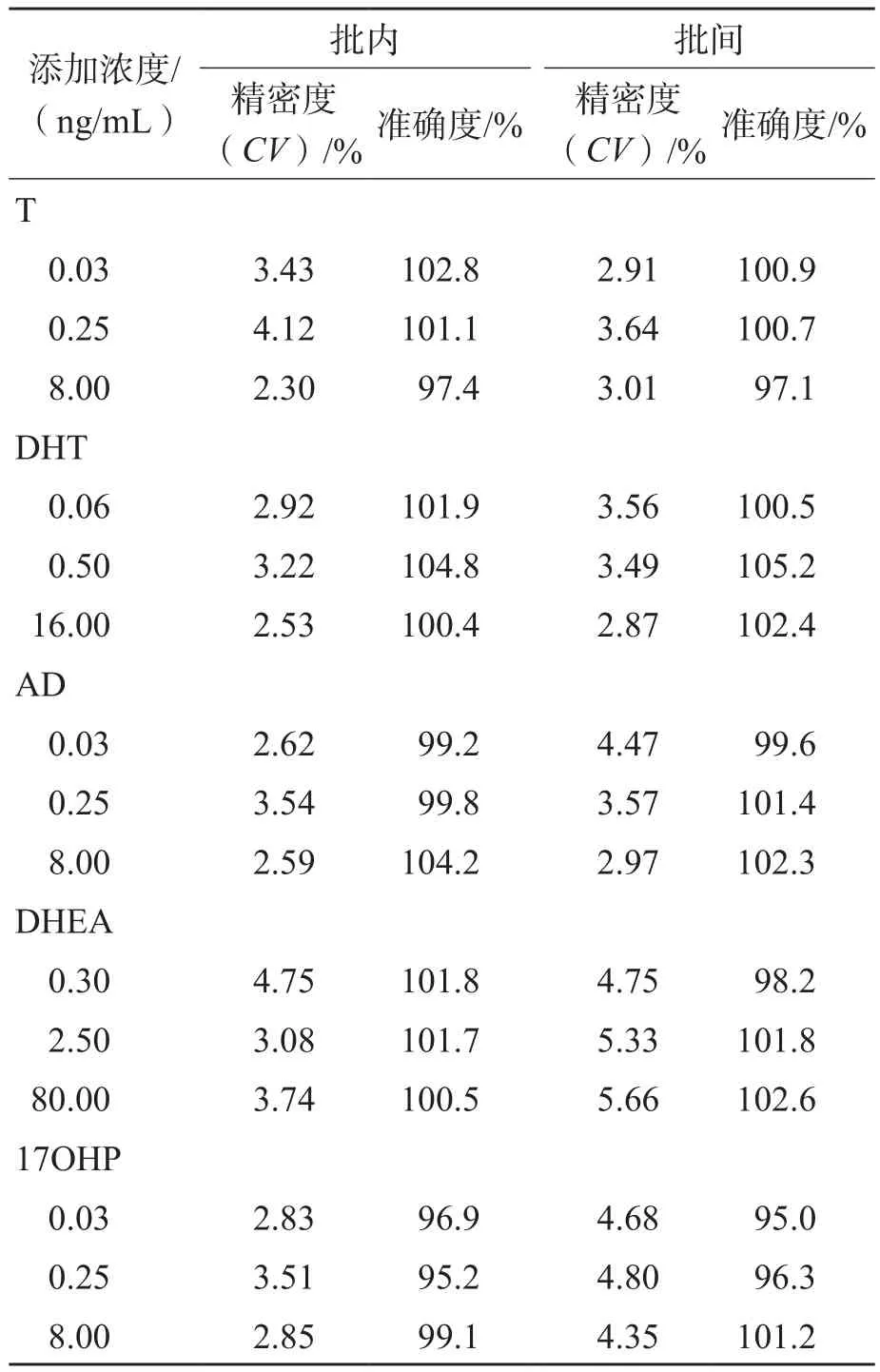
表3 批內和批間準確度與精密度
2.5 基質效應和提取回收率
5種甾體激素均存在一定程度的基質抑制,經內標校正后,T、DHT、AD、DHEA和17OHP的相對基質效應分別為0.945 3、1.005 0、1.003 0、0.966 9和1.009 0,表明同位素內標可校正基質效應。此外,各分析物及內標在血清中的提取回收率均>60%。見表4。
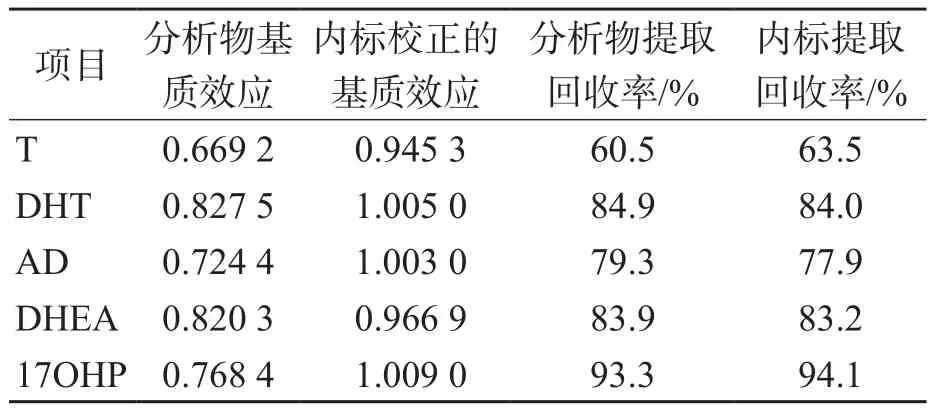
表4 5種甾體激素基質效應和提取回收率
2.6 選擇性
干擾實驗結果表明,8種潛在干擾物對甾體激素檢測結果的偏差為-9.90%~2.72%,均在可接受范圍內。溶血實驗結果表明,含有2%溶血細胞的血清樣本T、DHT、AD和17OHP測定結果的偏差為1.93%~9.49%,無明顯影響,但會導致DHEA測定結果偏低18.65%。高三酰甘油對5種甾體激素的測定結果偏差為0.15%~12.54%,對測定結果無干擾。
2.7 穩定性
穩定性實驗結果表明,血清樣本室溫放置24 h,除DHEA濃度下降-37.33%外,其他4種甾體激素均較穩定;此外,血清樣本分別在-25~-15 ℃和-90~-70 ℃下凍存100 d,檢測結果偏差均<±15%。見表5。
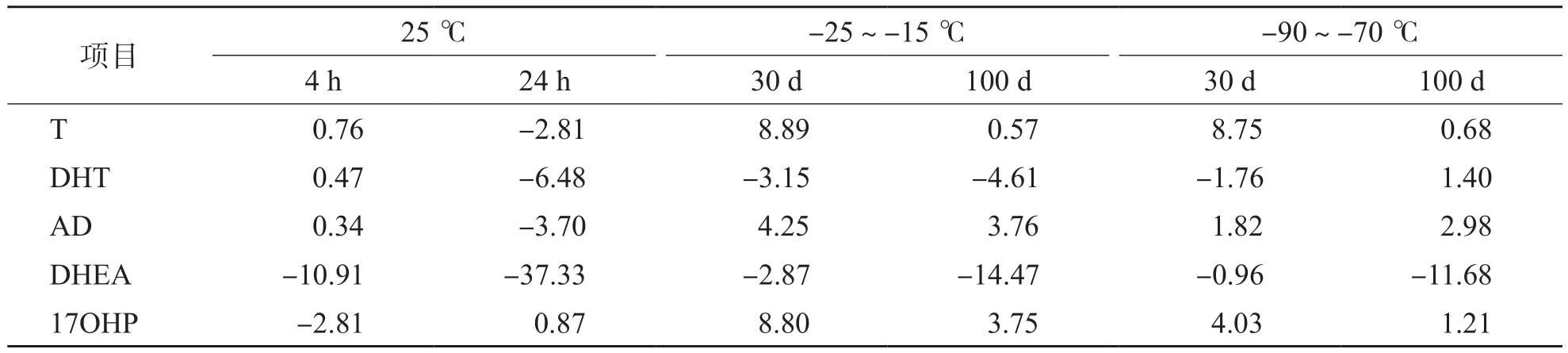
表5 5種甾體激素不同溫度放置不同時間對血清樣本穩定性(相對偏差)的影響 %
2.8 室間質量評價結果
采用本研究建立的UPLC-MS/MS方法參加2019年國家衛生健康委臨床檢驗中心全國內分泌正確度驗證質譜法調查,結果顯示,T、17OHP 2個項目測定結果與靶值的偏差為-5.00%~0.38%,均在可接受的范圍內,合格率為100%。相關室間質量評價結果見表6。
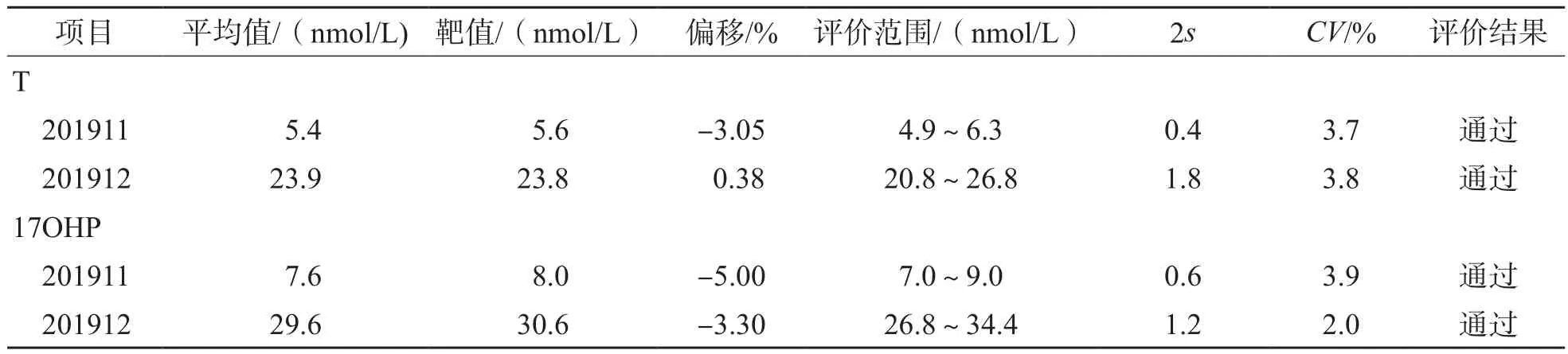
表6 2019年國家衛生健康委臨床檢驗中心T、17OHP相關室間質量評價結果
2.9 參考區間
2.9.1 離群值 采用Dixon法在女性研究對象T測定值中發現1個離群值(8.8 ng/mL),與相鄰值的D為8.1 ng/mL,R為8.73,D/R=0.93>1/3。故最終有367名研究對象納入本研究。
2.9.2 不同性別、年齡表觀健康者5種甾體激素水平比較 男、女性血清T、DHT、AD、DHEA和17OHP水平差異均有統計學意義(P<0.05),因此需按性別建立不同的參考區間。男性5個年齡段之間血清T、DHT、AD、DHEA和17OHP水平差異均無統計學意義(P>0.05),因此將男性不同年齡段合并后建立統一的參考區間。16~20歲、21~30歲和31~40歲女性血清T、DHT、AD、DHEA和17OHP水平與51~60歲、>61歲女性比較,差異均有統計學意義(P<0.05),而16~20歲、21~30歲、31~40歲女性之間和51~60歲、>61歲女性之間差異均無統計學意義(P<0.05)。因此女性按16~50歲和>50歲分別建立參考區間。見表7。
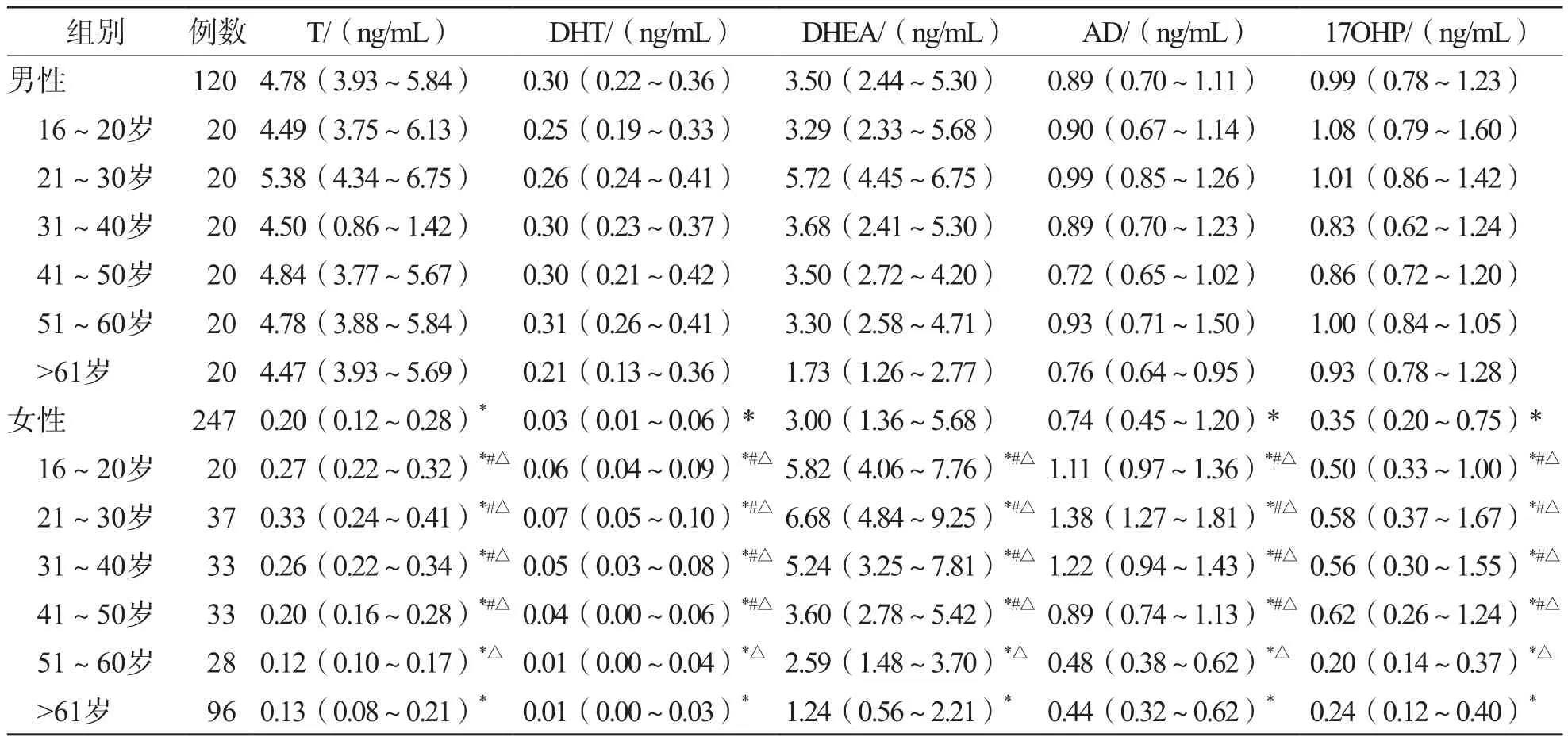
表7 不同性別及年齡的表觀健康者5種甾體激素比較
2.9.3 參考區間建立 正態性檢驗結果顯示,1 6~5 0歲女性血清D H T水平呈正態分布(P=0.200),男性和>50歲女性血清T、AD、DHT、DHEA和17OHP水平均呈非正態分布(P<0.05)。采用不同方式建立的參考區間見表8。
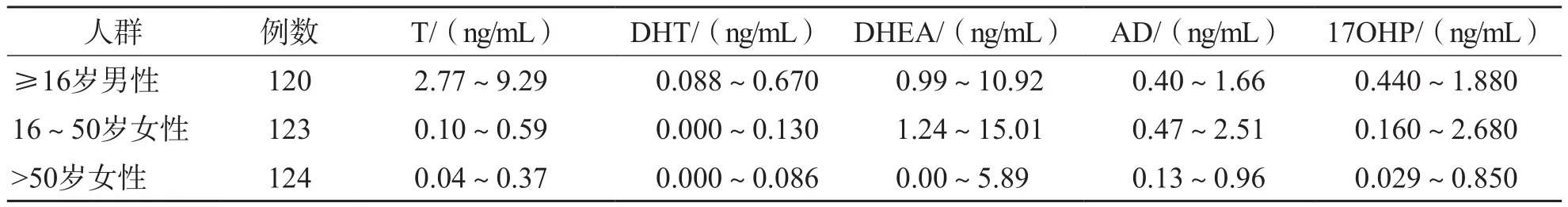
表8 5種甾體激素的參考區間
3 討論
本研究建立了一種選擇性高、準確好的檢測血清5種甾體激素(T、AD、DHT、DHEA和17OHP)的UPLC-MS/MS方法。血清樣品經甲醇沉淀等前處理后,用SOLAμ HRP固相萃取小柱純化,可以有效除去雜質干擾。各激素用其對應的穩定同位素作為內標,可減小基質干擾和前處理損失的影響,提高定量的準確度。本研究建立的LC-MS/MS檢測方法可排除其他結構類似的內源性激素的干擾,各激素檢測的線性范圍達到1 000倍,r2值均>0.999 5,可報告范圍達到5 000倍,在生理和病理濃度下均可被準確檢出。LLOQ低于以往的文獻報道[6],分別為0.01(T/17OHP /AD)、0.02(DHT)、0.10 ng/mL(DHEA),可靈敏且準確定量樣本中的低濃度甾體激素水平,在短時間內高效完成人體內痕量類固醇激素多組分的定量分析。此外,本研究還考察了溶血、脂血對于測定結果的影響,證實了溶血樣本會干擾DHEA的測定結果,建議在實際應用中,嚴格控制樣本溶血,保證檢驗質量。
本研究建立的方法參加2019年國家衛生健康委臨床檢驗中心開展的16種17OHP制備物和新鮮冰凍人血清基于2種評價方案的互通性研究結果顯示,所有正確度驗證材料和甾體激素標準物質在本實驗室和金域醫學實驗室2個LCMS/MS分析系統中表現出良好的互通性[17]。T和17OHP項目參加了2019年上半年國家衛生健康委臨床檢驗中心全國內分泌正確度驗證質譜法調查,合格率為100%。本研究建立的方法可實現對甾體激素多組分的分快速準確測定,可為臨床雄激素異常相關疾病的檢測和診斷提供準確、有效的依據。
T、AD、DHT、DHEA和17OHP是輔助臨床鑒別診斷多囊卵巢綜合征的重要指標,建立適合本地區臨床實驗室的參考區間可以更好地為相應疾病的診斷提供參考。本研究對367名體檢者血清樣本的激素水平進行了統計分析,并根據性別和年齡差異進行分組,建立了基于UPLCMS/MS方法的參考區間。雖然與文獻報道[18]存在微小的差異,但考慮到研究對象的地域、種族、生活習慣等因素,本研究結果更適用于為上海地區人群甾體激素相關疾病的診斷提供參考。后續將擴大樣本量對此參考區間進行進一步驗證。

