椰殼活性炭改性后對百草枯吸附能力的影響
范凱軒,鐘永科
(遵義醫科大學藥學院,貴州 遵義 563000)
百草枯是一種季銨鹽,由于其化學和物理性質,如在水中的高溶解性,其主要作為除草劑使用[1]。此外,已被證明百草枯對哺乳動物有毒,直接影響肺、肝臟和腎臟等器官[2]。已有研究表明百草枯可能與帕金森病引發有關[3,4]。使用活性炭、黏土、沸石和氧化鋁吸附已被證明對去除水中的百草枯非常有效。高吸附能力的活性炭[5,6]是吸附有機微污染物的最佳吸附劑之一。椰子殼作為現成的低成本材料,可以用于制造活性炭。因此,本研究探討椰殼活性炭改性后對百草枯吸附能力的影響,以期提高對百草枯的去除能力。
1 材料與方法
1.1 材料
百草枯(純度>98.0%,成都化學試劑有限公司);椰殼活性炭(80~100 目,承德冀北燕山活性炭有限公司);去離子水。
U-3010 型雙光束紫外可見分光光度計,日本Hitachi 公司;JW-BK122W 靜態氮吸附儀,北京精微高博科學技術有限公司。
1.2 活性炭的改性
取300 g 椰殼活性炭,加入HNO3溶液,加熱回流,每隔2 h 取出100 g 水洗至pH 恒定,烘干備用。將所得活性炭分別記為YK-2、YK-4 和YK-6,未處理的活性炭標記為YK-0。
1.3 吸附試驗
準確稱取0.02 g 活性炭于100 mL 錐形瓶中,加入百草枯溶液50.0 mL,放置在37 ℃的水浴搖床中,轉速為110 r/min,間隔一定時間,取上層液,在波長258 nm[7]處測定吸光度。

式中,q為吸附量,C0為百草枯的起始濃度(mg/L);C為吸附開始后某時刻百草枯的濃度(mg/L);V為百草枯溶液的體積(L);m是活性炭樣品的質量(g)。
2 結果與分析
2.1 動力學吸附
不同改性時間的活性碳,相同的初始濃度(50 mg/L)隨吸附時間的延長而變化。第一階段,2 h 前主要為碳外表面最易活化的位點進行結合。第二階段,2~9 h 為碳表面其他可結合位點的飽和路徑結合,以及復雜的孔徑結構的吸附。第三階段,9 h 以后為動力學的平臺期,表明吸附已達到平衡。從圖1 可以看出,平衡時間相同,4 種不同活性炭的吸附量變化主要在9 h 內完成。改性可明顯改善去除能力。

圖1 改性前后活性炭的吸附曲線
為進一步考察椰殼活性炭對百草枯的吸附情況,使用Lagergren 準一級動力學方程和Lagergren 準二級動力學方程,同時對其進行考察[8],其動力學方程如下。

式中,q和qt分別表示任一t時刻(min)的吸附量(mg/g)和吸附平衡時的最大吸附量(mg/g),K1、K2和K3分別表示準一級動力學吸附速率常數(min-1)、準二級速率方程吸附速率常數[g/(mg·min)]和顆粒內部擴散的速率常數[mg/(g·min1/2)]。結合圖2 和圖3分析可知,準一級動力學理論飽和吸附量與實際吸附量相近,且相關性系數良好,準二級動力學模型理論吸附量與實際吸附量相差較大,說明準一級動力學模型更能描述其吸附行為,同時也說明吸附體系中存在化學吸附作用[9]。

圖2 準一級動力學擬合曲線

圖3 準二級動力學擬合曲線
從表1 可以看出,各條曲線均未通過原點,C均大于0,并未通過原點,表明顆粒內擴散吸附并不是惟一的速率控制因素。

表1 椰殼活性炭的吸附動力學擬合參數
2.2 熱力學等溫吸附
以YK-6 為研究對象,應用Langmuir 模型擬合,該模型表明單層吸附通過在均勻介質周圍發生吸附的過程,其表達式如下。

式中,KL(L/g)為Langmuir 常數;Ce為平衡濃度(mg/L),qe為平衡時吸附的量(mg/g),qmax為吸附平衡時的最大容量(mg/g)。
Freundlich 模型表明吸附過程發生在碳表面的活性位點和異質表面上的易于結合的有效孔徑,線性形式如下。

式中,KF和n分別為與吸附容量(L/g)和吸附能力有關的常數。該模型的最大優點是可以計算出理論吸附量。
由圖4 可以看出,百草枯的qe隨熱力學溫度的升高而增加,這是熱力學驅動導致的結果。在相同條件下,溶液的溫度較高時,活性炭上的位點更容易被活化,并且這是一個非常有利的吸附過程。
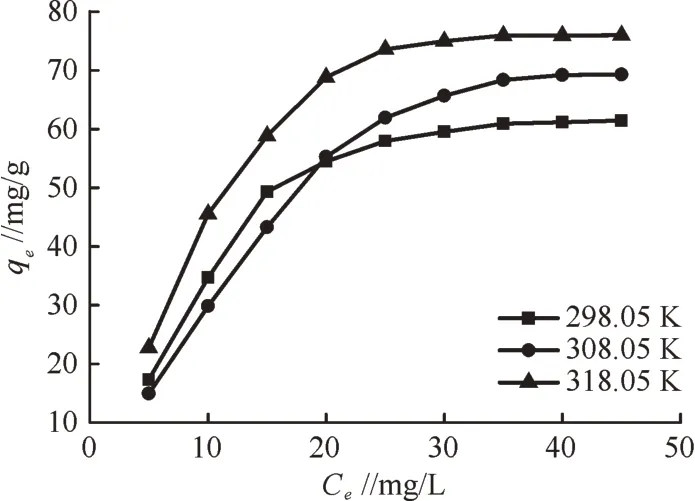
圖4 百草枯的等溫吸附線
結合圖5 和表2 可知,Langmuir 模型能更好地描述該吸附行為,參數1/n的值小于1,表明該吸附過程易于進行。在活性炭表面的多孔結構及其酸性官能團共同作用下,百草枯濃度越高,其吸附能力越強。

圖5 Langmuir 等溫擬合曲線
利用等式從Langmuir 因數計算霍爾分離因子(無量綱參數KL)的RL[10],公式如下。

式中,KL為Langmuir 的參數,C0為百草枯的初始濃度(mg/L)。所得到的RL可用于解釋吸附類型為不利(RL<0 或RL>1)、有利[RL<1 或RL=1(線性)]和不可逆(RL=0)[11]。在本研究中,RL在不同溫度處在0.72~0.86,表明百草枯在活性炭上的吸附是一個有利的過程。
Dubbininin-Redushkevuch(D-R)方程可以很好地描述化合物在炭材料上的吸附行為,通過對吸附等溫線用D-R 方程進行線性擬合,可得出活性炭的特征吸附能。D-R 方程的線性形式如下。

式中,Qe和Q0分別為平衡吸附量(mg/g)和理論飽和吸附量(mg/g);Ce為水中吸附質的平衡濃度(mg/L);KDR為D-R 等溫吸附模型常數(mol2/kJ2);R為理想氣體常數[kJ/(mol·K)];T為反應的熱力學溫度(K),通過活性炭的平均吸附自由能(E)(kJ/mol)能夠對吸附反應的類型作出判斷,當E為0~8 kJ/moL時,以物理吸附為主;當E>8 kJ/mol 時,以化學吸附為主。E的計算公式如下。

利用D-R 等溫吸附模型計算得到的不同溫度下活性炭對百草枯的平均吸附自由能為8.27~9.88 kJ/mol(表2),表明在不同溫度下活性炭對百草枯的吸附以化學吸附為主[12]。

表2 不同模型擬合參數
在298.05、308.05、318.05 K 條件下,研究了溫度對百草枯的去除影響,由圖5 可以看出,隨著溫度從298.05 K 升高到318.05 K,吸附容量也隨著熱力學溫度的升高而增加。此外,吸附容量隨百草枯濃度的增加而增加,這是動力學驅使的原因。相同條件下,百草枯濃度較高時,碳表面活性位點被結合的概率增加,百草枯將會更充分地被吸附。
使用Van't Hoff 方程計算熱力學過程中的焓變和熵變,其線性形式如下。

吉布斯自由能計算公式為:

式中,qe為吸附量(mg/g);Ce為平衡時的百草枯濃度(mg/L);T為以開爾文(K)表示的溫度;R為理想氣體常數[8.314 J/(mol·K)]。由表3 可以看出,焓變(ΔH)為正,表示是吸熱反應;ΔS為正,ΔG為負,表明百草枯的去除是一種自發可行的方式。

表3 熱力學擬合參數
2.3 熱改性對吸附的影響
為了進一步考察活性炭對百草枯的影響,把YK-6 在CO2的保護下進行改性,分別在200、250、300 ℃條件下加熱1 h,將其分別命名為YK-6-200、YK-6-250 和YK-6-300,如圖6 所示,加熱可使炭表面的羧基和酚羥基減少,內酯基增多,這是由于CO2條件下羧基和酚羥基發生酯化的原因,羧基和酚羥基屬于不穩定的官能團,內酯基穩定性較高[13]。百草枯分子和活性炭表面酸性官能團發生化學吸附,主要是靜電吸引和范德華力作用[14,15]。同時,熱改性中孔率有所提高,對吸附也有貢獻[16]。結果(表4、圖7)表明,百草枯的吸附量與酸性官能團數量和累積介孔體積的總和呈線性相關,相關系數(R2)為0.94,通過軟件Chemdraw 估算百草枯分子大小為1.3 nm×0.3 nm×0.36 nm,介孔大小為2.21~10.05 nm的適合容納百草枯分子[17]。酸性官能團數量對百草枯吸附能力的影響與介孔對活性炭的影響相同。

圖6 熱改性后動力學吸附曲線

表4 不同尺寸的累積介孔體積分布

圖7 吸附量與介孔體積和官能團數量的總和的線性相關性
3 小結
本研究利用硝酸對椰殼活性炭進行改性,考察了改性對百草枯吸附的影響,使用Boehm 滴定法和液態氮吸附對活性炭進行了表征。結果表明,硝酸改性的活性炭可以明顯提高對百草枯的去除能力,通過氧化增加椰殼活性炭的表面含氧官能團而增加吸附量,特別是增加羧基和羰基官能團,從而增加對百草枯的吸附量。研究發現,使用硝酸氧化的活性炭可以從水溶液中有效去除百草枯。該吸附過程由Langmuir 模型來描述更合適,在所研究的濃度范圍內,吸附服從一級動力學模型,證明了化學吸附是本次吸附研究中的一個速率控制參數。Dubbininin-Redushkevuch 模型表明活性碳吸附百草枯是一種化學吸附,Van't Hoff 模型表明吸附過程是以一種自發可行的方式進行,酸性官能團數量和累計介孔體積與吸附量有很好的線性關系,因此,椰殼是一種很有前途的活性炭前體。

