1596例結核分枝桿菌表型藥敏檢測與快速分子檢測結果分析
張亞會 潘稚芬 王蔚 彭草云 呂曉東


[摘要] 目的 比較結核分枝桿菌表型藥敏與快速分子檢測結果的一致性。方法 回顧性分析2017年1月至2020年12月浙江省嘉興市第一醫院確診的1750例涂陽肺結核患者痰液、肺泡灌洗液等標本,同時進行結核菌表型藥敏及快速分子檢測,對兩種檢測結果的一致性進行比較,并對不一致的原因進行分析。結果 1750例患者按流程操作共檢測得到結核分枝桿菌菌株1596例(91.20%),其中1542例利福平(RFP)兩種方法檢測結果一致(敏感1478例,耐藥64例),一致率為96.62%;54例RFP不一致(3.38%)。1520例異煙肼(INH)兩種方法檢測結果一致(敏感1465例,耐藥55例),一致率為95.24%;76例INH不一致(4.76%)。利福平(RFP)ropB基因突變位點分子檢測檢出率為94.79%(91/96),表型藥敏檢出率為93.02%(80/86)。異煙肼(INH)katG、inhA基因突變位點分子檢測檢出率為95.79%(91/95),表型藥敏檢出率為87.91%(80/91)。分析兩種檢測結果不一致的原因有檢測標本不一致、檢測技術局限性、不同突變類型、靜默突變、異質性耐藥及其他耐藥機制。結論 結核分枝桿菌表型藥敏與分子檢測結果的一致性高,差異無統計學意義,臨床上擴大分子藥敏作為初始診斷工具,可取得早診治、早防控的效果;當檢測結果不一致時,應及時分析原因,建議有條件的結核病定點醫院使用兩種檢測方法平行檢測以提高精準度。
[關鍵詞] 結核分枝桿菌;體外藥敏試驗;表型藥敏;分子檢測;一致性分析
[中圖分類號] R446.5 ? ? ? ? [文獻標識碼] B? ? ? ? ? [文章編號] 1673-9701(2022)05-0138-06
[Abstract] Objective To compare the consistency of phenotypic drug sensitivity and rapid molecular detection results of Mycobacterium tuberculosis. Methods Sputum and bronchoalveolar lavage fluid(BALF) samples from 1750 patients with smear-positive pulmonary tuberculosis diagnosed in the First Hospital of Jiaxing from January 2017 to December 2020 were retrospectively analyzed. Tuberculosis phenotypic drug sensitivity and rapid molecular detection were performed simultaneously. The consistency of the two detection results was compared. And the causes of inconsistency were analyzed. Results A total of 1596 cases (91.20%) of Mycobacterium tuberculosis strains were detected in 1750 patients according to the process, of which 1542 cases had consistent detection results in rifampicin (RFP) between the two methods (1478 sensitive and 64 resistant), with a concordance rate of 96.62%. Fifty-four cases RFP had inconsistent results (3.38%). The detection results of isoniazid(INH) in 1520 cases were consistent between the two methods (1465 sensitive and 55 resistant), with a concordance rate of 95.24%. Seventy-six cases INH were inconsistent (4.76%). The detection rate of the rifampicin (RFP) ropB gene mutation site was 94.79% (91/96), and the detection rate of phenotypic drug sensitivity was 93.02% (80/86). The detection rate of isoniazid (INH) katG and inhA gene mutation sites was 95.79% (91/95) and the detection rate of phenotypic drug sensitivity was 87.91% (80/91). The reasons for inconsistency between the two test results were as follows: inconsistency of test samples, limitation of detection technology, different mutation types, silent mutation, heterogeneous drug resistance, and other drug resistance mechanisms. Conclusion The consistency of phenotypic drug sensitivity and molecular detection results of Mycobacterium tuberculosis is high, and the difference is not significant. Expanding molecular drug sensitivity as an initial diagnostic tool in clinical practice can achieve the effect of early diagnosis and early treatment prevention and control. When the detection results are inconsistent, the causes should be analyzed in time, and it is recommended that conditional tuberculosis designated hospitals use parallel detection with two detection methods to improve the accuracy.
[Key words] Mycobacterium tuberculosis; In vitro drug sensitivity test; Phenotypic drug sensitivity; Molecular detection; Consistency analysis
結核病是由結核分枝桿菌(mycobacterium tuberculosis,M.tb)引起的呼吸道傳染性疾病[1]。耐多藥結核病[2](multidrug-resistant tuberculosis,MDR-TB)的流行是結核發病率居高不下的重要原因[3],也是世界性的公共衛生問題[4]。耐藥結核病的診斷主要依靠體外藥物敏感性試驗(drug susceptibility testing,DST)。根據WHO指南[5],耐多藥/利福平耐藥結核病(rifampicin resistant tuberculosis,MDR/RR-TB)的發現首先需要細菌學確認,進一步行快速分子檢測、痰培養或基因測序檢測結核菌耐藥情況[6]。因此,正確判讀快速分子檢測與表型藥敏檢測結果,選擇精準方案及療程具有十分重要的意義。本研究收集2017年1月至2020年12月浙江省嘉興市第一醫院臨床診斷為結核病患者的痰液、肺泡灌洗液等標本1750份,行快速分子檢測[7]及表型藥敏試驗[8],現報道如下。
1 材料與方法
1.1 病例及菌株來源
入選病例菌株均來自2017年1月至2020年12月浙江省嘉興市第一醫院結核門診及住院的涂陽肺結核患者痰液、肺泡灌洗液標本,行快速分子檢測(Xpert MTB/RIF、基因芯片)及結核菌培養(羅氏固體培養及液體BACTEC MGIT960培養)并進行藥敏試驗,共計1750例。
1.2 方法
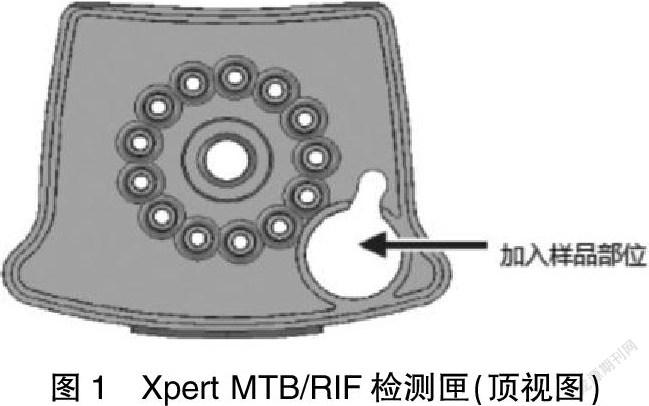
1.2.1 Xpert MTB/RIF檢測系統? 痰樣本前處理。收集1~4 ml痰液樣本置于一次性的防漏容器中,在Xpert MTB/RIF檢測匣側壁標記樣本序號(ID)。打開裝有痰液樣本的容器,加入痰液樣本2倍體積的樣本試劑(sample reagent,SR)。蓋上蓋子,劇烈搖動10~20次或渦旋震蕩至少10 s。將混合好的樣本在20~30℃孵育15 min。在孵育進行到5~10 min時,再次劇烈搖動裝有痰液樣本的容器10~20次或渦旋震蕩至少10 s。視樣本性狀,將1~2倍體積的4%氫氧化鈉(NaOH)加入前處理管中,旋緊處理管的螺旋蓋,在渦旋振蕩器上振蕩1 min左右直至痰樣本充分液化,將前處理管置于生物安全柜內,室溫靜置15 min;將45 ml磷酸緩沖鹽溶液(phosphoric acid buffer salt solution,PBS)加入液化好的痰液中,旋緊螺旋蓋,將前處理管在3000 r/min離心20 min;去上清,加入2 ml PBS。將樣品加入檢測匣后,打開檢測匣的蓋子,將處理后的樣品由檢測匣的加樣孔緩慢加入。見圖1。關閉檢測匣的蓋子,開始檢測,GeneXpert Dx軟件自動讀取信息進行自動檢測。
1.2.2 基因芯片檢測系統? 采用DNA 微陣列芯片法進行菌種鑒定,使用博奧生物分枝桿菌菌種鑒定試劑盒,具體步驟如下。①從固體培養基上挑取菌落于含核酸提取液的核酸提取管中;液體培養基內吸取≥1個麥氏濁度的菌懸液10~20 μl于含核酸提取液的核酸提取管中;使用Extractor 36核酸快速提取儀振蕩5 min,95℃水浴5 min,5000 r/mim離心1 min,得到的核酸放置-20℃暫存。②在標本制備區內進行PCR擴增反應、芯片雜交、芯片的洗滌與干燥等步驟,甩干后掃描。③使用晶芯微陣列芯片掃描儀LuxScan10K-B和相應軟件進行信號的讀取及結果判讀。陽性判斷值:對于IC(分枝桿菌屬)探針和結核分枝桿菌探針通過ROC方法確定其陽性判斷值。對于其他16種非結核分枝桿菌檢測探針均通過百分位數法確定其陽性判斷值。當探針信號值大于或等于該探針的陽性判斷值,則該探針判讀為陽性;當探針信號值小于該探針的陽性判斷值,則該探針判讀為陰性。試劑盒中各探針的陽性判斷值已整合到相應判讀軟件中,由軟件自動對樣品檢測結果進行判別。
1.2.3 臨床結核分枝桿菌的培養及體外藥敏試驗? ? (1)結核分枝桿菌固體培養。①前處理方法:痰液中加2~4倍量2%NaOH,振蕩器振蕩5~10 min,或置室溫30 min、其間振蕩2~3次,使痰液化。取前處理液化后痰液0.1 ml,無菌操作接種于培養基斜面上,每份標本同時接種兩支酸性改良羅氏培養基,置37℃孵育。對培養陽性的菌株進行分枝桿菌菌群鑒定,在試劑瓶中加入對硝基苯甲酸(PNB)和噻吩二羧酸肼(TCH)試劑,觀察菌株生長指數,如繼續生長為非結核分枝桿菌,如生長受到抑制則為結核分枝桿菌。②藥物敏感性檢測:選擇4種常用的一線抗結核藥物(異煙肼、利福平、鏈霉素、乙胺丁醇)進行體外藥物敏感試驗,抗結核藥物濃度分別為異煙肼0.1 mg/L、利福平1.0 mg/L、鏈霉素1.0 mg/L、乙胺丁醇5.0 mg/L,采用WHO/國際防癆與肺部疾病聯合會《耐藥檢測指南》推薦的比例法[9]。(2)結核分枝桿菌960液體培養。①培養管準備:MGIT營養添加劑(0.5%甘油,0.5%牛血清白蛋白,0.2%葡萄糖,140 mmol/L NaCl,OADC)為15 ml液體試劑,可直接使用,在每一根培養管中加入800 μl MGIT營養添加劑備用。②樣本準備:挑取1~2 ml膿性痰液部分至標記的50 ml離心試管中;加等量的2% N-乙酰半胱氨酸-氫氧化鈉-枸櫞酸鈉前處理液;漩渦震蕩20 s;靜置15 min;加無菌PBS(pH= 6.8)至約50 ml,蓋緊蓋子;離心3000 r/min,15 min;倒掉上清液;添加1~3 ml PBS以中和pH值至6.8。③樣本接種:將上述預處理好的樣本接種500 μl至MGIT培養管中。④MGIT培養管裝載至BACTECMGIT 960 System全自動分枝桿菌檢測/藥敏系統孵育培養。
1.3 統計學方法
采用SPSS 13.0統計學軟件進行數據處理,計數資料以[n(%)]表示,組間比較采用χ2檢驗(或Mc Nem),P<0.05為差異有統計學意義。通過Kappa檢驗分析兩種方法一致性(Kappa>0.75,一致性較好;0.40~0.75,一致性一般;<0.40,一致性較差)。
2 結果
2.1 分子DST檢測與表型DST藥敏檢測結果分析
2.1.1 兩種檢測方法耐藥性檢測結果一致率? 1750例標本按流程操作共檢測到結核分枝桿菌菌株1596例,陽性率為91.20%,非結核分枝桿菌(NTM)154例(8.80%)。其中快速分子DST檢測出利福平(RFP)耐藥菌株98例,耐藥率為6.14%(98/1596),表型DST藥敏檢測出利福平(RFP)耐藥菌株88例,耐藥率為5.51%(88/1596);兩種方法均檢出利福平(RFP)敏感1478例,均耐藥64例,共1542例利福平(RFP)檢測結果一致,一致率為96.62%。快速分子DST檢測出異煙肼(INH)耐藥95例,耐藥率為5.95%(95/1596),表型DST藥敏檢測出異煙肼(INH)91例,耐藥率為5.70%(91/1596),兩種方法異煙肼(INH)均敏感1465例,均耐藥55例,共1520例異煙肼(INH)分子DST檢測與表型DST藥敏檢測結果一致,一致率為95.24%。見表1。兩種方法共檢測出耐多藥肺結核(MDR-TB)患者34例,耐多藥率為2.13%(34/1596)。
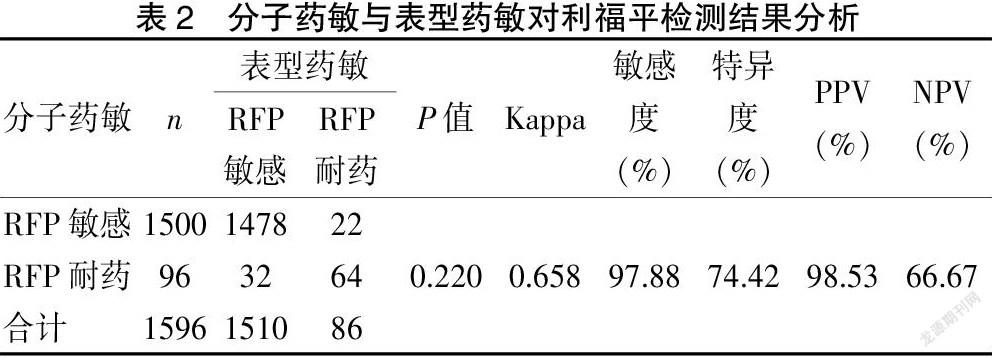
2.1.2 分子檢測與表型藥敏對利福平檢測結果分析? ? 54例患者利福平(RFP)分子DST檢測與表型DST藥敏結果不同,分子DST檢測利福平(RFP)耐藥而表型DST敏感32例;分子DST檢測利福平(RFP)敏感而表型DST耐藥22例,不一致率為3.38%;利福平分子檢測結果敏感度為97.88%,特異度為74.42%。見表2。
2.1.3 分子檢測與表型藥敏對異煙肼檢測結果分析? ? 76例患者異煙肼(INH)分子DST檢測與表型DST藥敏結果不同,分子DST檢測異煙肼(INH)耐藥而表型DST敏感40例,分子DST檢測敏感而表型DST耐藥36例,不一致率為4.76%。分子檢測對異煙肼檢測結果敏感度為97.34%,特異度為60.44%。見表3。
2.2 分子檢測基因突變位點與表型藥敏檢測結果分析
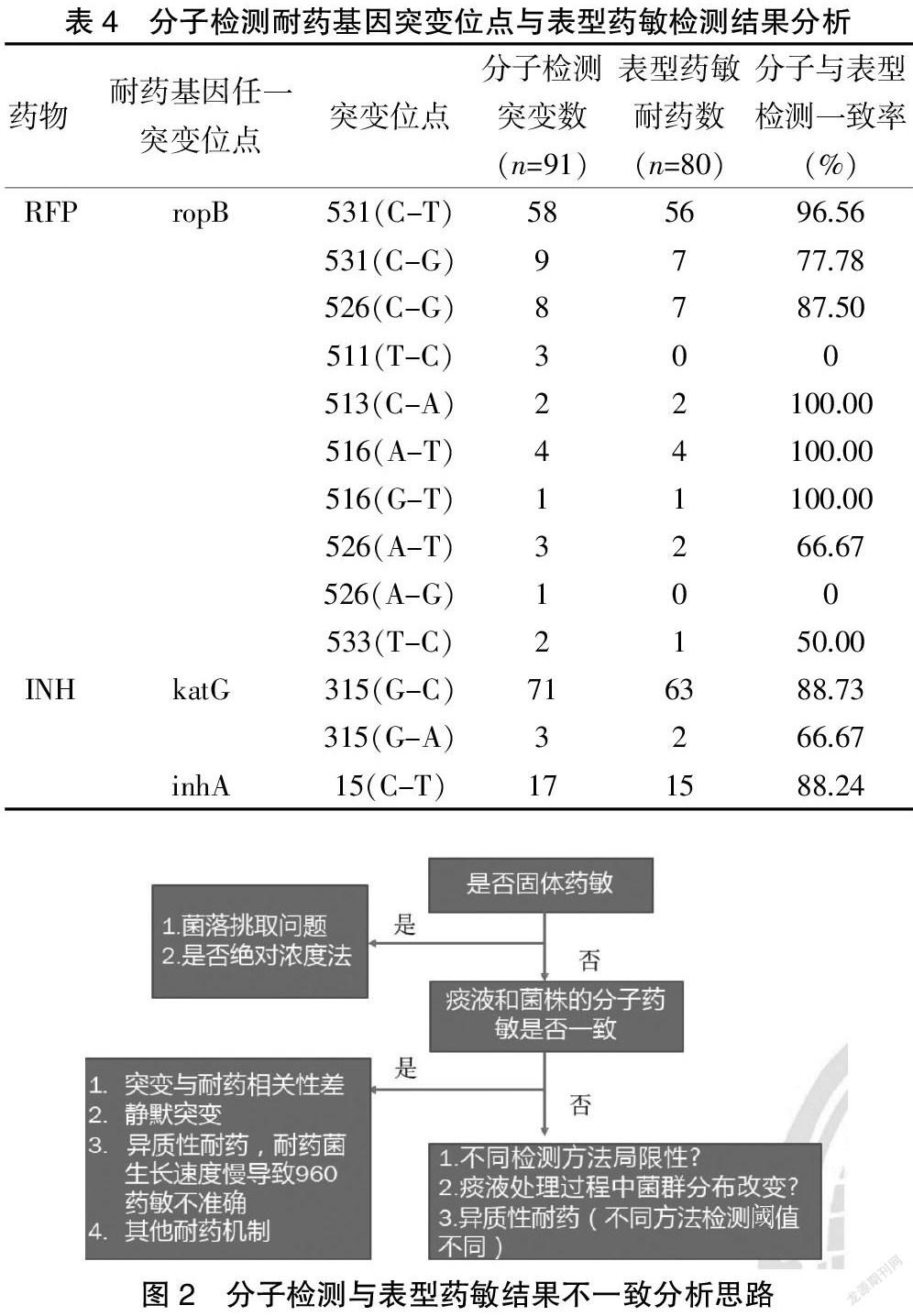
利福平(RFP)耐藥檢測中,快速分子DST檢測ropB基因突變檢出率為94.79%(91/96),表型DST藥敏利福平耐藥檢出率為93.02%(80/86),其中位點531(C-T)、513(C-A)、516(A-T)、516(G-T)突變位點的檢出一致率高(96.56%~100.00%);而526(A-G)、511(T-C)位點分子檢測出陽性,表型DST藥敏檢測未顯示;533(T-C)、531(C-G)、526(A-T)位點的一致符合率為50.00%、77.78%、66.67%;利福平(RFP)突變位點分子與表型DST藥敏一致率為87.91%(80/91)。
異煙肼(INH)檢測中,快速分子DST檢測katG、inhA基因突變位點的檢出率為95.79%(91/95);表型藥敏DST異煙肼耐藥檢出率為87.91%(80/91);其中katG315(G-C)、inhA15(C-T)位點的一致率較高,分別為88.73%、88.24%,但仍然發現尚有10例不一致;katG 315(G-A)有1例分子與表型DST藥敏結果不一致。見表4。初始分子檢測與表型藥敏結果不一致分析思路見圖2。
3 討論
2020年全球結核病報告顯示,2019年,全球有近50萬人罹患利福平耐藥(RR-TB)結核病,其中78%患有耐多藥(MDR-TB)。隨著分子診斷技術的臨床應用,2019年發現并登記MDR/RR-TB患者較2018年增加了10%,但其治療成功率僅為57%[5]。因此,提高細菌學確診的結核病患者比例,擴大細菌學確診的結核病患者耐藥檢測比例,提高治愈率,是遏制耐藥結核病傳播的重要措施。
Xpert MTB/RIF檢測系統是以實時熒光定量PCR技術為基礎,ropB基因為靶基因,檢測周期僅2 h,是目前WHO推薦的RFP耐藥的檢測方法[11]。本研究結果顯示,快速分子檢測ropB基因突變檢出率為94.79%(91/96),與李妍等[12]研究痰標本中Xpert MTB/RIF敏感度高達97.5%、特異度為95%~99%相一致。
基因芯片技術是將MTB的DNA擴增產物與固定在芯片上的探針雜交、掃描芯片及判讀結果,現已廣泛應用于臨床耐藥性的檢測及基因組的比較分析。楊映暉等[13]研究顯示,基因芯片檢測MDR-TB的敏感度與特異度分別為64.62%和97.75%。本研究結果顯示,異煙肼(INH)快速分子檢測中,katG、inhA基因突變位點的檢出率為95.79%(91/95),與相關文獻研究結果一致[14]。
本研究通過對2017年1月至2020年12月確診的1750例涂陽肺結核患者呼吸道標本中檢測到的1596例結核分枝桿菌菌株結果進行分析,快速分子DST檢測技術與表型DST藥敏檢測的利福平、異煙肼一致率分別達96.62%、95.24%,差異無統計學意義(P>0.05)。提示在臨床上可通過擴大分子檢測技術作為初始診斷工具,將所有肺結核患者的初次痰標本、肺泡灌洗液等呼吸道標本納入分子檢測初始診斷范圍,加大在基層醫院的推廣應用,才能確保所有診斷為耐藥(MR-TB)、耐多藥(MDR/RR-TB)的患者早期納入治療,改變耐藥結核納入治療率低的現狀。2019年全球納入治療的患者比例僅占估算MDR/RR-TB患者數的38%[15]。研究發現,嘉興市的耐多藥率僅為2.13%,低于浙江省耐多藥結核發病率[10],證實了嘉興市擴大分子初始檢測策略遏制耐藥結核傳播的有效性。
本研究結果還顯示,雖是同一標本平行檢測,也存在著分子檢測與表型藥敏檢測結果不一致的現象,尚有54例利福平(3.38%),76例異煙肼(4.76%)檢測結果不一致,給臨床個體治療方案的選擇帶來困惑,也是現階段耐藥結核治愈率低的因素之一。WHO報告顯示,2019年全球耐藥結核病治療成功率僅為57%[5]。因此,需認真查找分子DST檢測與表型DST藥敏檢測結果不一致的原因,及時分析,調整每一例耐藥結核患者的治療方案,盡早盡快實施個體化精準診療策略,才能提升治愈率。
本研究涉及到的54例利福平,76例異煙肼患者,針對兩種檢測結果不一致的原因分析如下:①檢測標本是否一致。仔細查找發現2例患者分子檢測與表型培養的標本不是同一個檢測標本;1例患者標本因條形碼掃碼差錯而出現偏差,予重新留取痰標本進行平行檢測。②檢測技術的局限性。Xpert MTB/RIF、基因芯片快速分子檢測可檢測到結核分枝桿菌的核酸,但無法區別活菌還是死菌;本研究發現其中1例分子檢測敏感,表型藥敏顯示耐藥,原因是操作過程中標本處理不充分,氫氧化鈉時間過長,消化過程中發生了結核分枝桿菌核酸(RNA)降解。1例肺泡灌洗液Xpert MTB/RIF檢測陽性,表型培養陰性,查找原因發現支氣管鏡檢查消毒清洗不徹底有死菌殘留存在,而Xpert MTB/RIF檢測DNA敏感度高所致。另外,還需分析在檢測過程中是否存在分子檢測系統的故障、溫度的錯誤、試劑盒儲存不合理等因素。表型固體培養存在絕對濃度法偏差較大、選取菌落時操作不當等因素。液體960自動培養時吡嗪酰胺(PZA)藥敏菌株過量,在代謝過程產生大量氨類物質,從而使整個液體培養環境的pH值升高,導致PZA失去殺菌能力而造成假陽性結果。可能導致其藥敏試驗結果重復性差,造成PZA分子與表型藥敏結果不一致。③不同突變類型與耐藥相關性。從突變位點分析,發現1例快速分子檢測利福平(RFP)基因ropB位點526(A-G)突變、3例利福平(RFP)511(T-C)位點分子檢測陽性,而表型藥敏檢測并不耐藥;1例利福平(RFP)基因533(T-C)、2例531(C-G)、1例526(A-T)位點突變不一致,提示基因突變位點不同,與表型藥敏試驗的相關性也是不同的。郭晶等[16]研究顯示,基因突變在不同年齡組人群中存在一定的差異。個別突變位點還應當結合臨床治療情況進行觀察與分析,不同突變位點應當結合患者的藥敏試驗結果與整體治療情況進行個體化治療。④靜默突變。沉默子突變只是改變核苷酸位點而不改變編碼蛋白質性質,此時Xpert MTB/RIF檢測結果表現為利福平假陽性,表型培養藥敏敏感;這些Xpert MTB/RIF檢測假陽性患者給予一線抗結核藥物仍然有成功治愈的可能,臨床需謹慎甄別。⑤異質性耐藥。異質性耐藥[17]是指在臨床同一類患者體內分離出結核分枝桿菌樣本中同時存在敏感和耐藥菌株,敏感和耐藥菌株共同感染或敏感株部分亞群發生耐藥突變所致。當存在異質性耐藥的MTB中耐藥亞群比例高于分子檢測的敏感度時,臨床檢測出并判斷為耐藥;當耐藥亞群比例低于分子檢測敏感度時,就會判讀為敏感,導致部分MTB的分子檢測與表型耐藥檢測結果不一致。本研究結果顯示,有22例快速分子檢測利福平(RFP)敏感,表型藥敏檢測耐藥,分子檢測假敏感可能與異質性耐藥有關。分子檢測需達到≥20%以上的耐藥亞群時才能檢測出,而表型藥敏可檢測出1%的耐藥菌株。異質性耐藥反映了MTB群體從部分耐藥向全體耐藥轉變的中間過程[18]。⑥基因突變以外的其他耐藥機制引起的MTB耐藥。另外2例異煙肼(INH)、利福平(RFP)分子檢測敏感但表型藥敏耐藥不一致的原因不明,可能存在藥物外排泵、MTB細胞壁增厚難以穿透、抗結核藥物失活等由基因突變以外的其他耐藥機制所致[19]。
綜上所述,分子DST檢測及表型DST藥敏診斷技術的應用,給“終結結核病策略”[20]提供了診斷工具,給臨床耐藥結核病的治療帶來了診斷“金標準”。建議在有條件的定點醫院結核病實驗室可使用兩種檢測方法平行檢測以提高精準度;當臨床檢測中發現初始分子檢測與表型藥敏結果不一致時,應認真分析原因、及時調整治療方案、實施個體化精準診療策略,提高耐藥結核患者的治愈率。
[參考文獻]
[1] 唐神結,高文,陳昶,等.臨床結核病學[M].北京:人民衛生出版社,2011:3-4.
[2] 唐神結,許紹發,李亮.耐藥結核病學[M].北京:人民衛生出版社,2014:62-65.
[3] 任坦坦,陸普選,鄧國防,等.2020WHO全球結核報告:全球與中國關鍵數據分析[J].新發傳染病電子雜志,2020, 5(4):280-284.
[4] 高靜韜,劉宇紅.2020年世界衛生組織全球結核病報告要點解讀[J].河北醫科大學學報,2021,42(1):1-6.
[5] Global tuberculosis report 2020.Geneva:World Health Organization;2020(https://www.who.int/tb/ publications/global_report/en/,accessed 15 October 2020).
[6] Global tuberculosis report 2019.Geneva:World Health Organization;2019(https://www.who.int/tb/ publications/global_report/en/,accessed 29 July 2020).
[7] 中華人民共和國國家衛生和計劃生育委員會.肺結核診斷標準(WS 288—2017)[J].新發傳染病電子雜志,2018,3(1):59-61.
[8] 郭海萍,逄宇.全面落實肺結核診斷國家行業標準提高分子技術診斷耐藥結核病能力[J].結核與肺部疾病雜志,2020,1(2):103-105.
[9] 趙雁林,王黎霞,成詩明,等.結核分枝桿菌藥物敏感性實驗標準化操作程序及質量保證手冊[M].北京:人民衛生出版社,2013:140.
[10] 柳正衛,何海波,王曉萌,等.浙江省第三次結核病耐藥性監測結果分析[J].中華預防醫學雜志,2011,45(2):171-173.
[11] Wang G,Wang S,Yang X,et al.Accuracy of Xpert MTB/RIF Ultra for the diagnosis of pleural TB in a multicenter cohort study[J].Chest,2020,157(2):268-275.
[12] 李妍,張天華,鮮小萍,等.Xpert MTB/RIF檢測技術診斷肺結核和肺外結核的價值[J].中國防癆雜志,2015, 37(6):586-589.
[13] 楊映暉,伍定輝,蘇偉明,等.基因芯片法在結核分枝桿菌耐藥基因快速診斷中的應用價值[J].中國防癆雜志,2020,42(11):60-64.
[14] 孫正松,曾方林,戴潔,等.基因芯片檢測結核分枝桿菌耐藥基因效能分析[J].國際檢驗醫學雜志,2018,39(22):57-59.
[15] 羅一婷,翁榕星,周芳,等.2019WHO全球結核報告:全球與中國關鍵數據分析[J].新發傳染病電子雜志,2020, 5(1):47-50.
[16] 郭晶,曾誼,林霏申,等.結核分枝桿菌表型及基因型一致性與患者預后的相關性研究[J].國際呼吸雜志,2018, 38(20):1574.
[17] 何容芳,唐仕萍,謝鑫,等.耐多藥結核病發生危險因素的Meta分析[J].四川醫學,2020,41(3):245-251.
[18] 袁陽.結核分枝桿菌異質性耐藥的檢測及其臨床意義[D].遵義:遵義醫學院,2018.
[19] 宋婧,車南穎.結核分枝桿菌耐藥機制和檢測方法的研究進展[J].中國醫藥導報,2018,15(29):29-34.
[20] 劉健雄,鐘球."終止結核病"面臨的挑戰與應對策略[J].中國防癆雜志,2020,42(4):14-16.
(收稿日期:2021-03-18)

