硫化氫對骨與關節保護作用機制的研究進展
張博文,閆景龍
(哈爾濱醫科大學附屬第二醫院脊柱外科,黑龍江 哈爾濱 150086)
硫化氫(H2S)是一種無色、具有典型臭雞蛋氣味的有毒氣體[1]。近幾十年來,許多文獻已經報道H2S存在于生物系統中并具有多種生物學功能,其中最主要的功能是維持生理穩態。它和一氧化氮、一氧化碳一樣是組織系統中內源性釋放的氣體遞質[1],在大腦、心臟、腎臟、胃腸道、骨骼肌和骨骼中產生[2]。在哺乳動物組織中,H2S主要在同型半胱氨酸代謝的轉硫途徑中內源產生,其中胱硫醚-β-合成酶(cystathionine-β-synthase,CBS)和胱硫醚-γ-裂解酶(cystathionine-γ-lyase,CSE)是生成H2S的兩種關鍵酶[2]。H2S不僅僅是這一途徑的二次反應產物,而且是調節多種組織生理功能的重要因子。
H2S的合成和分布取決于組織特異性,CBS主要在骨髓間充質干細胞(bone mesenchymal stem cells,BMSC)、中樞神經、回腸、腎臟及胰島中表達,CSE主要在心臟、腎臟、血管內皮和血管平滑肌中大量表達[3]。有報道指出,H2S通過調控BMSCs的表觀遺傳分化來維持骨骼合成代謝及穩態[3-4],這表明了H2S對骨的保護作用。還有研究表明H2S是免疫系統中維持T細胞內穩態的重要介體[5-6],它不僅可以起到抗氧化、抗炎,還具有平衡氧化還原和誘導抗氧化應激轉錄因子核因子E2相關因子2(nuclear factor erythroid 2-related factor,Nrf2)的作用[5,7],表明了H2S能夠抗炎癥性關節炎,體現了其對關節的保護作用。本文綜述了H2S對骨骼及關節的保護作用及其分子機制。
1 H2S通過抑制JNK-p-DNMT1通路抵抗高同型半胱氨酸血癥(hyperhomocysteinemia,HHcy)導致的骨質丟失
H2S作為一種內源性氣體遞質,具有抗炎、抗氧化和抗細胞凋亡的作用,與骨骼發育密切相關。H2S的生理和病理作用的相關研究清楚地解釋了H2S在骨骼疾病中的骨保護作用[1,3-4]。骨質疏松癥是一種以骨吸收和骨形成(破骨和成骨)失衡為特征的骨骼疾病。甲硫氨酸的過量攝入往往會導致骨骼脆弱而增加骨折的風險[8]。甲硫氨酸代謝途徑的紊亂會導致血清同型半胱氨酸升高,引起HHcy,它是一種涉及CBS的常染色體隱性疾病[8]。研究表明,H2S在逆轉HHcy誘導的骨丟失中有重要作用[9]。實驗人員以高甲硫氨酸飲食喂養小鼠,降低內源性H2S產生,誘發小鼠產生HHcy,HHcy激活C-Jun/JNK-p通路并進一步調節轉錄增強DNA甲基轉移酶1(DNA methyltransferase 1,DNMT1)的表達,DNMT1升高會導致破骨細胞抑制因子(osteoclastogenesis inhibitory factor,OPG)啟動子過度甲基化,從而導致BMSCs分化的成骨細胞功能障礙,并且HHcy使核因子κB受體活化因子配體(receptor activator for nuclear factor-kappa Bligand,RANKL)上調,增加了破骨細胞生成和骨質流失[9]。使用硫氫化鈉(H2S供體)能夠抑制JNK-p-DNMT1通路,使DNMT1表達減少,進而上調OPG,從而增加成骨,這顯示了H2S的骨保護特性[9](見圖1)。還有研究表明,HHcy可誘導蛋白磷酸酶2A磷酸化,進而下調p38 MAPK和叉形頭轉錄因子1(forkhead transcription factor 1,FOXO1)的表達,從而抑制OPG的合成,實驗中給予N-乙酰半胱氨酸可以提高骨骼中FOXO1和OPG的水平,從而逆轉HHcy介導的骨丟失[10]。調節H2S的代謝或使用H2S供體能夠在治療HHcy引起的骨質疏松方面發揮重要作用。
2 H2S通過維持組蛋白去乙酰化酶3(histone deacetylase-3,HDAC3)活性抵抗CBS缺乏導致的骨質流失
CBS表達水平在骨髓間充質干細胞成骨分化過程中升高,并發揮重要作用,由它介導生成的H2S可以維持骨髓間充質干細胞和成骨細胞的增殖和分化[11]。實驗數據表明,缺乏CBS小鼠的血清和細胞內H2S水平降低,使其血漿中的同型半胱氨酸水平升高,這會導致骨髓間充質干細胞的氧化損傷和功能障礙,從而導致嚴重的骨質疏松[11]。有研究表明,H2S缺乏會通過增強氧化損傷來抑制HDAC3的活性,使染色質的組蛋白(H3K27ac)上的乙酰化賴氨酸殘基與啟動子結合,進一步降低Runt相關轉錄因子2(Runt related transcription factor 2,RUNX2)的成骨作用,同時轉錄激活炎癥細胞因子白細胞介素(interleukin,IL)-6和腫瘤壞死因子α(tumor necrosis factor α,TNF-α)[5,12]。并且研究發現BMSCs分泌的IL-6可以誘導破骨細胞分化和骨吸收[12]。因此,H2S缺乏會減弱成骨作用,增強破骨作用。在缺乏CBS的小鼠中使用H2S能夠通過恢復BMSCs中的HDAC3活性來減弱組蛋白乙酰化依賴性炎癥,從而促進RUNX2介導的骨形成[12](見圖2)。總體而言,恢復血漿中的H2S水平可能是治療CBS缺乏引起代謝性骨質疏松癥的一種新方法。
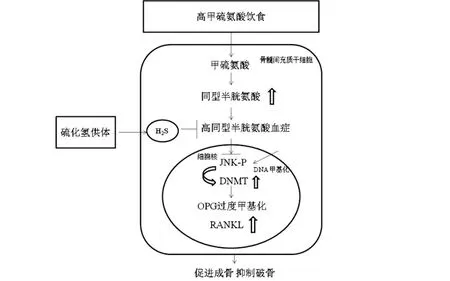
圖1 H2S通過抑制JNK-p-DNMT1通路抵抗HHcy導致的骨質丟失示意圖
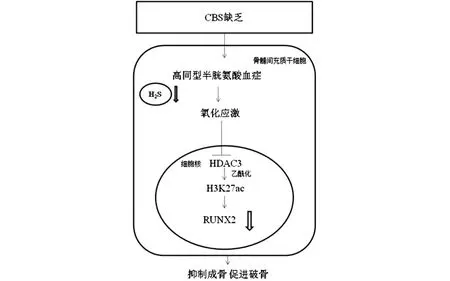
圖2 H2S通過維持HDAC3活性抵抗CBS缺乏導致的骨質流失示意圖
3 H2S通過調控Ca2+瞬態受體電位通道維持骨穩態
機制研究表明,BMSCs中H2S在生理水平上對維持細胞鈣通道的正常功能起著關鍵作用。H2S缺乏使多個Ca2+瞬態受體電位通道上半胱氨酸殘基的蛋白巰基化減少而導致細胞內Ca2+內流減少,而細胞內Ca2+流量水平降低進一步抑制了蛋白激酶C(protein kinase C,PKC)依賴的信號通路,使骨髓間充質干細胞的成骨分化減弱,最終導致嚴重的骨質疏松[11]。通過使用硫氫化鈉或GYY4137(H2S供體)使體內H2S濃度達到生理水平,從而在通道蛋白硫基化過程中,反應性半胱氨酸的巰基被修飾為-SSH基團,提高了半胱氨酸殘基的反應性,進而使BMSCs可以發生正常的級聯反應,最終恢復正常的骨穩態[11](見圖3)。總的來說,生理水平的H2S能夠確保BMSCs上Ca2+瞬態受體電位通道的正常功能,以維持機體骨穩態。
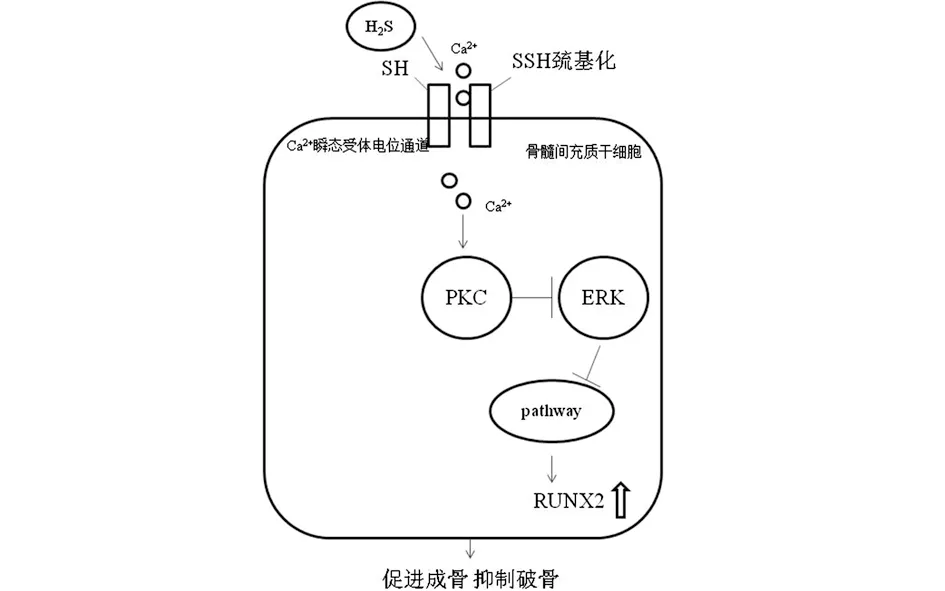
圖3 H2S通過調控Ca2+瞬態受體電位通道維持骨穩態示意圖
4 H2S能夠抵抗雌激素缺乏導致的骨質流失
雌激素由于具有抗氧化的活性和平衡體內磷酸鈣并維持骨代謝的作用,可以預防骨質疏松癥[8,13]。絕經后骨質疏松癥是一種常見的骨骼疾病,由于絕經后雌激素水平下降,使破骨細胞成熟而增加了骨吸收過程,最終導致骨小梁和皮質骨進一步改變,使骨質流失增加骨折風險[8,13]。有研究表明,遺傳因素對于確定雌激素缺乏后小鼠的骨質流失程度很重要,此報道提出更年期期間和之后的骨丟失可能是由部分遺傳因素調控的[13]。但是,仍然需要進一步地研究遺傳因素控制由雌激素缺乏引起骨骼變化的機制。有研究以去卵巢大鼠為研究對象,探討了H2S在機體缺乏雌激素的病理環境下的骨保護作用[14]。實驗人員通過卵巢切除術(oophorectomy,OVX)增加破骨細胞的形成來增強骨吸收,用以模擬雌激素缺乏的病理狀態[14]。通過使用GYY4137緩慢釋放H2S,最終使血漿H2S水平趨于正常化,能夠防止甚至逆轉OVX引起的骨小梁和骨皮質改變的結果[14]。實驗證明,使用H2S可以逆轉由雌激素缺乏引起的骨質疏松,增加骨骼的最大應力,減少骨質疏松及相關并發癥的發生[14]。實驗中使用GYY4137很好地模擬了內源性神經內分泌氣體信號分子H2S的骨保護作用,然而不足的是,他們沒有在臨床上探索GYY4137的治療效果,所以在人體上的治療結果可能會有所不同,并且GYY4137作用的分子機制還有待進一步研究。總體而言,恢復血漿H2S水平可能是治療絕經后骨質疏松癥的一種方法,為今后研究絕經后骨質疏松癥的治療靶點指明了方向。
5 H2S有調控細胞增殖、分化和凋亡的作用
H2S的作用與其他生長因子相似,能夠通過促進骨折處干細胞的增殖和分化來啟動修復過程[15]。研究報道指出在小鼠下頜骨缺損模型中,使用GYY4137可以促進骨折愈合[15]。此外,給予外源性H2S可以治療由模擬微重力和牽張成骨等引起的骨丟失[16]。在小鼠牽張成骨模型中,給予H2S可以加速骨小梁成熟微結構的形成和礦化,取代纖維結締組織,并改善骨痂在牽張間隙內愈合的力學性能[16]。機制研究表明,CSE是成骨細胞中主要表達促進H2S產生的酶,CSE-H2S系統作為一種新的反式激活調節劑通過使RUNX2巰基化促進細胞成骨分化,從而促進骨愈合[15]。已有報道提出H2S是各種細胞存活和凋亡的調節劑,給予H2S可以預防多種形式的應激(低氧、氧化損傷或血清剝奪)引起的細胞凋亡,促進間充質干細胞的增殖和存活[3,17-18]。例如,H2S可通過上調抗凋亡基因B淋巴細胞瘤-2(B-cell lymphoma-2,Bcl-2)的表達來調節間充質干細胞的功能,從而減弱缺氧引起的效應[17]。還有研究發現H2S通過抑制成骨細胞(MC3T3-E1細胞)中的促分裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK)信號通路和激活PI3K/Akt通路來防御氧化應激,保護MC3T3-E1細胞免受凋亡,起到骨保護的作用[19]。調節H2S代謝或使用H2S供體可能成為骨折的治療方法,然而要使H2S在臨床中直接給藥,還需要更深入的研究和實踐。
6 H2S能夠誘導細胞遷移
自體內皮祖細胞和骨髓間充質干細胞在骨缺損部位的募集是誘導骨組織修復的關鍵[20]。內皮祖細胞還在動脈損傷后的內皮修復中起著至關重要的作用,骨髓間充質干細胞的遷移能力是新生血管和血管再生重要的因素之一[20]。H2S在兩種類型的細胞中都有誘導遷移的功能,H2S的缺乏減弱了血管損傷后內皮祖細胞的動員,削弱了它們的黏附和克隆能力,CSE缺乏介導的H2S水平下降導致高糖處理的骨髓間充質干細胞遷移能力減弱,給予硫氫化鈉治療恢復了兩種細胞的上述能力[21-22]。此外,實驗還發現H2S增強了其他類型細胞的遷移能力,例如給予硫氫化鈉能加速皮膚成纖維細胞和人類角質形成細胞的遷移,從而促進傷口愈合[22]。
7 H2S具有抗氧化和抑制炎性因子的作用
H2S是一種可以限制自由基損傷和炎癥的內源性介質,是一種能夠與多種氧化應激源直接反應的強還原劑,在平衡細胞氧化還原狀態方面起著重要的作用[23]。此外,H2S能夠對抗脂質過氧化,逆轉線粒體功能障礙和增加參與細胞抗氧化防御的超氧化物歧化酶活性[23-24]。最近已經證實內源性H2S在不同的炎癥性疾病中的抗氧化和抗炎特性,它能夠抑制淋巴細胞和天然免疫細胞產生促炎介質,從而使促炎介質和黏附分子的表達減少[5]。在關節炎的早期階段,氧化應激是蛋白質翻譯后修飾和產生自身反應性抗體的原因,在啟動炎癥過程中起著關鍵作用[25]。促炎癥細胞因子、生長因子,尤其是血管內皮生長因子在滑膜中的放大表達,增加了失調的新生血管,導致滑膜缺氧[26]。關節炎活動期的特征是血管化、氧化應激和滑膜中免疫細胞浸潤,從而誘導成纖維細胞樣滑膜細胞(fibroblast-like synoviocytes,FLS)肥大,最終使炎癥持續,形成慢性循環,導致軟骨的損傷。這使得FLS、免疫細胞和促炎細胞因子能夠侵入軟骨下骨,形成特征性的骨質侵蝕[27]。核因子κB(nuclear factor kappa-B,NF-κB)是破骨細胞分化和成熟進而導致關節炎骨侵蝕的關鍵因素,而H2S對NF-κB活性的抑制能夠減少促炎細胞因子的產生[28](見圖4)。研究表明,能夠釋放H2S的化合物誘導了基質金屬蛋白酶的抑制和細胞外基質蛋白的產生,從而逆轉IL-1的分解作用[24]。H2S還能下調FLS中由IL-1誘導的IL-6、IL-8、基質金屬蛋白酶(matrix metalloproteinase,MMP)-2和MMP-14的表達[24]。此外,H2S還可以抑制炎性關節炎發病過程中必不可少的細胞因子TNF-α的活性[29]。這些研究表明,H2S具有對關節炎患者關節損傷的保護作用。已經有研究發現,H2S與非甾體抗炎藥偶聯可抑制破骨細胞的產生和成熟,這表明了H2S與非甾體抗炎藥偶聯用于治療炎癥性關節炎有疊加作用[30]。然而,H2S的關節保護作用并不是劑量依賴性的,有研究表明,在脂多糖刺激的小鼠巨噬細胞中,低濃度H2S(硫氫化鈉200 μmol/L)可以抑制幾種促炎介質(NO、NF-κB、IL-6和IL-1)的合成和激活,而高濃度H2S(硫氫化鈉1 000 μmol/L)卻能刺激巨噬細胞產生促炎分子[28]。H2S可以作為一種關節炎疾病中的調節性保護藥物,但H2S在臨床應用的方案還需要進一步的研究。
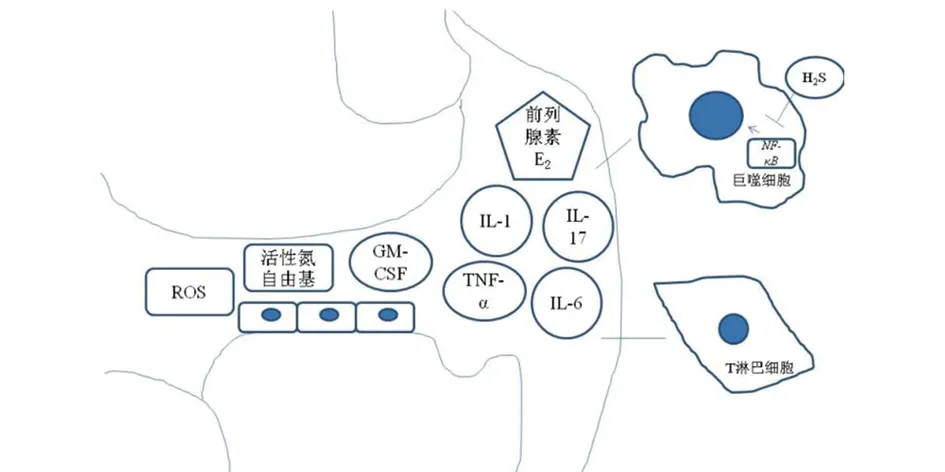
圖4 關節炎中重要的致病炎性因子示意圖
8 小結與展望
H2S是一種無色、具有典型臭雞蛋氣味的有毒氣體,到目前為止,還沒有解毒劑可用于對抗H2S毒性[1,31]。越來越多的證據證明,H2S在骨骼系統的生理和病理過程中發揮著重要的作用。已知H2S可以調節骨髓間充質干細胞的功能,確保骨骼代謝的動態平衡。在HHcy、去卵巢和骨折動物模型中,H2S對骨髓間充質干細胞的增殖、分化、功能調節起著至關重要的作用,應用H2S可以預防或逆轉病理性骨丟失。機制研究表明,H2S控制著關鍵的細胞信號通路、蛋白質的巰基化,以及骨骼組織中染色質水平的表觀遺傳。此外,H2S具有抗炎和誘導受損關節組織修復作用。因此,未來的研究有必要對H2S在骨與關節中的生理和病理作用及其機制進行深入地探索,并努力找到合適的H2S供體以供臨床使用,從而使H2S成為一種治療骨與關節疾病成熟有效的藥物。

