達格列凈對棕櫚酸誘導的人腎小管上皮細胞損傷的保護機制研究
丁庭庭,潘李萌,楊 光,楊 婧,鐘 興,潘天榮
全球糖尿病患病率在未來將繼續增加,預計到2045年,全球糖尿病患者數將達到6.93億[1]。糖尿病常常伴有多種并發癥,其中糖尿病腎病(diabetic kidney disease,DKD)是糖尿病最嚴重的并發癥之一,與糖尿病患者的高發病率與死亡率相關,是終末期腎衰竭最常見的病因之一[2]。DKD是一種以腎小球超濾及腎小球電荷和通透性改變為主的疾病,近來研究[3-4]表明腎小管損傷機制可能在DKD的病理生理中起重要作用,DKD患者腎功能下降與腎小管結構改變包括腎小管萎縮、腎小管間質纖維化等有關。鈉-葡萄糖共轉運蛋白2(sodium-glucose cotransporter 2,SGLT2)抑制劑——達格列凈可通過抑制腎臟對葡萄糖的重吸收、促進尿糖排泄降低血糖,并且對DKD有保護作用,但具體機制尚不清楚。該研究通過棕櫚酸誘導腎小管上皮細胞線粒體功能障礙及氧化應激模型,使用達格列凈干預后檢測腎小管上皮細胞線粒體功能、氧化應激及凋亡情況的變化,探討達格列凈對DKD的保護機制。
1 材料與方法
1.1 材料人腎小管上皮細胞HK-2購自美國Actt公司; DMEM/F12培養基、胎牛血清購自美國Gibco公司;PBS緩沖液購自美國Hyclone公司;0.25%含EDTA胰酶消化液購自上海源培公司;棕櫚酸購自美國Sigma公司(批號:P0500);達格列凈購自南京百鑫德諾生物科技公司(批號:BMS512148);CCK-8細胞活力檢測試劑盒購自武漢伊萊瑞特生物科技公司;Hoechst 33258染色細胞凋亡試劑盒購自上海貝博公司;JC-1染色線粒體膜電位檢測試劑盒、DCHF-DA細胞活性氧(reactive oxygen species,ROS)檢測試劑盒、細胞線粒體分離試劑盒購自上海碧云天生物技術有限公司;超氧化物歧化酶(superoxide dismutase,SOD)、丙二醛(malonaldehyde,MDA)檢測試劑盒購自南京建成生物公司;β-actin購自美國Engibody公司、caspase3、Cleaved caspase3、Cytochrome C抗體購自英國Abcam公司。
1.2 方法
1.2.1細胞培養與分組 將HK-2細胞置于含10%胎牛血清的DMEM/F12培養液中,同時加1%青-鏈霉素,在37 ℃、5% CO2飽和濕度的恒溫培養箱中,細胞呈貼壁生長,當細胞生長密度達70%~80%時傳代。選取生長狀態良好處于對數生長期的細胞進行隨機分組:正常對照(CON)組,含10%胎牛血清的DMEM/F12培養液對HK-2細胞進行培養;棕櫚酸(PA)組,使用棕櫚酸濃度為150 μmol/L的培養液培養HK-2細胞[5];棕櫚酸+達格列凈(PA+Dapa)組,使用棕櫚酸濃度為150 μmol/L和達格列凈濃度為2 μmol/L的培養液進行HK-2細胞培養;達格列凈(Dapa)組,使用含2 μmol/L達格列凈的培養液對HK-2細胞培養[6]。
1.2.2CCK-8實驗檢測細胞增殖力 在96孔板中接種細胞懸液(100 μl/孔),每孔約3 000個細胞進行培養,待細胞培養生長至接近單層時,給與相應的刺激,處理結束后每孔加入100 μl含有10% CCK-8的工作液,在37 ℃、5% CO2培養箱中避光孵育1 h,用酶標儀測定在450 nm處的吸光值。
1.2.3細胞內活性氧的檢測 HK-2細胞呈對數生長時,將細胞懸液滴加到6孔板中,放置于細胞培養箱中培養至細胞接近長成單層并給與相應刺激,使用預冷的PBS洗滌細胞3次,用無血清的DMEM/F12培養基稀釋DCFH-DA熒光染料至終濃度為10 μmol/L,將染料加入6孔板中,每孔1 ml,均勻覆蓋細胞表面,將6孔板放置于37 ℃、5% CO2的培養箱中避光孵育30 min,棄去染料,用無血清的DMEM/F12培養基洗滌細胞3次,然后在熒光顯微鏡下采集圖像。
1.2.4細胞線粒體膜電位的檢測 將HK-2細胞接種于6孔板中培養,給與相應刺激后,吸出6孔板中的培養液,使用PBS沖洗1次,加入1 ml細胞培養液和1 ml JC-1染色工作液,充分混勻后放置于細胞培養箱里避光孵育20 min,使用JC-1染色緩沖液(1×)洗滌2次,使用熒光顯微鏡采集圖像。
1.2.5Hoechst33258檢測細胞凋亡 將細胞玻片放置于12孔板中,將對數生長期的HK-2細胞以1×105個/孔的細胞密度接種于12孔板,給予相應藥物干預后,按照Hoechst33258染色試劑盒說明書進行細胞凋亡的檢測,最后使用熒光顯微鏡采集圖像。
1.2.6細胞氧化應激指標的檢測 HK-2細胞使用藥物干預后,在6孔板中加入100 μl /孔的裂解液冰上裂解30 min,然后收集樣品于EP管中,使用BCA蛋白濃度檢測試劑盒測量樣品的蛋白濃度用于計算,根據說明書檢測細胞內SOD、MDA含量。
1.2.7Western Blot法檢測細胞凋亡蛋白 細胞及線粒體成分中加入適量的裂解液,冰上裂解30 min,4 ℃、13 200 r/min離心30 min,取上清用BCA蛋白定量檢測試劑盒測量相應蛋白濃度。根據蛋白濃度加入適量的蛋白樣品(約30 μg/泳道)于SDS-PAGE進行電泳,將蛋白轉膜至PVDF膜上,使用5%脫脂奶粉室溫慢搖封閉2 h,封閉結束后放置于提前使用一抗稀釋液稀釋的一抗中,4 ℃孵育過夜,次日使用TBST液快搖洗滌10 min×3次,二抗孵育1 h后再用TBST快搖洗滌10 min×3次,用ECL化學發光試劑盒顯影,所有實驗重復3次,并使用Image J軟件對條帶進行灰度值分析。
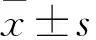
2 結果
2.1 達格列凈對棕櫚酸誘導的HK-2細胞的增殖力的影響CCK-8實驗結果顯示:四組間細胞活力水平比較差異有統計學意義(F=22.87,P<0.01);與CON組比較,PA組HK-2細胞的活力下降(P<0.05),而Dapa組細胞活力差異無統計學意義(P>0.05);與PA組比較,PA+Dapa組細胞活力增強,差異有統計學意義(P<0.05)。見圖1。
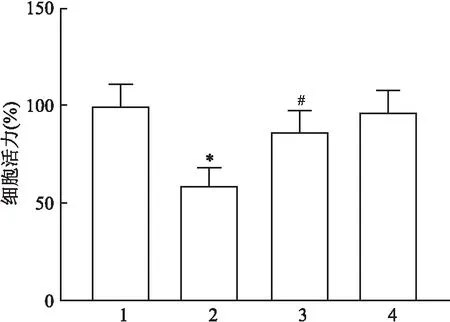
圖1 各組HK-2細胞增殖力的情況
2.2 達格列凈對棕櫚酸誘導的HK-2細胞內ROS表達的影響DCF免疫熒光結果顯示:四組間ROS水平差異有統計學意義(F=405.4,P<0.01);與CON組比較,PA組綠色熒光增強,提示ROS水平增強,差異有統計學意義(P<0.05),而Dapa組HK-2細胞綠色熒光強度差異無統計學意義(P>0.05);與PA組比較,PA+Dapa組HK-2細胞綠色熒光強度減弱,提示ROS水平降低(P<0.05)。見圖2。
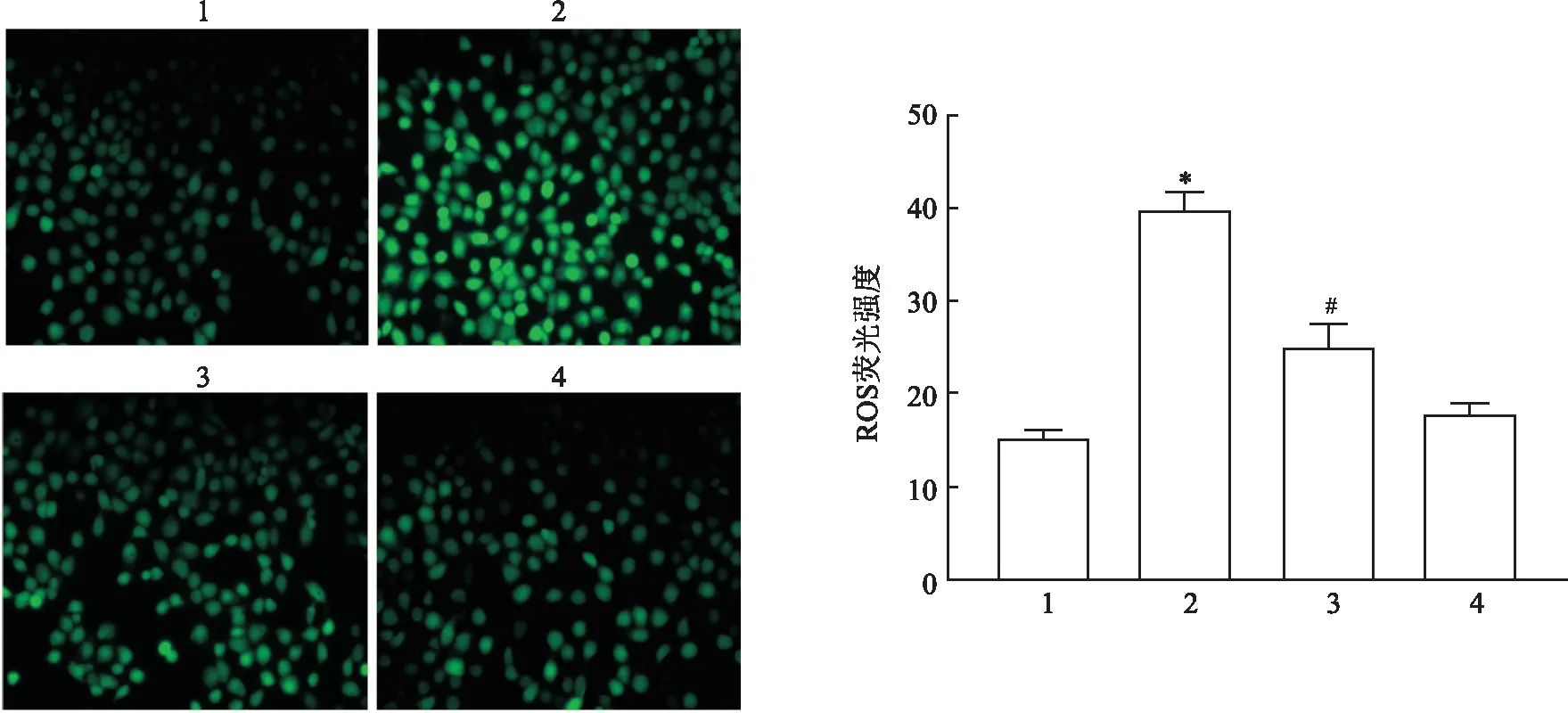
圖2 各組HK-2細胞內ROS水平的情況 ×200
2.3 達格列凈對棕櫚酸誘導的HK-2細胞線粒體膜電位的影響JC-1熒光染色結果顯示:四組間線粒體膜電位水平比較差異有統計學意義(F=16.05,P<0.01);與CON組比較,PA組紅色熒光強度與綠色熒光強度的比值降低(P<0.05),提示線粒體膜電位降低,而Dapa組紅色熒光強度與綠色熒光強度比值差異無統計學意義(P>0.05);與PA組比較,PA+Dapa組紅色熒光強度與綠色熒光強度的比值升高(P<0.05),提示膜電位水平升高。見圖3。
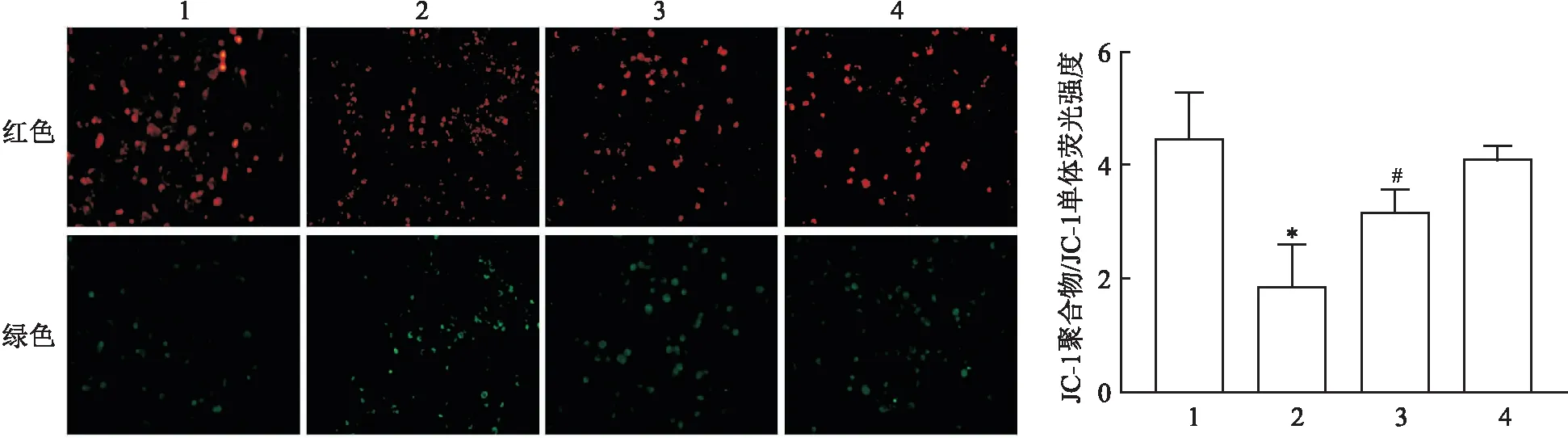
圖3 各組HK-2細胞內線粒體膜電位的變化 ×200
2.4 HK-2細胞氧化應激指標的變化SOD、MDA檢測試劑盒檢測結果顯示:四組間SOD、MDA水平比較差異均有統計學意義(F=41.0、26.02,均P<0.01);與CON組SOD、MDA水平比較[(154.40±6.43) U/mgprot、(0.63±0.13) nmol/mgprot],PA組細胞內SOD水平(109.97±3.37) U/mgprot降低,MDA水平(2.01±0.31) nmol/mgprot升高,差異有統計學意義(P<0.05),而Dapa組SOD及MDA水平[(141.75±5.08) U/mgprot、(0.93±0.15) nmol/mgprot]差異無統計學意義(P>0.05);與PA組比較,PA+Dapa組SOD水平(125.32±5.58) U/mgprot上升,MDA水平(1.33±0.17) nmol/mgprot下降,差異有統計學意義(P<0.05)。見圖4。
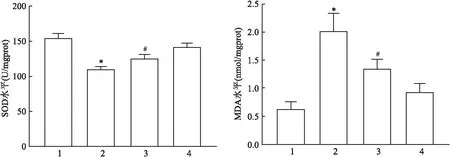
圖4 各組HK-2細胞內SOD、MDA水平變化
2.5 HK-2細胞內凋亡水平的變化Hoechast33258凋亡染色結果顯示:四組間凋亡水平比較差異有統計學意義(F=244.0,P<0.01);與CON組比較,PA組凋亡染色熒光強度增加,細胞凋亡水平增加,差異有統計學意義(P<0.05);與PA組比較,PA+Dapa組凋亡染色熒光強度降低,細胞凋亡水平下降,差異有統計學意義(P<0.05)。見圖5。
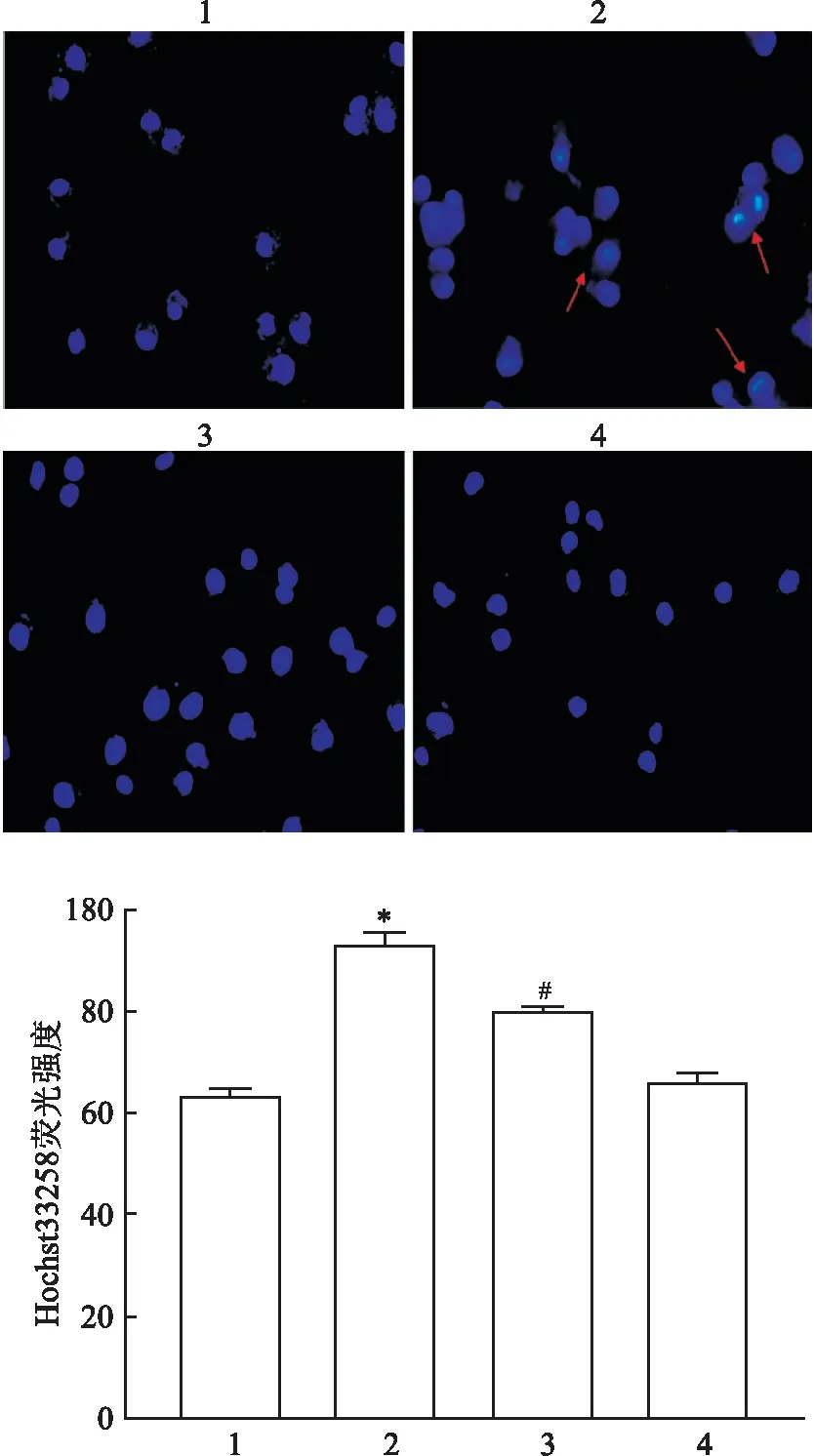
圖5 各組HK-2細胞內細胞凋亡水平的變化 ×200
2.6 HK-2細胞內凋亡蛋白和Cyto C蛋白的變化Western Blot結果顯示:四組間caspase3、Cleaved caspase3、Cyto C蛋白水平比較差異有統計學意義(F=78.51、179.8、132.3,均P<0.01);與CON組比較,PA組凋亡蛋白caspase3、Cleaved caspase3水平上升,胞漿Cyto C蛋白表達量升高,差異有統計學意義(P<0.05);與PA組比較,PA+Dapa組caspase3、Cleaved caspase3及Cyto C水平下降,差異有統計學意義(P<0.05)。見圖6。
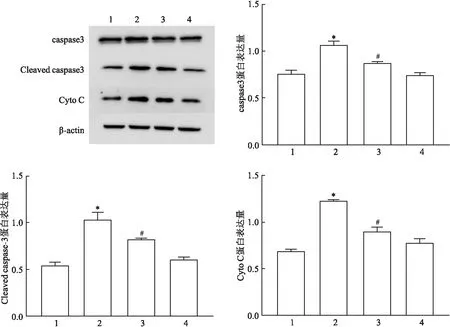
圖6 各組HK-2細胞內凋亡蛋白、Cyto C蛋白表達量情況
3 討論
DKD是慢性高血糖所致的慢性腎臟損害,臨床上以持續白蛋白尿和腎小球濾過率進行性下降為主要特征,進而發展為終末期腎病。DKD的治療主要包括控制體質量、血壓和血糖等,以延緩終末期腎病的發展。達格列凈是屬于SGLT2抑制劑的新型降糖藥物,SGLT在體內以主動轉運的形式逆濃度梯度轉運葡萄糖,參與腎臟對葡萄糖的重吸收。SGLT2表達于腎臟近曲小管,具有低親和力、高轉運能力,在腎臟重吸收約90%的葡萄糖。研究[7]表明,SGLT2抑制劑每天增加尿葡萄糖排泄約70~80 g,降低HbA1c約0.5%~0.8%。臨床研究[7]結果顯示,達格列凈治療降低了白蛋白尿,并且其降低白蛋白尿的作用很大程度上與血糖、血壓及體質量的降低無關,這表明達格列凈具有降糖之外的腎臟保護作用。另一項隨機交叉實驗的事后分析發現達格列凈降低了白蛋白尿,并且使腎小管損傷標志物Kim和炎癥因子IL-6排泄減少,達格列凈降低蛋白尿的作用可能是由于腎小球內壓力或腎小管細胞損傷減少所致[8]。本研究使用棕櫚酸刺激體外培養的HK-2細胞,結果示棕櫚酸可導致體外培養的HK-2細胞增殖力降低,檢測凋亡水平增加,達格列凈干預后細胞凋亡明顯改善,提示達格列凈可改善棕櫚酸誘導的HK-2細胞增殖力,降低細胞凋亡。
糖脂代謝異常是糖尿病最主要的疾病特征,近年來研究[9-10]認為2型糖尿病的發病機制與脂肪酸代謝紊亂導致的機體胰島素抵抗、胰島素分泌異常、糖代謝受損關系密切,游離脂肪酸升高被認為是誘發2型糖尿病的重要原因。同時,異位脂質(脂質在非脂肪組織中的積累)與系膜細胞、足細胞和近端腎小管上皮細胞的結構和功能變化有關,是導致腎臟損害的重要原因[11]。目前DKD的發病機制尚不完全清楚,可能與高血糖、微循環障礙、糖代謝異常、脂代謝異常及氧化應激有關。近來研究[12]表明,DKD的發生可能與線粒體功能障礙有關。而氧化磷酸化系統在線粒體內膜上發生,若內膜一旦被破壞,磷酸化解偶聯和電子傳遞系統完全失去運作平衡,導致氧化應激的發生;同時,發生氧化應激時,可引起線粒體功能損傷加重。實驗研究[13]發現高糖使得體外培養的HK-2細胞線粒體斷裂,線粒體膜電位降低,同時伴有線粒體蛋白Drp1和Fis1的表達增加,融合蛋白Mfn2表達降低。以上研究提示,在糖尿病模型中存在線粒體功能障礙。本研究通過體外培養人腎小管上皮HK-2細胞,使用棕櫚酸處理后結果顯示HK-2細胞凋亡增加,表現為線粒體膜電位下降,產生過量的ROS導致氧化應激的發生;同時胞漿Cyto C蛋白表達量增加,提示線粒體損傷膜通透性增加,從而使Cyto C從線粒體釋放至胞漿,激活caspase引起凋亡。
達格列凈對腎臟保護作用的潛在機制可能是多方面的。有研究[14]報道,使用達格列凈干預胰島素抵抗的代謝綜合征大鼠模型后,大鼠心肌細胞線粒體膜電位升高、ROS減少及Ca2+穩態得到良好控制,提示達格列凈通過改善線粒體功能及氧化應激對代謝綜合征大鼠的心臟進行保護作用。另一項體外研究[15]表明,達格列凈可以降低高葡萄糖所致的腎小管上皮細胞內ROS、IL-8、TGF-β水平及對高葡萄糖觸發的細胞凋亡發揮保護作用,提示達格列凈可改善腎小管氧化應激、炎癥和纖維化。Takagi et al[5]研究發現,在高脂喂養的小鼠中,近端腎小管出現空泡化、擴張和上皮細胞脫離,同時體外培養HK-2細胞,在高糖和棕櫚酸刺激下表現為線粒體明顯損傷,使用伊格列凈改善了上述癥狀。本研究結果同樣顯示,達格列凈可以提高棕櫚酸誘導的HK-2細胞線粒體膜電位,降低ROS水平及氧化應激水平,使HK-2細胞內凋亡蛋白水平降低,對棕櫚酸干預的HK-2細胞具有保護作用。
綜上所述,達格列凈使棕櫚酸干預的HK-2細胞線粒體功能及氧化應激水平得到改善,提示達格列凈可能通過改善線粒體功能障礙及氧化應激水平對DKD進行保護作用。

