早期自然流產胚胎染色體異常的危險因素分析
張哲慧,薛吟霜,何英明,向卉芬,曹云霞
自然流產(spontaneous abortion,SA)是指孕周在28周內,胎兒體質量不超過 1 kg而妊娠終止,在所有臨床妊娠中約占15%~20%[1-2]。孕周小于12周的SA稱為早期SA。早期SA的病因較為復雜,免疫學因素、易栓因素、女性生殖道解剖異常以及內分泌異常是最重要的4種母體病因。胚胎染色體異常在早期SA病因中較為常見,約占50%~60%[3]。對于夫妻雙方染色體正常情況下發生的胚胎染色體異常,國際上尚無較為詳盡的危險因素分析。該研究通過回顧性分析胚胎染色體異常的早期SA患者的臨床資料、生化指標及分布特征,探討其與胚胎染色體異常的關系,為臨床診治提供參考。
1 材料與方法
1.1 一般資料選擇2019年12月—2021年3月于安徽醫科大學第一附屬醫院生殖中心門診就診的315例早期SA并接受絨毛組織染色體檢測的患者。納入標準:① 年齡20~42歲;② 被診斷為超聲和組織學檢查支持的臨床意義上的SA。排除標準:① 男方和(或)女方染色體異常;② 供精和(或)供卵助孕等情況。
1.2 方法
1.2.1胚胎染色體檢測 將新鮮絨毛組織用大量等滲氯化鈉溶液沖洗3~5次,去除血液等雜質后,用組織剪剪取少量絨毛組織并浸泡入等滲氯化鈉溶液中。染色體微陣列分析(chromosomal microarray analysis,CMA)檢測采用染色體微陣列optima芯片,使用美國Affymetrix Genechip生物芯片檢測系統。
1.2.2分組 根據胚胎染色體檢測結果將315例早期SA患者分為正常組(150例)與異常組(165例)。
1.2.3臨床資料收集 采用統一調查表對兩組患者進行問卷調查,內容包括:① 基礎信息:雙方年齡、聯系電話、籍貫、女方民族、文化程度、職業;② 生活史與既往史:家族近親結婚史、女方吸煙飲酒情況、飲用咖啡因飲料情況、污染及輻射接觸史、既往疾病史、手術史、過敏史等;③ 月經及生育史。
1.2.4體質量指數(body mass index,BMI)及生化指標檢測 兩組患者空腹禁食超過8 h后測量身高、體質量,計算BMI=體重/身高2(kg/m2)。同時,全部患者均需空腹抽取肘靜脈血10 ml,測定血清各項生化指標,包括促甲狀腺激素(thyroid stimulating hormone,TSH)、25羥維生素D[25-hydroxyvitamin D,25-(OH)D]、抗核抗體(antinuclear antibody,ANA)、抗心磷脂抗體(anticardiolipin antibody,ACA)、甲狀腺過氧化物酶抗體(thyroid peroxidase antibody,TPOAb)、甲狀腺球蛋白抗體(thyroglobulin antibody,TgAb)、空腹胰島素(fasting insulin,FINS)、促卵泡激素(follicle stimulating hormone,FSH)、黃體生成素(luteinizing hormone,LH)、同型半胱氨酸(homocysteine,HCY)等。25-(OH)D采用化學發光免疫法檢測,使用LIAISON XL-2210全自動化學發光免疫分析儀;TSH、TgAb、TPOAb、FINS采用化學發光免疫法檢測,使用羅氏Cobas 601型電化學發光免疫儀器;ANA采用間接免疫熒光法,使用Sprinter XL型全自動間接免疫熒光操作/酶聯免疫一體機;ACA采用化學發光免疫法,使用Werfen 3710-0344型全自動化學發光免疫分析儀;FPG采用氧化酶法,采用羅氏Cobas701型全自動生化儀及配套試劑;HCY采用循環酶法,使用貝克曼AU5800型全自動生化分析儀。性激素于月經周期第2~4天測定,采用化學發光免疫法檢測,使用美國Beckman公司化學發光免疫儀器。
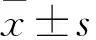
2 結果
2.1 早期SA患者異常胚胎染色體的分布早期SA的胚胎染色體異常率為52.38%(165/315)。在165例異常的胚胎染色體中,非整倍體、多倍體及染色體結構異常分別占71.52%(118/165)、8.48%(14/165)、20.00%(33/165)。在非整倍體中,X染色體單體占13.56%(16/118),常染色體三體占82.20%(97/118),其中16號染色體三體占比最高30.51%(36/118)。見圖1。

圖1 早期自然流產患者胚胎染色體異常結果分布
2.2 兩組基礎資料的比較異常組與正常組的女方民族、文化程度、職業以及男方年齡分布情況,差異無統計學意義(P>0.05) ;異常組女方年齡(30.87±4.46)歲高于正常組(29.75±3.72)歲,差異有統計學意義(P<0.05);高齡組(≥35歲)胚胎染色體異常率(66.67%)高于非高齡組(<35歲,49.62%),差異有統計學意義(P<0.05)。見表1。

表1 兩組患者基礎資料的比較(例)
2.3 兩組生活史與既往史的比較比較兩組患者的近親結婚情況、半年內吸煙飲酒飲用咖啡因飲料史、半年內污染輻射接觸史,差異無統計學差異(P>0.05)。比較兩組既往病史、手術史、過敏史、長期用藥史,差異無統計學差異(P>0.05)。見表2。

表2 兩組患者生活史與既往史的比較(例)
2.4 兩組患者月經史與生育史的比較通過統計比較發現,兩組患者的月經初潮年齡、藥物控制月經情況、既往孕次、不良妊娠史、計劃外流產史、異位妊娠史、活產史差異無統計學意義(P>0.05);此次妊娠使用輔助生殖技術(assisted reproductive technique,ART)助孕的患者,胚胎染色體異常率低于自然妊娠患者,差異有統計學意義(P<0.05)。見表3。

表3 兩組患者月經史與生育史的比較(例)
2.5 兩組生化指標的比較統計結果發現,兩組BMI、TgAb、TPOAb、ANA、ACA、FPG、FINS、HCY、FSH/LH差異無統計學意義(P>0.05);異常組患者血清25-(OH)D含量(15.95±7.52 )μg/L低于正常組(17.93±7.87) μg/L,差異有統計學意義(P<0.05);早期SA患者維生素D缺乏率為70.79%,異常組維生素D缺乏率為75.15%,正常組為66.00%;維生素D嚴重缺乏[25-(OH)D<10 μg/L]患者胚胎染色體異常率高于維生素D輕度缺乏[10 μg/L≤25-(OH)D<20 μg/L]患者,維生素D輕度缺乏患者胚胎染色體異常率高于維生素D充足[25-(OH)D≥20 μg/L]患者,差異有統計學意義(P<0.05);異常組患者血清TSH含量高于正常組,差異有統計學意義(P<0.05)。見表4、5。
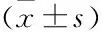
表4 兩組患者生化指標的比較

表5 兩組患者生化指標的比較(例)
2.6 胚胎染色體異常的多因素Logistic回歸分析在上述單因素分析的基礎上,對兩組間差異有統計學意義的指標進行多因素Logistic回歸分析,結果表明,高齡以及低血清25-(OH)D水平是胚胎染色體異常的獨立危險因素(P<0.05)。見表6。

表6 胚胎染色體異常危險因素Logistic回歸分析
3 討論
目前,SA已是一個較為常見的生殖健康問題,其病因中胚胎染色體異常較為常見。因此,對早期SA患者進行胚胎染色體檢測對病因診斷以及下一次妊娠有一定的指導意義。本研究在分析早期SA患者的臨床資料、生化指標水平及其分布特征的基礎上,發現女性高齡以及低血清25-(OH)D水平是胚胎染色體異常的獨立危險因素。
有研究[4-5]分析常染色體三體在異常染色體中最為常見,約占60%,其中16號染色體三體作為致死性三體占異常染色體的20.00%。本次研究對象均為染色體正常的早期SA夫妻,胚胎染色體異常率為52.38%(165/315),常染色體三體占58.79%(97/165),其中16號染色體三體在異常染色體中占21.82%(36/165),這與相關研究一致[4-5]。胚胎染色體異常的原因包括生殖細胞減數分裂錯誤與受精卵細胞早期發育中有絲分裂錯誤,其中多數常染色體三體來源于母源減數分裂錯誤,大部分16號染色體三體都起源于卵子減數分裂Ⅰ[6]。在本研究中,女方年齡<35歲胚胎染色體異常率為49.62%,而年齡≥35歲的女方胚胎染色體異常率高達66.67%。隨著女性年齡的增長,其生殖能力發生變化。在35歲后女性卵巢儲備功能與卵子質量逐漸下降,卵母細胞的染色體非整倍體率明顯上升,這可能與高齡女性卵母細胞端粒縮短、紡錘體老化導致減數分裂錯誤率提高有關[7]。女方年齡雖是至今唯一被證實與胚胎染色體異常相關的因素,但并非所有的染色體異常均與女方高齡相關。一項回顧性研究[8]發現,16號染色體三體與X單體的發生率在高齡組與非高齡組中并無統計學差異,這也從一定程度上證明了女方年齡并非唯一導致胚胎染色體異常的危險因素。
目前我國育齡期女性維生素D缺乏的現象較為普遍,且尚無維生素D分類的統一標準。在本研究中,維生素D缺乏的參考值采用美國醫學研究院(IOM)推薦[9-10],即25-(OH)D < 20 μg/L。在早期SA的患者中維生素D缺乏率高達70.79%。胚胎染色體異常組的維生素D缺乏率(75.15%)高于正常組(66.00%),同時異常組中血清25-(OH)D水平低于正常組。維生素D作為人體必需的維生素,除了維持人體的鈣磷平衡,調節細胞增殖、免疫、肌肉功能、皮膚分化、血管以及代謝水平,還參與生殖系統中多種功能的調節。在女性生殖系統中,維生素D受體存在于下丘腦、垂體、卵巢、子宮內膜、輸卵管上皮、胎盤等組織,維生素D缺乏與不孕、子宮內膜異位癥、多囊卵巢綜合征、SA、先兆子癇以及妊娠期糖尿病有關[11]。本研究首次發現低血清25-(OH)D是導致胚胎染色體異常的獨立危險因素,但目前母體血清維生素D在胚胎染色體中的風險機制尚不明確。Malloy et al[12]發現抗苗勒氏管激素(anti-mullerian hormone,AMH)的啟動子包含一個功能性維生素D應答元件,維生素D通過這個應答元件直接上調AMH基因表達。AMH作為卵巢儲備功能的預測指標,在卵泡發育與周期募集中起調節作用。維生素D缺乏可能通過下調AMH的表達來影響卵子質量,從而導致胚胎染色體異常。目前仍缺少維生素D影響胚胎染色體的直接證據,本次研究對象均來自就診于安徽醫科大學第一附屬生殖中心的早期SA患者,納入樣本量較少,可能對結果造成偏倚,后期需擴大樣本量并深入基礎研究。
此外,在本研究中還發現異常組與正常組在妊娠方式和TSH水平上差異有統計學意義。自然妊娠患者胚胎染色體異常率(56.33%)高于ART助孕患者(41.86%),差異有統計學意義。方有燕 等[4]研究發現,自然妊娠組絨毛染色體異常發生率顯著高于ART組(52.85%vs40.68%,P=0.033),而在郭楠 等[13]的研究中自然妊娠組的胚胎染色體異常率(43.75%)低于ART組(59.26%),差異無統計學意義。本研究與前者相符,在一定程度上說明ART可能并不增加胚胎染色體異常的風險。此外,本研究發現胚胎染色體異常組的TSH水平高于正常組[(2.75±2.13)mIU/Lvs(2.33±1.27) mIU/L,P=0.048],差異有統計學意義。亞臨床甲狀腺功能減退(subclinical hypothyroidism,SCH)在育齡期女性中發病率約為0.5%~5.0%,臨床上針對復發性流產患者,常將TSH>2.5 mIU/L作為篩選標準。SCH可導致月經紊亂、不孕、流產及妊娠并發癥等生殖系統疾病[14],可能影響顆粒細胞的生存率、類固醇的生成和卵母細胞的成熟[15],但目前尚無有價值的研究支持TSH對胚胎染色體有直接作用。
綜上所述,女方高齡以及維生素D缺乏是胚胎染色體異常的獨立危險因素。因此,對既往有早期SA史尤其是有胚胎染色體異常史的患者建議進行常規血清25-(OH)D的篩查,并積極診斷及治療。這對防止下次妊娠再次出現胚胎染色體異常可能有積極意義。

