采用細胞毒性試驗對23個藥用包裝材料進行生物安全性評價
黃雅理,孫會敏,林 飛,趙 霞,*,湯 龍,*
(1.中國食品藥品檢定研究院,北京 100050;2.海關總署國際檢驗檢疫標準與技術法規研究中心,北京 100013)
藥用包裝材料包括注射劑、輸液劑、儲血、輸血材料及其在體內長期滯留的設備或替代品的包裝等,由于藥用包裝材料絕大部分是不溶物質,可能對人體安全性危害的風險較大。其體外細胞毒性試驗如何設計,目前尚無明確的技術規范或國家標準。目前,藥用包裝材料的生物學評價多根據《國家藥包材標準》第7部分方法類藥包材標準[1]進行。但該標準只頒布了包括細胞毒性檢查法等7個生物學試驗項目,并未規定受試物前處理的詳細方法,檢測單位多參考《GB/T 16886.12-2017醫療器械生物學評價》第12部分樣品制備與參照樣品[2]的要求進行,但可變條件多、針對性不強、檢測樣品不能最大限度的進行加嚴和加速浸提,其毒理學風險性評估受到限制。
本研究參考多個國家標準(規范)對受試物前處理的要求[3-5],針對醫療器械和包裝材料的特殊性,選擇用于注射、體內滯留等對人體風險性較高的23個包裝材料,用MEM培養液和水(氯化鈉注射液和超純去離子水)兩種前處理方法,制備檢測樣品浸提液作為溶劑,配制加胎牛血清的完全培養液,經與培養細胞接觸之后,確認各檢測樣品浸提液是否能引起細胞毒性反應。
1 材料與方法
1.1 材 料
1.1.1 檢測樣品藥用包裝材料來自16個企業共23個樣品,詳見表1。將圓粒樣品和橡膠樣品剪切成≤25 mm×10 mm×5 mm;薄膜樣品裁剪成25 mm×5 mm;如樣品規格≤上述體積,不做剪切。用常溫去離子水在2號標準篩中清洗2遍,置50℃恒溫干燥箱中烘干備用。
1.1.2 培養基MEM干粉培養基,每袋93.9 g,購于美國Gibco公司。
1.1.3 浸提介質氯化鈉注射液,由石家莊四藥股份有限公司生產;自制超純去離子水和MEM培養液。
1.1.4 對照品細胞毒性陰性對照品為高密度聚乙烯膜(面積25 mm×5 mm),由中國食品藥品檢定研究院提供。陽性對照品為二甲基亞砜(DMSO),分析純,由天津市福晨化學試劑廠生產。
1.1.5 細胞株小鼠成纖維細胞L929,由中國科學院上海生物化學與細胞生物學研究所提供。
1.1.6 儀器及其他本研究使用的主要儀器和實驗物品包括:CO2培養箱,倒置顯微鏡,酶標儀,分度值(d)0.001 g的電子天平,超純水制備系統,pH計,滲透壓分析儀;2G砂芯抽濾漏斗,0.22μm濾膜除菌器,96孔培養板,25 mL細胞培養瓶等。
1.1.7 實驗室環境在100級潔凈度的超凈工作臺中操作。室溫20~25℃,相對濕度40%~70%。
1.2 方 法
1.2.1 細胞培養小鼠成纖維細胞L929采用含10%胎牛血清的MEM培養液(完全培養液),置于CO2培養箱中37℃條件下培養48~72 h,取生長旺盛的細胞用于當天試驗[6]。
1.2.2 檢測樣品培養基浸提液制備分別稱取5.0 g高壓滅菌后的檢測樣品,按0.2 g/mL計算浸提液體積,加入無血清MEM培養液至25 mL。經37℃振蕩浸提24 h,其浸提液用2G砂芯抽濾漏斗濾除浸提液粗沉淀物和檢測樣品后,加10%胎牛血清,經0.22 μm濾膜除菌器濾除細菌后用于試驗[2]。
1.2.3 檢測樣品水浸提液制備分別稱取5.0 g檢測樣品,按0.2 g/mL計算浸提液體積,加氯化鈉注射液或超純去離子水至25 mL。在高壓滅菌鍋中121℃(壓力0.105 MPa)下浸提1 h,其浸提液用2G砂芯抽濾漏斗濾除浸提液粗沉淀物和檢測樣品后,作為溶劑配制MEM培養基,加10%胎牛血清,經0.22μm濾膜除菌器濾除細菌后用于試驗[2,7]。
1.2.4 實驗分組空白對照組為不加任何物質的完全培養液。陰性對照組為高密度聚乙烯膜按3 cm2/mL制備的水浸提液(方法同1.2.3)。陽性對照組是在完全培養液中加入10%的DMSO。試驗組分為MEM培養基浸提液、氯化鈉注射液浸提液和超純去離子水浸提液。
1.2.5 檢測浸提液制備條件對細胞毒性反應的影響選擇2個細胞毒性反應為4級的氯化鈉注射液浸提液檢測樣品,改變浸提溫度和時間,制備121℃、20 min,121℃、30 min,121℃、1 h,70℃、24 h,50℃、72 h共5個條件下的浸提液,比較細胞毒性反應大小。
1.2.6 滲透壓和p H值的測定為了解不同條件下制備的浸提液滲透壓和PH值變化,制備121℃、20 min,121℃、30 min,121℃、1 h,70℃、24 h,50℃、72 h共5個條件下的氯化鈉注射液和超純去離子水浸提液,用滲透壓分析儀和pH計測定濃度和pH值,確定數值變化范圍[5]。
1.2.7 細胞毒性試驗用完全培養液將L929細胞配制成濃度為1×104個/mL的細胞懸液接種于4個96孔培養板,每孔接種100μL。置于CO2培養箱(CO2體積分數為5%)37℃靜置培養24 h,細胞貼壁生長后,棄除每孔中的上層液體。設空白對照、陰性對照、陽性對照、23個MEM培養基浸提液處理組和23個氯化鈉注射液浸提液處理組,每組各設6孔,每孔加入100μL完全培養液或由浸提液配制的完全培養液,置于CO2培養箱繼續靜置培養。
細胞接觸檢測樣品48 h,取出96孔培養板,于倒置顯微鏡下觀察細胞形態。每孔加入20μL質量濃度為0.5%的MTT溶液,混合均勻后,繼續培養4 h,棄除每孔中的上層液體。加入150μL DMSO,于振蕩器上振蕩10 min,用酶標儀在570和630 nm波長下測定吸光度值。
1.2.8 統計學分析用各試驗組(包括陰性對照、陽性對照)和空白對照組測出的吸光度平均值計算細胞相對增殖率(relative growth rate,RGR)不進行組間數值差異性分析。
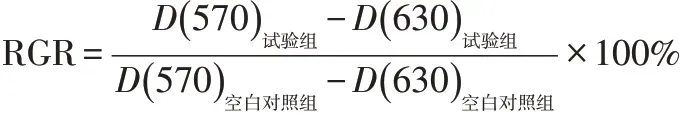
1.2.9 結果判定與評價細胞毒性反應分級標準[6]按:RGR≥100%為0級;RGR在80%(含)~100%為1級;RGR在50%(含)~80%為2級;RGR在30%(含)~50%為3級;RGR在0(含)~30%為4級。≤1級為陰性,2級為可疑陽性,≥3級為陽性。空白對照組細胞生長良好,陰性對照組的RGR>80%,陽性對照組的RGR<30%,本次試驗結果成立。如果RGR不在此范圍,則應重新進行試驗。
2 結果
2.1 3種浸提液的細胞毒性試驗結果
陰性對照組的RGR>91%,細胞毒性反應為0~1級;陽性對照組的RGR<16%,細胞毒性反應均為4級。檢測樣品MEM培養基浸提液的RGR為86%~109%,細胞毒性反應為0~1級;檢測樣品氯化鈉注射液浸提液的RGR為6%~92%,細胞毒性反應為1~4級;其中氯化鈉注射液浸提液≥2級的9個檢測樣品用超純去離子水浸提液復試其RGR為45%~105%,細胞毒性反應為1~3級。見表2。
2.2 改變浸提溫度和時間對細胞毒性試驗的影響
氯化鈉注射液浸提液細胞毒性反應為4級的2個檢測樣品,在低于121℃、30 min條件的浸提液,其RGR為72%~94%,細胞毒性反應為1~2級;而121℃、60 min浸提液RGR為15%~40%,細胞毒性反應為3~4級。見表3。

表3 氯化鈉注射液不同浸提條件對細胞毒性試驗的影響
2.3 改變浸提條件對浸提液滲透壓和p H值的影響
隨著溫度和時間的增加,浸提液的滲透壓有一定升高。在121℃、60 min條件下,氯化鈉注射液浸提液配制的培養液溶出值最高為534.00 mol/L,超純去離子水浸提液配制的培養液次之為352.33 mol/L;用兩種浸提介質配制的完全培養液其濃度相差181.67 mol/L。其滲透壓數值增加對表2試驗結果存在一定影響,而上述條件的改變對pH值影響不大,其范圍在0.25~0.37之間波動。見表4、5。

表2 3種浸提液的細胞毒性試驗結果

表4 雙向拉伸聚酯薄膜不同浸提條件對滲透壓的影響
3 討論
小鼠成纖維細胞L929的細胞毒性試驗是一種體外檢測方法,與體內試驗方法相比具有簡便、快速、重復性好、干擾少、敏感性高、可避免倫理問題等優點[7],已納入國內、外生物材料臨床前常規檢測項目,在評價生物安全性方面發揮著重要作用。
隨著現代細胞生物學與分子生物學技術的不斷發展,新材料的不斷涌現[8],用于臨床的藥用包裝材料的風險性在提高[9]。由于絕大多數藥用包裝材料不易溶解,用前處理方法制備浸提液,在相關標準中均未明確說明。實際工作中,同樣材料進行的細胞毒性試驗,由于前處理方法不得當[10],很可能出現不同的試驗結果。所用浸提介質和浸提條件應結合受試樣品的特性和臨床應用情況,在不改變材料物理和化學性能同時,在標準規定范圍,使用能溶出物質更多的高濃度、高溫度、長時間、攪拌等加嚴和加速浸提條件[2],能準確評估受試樣品的風險。

表5 雙向拉伸聚酯薄膜不同浸提條件對p H值的影響*
體外細胞毒性試驗受外界因素影響較大,樣品浸提方式及浸提介質的合理性,浸提液中浸提物質粒子大小、數量、pH值、滲透壓、無菌性、穩定性、儲存時間和溫度的變化等存在多項不確定性,建議上述理化指標經預試驗滿足基本要求[11]后,再開始進行正式試驗。
在本實驗室條件下,小鼠成纖維細胞對23個原料樣品用氯化鈉注射液作為浸提介質在121℃、60 min浸提后進行檢測,發現細胞毒性反應1級的14個;2級的6個;3級的1個;4級的2個。顯示藥品包裝材料通過體外細胞毒性試驗,能夠發現存在毒性反應的受試樣品。
用培養基浸提液作為浸提介質經37℃、24 h浸提后進行檢測,發現細胞毒性反應全部是0級和1級;50℃和70℃所制備出的浸提液雖然延長了浸提時間,但溶出物質仍然有限,對濃度、滲透壓比值、pH值等影響很小。證實該浸提條件不能最大限度的浸提出受試樣品中的物質,容易漏判可檢出陽性的醫用材料,如不是對高溫有影響的受試樣品建議不作為首選。
用超純去離子水作為浸提介質在121℃、60 min浸提后進行細胞毒性檢測,是對溶出度較高、滲透壓值增加,對試驗結果存在一定影響的補充試驗,前期需經過對濃度、滲透壓比值、pH值以及粒子數量、大小等檢測,如能符合試驗要求,其結果能排除外來因素的影響,較準確發現存在毒性反應的物質。
綜合以上結果,本實驗在不改變檢測樣品物理和化學性能同時,使用最大可溶出物質的檢測樣品浸提液作為溶劑配制MEM培養基,發現3個檢測樣品的細胞毒性反應結果陽性。因此,臨床如在高溫、高濕、高壓下滅菌使用這些樣品,須進行毒理學安全性風險評估。

