LincRNA00858靶向miR?3126?5p影響肝癌細胞的增殖、遷移和侵襲
雷林翰 鄭迪杰 吳純宸 鄭戩 謝華華 華豪 孫誠誼 喻超
貴州醫科大學臨床醫學院(貴陽 550004);貴州醫科大學附屬醫院肝膽外科,貴州醫科大學肝膽胰脾重點實驗室,貴州省肝膽胰脾疾病研究所(貴陽 550004)
肝細胞癌(hepatocellular carcinoma,HCC)是侵襲性較強的惡性腫瘤,也是臨床上最常見的肝癌類型,預計到2025年全球肝癌發病人數將超過100 萬例[1],但HCC 的治療情況并不令人滿意,究其原因主要在于發病機制尚未完全闡明,缺乏針對性的有效手段[2]。因此,深入研究HCC 病變過程的分子生物學機制及發現潛在治療靶點是攻克HCC 的當務之急。目前研究發現長鏈非編碼RNA(LncRNA)在肝癌、胰腺癌等各種癌癥中失調,這表明lncRNA可以作為新的治療靶點和潛在的生物標志物用于患者的診斷和預后[3-5]。Linc00858 長度為2 685 個核苷酸,在胃癌、結腸癌、卵巢癌、宮頸癌等惡性腫瘤中均為異常高表達。有研究[6-9]指出Linc00858 可以通過調控多種microRNA,從而影響腫瘤細胞的增殖、侵襲、轉移和凋亡,另外高表達Linc00858 還與腫瘤的臨床分期、淋巴結轉移密切相關[10]。因此Linc00858 是在腫瘤靶向治療中很有前景的候選基因,然而在HCC 中Linc00858 的研究尚少。根據生物信息學分析,本研究選擇微小RNA?3126?5p(miR?3126?5p)作為Linc00858 的調控對象,通過初步探索Linc00858通過靶向調控miR?3126?5p 參與HCC 的增殖、遷移和侵襲的分子機制,以期探索新的HCC 治療靶點。
1 材料與方法
1.1 臨床樣本及細胞系通過收集2018年9月至2020年12月貴州醫科大學附屬醫院肝膽外科共24 例經病理診斷為肝細胞肝癌的手術切除標本。所有患者在手術前均未接受任何輔助放、化療。每例標本均取得癌組織和相應的癌旁組織,所有手術標本使用液氮速凍,放置于-80 ℃冰箱保存。本研究獲得貴州醫科大學附屬醫院倫理委員會同意,患者均簽署知情同意書。人正常肝細胞LO2和人肝癌細胞HUH?7,SK?HEP?1,HEP3B,MHCC?97H 及HEPG2 細胞系均購自中國科學院上海細胞生物研究所細胞庫。
1.2 實驗材料DMEM/High Glucose 培養基、0.25%胰蛋白酶消化液(含EDTA,含酚紅)均購自武漢賽維爾生物科技有限公司;胎牛血清(Fetal Bovine Serum)購自以色列biological industries 公司;Trizol 試劑購自美國Invitrogen 公司;逆轉錄和PCR SYBRGREEN定量試劑盒均購自日本Takara生物技術有限公司,CCK?8 試劑盒購自江蘇凱基生物技術股份有限公司,Transwell 小室和Matrigel 基質膠均購自美國Corning 公司,雙熒光素酶試劑盒購自美國Promega公司;兔抗人波形蛋白(Vimentin)單克隆抗體、小鼠抗人E?鈣粘蛋白(E?cdherin)單克隆抗體、兔抗人細胞周期蛋白E1(cyclinE1)單克隆抗體、兔抗人周期素依賴性激酶2(CDK2)單克隆抗體、兔抗人抗Kip1(p27)單克隆抗體、兔抗人GAPDH 單克隆抗體均購自武漢三鷹生物工程有限公司;RIPA 裂解液、辣根過氧化物酶標記的羊抗小鼠和兔IgG(二抗)、超敏ECL化學發光即用型底物劑盒均購自武漢博士德生物工程有限公司;PVDF 膜購自美國Sigma?Aldrich 公司;攜帶Linc00858cDNA的重組慢病毒及其陰性對照慢病毒、攜帶Linc00858?shRNA 的重組慢病毒及其陰性對照慢病毒、慢病毒感染增強液HitransG A 均購自上海吉凱基因化學技術有限公司;miR?3126?5p mimics 和miR?3126?5p inhibitor 及其相應陰性對照均購自廣州瑞博生物科技有限公司。Linc00858 上游引物序列5'?TG?CAATCTGTTTAATGTGCCAGT?3',下游引物序列5'?CTGGAGCACCTCTCTAAGAACC?3';miR?3126?5p上游引物序列5'?ATGCGTGAGGGACAGATGC?3',下游引物序列5'?GTCGTATCCAGTGCAGGGTC?3';GAPDH 上游引物序列5'?GGAGCGAGATCCCTC?CAAAAT?3',下游引物序列5'?GGCTGTTGTCATA?CTTCTCATGG?3';U6 上游引物序列5'?CTCGCTTC?GGCAGCACA?3',下游引物序列5'?ACGCTTCAC?GAATTTGCGT?3'。
1.3 試驗方法
1.3.1 實時熒光定量PCR使用Trizol 法提取出總RNA。使用PrimeScriptTMRT reagent Kit(日本Takara 公司)對提取出的總RNA 進行逆轉錄以獲得cDNA;采用SYBR?Premix Ex TaqTM ⅡKit(日本Takara 公司)進行qRT?PCR 分析;分別以GAPDH 和U6 作為Linc00858 和miR?3126?5p 的內參。以2?ΔΔCt法值表示目的基因的相對表達水平。
1.3.2 細胞轉染和分組將正常肝細胞和各肝癌細胞系從液氮罐中取出,37 ℃水浴鍋復蘇,用DMEM完全培養基培養(10%FBS、1%青鏈霉素),放置于恒溫37 ℃、體積分數5%CO2的培養箱中進行培養。選取生長狀態良好的HUH?7 細胞,將其在6 孔板中進行鋪板,每孔密度為1×105個/孔,使用慢病毒感染增強液HitransG A 進行重組慢病毒感染,12~16 h 后更換新鮮培養基;分組為Empty Vector組(陰性對照組)和pcDNA?Linc00858 組;分別使用mimics?NC、miR?3126?5p mimics 與Linc00858 過表達慢病毒共轉染HUH?7 細胞,分組為pcDNA?Linc00858+miR?NC 組與pcDNA?Linc00858+miR?3126?5p mimics 組;MCHH?97H 細胞的轉染方式如上,分組為sh?NC 組(陰性對照)組和sh?Linc00858組,分別使用inhibitor?NC、miR?3126?5p inhibitor 與sh?Linc00858 共轉染MCHH?97H 細胞,分組為sh?Linc00858+anti?NC 組和sh?Linc00858+anti?miR?3126?5p 組;以上步驟均嚴格按照吉凱基因公司《重組慢病毒載體使用手冊》和銳博生物公司《miRNA 產品使用說明》進行操作,篩選出穩定表達的細胞株,并采用qRT?PCR 法檢測轉染效率。
1.3.3 CCK?8法檢測細胞增殖各組細胞按照3×103個/孔的密度接種于96 孔板中,四周每孔加入100 μL PBS 以減少蒸發,隨后放入培養箱中培養,待細胞貼壁后觀察。分別取6、24、48、72 h 共4 個時間點,每孔加入10 μL 的CCK?8 試劑后避光孵育2 h,隨后利用酶標儀在450 nm 的波長下檢測其吸光值(OD值),并繪制生長曲線。每組設置5 個復孔,且每組實驗重復3 次。
1.3.4 Transwell 法檢測細胞遷移和侵襲能力將Matrigel 膠與無血清DMEM 培養基按1∶8 的比例配比稀釋,在每個小室中加入60 μL 基質,置37 ℃30~60 min(培養箱內)使膠凝固。用200 μL 的無血清培養基將各組細胞密度調整為1×105個/孔,將其加入到侵襲小室內,每種細胞種3 個小室。下室加入含20% FBS 的完全培養基600 μL,培養24~48 h 后。棄去小室內培養基,用PBS漂洗3次。4%的多聚甲醇固定20~30 min,用0.1%結晶紫染色20~30 min,用清水洗3 次,用棉簽輕輕拭去小室的上室膜中未穿過小室的細胞,待烘箱將其烘干后,在倒置光學顯微鏡選取5 個視野拍照記錄,將各組細胞進行計數匯總,再進行統計學分析。Transwell 遷移實驗中,小室不鋪Matrigel 膠,其余步驟與前述的侵襲實驗相同。
1.3.5 雙熒光素酶報告基因檢測構建含有miR?3126?5p 結合位點的(3'UTR)雙熒光報告基因載體(廣州市銳博生物科技有限公司),即linc00858野生型(linc00858?wt)質粒、linc00858突變型(linc00858?mut)質粒。將HUH?7 細胞接種于96 孔板中,孵育至細胞密度達70%。然后,將WT·Linc00858、MUT·Linc00858 與miR?3126?5p mimics 共轉染HUH?7 細胞中。根據生產廠家的說明書,采用雙熒光素酶試劑盒(美國promega 公司)測定各組細胞的熒光素酶活性。
1.3.6 蛋白質印跡法檢測HUH?7 和MHCC?97H細胞中上皮?間質轉化(epithelial mesenchymal transition,EMT)和細胞周期相關的蛋白表達水平的影響使用胰蛋白酶將各組細胞消化處理后,使用RIPA 細胞裂解液分別提取各組細胞的總蛋白,行SDS?PAGE,在90 V 下分離處理后的蛋白樣本30 min 后再在110 V 下分離70 min,然后將分離后的蛋白轉移到PVDF 膜上,用5% 脫脂牛奶的封閉液封閉2 h,放置于針對Vimentin、E?cdherin、cyclin E1、CDK2、p27 和GAPDH 的特異性一抗(體積稀釋比例均為1∶1 000)中,于4 ℃下搖床反應過夜;隨后加入辣根過氧化物酶標記的羊抗兔/小鼠IgG(體積稀釋比例均為1∶5 000)的二抗中,室溫下搖床反應2 h,然后將超敏ECL 化學發光液(A 液:B 液為1∶1)滴加在條帶上,凝膠成像儀采集圖像,最后用ImageJ1.42 軟件進行灰度分析。
1.4 統計學方法所有實驗至少獨立重復3次,統計分析使用SPSS 22.0 軟件。正態分布的計量資料以(±s)表示,兩組間比較采用LSD?t檢驗。以P<0.05 為差異有統計學意義。
2 結果
2.1 Linc00858 在人肝癌組織和肝癌細胞系中高表達根據TCGA 數據庫的數據分析,Linc00858在肝癌組織中的表達情況明顯高于癌旁組織(P<0.05),見圖1A。qRT?PCR 結果顯示,相比癌旁正常組織,肝癌組織中Linc00858 的表達水平較高(P<0.05),見圖1B;在肝癌細胞系中的Linc00858的相對表達量也顯著高于正常肝細胞LO2(P<0.05),見圖1C;篩選出相對表達量最高的MHCC?97H 和最低的HUH?7 作為后續研究對象。

圖1 Linc00858 在肝癌組織及細胞中表達情況Fig.1 The expression of Linc00858 in hepatoma tissue and cell
2.2 Linc00858 對肝癌細胞增殖、遷移和侵襲能力的影響qRT?PCR檢測結果顯示:pcDNA?Linc00858組的Linc00858 表達水平明顯高于Empty Vector組,sh?Linc00858 組的Linc00858 表達水平明顯低于sh?NC組(P<0.05),見圖2A。與Empty Vector 組對比,pcDNA?Linc00858 組的細胞增殖、遷移和侵襲能力均顯著上升(P<0.05),見圖2B-D,同時cyclin E1、Vimentin 和CDK2 的蛋白表達水平明顯上升,而p27 和E?cadherin 的表達水平則明顯下降,差異均有統計學意義(P<0.05),見圖2E。和sh?NC 組比較顯示,sh?Linc00858 組的MHCC?97H細胞增殖、遷移和侵襲能力明顯下降(P<0.05),見圖2B、C、D;同時cyclin E1、Vimentin 和CDK2 的蛋白表達水平明顯下降,而p27 和E?cadherin 的表達水平則明顯上升,差異均有統計學意義(P<0.05),見圖2E。
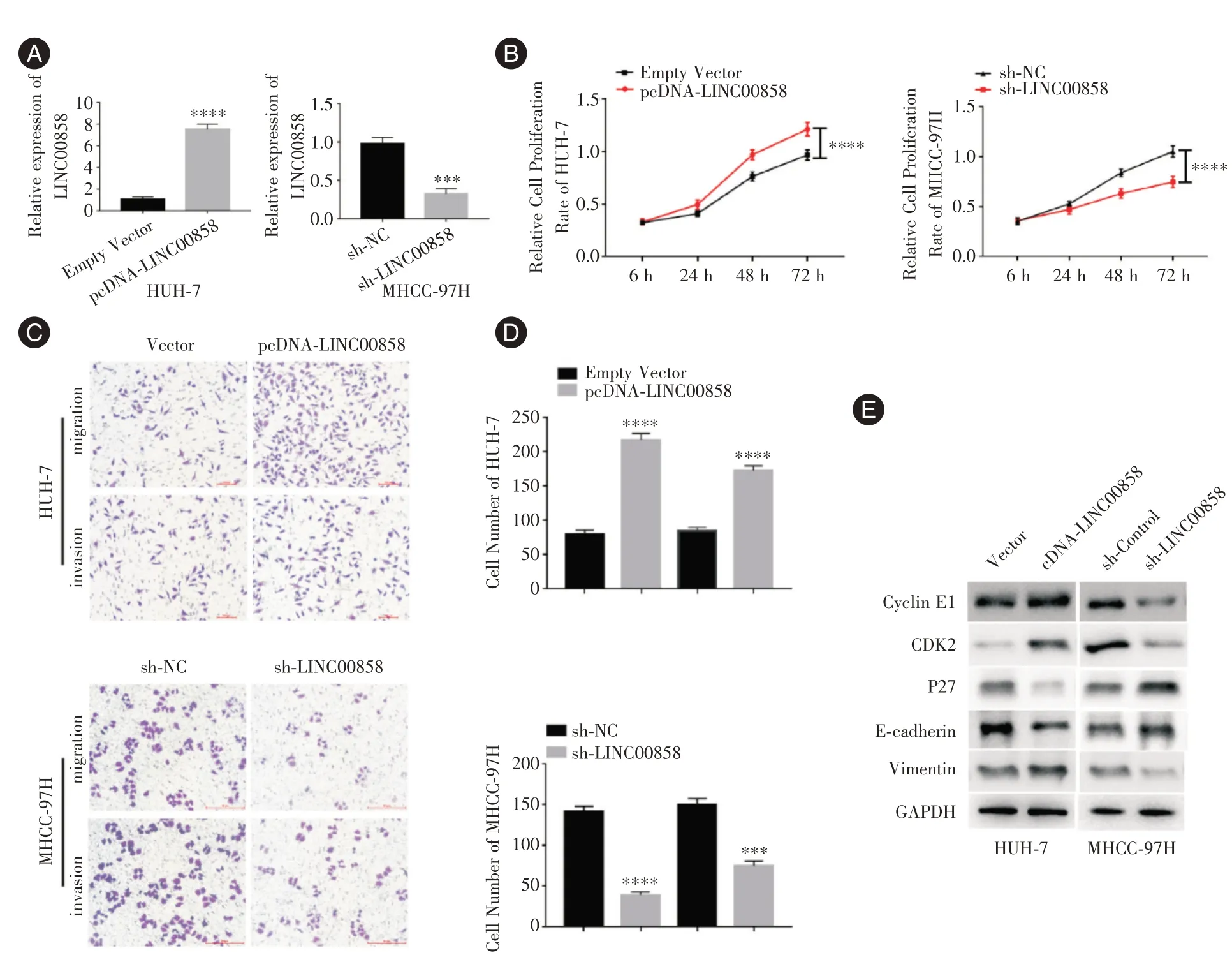
圖2 改變Linc00858 的表達后對肝癌細胞增殖、遷移、侵襲能力和相關蛋白表達情況的影響Fig.2 Effects of altered expression of Linc00858 on proliferation,migration,invasion and expression of related proteins in hepatocellular carcinoma cells
2.3 Linc00858靶向調控miR?3126?5p的表達通過starbase 網站(https://starbase.sysu.edu.cn/index.php)和LncBASE 網站(https://labworm.com/tool/diana?lncbase)發現共有10 個microRNA 可能是其潛在的下游靶基因(圖3A)。qRT?PCR 檢測結果表示,在各組的對比中,miR?3126?5p 的表達量變化差異最為顯著(圖3B)。雙熒光素酶報告實驗結果表明,miR?3126?5p mimics 能明顯降低WT?Linc00858 的熒光素酶活性(P<0.05),對MUT?Linc00858 則無明顯影響(圖3C)。qRT?PCR 檢測結果顯示,miR?3126?5p 在肝癌細胞系中的表達量也顯著低于人正常肝細胞LO2(P<0.05,圖3D);Spearman 等級相關性實驗顯示,Linc00858 的表達和miR?3126?5p 呈負相關(圖3E)。以上結果均提示Linc00858 可以負向調控miR?3126?5p 的表達。

圖3 Linc00858 負向調控miR?3126?5p 的表達Fig.3 Linc00858 negatively regulates the expression of miR?3126?5p
2.4 改變miR?3126?5p 的表達水平能夠逆轉Linc00858 對肝癌細胞增殖、遷移和侵襲能力的影響在HUH?7 細胞中,mimics?miR?3126?5p 組的miR?3126?5p 表達水平明顯高于mimics?NC 組;而在MHCC?97H 細胞中,anti?miR?3126?5p 組的miR?3126?5p 表達水平明顯低于anti?NC 組(P<0.05,圖4A)。與pcDNA?Linc00858+mimics?NC 組相比,pcDNA?Linc00858+mimics?miR?3126?5p 組在HUH?7細胞中增殖、遷移及侵襲能力減弱;蛋白質印跡法檢測結果顯示對比pcDNA?Linc00858+mimics?NC 組,pcDNA?Linc00858+mimics?miR?3126?5p 組cyclin E1、Vimentin 和CDK2 的蛋白表達水平下降,而p27 和E?cadherin 的表達水平則上升(圖4E);與sh?Linc00858+anti?NC 組相比,sh?Linc00858+anti?miR?3126?5p 組在MHCC?97H 細胞中增殖、遷移及侵襲能力增強,發生了逆轉(圖4B-D),蛋白質印跡法檢測結果顯示對比sh?Linc00858+anti?NC 組,sh?Linc00858+anti?miR?3126?5p 組的cyclin E1、Vi?mentin 和CDK2 的蛋白表達水平上升,而p27 和E?cadherin 的表達水平則下降(圖4E)。

圖4 改變miR?3126?5p 的表達水平后對Linc00858 導致的肝癌細胞增殖、遷移、侵襲能力和相關蛋白表達情況的影響Fig.4 Effects of altered miR?3126?5p expression on proliferation,migration,invasion and related protein expression of hepatoma cells induced by Linc00858
3 討論
HCC 是世界范圍內最常見的惡性腫瘤之一,是全球癌癥相關死亡率的第二大原因[11],其中發生侵襲轉移和術后復發是影響患者結局的主要原因之一[12]。目前,手術切除后化療是最常見的HCC 治療方案,但患者結局卻不盡如人意,患者生存時間未能明顯延長[13],因此探索侵襲轉移的分子機制對于HCC 的分子診斷、預防和治療具有重要意義。LncRNA 通常位于細胞的細胞核和細胞質中,盡管不參與編碼蛋白質,但許多研究表明LncRNA 在細胞發育、分化和遷移等生物學過程扮演了重要角色[14-16]。劉澤鋒等[17]發現,LncRNA DUXAP8 通過增加m6A 甲基化介導的穩定性來維持其表達上調核糖核酸。DUXAP8 水平,這與肝癌細胞增殖、遷移、侵襲和化療耐藥正相關。LncRNA有作為HCC 潛在的生物標志物和分子靶向治療靶標的可能性。
本研究發現Linc00858 在肝癌組織和細胞中的均呈高表達,并且其能促進肝癌細胞的增殖、遷移和侵襲。在抑制Linc00858 的表達后,其能通過上調p27 的表達,從而抑制CDK2?Cyclin E1 的蛋白激酶復合物,而cyclin E1和CDK2是細胞周期G1和S 期轉換的限速因子,p27 能抑制cyclin E1 與細胞周期依賴性蛋白結合并誘導細胞周期阻滯從而抑制細胞的增殖;另外在上調了Linc00858表達后,上皮樣標志物E?cadherin 的表達降低,而間質樣標志物Vimentin的表達上升,這提示Linc00858可能是通過EMT 現象增強了肝癌細胞的遷移和侵襲能力。本研究利用生物信息學數據庫分析miR?3126?5p可能是Linc00858 的潛在下游靶點,而目前研究[18]指出,在HCC 患者血清中的miR?3126?5p 的表達水平比健康人群顯著降低,并且其有可能作為HCC早期診斷的重要標記物。雙熒光素酶報告基因實驗和qRT?PCR 結果顯示miR?3126?5p 的表達水平和Linc00858 呈負相關,且Linc00858 可以靶向調控miR?3126?5p 的表達。通過改變miR?3126?5p 的表達,本研究發現Linc00858 帶來的肝癌增殖、遷移和侵襲能力發生了逆轉,此外細胞周期蛋白和EMT 相關蛋白的表達水平也發生了逆轉。即Linc00858 可通過發揮ceRNA 機制來競爭性吸附miR?3126?5p,進而誘導細胞周期蛋白和EMT 相關蛋白的表達。此外,對于Linc00858 和細胞周期與EMT 相關蛋白之間的關系,仍需要進一步研究來闡明其具體調控機制。
綜上所述,本研究表明Linc00858 可以通過miR?3126?5p 調節細胞周期蛋白和EMT 相關蛋白的表達,并促進肝癌細胞的增殖、侵襲和遷移,這表明Linc00858 有望成為肝癌治療的重要靶點。

