麻竹葉提取物的超聲輔助酸水解工藝研究
張芳,戴毅,李洪慶*,陶文亮,許子競(jìng)
(1.貴州民族大學(xué) 化學(xué)工程學(xué)院,貴陽(yáng) 550025;2.貴州工程應(yīng)用技術(shù)學(xué)院 化學(xué)工程學(xué)院,貴州 畢節(jié) 551700)
麻竹(DendrocalamuslatiflorusMunro)是禾本竹亞科牡竹屬多年生木本植物[1],主要分布于福建、四川、貴州和云南等地[2]。麻竹應(yīng)用廣泛,竹材可用于建筑、造紙和手工藝術(shù)品等[3],竹筍可食用[4],在麻竹的開(kāi)發(fā)利用過(guò)程中產(chǎn)生的大量竹葉被當(dāng)作廢棄物丟棄,不僅浪費(fèi)資源,而且污染環(huán)境。有研究發(fā)現(xiàn),麻竹葉中的黃酮類化合物具有抗氧化、消炎和抑菌等作用[5-6],竹葉黃酮類物質(zhì)作為一種功能性食品[7-8],可作為食品添加劑廣泛應(yīng)用于保鮮劑[9-10]、飼料添加劑[11-12]及調(diào)味劑[13-14]等生產(chǎn)中。因此,對(duì)麻竹葉中黃酮類化合物進(jìn)行研究具有重要理論意義。
竹葉中的黃酮類化合物主要以碳苷黃酮為主,其次為氧苷黃酮[15];碳苷黃酮的水溶性較強(qiáng),且具有較高的穩(wěn)定性,不易被酸水解,而氧苷黃酮結(jié)構(gòu)不穩(wěn)定,易被水解[16]。文獻(xiàn)調(diào)研發(fā)現(xiàn),有關(guān)酸水解竹葉黃酮類化合物的研究較少,主要有:張英等[17]發(fā)現(xiàn)毛金竹竹葉中碳苷黃酮的鍵能較強(qiáng),酸水解條件控制不當(dāng)會(huì)造成含量測(cè)定誤差;Guo等[18]運(yùn)用HPLC-光電二極管陣列檢測(cè)器(DAD)測(cè)定筠竹竹葉提取物水解液中的化合物,利用液相色譜-電噴霧離子化-質(zhì)譜法(LC-ESI-MS)分離鑒定出葒草苷(orientin)、異葒草苷(isoorientin)、牡荊苷(vitexin)和異牡荊苷(isovitexin)等碳苷黃酮。目前,國(guó)內(nèi)外對(duì)麻竹葉黃酮類化合物的超聲波輔助酸水解工藝研究未見(jiàn)報(bào)道。
本文以赤水麻竹葉的提取物為研究對(duì)象,考察超聲功率、底物濃度、鹽酸濃度、時(shí)間和溫度等因素對(duì)4種碳苷黃酮含量的影響,通過(guò)響應(yīng)面法優(yōu)化超聲波輔助酸水解工藝,為進(jìn)一步開(kāi)發(fā)麻竹葉資源提供了理論依據(jù)。
1 材料與方法
1.1 原料及儀器
1.1.1 實(shí)驗(yàn)原料
麻竹葉:由貴州赤天化紙業(yè)股份有限公司提供,經(jīng)貴州民族大學(xué)生態(tài)環(huán)境工程學(xué)院蘇春花副教授鑒定。
1.1.2 實(shí)驗(yàn)儀器

1.1.3 實(shí)驗(yàn)試劑
葒草苷、異葒草苷、牡荊苷和異牡荊苷標(biāo)準(zhǔn)品:純度>98%,成都植標(biāo)化純生物技術(shù)有限公司;鹽酸、冰醋酸和甲醇:分析純,重慶川東化工有限公司;甲醇:色譜純,安徽天地高純?nèi)軇┯邢薰荆怀兯簩?shí)驗(yàn)室自制。
1.2 實(shí)驗(yàn)方法
1.2.1 標(biāo)準(zhǔn)品溶液配制及標(biāo)準(zhǔn)曲線繪制
精密稱取適量葒草苷、異葒草苷、牡荊苷和異牡荊苷標(biāo)準(zhǔn)品,用甲醇超聲溶解,定容至25 mL容量瓶中,得到單標(biāo)對(duì)照品儲(chǔ)備液,見(jiàn)表1。
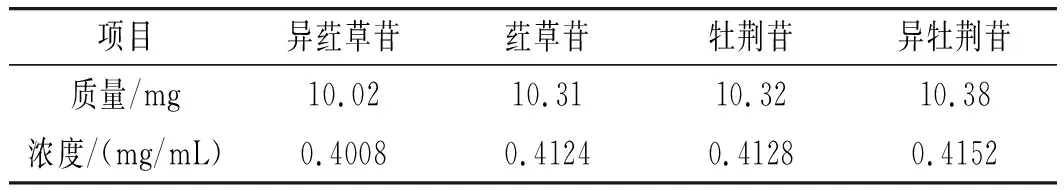
表1 4種碳苷標(biāo)準(zhǔn)品儲(chǔ)備液制備Table 1 The preparation of four C-glycoside standard sample stock solution
分別吸取單標(biāo)儲(chǔ)備液,配制成一定濃度的混合對(duì)照品標(biāo)準(zhǔn)溶液(見(jiàn)表2),繪制標(biāo)準(zhǔn)曲線。

表2 混合對(duì)照品標(biāo)準(zhǔn)溶液濃度Table 2 The concentration of standard solution of mixed reference sample μg/mL
1.2.2 麻竹葉提取物制備
準(zhǔn)確稱取過(guò)60目篩的麻竹葉粉100.0 g于2000 mL燒瓶中,加入1600 mL 80%乙醇,在70 ℃下超聲(300 W)回流提取50 min,提取3次,合并提取液,減壓濃縮,除醇,冷凍干燥,得麻竹葉提取物。
1.2.3 樣品溶液制備
精確稱取一定質(zhì)量的麻竹葉提取物于25 mL容量瓶中,加入甲醇定容,制成一定濃度的麻竹葉提取物樣品溶液。從中精密吸取0.5 mL于10 mL水解管中,加入3.5 mL甲醇稀釋,搖勻,再加入1 mL一定濃度的鹽酸,密封,搖勻,于超聲清洗儀中設(shè)置一定功率、時(shí)間和溫度進(jìn)行水解。超聲結(jié)束后,冷卻至室溫,轉(zhuǎn)移到10 mL容量瓶中,用少量甲醇沖洗水解管3次,合并沖洗液與水解液,定容,過(guò)0.22 μm濾膜,得樣品溶液。
1.2.4 高效液相色譜條件
采用Agilent TC-C18色譜柱(250 mm×4.6 mm,5 μm),流動(dòng)相為甲醇(A)-0.1%冰醋酸水溶液(B),體積流量1.00 mL/min,柱溫30 ℃,檢測(cè)波長(zhǎng)330 nm,進(jìn)樣量10 μL,梯度洗脫條件見(jiàn)表3。

表3 流動(dòng)相梯度洗脫程序Table 3 The mobile phase gradient elution program
1.2.5 單因素實(shí)驗(yàn)
分別考察超聲功率(200,250,300,350,400 W)、底物濃度(0.25,0.5,1,1.5,2 mg/mL)、鹽酸濃度(0.6,0.8,1.0,1.2,1.4 mol/L)、時(shí)間(90,120,150,180,210 min)和溫度(55,60,65,70,75 ℃)等因素對(duì)4種碳苷黃酮含量的影響。
總含量(%)=異葒草苷含量(%)+葒草苷含量(%)+牡荊苷含量(%)+異牡荊苷含量(%)。
式中:C標(biāo)為標(biāo)準(zhǔn)品混合液中某種碳苷黃酮濃度,mg/mL;S樣為樣品溶液中某種碳苷黃酮峰高,mAU;V0為稱樣后定容體積,mL;V1為取樣體積,mL;V2為取樣后定容體積,mL;S標(biāo)為標(biāo)準(zhǔn)品混合液中某種碳苷黃酮峰高,mAU;M為樣品稱樣量,mg。
1.2.6 響應(yīng)面實(shí)驗(yàn)
根據(jù)1.2.5中的單因素實(shí)驗(yàn)結(jié)果,以4種碳苷黃酮的含量為響應(yīng)值Y,以鹽酸濃度(A)、時(shí)間(B)和溫度(C)為變量,進(jìn)行響應(yīng)面實(shí)驗(yàn)設(shè)計(jì),因子編碼及水平見(jiàn)表4。
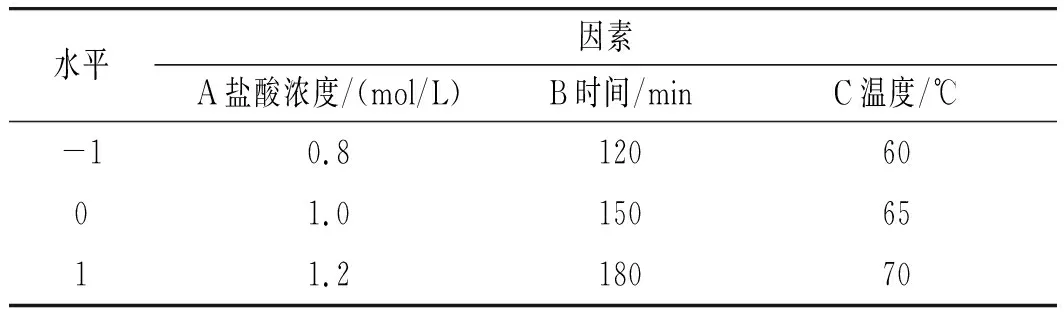
表4 三因素和三水平設(shè)計(jì)Table 4 Three-factor and three-level design
2 結(jié)果與分析
2.1 標(biāo)準(zhǔn)曲線線性關(guān)系
由圖1可知,在1.2.3液相色譜條件下,異葒草苷、葒草苷、牡荊苷和異牡荊苷的出峰時(shí)間依次為29.50,30.75,32.78,36.58 min,具有較好的分離效果。以峰面積為縱坐標(biāo)、濃度為橫坐標(biāo),繪制標(biāo)準(zhǔn)曲線,見(jiàn)圖2。

圖1 標(biāo)準(zhǔn)品色譜圖Fig.1 The chromatogram of standard sample
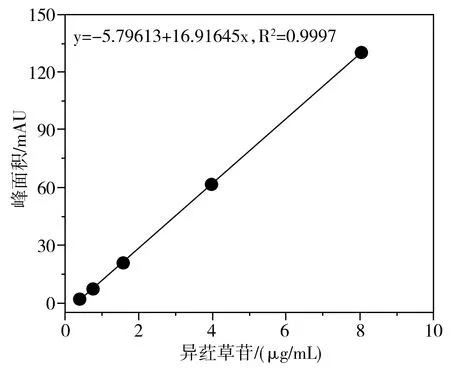
結(jié)果表明,相關(guān)系數(shù)均接近1,可在相應(yīng)的線性范圍內(nèi)分別對(duì)4種碳苷黃酮進(jìn)行定量測(cè)定。
2.2 單因素對(duì)麻竹葉提取物4種碳苷黃酮含量的影響
2.2.1 超聲功率的影響
由圖3可知,超聲功率在200~400 W范圍內(nèi),酸水解對(duì)碳苷黃酮含量的影響不明顯,但300 W時(shí)得率最高。因此,固定超聲功率為300 W。
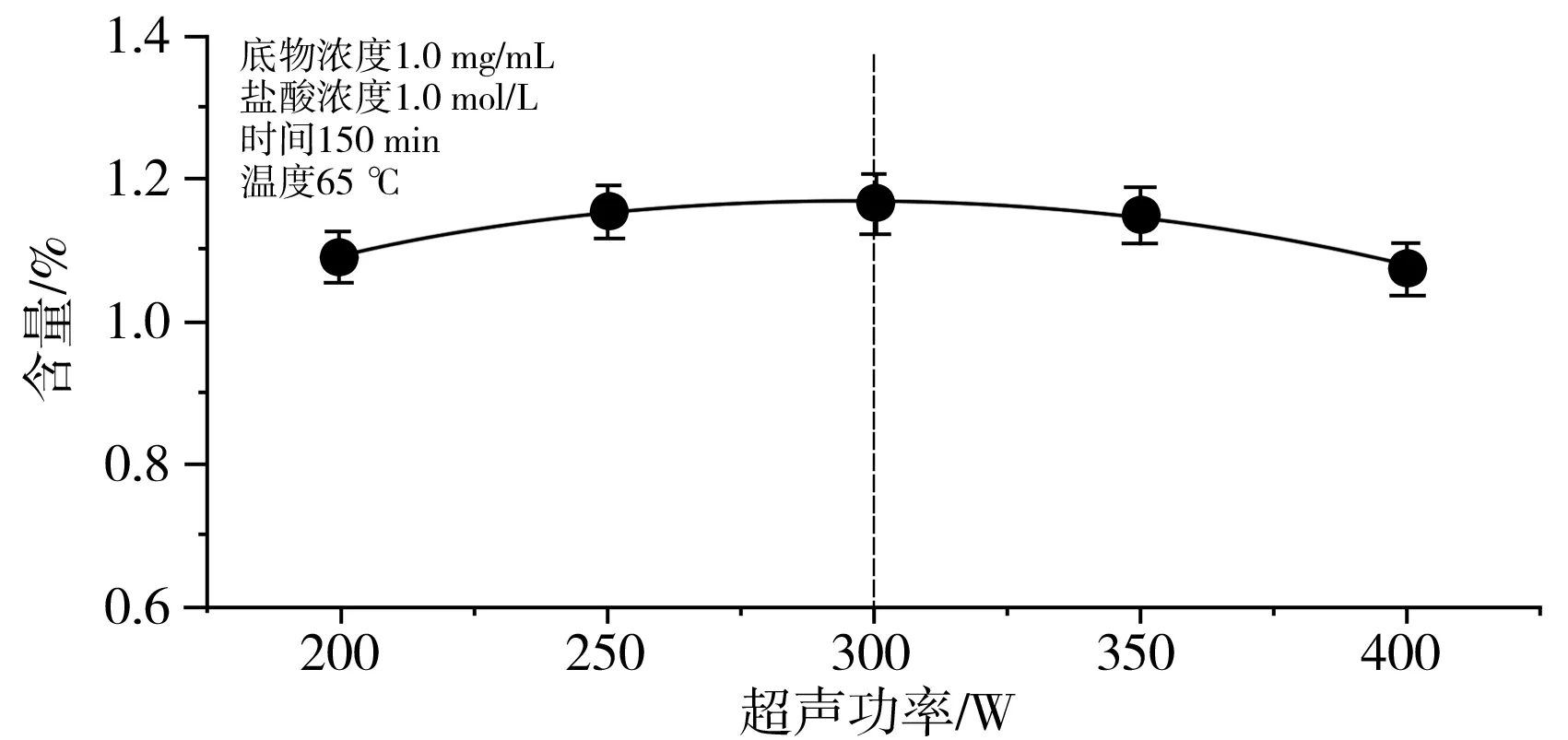
圖3 不同超聲功率的影響
2.2.2 底物濃度的影響
由圖4可知,底物濃度在0.25~2 mg/mL范圍內(nèi),酸水解對(duì)碳苷黃酮含量的影響不明顯,但1 mg/mL后得率開(kāi)始趨于平緩。因此,固定底物濃度為1 mg/mL。

圖4 不同底物濃度的影響Fig.4 The effect of different substrate concentration
2.2.3 鹽酸濃度的影響
由圖5可知,鹽酸濃度在0.6~1.0 mol/L的范圍內(nèi),增加鹽酸濃度有利于提高碳苷黃酮含量,其原因可能是在水解過(guò)程中,碳苷黃酮的衍生物轉(zhuǎn)化生成4種碳苷黃酮[19]。當(dāng)鹽酸濃度超過(guò)1.0 mol/L時(shí),碳苷黃酮含量開(kāi)始下降,其原因可能是過(guò)高的鹽酸濃度加劇了黃酮結(jié)構(gòu)的破壞。因此,鹽酸濃度選擇1.0 mol/L為宜。

圖5 不同鹽酸濃度的影響Fig.5 The effect of different hydrochloric acid concentration
2.2.4 時(shí)間的影響
由圖6可知,碳苷黃酮含量隨著時(shí)間的延長(zhǎng)呈先升后降的趨勢(shì);時(shí)間為150 min時(shí),總含量達(dá)到最大值,推測(cè)為水解過(guò)程基本完成;繼續(xù)延長(zhǎng)時(shí)間,可能會(huì)更多地破壞黃酮結(jié)構(gòu)。因此,時(shí)間選擇150 min為宜。

圖6 不同時(shí)間的影響Fig.6 The effect of different time
2.2.5 溫度的影響
由圖7可知,碳苷黃酮含量隨著溫度的升高呈先升后降的趨勢(shì);當(dāng)溫度超過(guò)65 ℃時(shí),過(guò)高的溫度有可能會(huì)加速黃酮結(jié)構(gòu)的破壞。因此,溫度選擇65 ℃為宜。
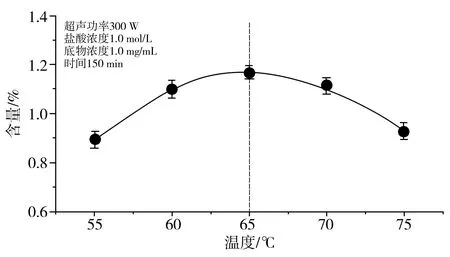
圖7 不同溫度的影響Fig.7 The effect of different temperatures
2.3 響應(yīng)面實(shí)驗(yàn)優(yōu)選最優(yōu)條件
2.3.1 超聲波輔助酸水解響應(yīng)面工藝優(yōu)化
通過(guò)響應(yīng)面Design-Expert軟件進(jìn)行方差分析,得到以下結(jié)果:
將上述實(shí)驗(yàn)數(shù)據(jù)進(jìn)行多元回歸擬合,以麻竹葉提取物4種碳苷黃酮的含量(Y)為評(píng)價(jià)指標(biāo)[20],對(duì)鹽酸濃度(A)、時(shí)間(B)和溫度(C)進(jìn)行二次多項(xiàng)式模型方程擬合得到回歸模型為:
Y=-11.45985+0.47437A+0.024779B+0.32301C-3.91667×10-3AB+0.03375AC-1.45×10-4BC-1.0575A2-3.86667×10-5B2-2.562×10-3C2。
對(duì)該模型進(jìn)行顯著性方差分析,分析結(jié)果見(jiàn)表6。

表5 實(shí)驗(yàn)設(shè)計(jì)與結(jié)果Table 5 The experimental design and results
由表6可知,該模型中F值為102.34,P值<0.0001,差異極顯著;相關(guān)系數(shù)R2=0.9925,校正系數(shù)RAdj2=0.9828,表明實(shí)驗(yàn)結(jié)果有98.28%以上受到各因素的影響;失擬項(xiàng)的P>0.05,差異不顯著,表明該模型可靠。

表6 回歸系數(shù)的顯著性分析Table 6 The significance analysis of regression coefficients
交互項(xiàng)AB、AC和BC的P值均<0.01,說(shuō)明A、B和C之間交互影響較大,對(duì)4種碳苷黃酮含量的影響顯著;根據(jù)表6中F值推出3個(gè)因素的主效關(guān)系:溫度(C)>鹽酸濃度(A)>時(shí)間(B)。
對(duì)上述回歸方程進(jìn)行求解,得到最優(yōu)酸水解工藝:鹽酸濃度為0.995 mol/L,時(shí)間為147.350 min和溫度為65.426 ℃,4種碳苷黃酮含量為1.168%。
2.3.2 響應(yīng)面交互因素
根據(jù)鹽酸濃度(A)、時(shí)間(B)和溫度(C)對(duì)碳苷黃酮含量的影響,做響應(yīng)曲面和等高線圖[21],見(jiàn)圖8。
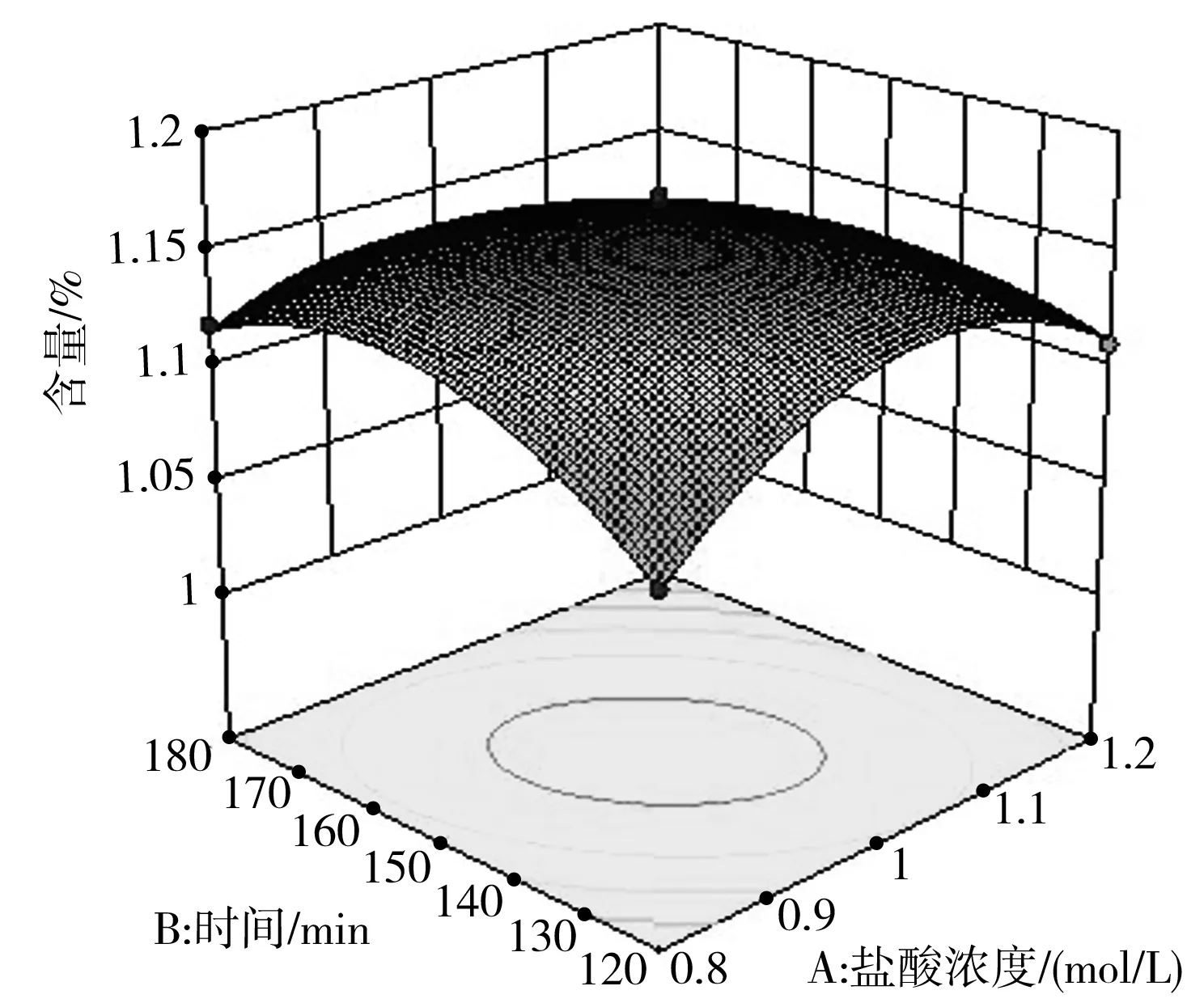
由圖8可知,在AB響應(yīng)面圖中,A因素的坡度較陡,對(duì)其得率的影響大于B因素[22];同法考察 AC和BC響應(yīng)面圖,確定各因素的影響程度依次為溫度(C)>鹽酸濃度(A)>時(shí)間(B),與方差分析結(jié)果一致。本實(shí)驗(yàn)中AB、AC和BC的等高線圖呈橢圓形,各因素之間的交互作用對(duì)酸水解麻竹葉提取物的影響較顯著。
2.3.3 工藝驗(yàn)證
結(jié)合實(shí)際條件,將2.3.1項(xiàng)下優(yōu)化的超聲波輔助酸水解工藝參數(shù)調(diào)整為:鹽酸濃度為1.0 mol/L、溫度為65 ℃和時(shí)間為147 min。按照1.2.4項(xiàng)色譜條件對(duì)酸水解前與酸水解后碳苷黃酮的含量進(jìn)行測(cè)定,結(jié)果見(jiàn)表7。

表7 平行實(shí)驗(yàn)結(jié)果Table 7 The results of parallel experiments %
由表7可知,驗(yàn)證實(shí)驗(yàn)得到的4種碳苷黃酮含量為1.157%(n=3,RSD=0.22%),與預(yù)測(cè)值1.168%的相對(duì)誤差為0.94%,比酸水解前的4種碳苷黃酮含量高1.384倍,說(shuō)明該工藝可行。
3 結(jié)論
本文在單因素實(shí)驗(yàn)基礎(chǔ)上,通過(guò)固定超聲功率(300 W)和底物濃度(1 mg/mL),利用響應(yīng)面法優(yōu)化了麻竹葉提取物的超聲波輔助酸水解工藝。結(jié)果表明,影響因素的主效關(guān)系為:溫度的影響最大,鹽酸濃度次之,時(shí)間的影響最小;根據(jù)實(shí)際情況調(diào)整后的工藝為:鹽酸濃度為1 mol/L、溫度為65 ℃和時(shí)間為147 min;在此條件下,得到酸水解后麻竹葉提取物4種碳苷黃酮含量平均值為1.157%,與預(yù)測(cè)值1.168%的相對(duì)誤差為0.94%,比酸水解前得率高1.384倍。在食品中添加適量的黃酮化合物可以增加食品的抗脂質(zhì)氧化性,改善其風(fēng)味及口感,提高食品性能。因此,深入開(kāi)展麻竹葉提取物的研究對(duì)綜合利用麻竹葉黃酮類化合物具有一定的指導(dǎo)和應(yīng)用價(jià)值。

