雙源CT雙能量碘圖對甲狀腺結節的鑒別價值
王慶云,吳凌梅,高鳳霄
(1.邢臺市人民醫院 CTMRI科,河北 054031;2.邢臺市人民醫院 核醫學科,河北 054031)
甲狀腺是人體的重要組織,位于喉與氣管的前外側,包括左右兩葉,中間由峽部相連[1]。甲狀腺結節是常見的甲狀腺疾病,多發病于成年人,主要包括結節性甲狀腺腫、甲狀腺癌、甲狀腺瘤,早期明確結節的良惡性對于指導治療方案具有重要意義[2]。隨著影像學技術的發展和應用,甲狀腺結節的檢出率越來越高,且檢出的甲狀腺結節體積越來越小,但是良惡性結節的影像學表現不典型,術前的良惡性鑒別診斷難度依然較大[3]。雙源CT是利用雙能量成像的原理,將含碘的物質從其他組織中分離出來。人體的甲狀腺是含碘組織,因此雙源CT雙能量掃描能通過測定甲狀腺正常組織與病灶組織的碘含量來鑒別診斷結節的良惡性[4]。基于此,本研究探索雙源CT雙能量碘圖在甲狀腺結節良惡性中的鑒別診斷價值,報道如下。
1 資料與方法
1.1 研究對象
本組的102例研究對象來自邢臺市人民醫院于2013年6月-2019年6月診治的甲狀腺結節患者。納入標準:①均經手術病理或穿刺活檢證實結節的良惡性;②接受雙源CT雙能量平掃和增強掃描;③在CT掃描后2周內接受甲狀腺結節手術治療;④無嚴重心、肺、腎等功能不全。排除標準:①經CT掃描顯示單純囊性病灶、結節廣泛囊性變或無正常甲狀腺組織存留者;②病灶大面積鈣化者;③病灶直徑<1.0cm者。本組的102例患者中,男40例,女 62 例,年齡 33-75 歲,平均(45.9±10.2)歲;共有結節142個,結節直徑為1.2-8.5cm,平均 (3.87±0.45)cm;良性結節82個,惡性結節60個。
1.2 方法
掃描方法:選用德國Siemens SOMATOM Definition Flash雙源CT掃描儀,采用雙能量掃描模式。患者取仰臥位,頭-足位掃描,掃描范圍為下頜部到縱膈上部,叮囑患者掃描期間不得進行吞咽動作。首先進行雙能量平掃,然后進行增強掃描。采用高壓注射器經肘靜脈注射非離子型對比劑碘海醇50ml,注射速率為2.5-4.0ml/s,追加注射生理鹽水30ml,采用自動掃描觸發軟件進行觸發掃描,監測點位于左側頸總動脈,當閾值達到100HU時觸發掃描動脈期,延遲15s進行靜脈期掃描。掃描參數,A和B管的管電壓分別為80、140KVp,參考管電流為350mAs、0.33s/r,螺距為 0.85,融合系數為 0.5,FOV為15cm×15cm,重建層厚為0.75mm,間隔0.5mm。
圖像分析:經過后處理工作站的軟件處理,得到碘圖圖像,測量甲狀腺結節實性成分和周圍正常甲狀腺組織的碘值,選擇感興趣區(ROI)時避開結節內的鈣化區、壞死區、血管區以及CT值較大的組織交界區,ROI位于病灶中心、正常甲狀腺和同層面頸動脈中心,面積約為5-8mm,選擇3個層面測量數據,每次測量3次取平均值。
評價標準:惡性的標準:①結節邊界不清晰、無包膜或包膜不完整;②結節內可見微小鈣化;③結節內部密度不均;④結節形態不規則或是分葉狀;⑤頸部淋巴結腫大。若符合上述任意2條及以上的則考慮為惡性結節。
1.3 觀察指標
①計算良惡性結節的標準化碘濃度比(NIC)和標準化CT值。其中,NIC=病灶內碘濃度/相頸動脈內碘濃度;標準化CT值=病灶內CT值/相頸動脈內CT值。對比良惡性結節在動脈期和靜脈期的NIC和標準化CT值。②良惡性結節的形態學特征,包括形態規則檢出率、包膜不完整/無包膜檢出率、鈣化檢出率。③診斷效能。
1.4 統計學方法
使用SPSS23.0軟件檢驗數據資料,計數數據比較采用X2檢驗,計量數據比較采用t檢驗。繪制受試者工作特征曲線 (ROC),計算曲線下的面積(AUC),選取最大敏感度和特異度的臨界值,診斷結果的一致性采用Kappa檢驗,P<0.05差異有統計學意義。
2 結果
2.1 良惡性結節的NIC和標準化CT值比較
良惡性結節在動脈期的NIC和標準化CT值比較,差異均無統計學意義,P>0.05;在靜脈期,良性結節的NIC和標準化CT值均高于惡性結節,P<0.05,詳見表1。
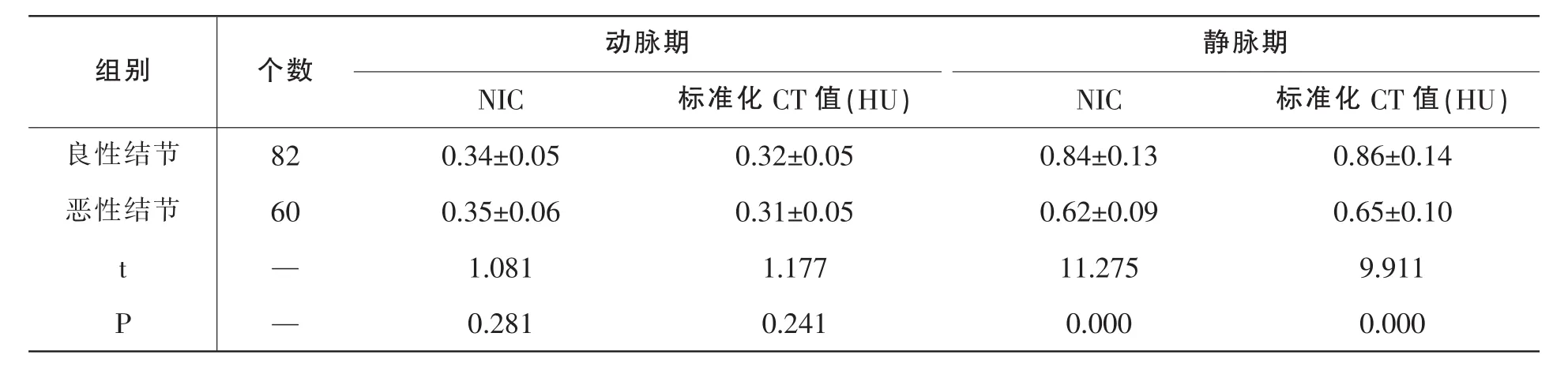
表1 良惡性結節的NIC和標準化CT值
2.2 良惡性結節的形態學特征比較
見表2所示,良性結節的形態規則檢出率明顯高于惡性結節,P<0.05;良性結節的包膜不完整/無包膜和鈣化檢出率均低于惡性結節,P<0.05。

表2 良惡性結節的形態學特征
2.3 診斷效能
根據ROC曲線得出靜脈期鑒別良惡性結節的最佳臨界NIC為0.75,標準化CT值為0.78HU。當NIC<0.75,標準化CT值<0.78HU時,診斷為惡性結節,AUC值分別為0.90、0.92,其中NIC鑒別診斷的敏感度和特異度分別為92.68%(76/82)、96.67%(58/60),標準化CT值鑒別診斷的敏感度和特異度分別為 93.90%(77/82)、98.33%(59/60)。經形態學特征鑒別診斷,其中良性結節79個,惡性結節63個,4個良性結節誤診為惡性結節,1個惡性結節誤診為良性結節,診斷敏感度和特異度分別為95.12%(78/82)、98.33%(59/60);經Kappa檢驗,靜脈期的 NIC和標準化CT值鑒別診斷與形態學鑒別診斷的一致性高(Kappa=0.795、0.812)。
3 討論
正常的甲狀腺是甲狀腺激素的代謝場所,由大量的濾泡細胞構成。濾泡細胞上有Na+/I-轉運蛋白,能攝碘,胞內有酶形成氧化碘,并合成絡氨酸,兩者相互作用后形成一碘、二碘絡氨酸,然后參與到甲狀腺激素的代謝合成中,因此人體正常甲狀腺組織中含有大量的碘[5-6]。甲狀腺球蛋白隨著人體的血液循環進入到各個器官,在腎臟、肝臟等臟器中裂解、脫下碘,而甲狀腺會再次吸收脫掉的碘,從而形成全身的碘循環[7-8]。在碘循環的過程中,大部分碘會隨著尿液、糞便等排出體外,當機體的碘供給遠遠少于需求量,甲狀腺就會發生病變,形成甲狀腺結節等。甲狀腺結節可以分成良性和惡性,其中良性結節主要有結節性甲狀腺腫、甲狀腺腺瘤等,惡性主要為甲狀腺癌[9-10]。
早期明確甲狀腺結節的良惡性對于手術方案的選擇、預后評估等有積極意義,尋求更加有效的術前鑒別診斷方法十分重要[11-12]。雙源CT有兩套獨立的X線球管探測器系統,能同時掃描,根據同種物質在不同X射線能量下的衰減系數不同這一原理區分碘與其他物質,獲得碘基物質的空間分布彩色圖像,在碘圖中測定甲狀腺結節的碘濃度和周圍正常甲狀腺組織的碘濃度,從而輔助判斷結節的良惡性,這為甲狀腺的定性診斷提供了新的手段。
本次研究結果顯示:良惡性結節在動脈期的NIC和標準化CT值差異均無統計學意義,P>0.05;在靜脈期的NIC和標準化CT值,良性結節均高于惡性結節,P<0.05。與惡性結節相比,良性結節仍存在部分具有攝碘功能的濾泡細胞,故此良性結節的攝碘率高于惡性結節。經增強掃描后,動脈期能顯示結節的血供,惡性結節內癌細胞生長旺盛而導致缺氧,從而使得大量血管內皮因子產生,誘導血管新生;而良性結節因上皮細胞增生也會有新生血管生成來供應上皮細胞血液。惡性結節的新生血管雖然比良性的多,但是惡性結節在生長的同時也會破壞包含血管在內的組織結構,血管壁被癌細胞穿透在附壁形成癌栓,進一步導致大量血管壞死。因此,在動脈期良惡性結節的NIC差異不明顯。但是由于惡性結節內豐富的血管多會形成動靜脈瘺且血流快,癌灶內血管內皮細胞之間的間隙大、基底膜不完全發育等導致血管的通透性高[13-14]。在靜脈期惡性結節的對比劑迅速廓清,從而導致靜脈期的NIC值惡性結節低于良性結節。
雙源CT雙能量碘圖能將碘含量直觀反映在圖像上,圖像越亮則組織含碘量越高,從而利于辨別結節邊緣和包膜情況[15-16]。一般良性結節的邊界較為清晰、包膜完整,且周圍正常甲狀腺組織不受侵犯。而惡性結節邊界不規則、呈浸潤性生長,常常侵犯鄰近的正常濾泡上皮細胞,突破包膜,邊界不清晰。本次研究中,根據碘圖的形態學,良性結節的形態規則檢出率明顯高于惡性結節,P<0.05;良性結節的包膜不完整/無包膜和鈣化檢出率均低于惡性結節,P<0.05;對良惡性結節的鑒別診斷敏感度和特異度分別為95.12%、98.33%。NIC值與標準化CT值對良惡性結節的鑒別診斷敏感度和特異度均較高,在90%以上,三者的鑒別診斷敏感度和特異度一致性高。
總之,雙源CT雙能量碘圖在甲狀腺良惡性結節鑒別診斷中應用價值高,靜脈期NIC值、標準化CT值和碘圖形態學的鑒別診斷價值均較高,利于臨床醫師早期鑒別結節的良惡性,指導臨床治療,值得推廣。

