“素養為本”的主題式教學實踐與反思
李婷妹


[摘 要]文章以“Fe3+與Fe2+的檢驗及相互轉化”為主題,以檢驗久置FeSO4溶液是否變質為導引, 讓學生通過小組實驗探究鐵鹽與亞鐵鹽之間的轉化關系,充分發揮學生的主體作用,培養學生分析和解決問題的能力,提升學生的化學學科核心素養。
[關鍵詞]Fe3+與Fe2+的檢驗;相互轉化;主題式教學;素養為本
[中圖分類號]? ? G633.8? ? ? ? ? ? [文獻標識碼]? ? A? ? ? ? ? [文章編號]? ? 1674-6058(2022)05-0066-03
《普通高中化學課程標準(2017年版)》(簡稱課標)的基本理念中提到,重視開展“素養為本”的教學,倡導真實問題情境的創設,開展以化學實驗為主的多種探究活動,重視教學內容的結構化設計,激發學生學習化學的興趣,促進學生學習方式的改變,培養他們的創新精神和實踐能力[1]。
化學主題式教學立足生活實際,結合前沿科學技術信息材料創設情境,由教師圍繞主題設計問題,引導學生思考及探究,讓學生通過查閱資料、做實驗等多樣化的方式去學習新知識,并運用學到的知識分析解決問題,使學生的化學學科核心素養得到提升[2]。
筆者以人教版化學教材必修第一冊第三章第一節“鐵及其化合物”中“Fe3+與Fe2+的檢驗及相互轉化”為例,開展“素養為本”的主題式教學,并進行反思。
一、 教學設計
課標中提出“鐵及其化合物的性質”實驗是學生必做的實驗,通過建立“鐵三角”轉化關系的認知模型,外顯學生的思維過程,培養學生“宏觀辨識與微觀探析”“證據推理與模型認知”核心素養。
本節課以“Fe3+與Fe2+的檢驗及相互轉化”為主題,創設檢驗久置FeSO4溶液是否變質的問題情境,讓學生小組合作探究,促使學生學會建立觀點、結論和證據之間的邏輯關系;布置任務讓學生查閱資料了解鐵鹽在生活中的應用,進而深刻認識到化學可以讓生活更美好,使學生產生“努力學好化學”的社會責任感。
二、教學思路
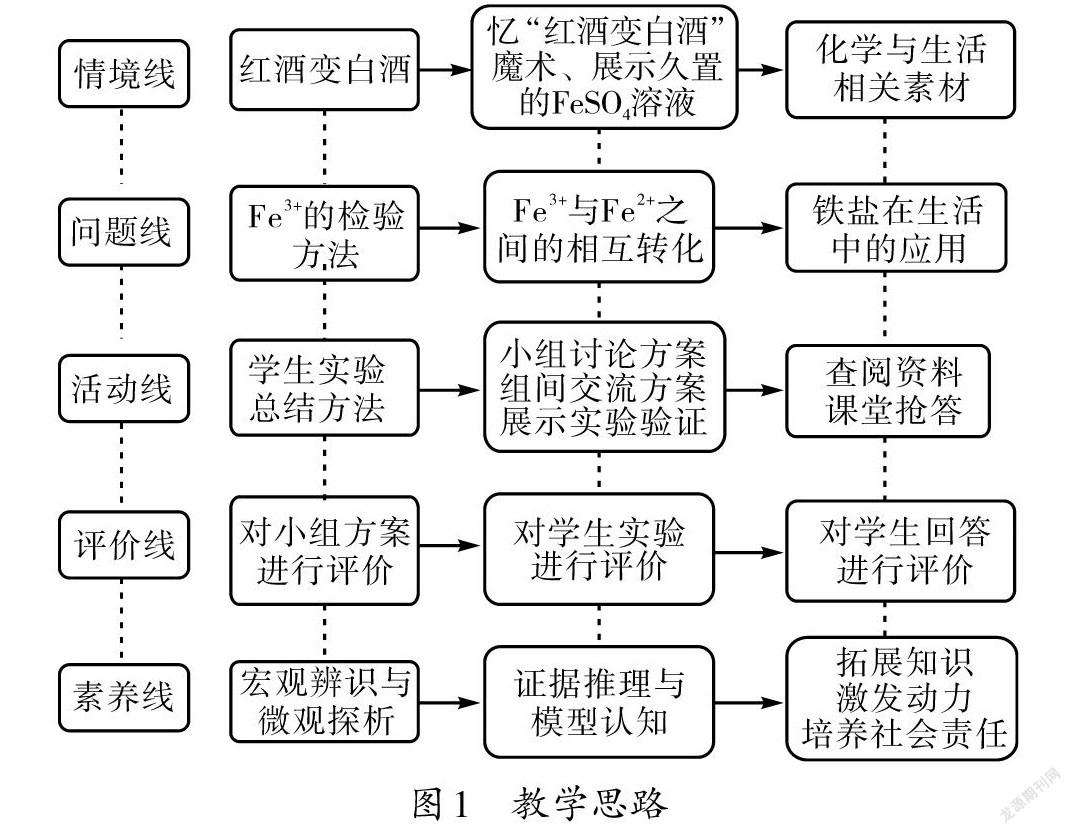
筆者結合“Fe3+與Fe2+的檢驗及相互轉化”主題內容創設“紅酒變白酒”的有趣情境,激發學生的學習興趣,引導學生小組合作設計實驗方案、驗證實驗方案,并開展相關實驗探究。實施主題式教學旨在發揮學生課堂學習的積極性與主動性,提高學生的思考能力、探究能力以及解決問題的能力,培養學生的化學學科核心素養。具體的教學思路如圖1所示。
三、教學過程
環節一 Fe3+與Fe2+的檢驗
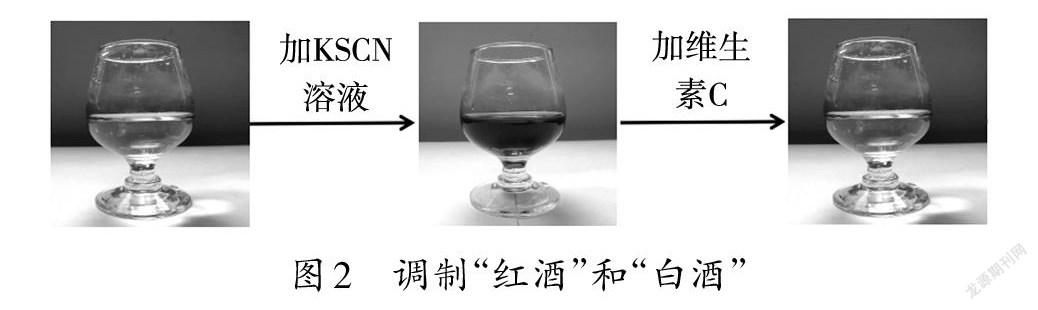
【情境導入】同學們,你們知道怎么調制“紅酒”嗎?現在我手上有一杯“白酒”,往里面添加試劑1就可以調制“紅酒”,再往里添加試劑2,“紅酒”顏色就會褪去變回“白酒”(如圖2)。同學們想知道其中的奧秘嗎?
【過渡】同學們要想知道酒里的秘密,需要先學習Fe3+的檢驗。實驗臺上有兩瓶失去標簽的FeSO4溶液和Fe2(SO4)3溶液(溶液較稀,無法通過肉眼辨色來區分)。請用盡可能多的方法鑒別這兩種溶液。
【學生實驗】取樣,滴加幾滴KSCN溶液或NaOH溶液進行鑒別。
【小結】
①往待測液中滴加幾滴KSCN溶液,若變血紅色,證明待測液中含有Fe3+,原理是Fe3++ 3SCN- =Fe(SCN)3(血紅色)。
②往待測液中滴加幾滴NaOH溶液,若生成紅褐色沉淀,證明待測液中含有Fe3+,原理是Fe3++ 3OH-? =Fe(OH)3↓(紅褐色)。
設計意圖:通過“紅酒變白酒”的實驗,激發學生的學習興趣,使學生樂學、善學,滿足課標提出的主題內容情境化要求;解釋溶液顏色變血紅色的本質原因,讓學生深入理解Fe3+的檢驗原理,培養學生“宏觀辨識與微觀探析”核心素養。
環節二 Fe3+與Fe2+之間的相互轉化
【提問】實驗室有一瓶久置的FeSO4溶液,請設計實驗鑒別該溶液是否變質。
【學生實驗】取1~2 mL FeSO4溶液于試管中,滴加1~2滴KSCN溶液。若溶液顏色變血紅色,則證明FeSO4溶液變質,否則沒變質。
【過渡】用什么辦法可恢復變質的FeSO4溶液?
【提問】回顧“紅酒變白酒”魔術,請同學們從氧化還原反應的角度去分析Fe3+與Fe2+之間的相互轉化關系。
【學生分析】Fe2+要轉化成Fe3+,須發生氧化反應,可通過加氧化劑(如過氧化氫、氧氣或硝酸)來實現;Fe3+要轉化成Fe2+,須發生還原反應,可通過加還原劑(如鐵粉、銅粉或氫硫酸)來實現。
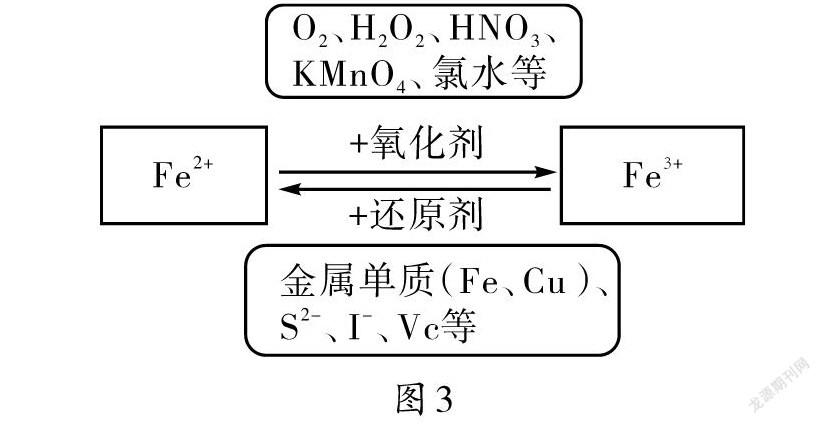
【PPT展示】總結Fe3+轉化成Fe2+常用的還原劑以及Fe2+轉化成Fe3+常用的氧化劑(如圖3)。
設計意圖:設置判斷實驗室久置FeSO4溶液是否變質這一問題,目的是讓學生學會運用剛學的檢驗Fe3+的知識去解決問題,通過學以致用加深理解;通過提問“用什么辦法可恢復變質的FeSO4溶液”,使問題深度層層遞進,進一步引出本節課的重點內容“Fe3+與Fe2+之間的相互轉化”,讓學生學會用氧化還原反應的理論及知識分析和解決相關問題,提升學生運用所學知識分析和解決問題的能力,培養學生遷移知識的能力和“模型認知”核心素養。
【提問】怎么設計實驗證明Fe3+與Fe2+發生了相互轉化?請以小組為單位進行討論,設計實驗方案,開展探究實驗以得出結論。
[實驗室提供的試劑有H2O2 溶液(H+)、KSCN溶液、氯水、鐵粉、FeSO4溶液、Fe2(SO4)3溶液]
【教師引導】設計實驗前,首先選定氧化劑和還原劑,其次思考三個問題:①驗證Fe2+轉化成Fe3+前要考慮Fe2+是否變質嗎?②加什么試劑可使Fe2+轉化成Fe3+?③如何驗證生成了Fe3+?同樣地,驗證Fe3+轉化成Fe2+也需考慮以上三個問題。
【組1方案】Fe2+轉化成Fe3+:取1~2 mL FeSO4溶液于試管中,先滴加2滴氯水,再滴加2滴KSCN溶液,若溶液顏色變血紅色,則證明FeSO4被氧化成Fe2(SO4)3。
【組2方案】Fe2+轉化成Fe3+:滴加KSCN溶液和滴加氯水的前后順序與組1方案不同。取1~2 mL FeSO4溶液于試管中,先滴加2滴KSCN溶液(無明顯現象),后滴加2滴氯水,若溶液顏色變血紅色,則證明FeSO4被氧化成Fe2(SO4)3。
【教師評價】組2方案更優,因為先滴加KSCN溶液可排除FeSO4變質產生的干擾。
【提問】如何設計實驗證明Fe3+轉化成Fe2+?
【組3方案】Fe3+轉化成Fe2+:取1~2 mL的Fe2(SO4)3溶液于試管中,滴加2滴KSCN溶液,溶液顏色變血紅色,再加入適量的鐵粉或VC,若溶液血紅色消失,則證明Fe2(SO4)3被還原成FeSO4。
【教師評價】同學們設計的方案很合理,思路清晰。
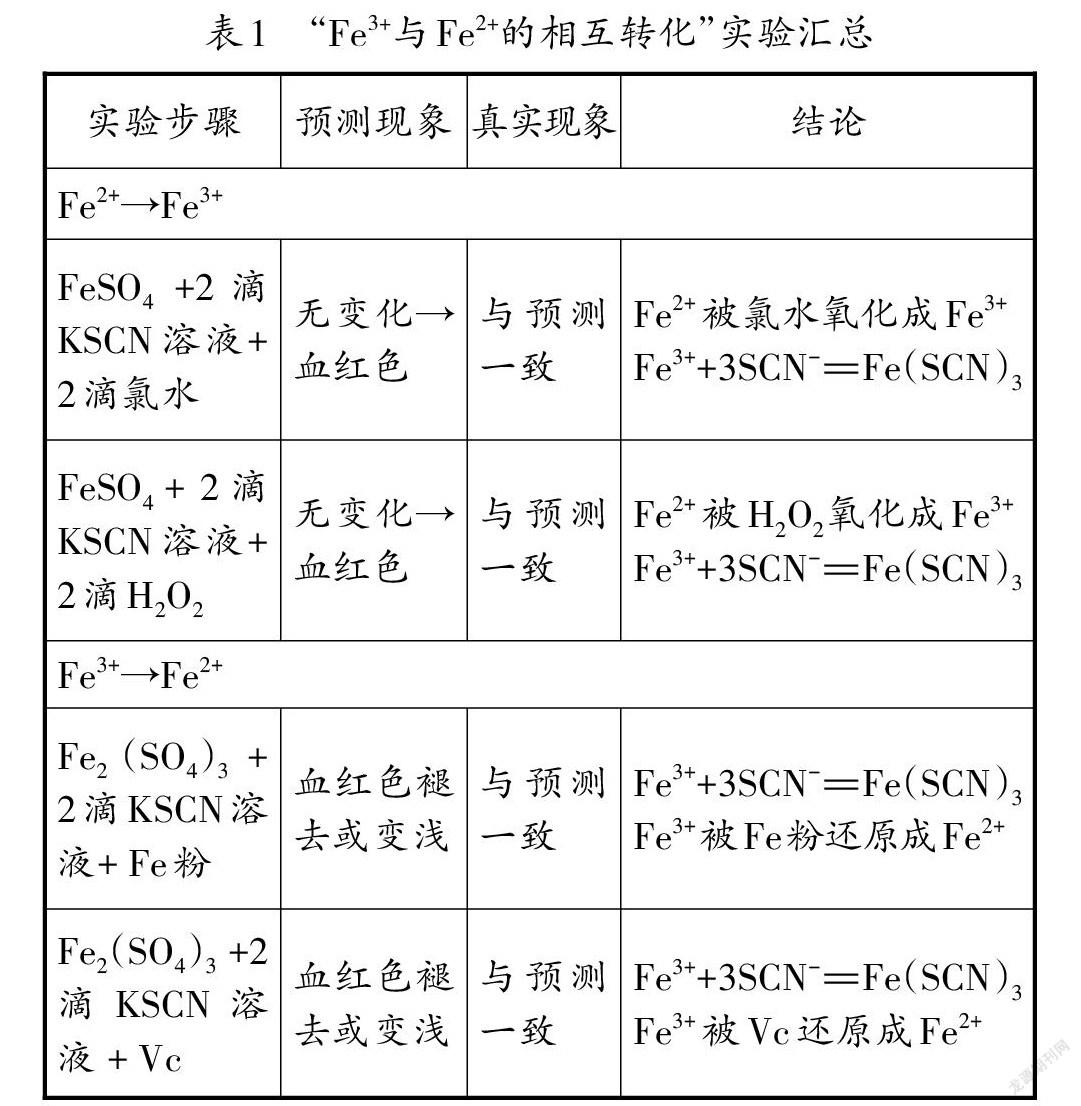
【學生實驗】學生小組實驗展示并匯總(見表1)。
【提問】用什么辦法可恢復變質的FeSO4溶液?怎樣驗證FeSO4溶液是否完全變質?
【學生回答】可以加鐵粉恢復變質的FeSO4溶液;可以滴加幾滴酸性高錳酸鉀溶液,若溶液褪色,則說明FeSO4溶液部分變質,否則完全變質。
設計意圖:讓學生以小組為單位進行實驗設計及探究,并開展組內討論和組間交流,從而使學生碰撞出思維的火花,突破難點獲得最優實驗方案,提高學生的自主學習能力,培養學生團結合作的精神和嚴謹求知的科學態度;使用希沃授課助手進行手機投屏,展示小組探究實驗的過程,激發學生實驗探究的興趣;讓學生在實驗中觀察、討論、分析現象,培養學生獨立思考的能力,提升學生“科學探究與創新意識”“宏觀辨識與微觀探析”“證據推理與模型認知”等核心素養。
環節三 Fe元素在生活中的應用
【過渡】同學們通過查閱資料了解了鐵元素在生活中的應用,那么鐵元素在生活中扮演什么角色呢?鐵元素是組成血紅蛋白、肌紅蛋白和腦紅蛋白的重要元素。鐵元素會影響人體的免疫系統,它參與人體內氧的運輸與儲存以及能量代謝,與我們的健康息息相關。
【PPT展示】血紅蛋白相關圖片(如圖4)。
【生活情境1】人貧血時需要吃補鐵劑——硫酸亞鐵片。
【信息提示】人體能吸收的離子是亞鐵離子。
【提問】為什么與維生素C同服有助于本品吸收?
【學生回答】因為硫酸亞鐵容易被氧化,而維生素C可以抗氧化。
【小結】亞鐵離子具有還原性,容易被氧化成三價鐵,三價鐵不易被吸收,而同時服用維生素C有助于亞鐵離子抗氧化,提高鐵元素的吸收率。此外,食物中的鐵一般以三價鐵的形式存在,食用維生素C還可以提高食物中鐵元素的吸收率。
【生活情境2】健康飲食,通過食療補鐵。
【過渡】我們平時如何補充鐵元素?
【PPT展示】吃富含鐵元素的食物。
【提問】飯后吃水果更健康,為什么?
【學生回答】水果富含維生素C,有利于鐵元素的吸收。富含維生素C的水果有獼猴桃、草莓、柑橘、柚子、蘋果等。
設計意圖:介紹鐵元素在生活中的應用,拓展學生視野,讓學生了解鐵元素是構成血紅蛋白的重要元素,與我們的健康息息相關;讓學生了解常見的富含鐵元素的水果蔬菜,使學生學會用已學的知識來解決生活中的問題,同時深刻體會到化學對滿足人們日益增長的生活需求有重大貢獻。
四、教學反思
本節課以“Fe3+與Fe2+的檢驗及相互轉化”為主題展開教學,打破了傳統的“滿堂灌”教學模式,先引入主題,而后圍繞主題設計層層遞進、環環相扣的問題,使知識問題化,問題情境化,情境生活化。“Fe3+與Fe2+的相互轉化”的教學采用探究實驗的方式,讓學生以小組為單位進行討論,得出最優方案并進行實驗操作,培養學生自主學習的習慣、善于合作的能力、敢于批評與質疑的精神、證據推理的能力以及嚴謹求實的科學態度。主題式教學對教師來說充滿了挑戰,需要教師充分備課,查找資料,把握好問題的設計技巧,使問題間既有聯系又有遞進,構架清晰的知識脈絡。學生很喜歡這種有情境有主題的課堂,它能夠激發學生的學習興趣和動力,培養學生的學科核心素養。
[? ?參? ?考? ?文? ?獻? ?]
[1]? 中華人民共和國教育部.普通高中化學課程標準(2017年版)[M].北京:人民教育出版社,2018.
[2]? 黃燕,謝培林.主題式教學的實踐與反思:用電浮選凝聚法復習電解池[J].中學化學教學參考,2018(19):49-52.
(責任編輯 羅 艷)

