解毒消癥飲通過VEGF-C/VEGFR-3信號途徑抑制肝癌淋巴管生成的機(jī)制研究
楊寓寧,魯 琴,林明和,杜 建,曹治云*
(1.福建中醫(yī)藥大學(xué)中西醫(yī)結(jié)合研究院,福建 福州 350122;2.福建省中西醫(yī)結(jié)合老年性疾病重點(diǎn)實(shí)驗(yàn)室,福建 福州 350122)
腫瘤轉(zhuǎn)移是腫瘤致死的重要原因,腫瘤初期的生長主要通過誘導(dǎo)血管新生來提供其所需要的營養(yǎng),而腫瘤轉(zhuǎn)移的主要途徑是通過誘導(dǎo)的新生淋巴管進(jìn)行[1]。血管內(nèi)皮生長因子(vascular endothelial growth factor,VEGF)的表達(dá)和分泌可作為刺激因子,啟動血管內(nèi)皮細(xì)胞和淋巴管內(nèi)皮細(xì)胞相關(guān)信號通路,進(jìn)而達(dá)到促血管新生和淋巴管生成的目的[2-4]。基質(zhì)金屬蛋白酶(matrix metalloproteinases,MMPs)通過降解細(xì)胞周圍細(xì)胞外基質(zhì)進(jìn)而促進(jìn)淋巴管細(xì)胞侵襲和遷移。由此可知血管內(nèi)皮生長因子C(VEGF-C)/血管內(nèi)皮生長因子受體3(VEGFR-3)通路及其下游MMPs在調(diào)節(jié)淋巴管的新生、重構(gòu)和穩(wěn)態(tài)中具有重要作用。解毒消癥飲(JXY)是清熱解毒的中藥驗(yàn)方,主要由白花蛇舌草、夏枯草、山慈姑、苦參4味中藥組成。前期研究結(jié)果表明,JXY能夠抑制移植瘤小鼠VEGF的表達(dá)[5];還可通過抑制肝癌細(xì)胞核內(nèi)p300和CBP的表達(dá),進(jìn)而抑制其與低氧誘導(dǎo)因子1α(hypoxia-inducible factor-1α,HIF-1α)結(jié)合形成低氧誘導(dǎo)復(fù)合物,從而抑制VEGF的表達(dá),最終下調(diào)腫瘤新生血管的生成[6]。基于JXY抗血管新生的作用及下調(diào)肝癌細(xì)胞表達(dá)VEGF-C的水平,本研究以VEGF-C/VEGFR-3為核心,進(jìn)一步探討JXY抗肝癌淋巴管新生的作用機(jī)制,為JXY的進(jìn)一步臨床應(yīng)用提供理論依據(jù)。
1 實(shí)驗(yàn)材料
1.1 實(shí)驗(yàn)細(xì)胞 人淋巴管內(nèi)皮細(xì)胞HLEC購自廣州吉尼歐生物技術(shù)有限公司,人肝癌細(xì)胞株HepG2購自中國科學(xué)院上海生命科學(xué)研究院。
1.2 實(shí)驗(yàn)藥物 JXY藥物組成:白花蛇舌草、夏枯草、山慈菇、苦參,購自福建中醫(yī)藥大學(xué)國醫(yī)堂。JXY經(jīng)95%乙醇后,乙酸乙酯提取,水浴干燥后備用。JXY經(jīng)DMSO溶解后制備成200 mg/mL的母液,超聲助溶,采用常溫PBS稀釋成實(shí)驗(yàn)濃度。實(shí)驗(yàn)中所需要的外源性VEGF-C,按照說明書指示將其溶解于雙蒸水,稀釋后使?jié)舛冗_(dá)到5 ng/mL,超聲助溶后備用。
1.3 實(shí)驗(yàn)試劑 ECM培養(yǎng)基(美國ScienCell公司);高糖DMEM培養(yǎng)基(GIBCO公司);胎牛血清(FBS)、0.25%胰蛋白酶、磷酸鹽緩沖液(PBS)(美國life technologies公司);青霉素-鏈霉素混合液(美國Thermo Fisher Scientific公司);MTT粉末(M8180)(江蘇凱基生物技術(shù)股份有限公司);管腔形成試劑盒(德國Merck Millipore公司);VEGF-C、VEGFR-3、MMP-2、MMP-9抗體(美國CST公司);遷移小室(美國Corning公司);Hoechst 33258染色試劑盒(北京索萊寶科技有限公司)。
2 實(shí)驗(yàn)方法
2.1 細(xì)胞培養(yǎng) 將HLEC細(xì)胞株和HepG2細(xì)胞株分別置于ECM完全培養(yǎng)基和DMEM完全培養(yǎng)基中,放置于恒溫箱內(nèi)進(jìn)行培養(yǎng)。當(dāng)細(xì)胞匯合度達(dá)到70%~80%時(shí),加入2 mL的胰蛋白酶消化2~3 min,隨后加入4 mL完全培養(yǎng)基終止消化,1 000 r/min離心3min后,吸棄上清并收集沉淀細(xì)胞用于后續(xù)實(shí)驗(yàn)。
2.2 不同JXY濃度對細(xì)胞活力的影響 取對數(shù)生長期的細(xì)胞,以1×105/mL的密度接種于96孔板(100μL/孔),置于恒溫箱中培養(yǎng)過夜,當(dāng)匯合度達(dá)到50%~60%時(shí),將細(xì)胞分為0、0.05、0.1、0.2 mg/mL組,每組設(shè)置6個(gè)復(fù)孔,分別予相應(yīng)濃度JXY干預(yù)培養(yǎng)24 h。培養(yǎng)后于顯微鏡下觀察不同藥物濃度下細(xì)胞的生長狀態(tài)和密度是否發(fā)生變化。拍照后吸棄培養(yǎng)液,加入100μL/孔的MTT,置于恒溫箱內(nèi)4 h,棄舊液加入100μL/孔DMSO。最后在酶標(biāo)儀內(nèi)570 nm波長的設(shè)置下檢測OD值。

2.3 細(xì)胞分組 將細(xì)胞分為對照組、VEGF-C組、JXY低劑量組(簡稱低劑量組)、JXY中劑量組(簡稱中劑量組)、JXY高劑量組(簡稱高劑量組)。對照組每孔加入100μL ECM完全培養(yǎng)基,VEGF-C組予外源性因子VEGF-C(5 ng/mL)干預(yù),低、中、高劑量組分別予VEGF-C(5 ng/mL)聯(lián)合不同濃度JXY(0.05、0.1、0.2 mg/mL)進(jìn)行干預(yù),每組均干預(yù)24 h。
2.4 細(xì)胞形態(tài)觀察 取對數(shù)生長期的HLEC細(xì)胞,按照1×105/mL的密度接種于6孔板中,當(dāng)細(xì)胞平鋪于板底60%左右時(shí),按“2.3”項(xiàng)進(jìn)行分組干預(yù)。24 h后分別放置于倒置顯微鏡下觀察細(xì)胞生長狀態(tài)及形態(tài)并拍照。
2.5 MTT檢測細(xì)胞活力 取對數(shù)生長期的細(xì)胞,以1×105/mL的密度接種于96孔板,置于恒溫箱中培養(yǎng)過夜,當(dāng)匯合度達(dá)到50%~60%時(shí),按“2.3”項(xiàng)進(jìn)行分組干預(yù),每組設(shè)置6個(gè)復(fù)孔。24 h后于顯微鏡下觀察在不同藥物濃度下細(xì)胞的生長狀態(tài)和密度是否發(fā)生變化。拍照后吸棄培養(yǎng)液后加入100μL/孔的MTT,置于恒溫箱內(nèi)4 h,棄舊液加入100μL/孔DMSO。最后在酶標(biāo)儀內(nèi)570 nm波長的設(shè)置下檢測吸光度值。
2.6 細(xì)胞凋亡實(shí)驗(yàn) 采用Hoechst 33258染色法觀察細(xì)胞凋亡情況。取對數(shù)生長期的HLEC,按照1×105/mL的密度接種于6孔板,當(dāng)細(xì)胞平鋪于板底60%左右時(shí),按“2.3”項(xiàng)進(jìn)行分組干預(yù),干預(yù)后吸棄并使用1×PBS清洗,使用10%福爾馬林固定15 min,使用Hoechst 33258染色10 min(避光操作),隨后用熒光顯微鏡拍攝。
2.7 細(xì)胞遷移實(shí)驗(yàn) 采用Transwell法檢測細(xì)胞遷移能力。取對數(shù)生長期的HLEC,按照1×105/mL的密度接種于6孔板,當(dāng)細(xì)胞平鋪于板底60%左右時(shí),按“2.3”項(xiàng)進(jìn)行分組干預(yù)。干預(yù)后消化,空白ECM培養(yǎng)基重懸計(jì)數(shù),將細(xì)胞稀釋為2.5×105/mL,并于Transwell上室、下室分別添加200μL基礎(chǔ)培養(yǎng)基和700μL ECM完全培養(yǎng)基,隨后置于恒溫培養(yǎng)箱孵育12 h。孵育后吸棄原培養(yǎng)基,使用10%福爾馬林固定和結(jié)晶紫染色各15 min,雙蒸水反復(fù)洗滌3次,用無塵紙擦拭干凈上室的貼壁細(xì)胞,晾置干燥后,放置于倒置顯微鏡鏡下拍照。
2.8 細(xì)胞劃痕實(shí)驗(yàn) 應(yīng)用劃痕實(shí)驗(yàn)檢測細(xì)胞遷移能力。取對數(shù)生長期的HLEC,按照2.5×105/mL的密度接入6孔板進(jìn)行培養(yǎng),匯合度達(dá)到80%左右時(shí),用無菌槍頭在6孔板底部劃一痕跡,用PBS清洗3次,拍照。按“2.3”項(xiàng)進(jìn)行分組干預(yù),分別于6、12、24 h不同時(shí)間點(diǎn)進(jìn)行拍照并測量。
2.9 細(xì)胞管腔形成實(shí)驗(yàn) 應(yīng)用Tube Formation檢測體外淋巴管生成情況。取對數(shù)生長期的HLEC細(xì)胞,按照1×105/mL的密度接入6孔板,當(dāng)細(xì)胞平鋪于板底60%左右時(shí),按“2.3”項(xiàng)進(jìn)行分組干預(yù)。干預(yù)后按照試劑盒說明書操作指示,于冷凍盒上配置基質(zhì)膠150μL/孔平鋪于48孔板內(nèi),置于恒溫箱凝膠1 h。在此期間處理細(xì)胞,將細(xì)胞稀釋為2×105/mL,按200μL/孔加入已放有基質(zhì)膠的48孔板中,再放入恒溫箱內(nèi)孵育3 h,隨后在顯微鏡下鏡檢觀察并拍照。
2.10 Western blot法檢測VEGFR-3、MMP-9、MMP-2蛋白表達(dá) 取對數(shù)生長期的HLEC和HepG2細(xì)胞,分別按照1×105/mL的密度接種于6 cm小皿中,當(dāng)細(xì)胞平鋪于板底60%左右時(shí),將HepG2細(xì)胞分為0 mg/mL組和0.1 mg/mL組,0.1 mg/mL組予0.1 mg/mL JXY干預(yù)24 h,檢測2組VEGF-C蛋白表達(dá);HLEC細(xì)胞按“2.3”項(xiàng)進(jìn)行分組干預(yù),檢測5組VEGFR-3、MMP-9、MMP-2蛋白表達(dá)。
2.11 統(tǒng)計(jì)學(xué)方法 采用SPSS 24.0軟件包進(jìn)行數(shù)據(jù)分析。計(jì)量資料符合正態(tài)分布的以(±s)表示;組間比較采用單因素方差分析。不符合正態(tài)分布以中位數(shù)和四分位數(shù)描述,組間比較采用非參數(shù)檢驗(yàn)。
3 結(jié)果
3.1 不同濃度JXY對HepG2細(xì)胞活力和VEGF-C蛋白的影響 MMT法檢測細(xì)胞活力結(jié)果顯示,與對照組比較,JXY干預(yù)后各組細(xì)胞活力均有不同程度的下降,說明JXY對HepG2細(xì)胞活力有抑制作用,且呈現(xiàn)濃度依賴性(P<0.01,圖1A)。Western Blot檢測JXY(0 mg/mL、0.1 mg/mL)干預(yù)24 h后的HepG2細(xì)胞VEGF-C蛋白的表達(dá),結(jié)果如圖1B所示,同0 mg/mL組比較,0.1 mg/mL組的VEGF-C顯著下調(diào)(P<0.01)。不同濃度JXY(0 mg/mL、0.05 mg/mL、0.1 mg/mL、0.2 mg/mL)干預(yù)后發(fā)現(xiàn)細(xì)胞數(shù)量隨著JXY藥物濃度的增加呈梯度減少,結(jié)果如圖1C所示。
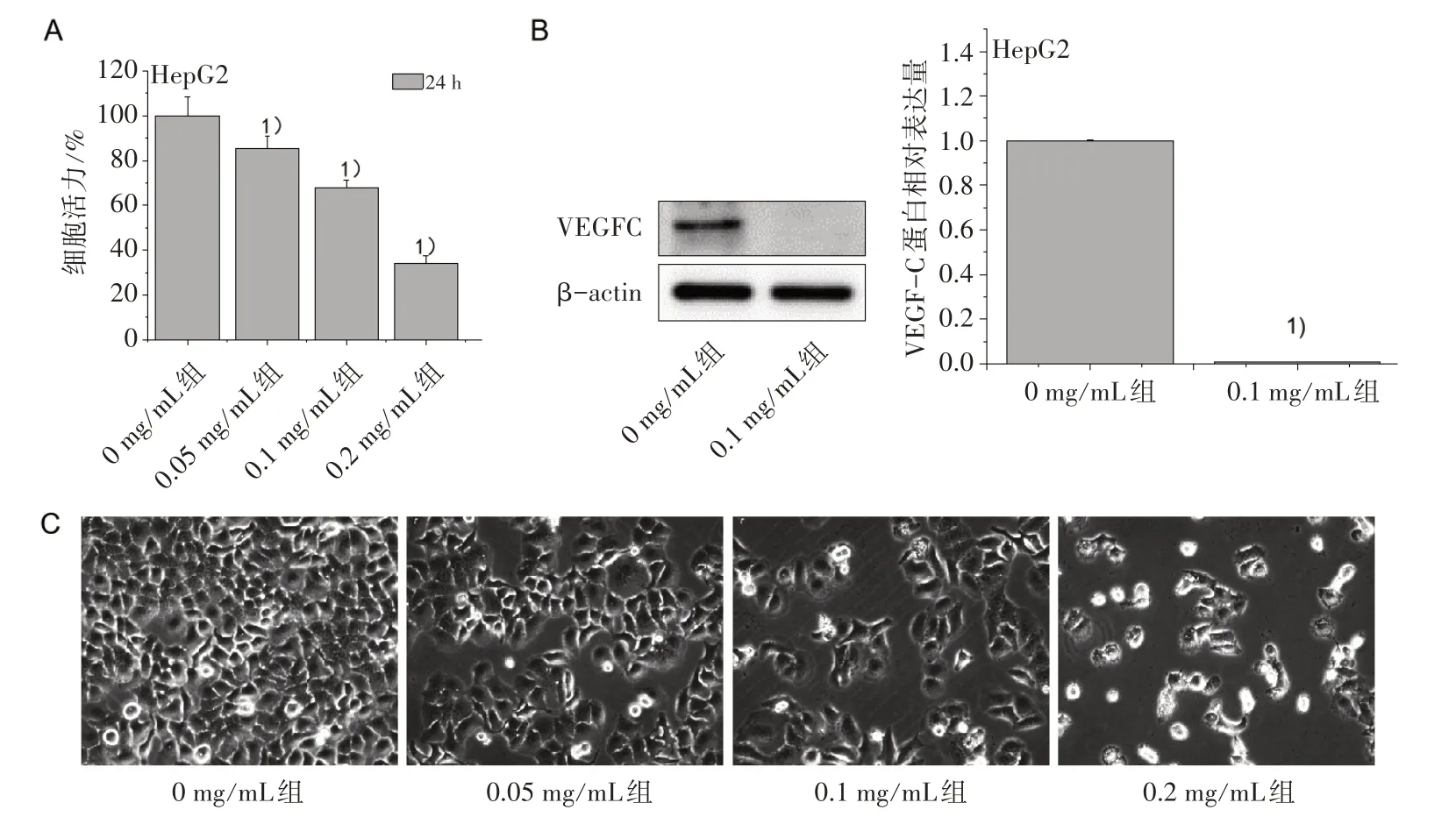
圖1 不同濃度JXY對Hep G2細(xì)胞活力及VEGF-C蛋白表達(dá)的影響(×200)
3.2 5組HLEC細(xì)胞形態(tài)及活力情況比較 如圖2所示,VEGF-C組與對照組比較,HLEC細(xì)胞生長形態(tài)正常,細(xì)胞密度顯著增大,細(xì)胞活力增高。各劑量組細(xì)胞形態(tài)出現(xiàn)固縮,細(xì)胞數(shù)量隨著JXY藥物濃度的增加呈梯度減少,細(xì)胞活力呈劑量依賴性的降低。
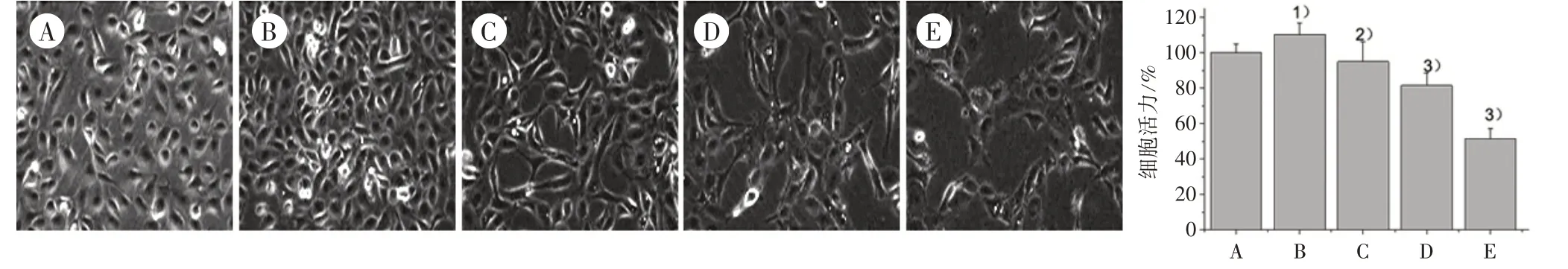
圖2 5組HLEC細(xì)胞形態(tài)及活力情況比較(×200)
3.3 5組HLEC細(xì)胞凋亡情況比較 如圖3所示,對照組細(xì)胞呈現(xiàn)弱藍(lán)色,有少許強(qiáng)熒光;VEGF-C組不僅細(xì)胞數(shù)量增加,還呈現(xiàn)出強(qiáng)熒光點(diǎn)減少,凋亡率與對照組比較明顯降低(P<0.01);各劑量組細(xì)胞數(shù)量減少,染色強(qiáng)熒光增加,且呈現(xiàn)出濃度依賴性,凋亡率與VEGF-C組比較明顯提高(P<0.01)。

圖3 5組HLEC細(xì)胞凋亡情況比較(×200)
3.4 5組HLEC細(xì)胞遷移能力比較 如圖4所示,VEGF-C組細(xì)胞遷移數(shù)目較對照組顯著增加(P<0.01)。與模型組比較,各劑量組遷移率逐漸下降(P<0.01)。
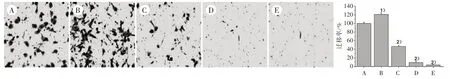
圖4 5組HLEC細(xì)胞遷移能力比較(×200)
3.5 5組HLEC細(xì)胞損傷修復(fù)能力比較 如圖5所示,JXY具有抑制HLEC損傷修復(fù)能力的作用。劃痕24 h后,對照組HLEC細(xì)胞呈現(xiàn)出較好的遷移和自我損傷修復(fù)能力;VEGF-C組細(xì)胞的自我損傷修復(fù)能力較正常組有所提高。各劑量組細(xì)胞的遷移和損傷修復(fù)能力有所下降,且呈現(xiàn)濃度依賴性。
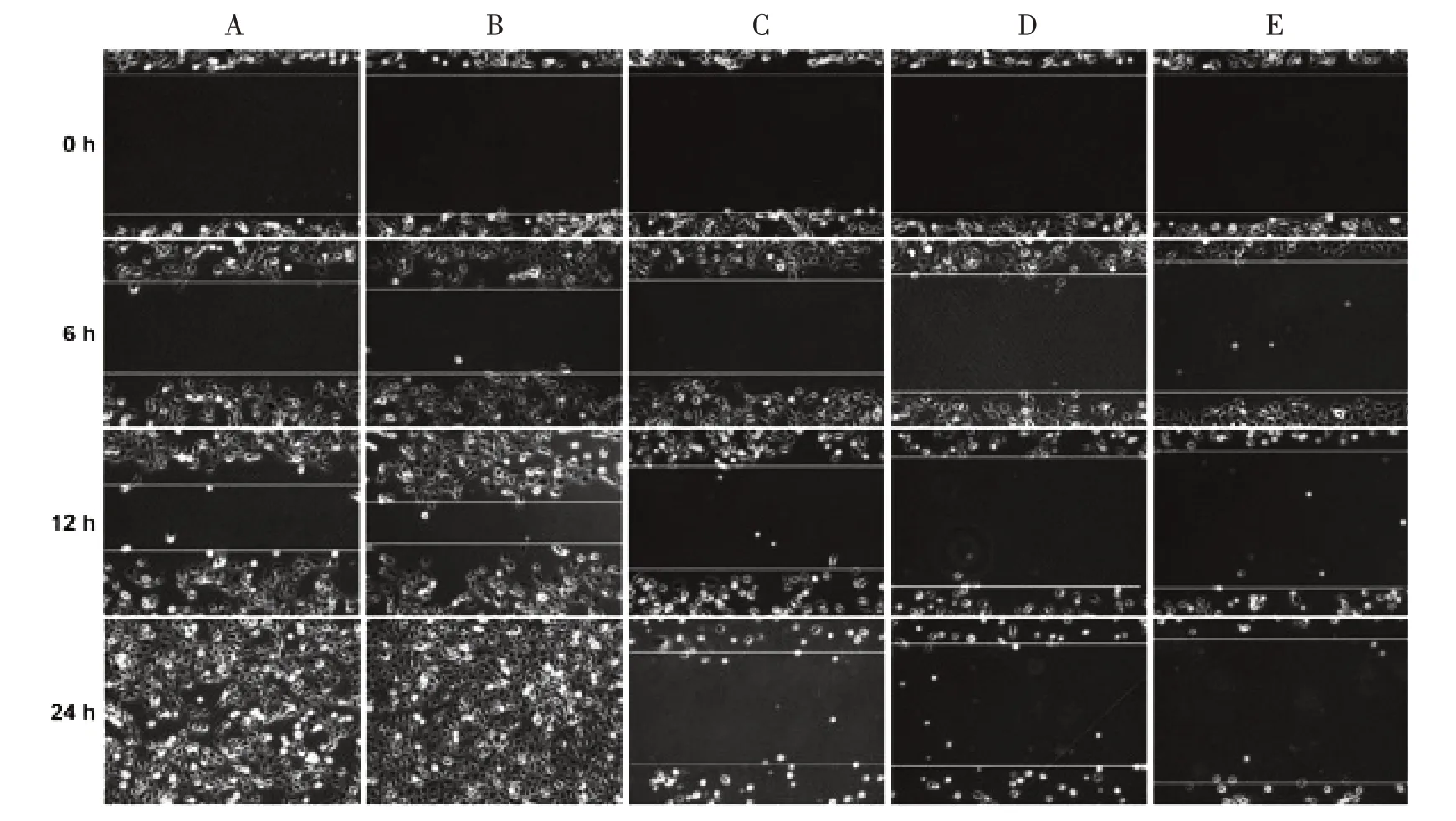
圖5 5組HLEC細(xì)胞損傷修復(fù)能力比較(×100)
3.6 5組細(xì)胞淋巴管生成情況比較 與對照組比較,VEGF-C組淋巴管生成管腔結(jié)構(gòu)更加完整,數(shù)目顯著增加(P<0.01);各劑量組幾乎不能形成管腔,與VEGF-C組比較,管腔形成數(shù)量差異具有統(tǒng)計(jì)學(xué)意義(P<0.01),見圖6。

圖6 5組細(xì)胞淋巴管生成情況比較(×100)
3.7 5組VEGFR-3、MMP-9、MMP-2蛋白表達(dá)比較 如圖7所示,與對照組比較,VEGF-C組VEGFR-3、MMP-9、MMP-2蛋白表達(dá)水平明顯升高(P<0.01);與VEGF-C組比較,各劑量組VEGFR-3、MMP-9、MMP-2蛋白表達(dá)明顯下降(P<0.01),且呈現(xiàn)劑量依賴性。
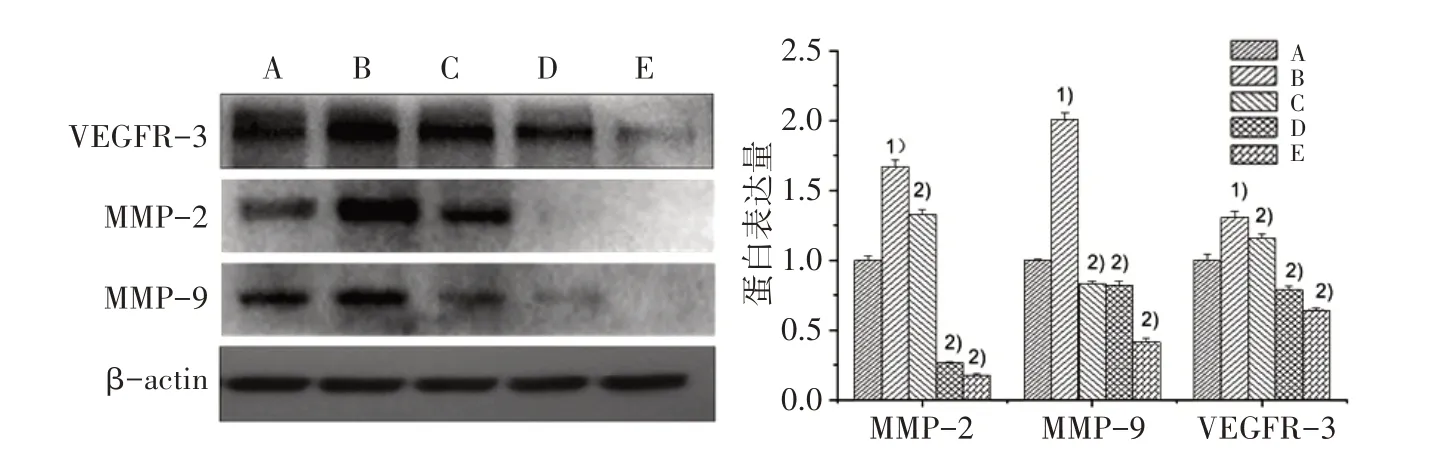
圖7 5組VEGFR-3、MMP-9、MMP-2蛋白表達(dá)比較
4 討論
淋巴管新生和重塑是腫瘤發(fā)生淋巴轉(zhuǎn)移的主要方式之一,其為腫瘤細(xì)胞提供了進(jìn)入?yún)^(qū)域淋巴結(jié)的主要通道。而腫瘤細(xì)胞通過新生淋巴管轉(zhuǎn)移至淋巴結(jié)被視為腫瘤轉(zhuǎn)移的預(yù)后指標(biāo),抑制腫瘤的淋巴管新生被認(rèn)為是抑制腫瘤轉(zhuǎn)移的有效方式,亦是腫瘤治療的重要靶點(diǎn)[7]。VEGFs家族是腫瘤血管新生與淋巴管新生的重要調(diào)控因子,腫瘤細(xì)胞分泌的VEGF-C與HLEC細(xì)胞表面的特異性受體VEGFR-3結(jié)合后,激活絲氨酸/蘇氨酸激酶AKT和ERK并使之入核,上調(diào)MMP-2、MMP-9的表達(dá),以調(diào)控HLEC細(xì)胞的增殖和遷移,進(jìn)而引起腫瘤轉(zhuǎn)移[2]。MMP-2和MMP-9同時(shí)可誘導(dǎo)VEGF-A的表達(dá),VEGF-A是目前最強(qiáng)的促腫瘤血管新生的細(xì)胞因子,其與血管內(nèi)皮細(xì)胞特異性受體VEGFR-2結(jié)合后可增強(qiáng)血管通透性、促使細(xì)胞外基質(zhì)變性、增強(qiáng)血管內(nèi)皮細(xì)胞遷移、增殖和血管形成等,進(jìn)而促進(jìn)腫瘤的發(fā)展及轉(zhuǎn)移[4,8-10]。前期研究已表明JXY具有通過調(diào)控VEGF-A及VEGFR-2的表達(dá),從而抑制體內(nèi)外肝癌血管新生的作用[11]。鑒于VEGF家族及其受體在腫瘤生長及轉(zhuǎn)移中的核心調(diào)控作用,本研究進(jìn)一步進(jìn)行了JXY對肝癌淋巴管新生的影響研究,為模擬腫瘤微環(huán)境,以VEGF-C刺激的HLEC細(xì)胞為模型,經(jīng)JXY干預(yù)后結(jié)果表明,JXY顯著抑制了體外HLEC的淋巴管生成,同時(shí)顯著下調(diào)了VEGFR-3和MMP-2、MMP-9的表達(dá)。
據(jù)報(bào)道,MMP-2和MMP-9能夠通過激活特定的細(xì)胞受體和生長因子將靶細(xì)胞從細(xì)胞外基質(zhì)中釋放出來,從而調(diào)節(jié)細(xì)胞的增殖、凋亡和遷移[8]。同時(shí),MMP-2和MMP-9可增強(qiáng)腫瘤細(xì)胞抵抗微環(huán)境中淋巴細(xì)胞對其誘導(dǎo)的凋亡。應(yīng)用MMP-2和MMP-9的抑制劑與細(xì)胞因子TNF-α及TNF受體樣凋亡誘導(dǎo)配體具有協(xié)同促凋亡作用,可增強(qiáng)化療藥物的細(xì)胞毒性[12-13]。
本研究表明JXY不僅抑制HLEC模型細(xì)胞MMP-2、MMP-9的表達(dá),同時(shí)促進(jìn)了HLEC細(xì)胞的凋亡,抑制了HLEC細(xì)胞的遷移,這可能與前期報(bào)道的JXY增強(qiáng)5-FU化療效果有直接相關(guān)性。結(jié)合前期研究結(jié)果,JXY具有顯著抑制VEGFs及其受體的作用,而VEGF家族在調(diào)控腫瘤血管新生及淋巴管新生中均起著核心作用,通過抑制其特異性受體的表達(dá)及對MMPs蛋白的調(diào)控,抑制了細(xì)胞外基質(zhì)的變性及血管內(nèi)皮細(xì)胞、HLEC細(xì)胞的增殖及遷移,誘導(dǎo)了凋亡,從而達(dá)到抑制腫瘤轉(zhuǎn)移的目的。針對JXY抑制腫瘤轉(zhuǎn)移的具體信號通路有待進(jìn)一步闡明。

