西門(mén)子 Atellica CH930 全自動(dòng)生化分析儀常規(guī)生化檢測(cè)項(xiàng)目性能驗(yàn)證
吳波 許安春 江澤友 張瓊芳 沈漪萍


【摘要】目的:對(duì)西門(mén)子Atellica CH930全自動(dòng)生化分析儀常規(guī)生化檢測(cè)項(xiàng)目:總蛋白(TP)、白蛋白(ALB)、天門(mén)冬氨酸氨基轉(zhuǎn)移酶(AST)、谷氨酸氨基轉(zhuǎn)移酶(ALT)、堿性磷酸酶(AKP)、尿素(UN)、肌酐(CREA)、尿酸(UA)、血糖(GLU)、膽固醇(Cho)、甘油三酯(TG)的分析性能進(jìn)行驗(yàn)證。方法:參考《臨床實(shí)驗(yàn)室對(duì)商品定量試劑盒分析性能的驗(yàn)證》、《臨床化學(xué)定量檢驗(yàn)程序性能驗(yàn)證指南》并結(jié)合檢驗(yàn)工作實(shí)際情況,對(duì)Atellica CH930全自動(dòng)生化分析儀測(cè)定血清總蛋白等13項(xiàng)常規(guī)生化項(xiàng)目的精密度、正確度、臨床分析測(cè)量范圍以及生物參考區(qū)間進(jìn)行驗(yàn)證和評(píng)價(jià)。結(jié)果:總蛋白等11項(xiàng)常規(guī)生化檢測(cè)項(xiàng)目在2個(gè)不同濃度水平測(cè)定的期間標(biāo)準(zhǔn)差都小于廠家規(guī)定的不精密度要求;采用室間質(zhì)評(píng)樣本作為參考物質(zhì),11項(xiàng)常規(guī)生化檢測(cè)項(xiàng)目的參考物質(zhì)偏移值小于參考物質(zhì)賦值的不確定度,驗(yàn)證廠家聲稱(chēng)可靠;驗(yàn)證的分析測(cè)量范圍分別為:TP 21.35~108.9 g/L,ALB 13.5~57.4 g/L,AST 9.5~862 U/L,ALT 11~776 U/L,AKP 11~931 U/ L,UN 2.04~48.77 mmoml/L,CREA 14.85~2400.65 Umol/L,UA 39.5~1095 mmol/L,GLU 0.75~38.27 mmol/L, Cho 0.87~7.59 mmol/L,TG 0.14~5.82 mmol/L;經(jīng)驗(yàn)證儀器自動(dòng)稀釋功能稀釋檢測(cè)后,臨床可報(bào)告范圍分別為:TP 21.35~217.8 g/L,ALB 13.5~114.8 g/L,AST 9.5~5172 U/L,ALT 11~2329 U/L,AKP 11~2793 U/L,UN 2.04~97.54 mmoml/L,CREA 14.85~12003.25 Umol/L,UA 39.5~5475 mmol/L,GLU 0.75~84.81 mmol/L,Cho 0.87~15.18 mmol/L,TG 0.14~11.64 mmol/L;生物參考區(qū)間驗(yàn)證結(jié)果均在設(shè)定的范圍之內(nèi)。結(jié)論:西門(mén)子Atellica CH930 全自動(dòng)生化分析儀測(cè)定總蛋白等11項(xiàng)常規(guī)生化項(xiàng)目的分析性能滿足廠商聲明的質(zhì)量和性能要求,符合臨床的要求,可應(yīng)用于臨床。
【關(guān)鍵詞】全自動(dòng)生化分析儀;性能驗(yàn)證;精密度;正確度
[中圖分類(lèi)號(hào)]R446.1[文獻(xiàn)標(biāo)識(shí)碼]A[文章編號(hào)]2096-5249(2022)01-0033-04
Performance evaluation of SIEMENS Atellica CH930 automatic biochemical analyzer for detecting routine biochemical testing items
WU Bo1, XUAn-chun1, JIANG Ze-you1, ZHANG Qiong-fang1, SHEN Yi-ping2* (1.Clinical Laboratory, Affiliated Hospital ofChengduUniversityofTraditional Chinese Medicine, Chengdu 610072, China;2.Clinical Laboratory ofSichuan Integrated Traditional Chinese andWestern Medicine Hospital, Chengdu, Sichuan 610041, China)
[Abstract] Objective: To evaluate the performace verification of serum routine biochemical testing items (TP、ALB、ALT、AST、AKP、UN、CREA、UA、GLU、CHO、TG) detected by SIEMENS Atellica CH930 automatic biochemical analyzer. Methods: According to clinical and practial requirements, the accuracy and precision of these items were detected by Atellica CH930, and their linear range, biological reference and maximum dilution multiple were evaluated referring to the evaluation method of“Verification of the analytical performance of commercial quantitative kits by clinical laboratories” and Guidelines for performance verification of clinical chemistry quantitative testing procedures. Results: The standard deviation of 11 routine biochemical test items such as total protein during the measurement at 2 different concentration levels meets the imprecision requirements specified by the manufacturer. Using PT samples as reference substances, the reference substance offset value of 11 items is less than the uncertainty of the reference substance assignment, which verifies that the manufacturer claims to be reliable. The analytical measurement ranges verified were: TP 21.35~108.9 g/L,ALB 13.5~57.4 g/L,AST 9.5~862 U/L, ALT 11~776 U/L, AKP 11~931 U/L, UN 2.04~48.77 mmoml/L, CREA 14.85-2400.65 Umol/L,UA 39.5-1095 mmol/L,GLU 0.75-38.27 mmol/ L,Chol 0.87~7.59 mmol/L,TG 0.14~5.82 mmol/L. After the dilution test of the automatic dilution function of the verified instrument, the clinical reportable ranges were: TP 21.35~217.8 g/L,ALB 13.5~114.8 g/L,AST 9.5~5172 U/L, ALT 11~2329 U/L, AKP 11~2793 U/L, UN 2.04~97.54 mmoml/L, CREA 14.85~12003.25 Umol/L,UA 39.5~5475 mmol/L,GLU 0.75~84.81 mmol/L,Chol 0.87~15.18 mmol/L,TG 0.14~11.64 mmol/L. Biological reference interval verification results are within the set range. Conclusion: The main analysis performance of SIEMENS Atellica CH930 automatic biochemical analyzer meets the manufacturer’s declared quality and performance requirements, meets the clinical requirements, and can be used in clinical applications.
[Key words] Automatic biochemical analyzer; Performance verification; Precision; Accuracy
TP 等11項(xiàng)常規(guī)生化項(xiàng)目是評(píng)估患者基本狀態(tài)的常用指標(biāo)。TP、ALB、AST、ALT、AKP 用于肝功能檢測(cè),UN、CREA、UA 用于腎功能評(píng)估,GLU 作為糖尿病篩查,CHO、TG 用于脂代謝評(píng)估。筆者參考《臨床實(shí)驗(yàn)室對(duì)商品定量試劑盒分析性能的驗(yàn)證》[1]《臨床化學(xué)定量檢驗(yàn)程序性能驗(yàn)證指南》[2] 并結(jié)合檢驗(yàn)實(shí)際,對(duì)Atellica CH930全自動(dòng)生化分析儀測(cè)定TP 等11項(xiàng)常規(guī)生化項(xiàng)目的精密度、正確度、分析測(cè)量范圍和生物參考區(qū)間進(jìn)行驗(yàn)證和評(píng)價(jià)。
1 材料和方法
1.1材料儀器西門(mén)子Atellica CH930全自動(dòng)生化分析儀。試劑:①西門(mén)子Atellica CH930配套試劑、校準(zhǔn)品;②朗道質(zhì)控血清水平2,3。樣本:選取成都中醫(yī)藥大學(xué)附屬醫(yī)院2020年4月至5月門(mén)診和住院部患者標(biāo)本,3000 r/min 離心10 min,取血清檢測(cè)。排除標(biāo)準(zhǔn):嚴(yán)重脂血、溶血、黃疸樣本。
1.2方法①精密度驗(yàn)證:本次驗(yàn)證5 d 共計(jì)5 個(gè)批次,每批需檢測(cè)高、低兩個(gè)濃度血清。每次測(cè)量前按照制造商建議校準(zhǔn),測(cè)量前后均進(jìn)行室內(nèi)質(zhì)控檢測(cè),如有失控,則棄去,重新增加1個(gè)批次。每個(gè)批次需要重復(fù)測(cè)量3次。根據(jù)公式[3]分別計(jì)算重復(fù)標(biāo)準(zhǔn)差(Sr),期間標(biāo)準(zhǔn)差(Sl),廠家聲稱(chēng)值σl,根據(jù)計(jì)算值進(jìn)行相應(yīng)判斷。②正確度驗(yàn)證:正確度驗(yàn)證進(jìn)行5個(gè)批次,每個(gè)批次測(cè)定2次,選取2019年第二次、第三次常規(guī)化學(xué)室間質(zhì)評(píng)樣本作為參考物質(zhì)進(jìn)行測(cè)量。校準(zhǔn)、室內(nèi)質(zhì)控的要求同精密度驗(yàn)證。按照公式[3]分別計(jì)算測(cè)量均值(x)、標(biāo)準(zhǔn)差(SX)及參考物質(zhì)測(cè)量偏移值(b參),將計(jì)算值與參考物質(zhì)賦值的不確定度(Sa)進(jìn)行比較,如測(cè)定值大于 Sa,則需要將驗(yàn)證區(qū)間與賦值進(jìn)行比較。③分析測(cè)量范圍驗(yàn)證:按照參考文獻(xiàn)[4-6],選取5~7個(gè)濃度樣本,要求盡量覆蓋廠家聲稱(chēng)的線性范圍。準(zhǔn)備高、低值濃度樣本,分別命名樣本5(H)和樣本1(L),按照4L、3 L+1 h、2 L+2 h、2 L+3 h、4 h 關(guān)系配置,形成系列濃度梯度,每個(gè)濃度水平至少測(cè)定2次。校準(zhǔn)及室內(nèi)質(zhì)控要求同精密度驗(yàn)證。根據(jù)公式計(jì)算線性回歸方程和相關(guān)系數(shù) r ,若 r >0.995,用 SPSS19.0統(tǒng)計(jì)軟件進(jìn)行曲線回歸分析,若最佳擬合曲線為一階,則線性驗(yàn)證通過(guò),若最佳擬合曲線為二階或者三階,則需要進(jìn)行精密度驗(yàn)證以判斷該非線性能否為臨床可接受,將實(shí)測(cè)值的隨機(jī)誤差范圍與線性理論值的允許總誤差范圍進(jìn)行比較,實(shí)測(cè)值的隨機(jī)誤差范圍應(yīng)小于線性理論值的允許總誤差范圍,否則降低濃度重新計(jì)算。④稀釋倍數(shù)驗(yàn)證:取1份高濃度標(biāo)本分成兩份,一份不做任何處理,一份按照制造商建議的稀釋倍數(shù)做自動(dòng)稀釋?zhuān)總€(gè)樣本重復(fù)檢測(cè)4次,計(jì)算稀釋檢測(cè)值和理論值的偏差,判斷標(biāo)準(zhǔn)為1/2 總允許誤差范圍。⑤生物參考區(qū)間驗(yàn)證:參考 CLSIC28-A2文件[7],選取健康體檢者各20例,根據(jù)項(xiàng)目要求分性別、年齡進(jìn)行參考區(qū)間驗(yàn)證。按照實(shí)驗(yàn)室規(guī)定的操作程序進(jìn)行檢測(cè),將檢數(shù)據(jù)進(jìn)行統(tǒng)計(jì)并與待驗(yàn)證的參考區(qū)間進(jìn)行比較,若20例樣本的檢測(cè)數(shù)據(jù)不超過(guò)兩份標(biāo)本超出待驗(yàn)證參考區(qū)間,則驗(yàn)證通過(guò)。否則,需要進(jìn)行確認(rèn)實(shí)驗(yàn)。
1.3統(tǒng)計(jì)學(xué)處理使用 SPSS19.0統(tǒng)計(jì)軟件進(jìn)行數(shù)據(jù)分析。
2 結(jié)果
2.1精密度驗(yàn)證結(jié)果11項(xiàng)常規(guī)生化項(xiàng)目精密度驗(yàn)證結(jié)果,詳見(jiàn)表1。
2.2正確度驗(yàn)證結(jié)果11項(xiàng)常規(guī)生化項(xiàng)目正確度驗(yàn)證結(jié)果,詳見(jiàn)表2。
2.3分析測(cè)量范圍及稀釋倍數(shù)驗(yàn)證11項(xiàng)常規(guī)生化項(xiàng)目分析測(cè)量范圍及臨床可報(bào)告范圍驗(yàn)證,詳見(jiàn)表 3。
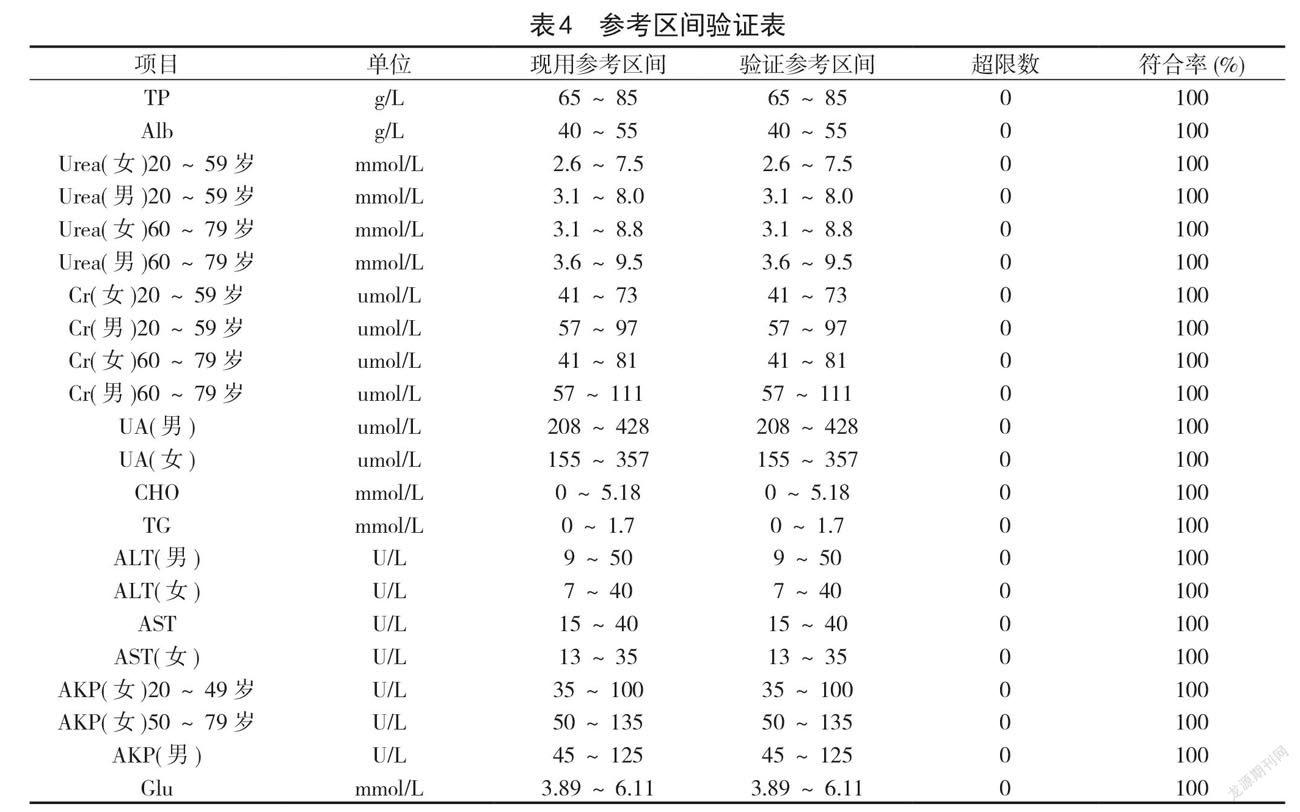
2.4參考區(qū)間驗(yàn)證參考區(qū)間驗(yàn)證數(shù)據(jù)詳見(jiàn)表4。
3 討論
按照《醫(yī)療機(jī)構(gòu)臨床實(shí)驗(yàn)室管理辦法》的要求 [8-9],臨床實(shí)驗(yàn)室為了保證檢驗(yàn)結(jié)果的準(zhǔn)確性,應(yīng)對(duì)所選購(gòu)的試劑盒進(jìn)行性能驗(yàn)證,以此保證其能滿足在臨床使用,分析測(cè)量,經(jīng)濟(jì)技術(shù)等各方面的要求 [10]。本實(shí)驗(yàn)對(duì)Atellica全自動(dòng)生化分析儀進(jìn)行了包括 TP 等11項(xiàng)常規(guī)生化項(xiàng)目的不精密度、不準(zhǔn)確度、分析測(cè)量范圍、生物參考區(qū)間驗(yàn)證,以此來(lái)了解Atellica系統(tǒng)的分析性能。
精密度經(jīng)常被用于評(píng)價(jià)檢測(cè)系統(tǒng)的穩(wěn)定性,是性能分析和評(píng)價(jià)的基礎(chǔ)和前提[11]。從表1的結(jié)果分析來(lái)看,11個(gè)項(xiàng)目5個(gè)批次在兩個(gè)濃度水平的期間標(biāo)準(zhǔn)差均小于制造商聲明的分析性能,具有良好的精密度,滿足性能要求。
正確度也是系統(tǒng)誤差的衡量指標(biāo),用于評(píng)估靶值與實(shí)際檢測(cè)值的差異[12]。正確度的驗(yàn)證有多種方式,可以使用患者樣本,也可以采用參考物質(zhì)[13]。本研究使用衛(wèi)健委臨檢中心2019年第二次、第三次常規(guī)化學(xué)室間質(zhì)評(píng)樣本,從表2的結(jié)果可以看出,部分常規(guī)生化項(xiàng)目的參考物質(zhì)偏移值大于參考物質(zhì)賦值的不確定度,通過(guò)自由度計(jì)算驗(yàn)證區(qū)間上下限,所測(cè)均值在驗(yàn)證區(qū)間范圍內(nèi),亦驗(yàn)證廠家聲稱(chēng)可靠。
線性范圍即標(biāo)本在未經(jīng)濃縮、稀釋等預(yù)處理的情況下可被直接測(cè)定出檢測(cè)物的范圍[14],是方法學(xué)性能的又一衡量指標(biāo)。因高濃度樣本臨床不易得,本實(shí)驗(yàn)均選用較高濃度樣本進(jìn)行線性范圍驗(yàn)證。從表3看出,11項(xiàng)常規(guī)生化項(xiàng)目的相關(guān)系數(shù) r2>0.999,線性驗(yàn)證符合要求。同時(shí),通過(guò)對(duì)儀器自動(dòng)稀釋倍數(shù)的驗(yàn)證,可以給予臨床更大的臨床可報(bào)告范圍,滿足臨床診斷和治療的要求。
生物參考區(qū)間是95%“正常”值范圍,實(shí)驗(yàn)室應(yīng)保證檢驗(yàn)項(xiàng)目的生物參考區(qū)間具有正確性和適用性 [15]。本試驗(yàn)根據(jù)檢測(cè)項(xiàng)目的具體要求,將健康體檢者按照年齡、性別進(jìn)行分組驗(yàn)證,結(jié)果表明,11項(xiàng)指標(biāo)的驗(yàn)證符合率及項(xiàng)目分組參考區(qū)間符合率均≥ 95%,20例樣本的血清濃度均在驗(yàn)證的參考區(qū)間范圍內(nèi),則認(rèn)為此參考區(qū)間適用于本實(shí)驗(yàn)室。
綜上所述,本研究參考試劑制造商、CLSI 文件,對(duì)Atellica CH930全自動(dòng)生化分析儀上檢測(cè)的 TP 等11項(xiàng)常規(guī)生化項(xiàng)目的性能進(jìn)行了驗(yàn)證和評(píng)估,基本與試劑制造商的聲明一致,該檢測(cè)系統(tǒng)可用于臨床。
參考文獻(xiàn)
[1]尚紅 , 王毓三 ,申子瑜.全國(guó)臨床檢驗(yàn)操作規(guī)程[M].北京:人民衛(wèi)生出版社 , 2015:320-326.
[2]中國(guó)合格評(píng)定國(guó)家認(rèn)可委員會(huì).臨床化學(xué)定量檢驗(yàn)程序性能驗(yàn)證指南[S]. CNAS-GL37:2019.
[3]中華人民共和國(guó)國(guó)家衛(wèi)生和計(jì)劃生育委員會(huì).臨床實(shí)驗(yàn)室對(duì)商品定量試劑盒分析性能的驗(yàn)證[S].WS/T 420-2013.
[4]王治國(guó).臨床檢驗(yàn)方法確認(rèn)與性能驗(yàn)證[M].北京:人民衛(wèi)生出版社 , 2009:153-159.
[5] 馮仁豐.臨床檢驗(yàn)質(zhì)量管理技術(shù)基礎(chǔ)第二版[M].上海科學(xué)文獻(xiàn)技術(shù)出版社 , 2008:111-138.
[6]張秀明 , 莊俊華 , 鄭松柏 , 等.臨床化學(xué)發(fā)光免疫法檢測(cè)AFP 的分析性能驗(yàn)證與實(shí)驗(yàn)方法[J].中華檢驗(yàn)醫(yī)學(xué)雜志 ,2007, 30(11): 1293.
[7]CLSI C28-A2. how to define and determine referenceintervals in the clinical laboratory, 2000:1-31.
[8]黃勤烽 , 黃少鈴 , 王美珠 , 等.羅氏尿微量清蛋白檢測(cè)試劑盒性能評(píng)價(jià)[J]. 國(guó)際檢驗(yàn)醫(yī)學(xué)雜志 , 2016, 37(15):2055-2057.
[9]于淼琛 , 孫芹敏 , 姜鳳全.強(qiáng)生 VITROS 5600全自動(dòng)生化免疫分析儀性能驗(yàn)證報(bào)告[J]. 國(guó)際檢驗(yàn)醫(yī)學(xué)雜志 , 2017, 38(1):56-60.
[10]國(guó)家衛(wèi)生和健康委員會(huì). 《醫(yī)療機(jī)構(gòu)臨床實(shí)驗(yàn)室管理辦法》. [EB/OL].(2018-08-16)https://www. nccl. org. cn/showSearchDetail?code=07&id=4
[11]張秀明 , 范勇利 , 溫冬梅 , 等.臨床化學(xué)自建檢測(cè)系統(tǒng)性能確認(rèn)的精密度與正確度及準(zhǔn)確度的研究[J].中華檢驗(yàn)醫(yī)學(xué)雜志 , 2016, 39(9):715-719.
[12]張?jiān)娫?shī) , 王薇 , 趙海建 , 等.臨床化學(xué)檢驗(yàn)中精密度、正確度、總誤差和測(cè)量不確定度的討論[J].臨床檢驗(yàn)雜志 , 2017, 35(9):641-643.
[13]徐建華 , 莊俊華 , 鄭松柏 , 等.常規(guī)方法檢測(cè)血清總膽紅素的正確度評(píng)價(jià)[J].臨床檢驗(yàn)雜志 , 2012, 30(12):946-949.
[14]吳金斌 , 歐嘉文. VITROS5600分析儀檢測(cè)3項(xiàng)心肌損傷標(biāo)志物的性能評(píng)價(jià)[J].檢驗(yàn)醫(yī)學(xué)與臨床 , 2015, 12(2):3256-3259.
[15]趙有利 , 姜雯雯 , 李飛 , 等.羅氏 Cobas8000全自動(dòng)生化分析儀檢測(cè)心肌酶譜的性能評(píng)價(jià)[J].國(guó)際檢驗(yàn)醫(yī)學(xué)雜志 ,
2020, 41(5):540-543.
作者簡(jiǎn)介:吳波(1981-),漢族,四川汶川人,碩士,主管技師,研究方向:臨床生化檢驗(yàn)。
*通信作者:沈漪萍,四川省中西醫(yī)結(jié)合醫(yī)院檢驗(yàn)科。 E-mail:2079075856@qq.com
(收稿日期:2021-6-29 接受日期:2021-8-20)

