內科胸腔鏡確診表現為大量胸腔積液的胸膜肺結節病1例并文獻復習
談潔 于晶 陳文靜 閆冰迪
結節病是一種累及全身多系統的肉芽腫性疾病,原因未明,最易侵犯肺組織,其中累及胸膜者稱為胸膜肺結節病(pleuropulmonary sarcoidosis,PPS)。PPS患者胸膜結節可與肺結節同時出現,也可繼發于肺結節之后,臨床上多表現為胸悶、氣促等胸腔積液的表現,易誤診為結核性胸腔積液、惡性胸腔積液。本文通過報道一例經內科胸腔鏡確診的PPS,提高廣大醫生對PPS的認識。
臨床資料
患者,女,52歲,以“胸悶、氣短6個月”為主訴入院。患者6個月前無明顯誘因出現胸悶、氣短,活動后加重,自行口服藥物治療,癥狀略緩解,未正規診治。6個月來上述癥狀反復加重,1天前于我院門診行胸部CT檢查示右肺門軟組織密度影,兩肺多發結節,縱隔多發淋巴結,右側大量胸腔積液(見圖1)(A、B),為求進一步診治收入我科。入院查體:體溫:36.7 ℃,心率:76次/分,呼吸:18次/分,血壓:125/75 mmHg。右下肺語顫減弱,語音傳導減弱,右肺呼吸音弱,左肺呼吸音正常,未聞及干濕性啰音及胸膜摩擦音,未觸及淺表淋巴結腫大。余查體無明顯異常。入院后肝功示總蛋白 64.3 g/L,白蛋白39.1g/L,血沉17.0 mm,ANA譜示抗線粒體M2抗體:++;TO-1抗體:++;余化驗檢查均未見明顯異常。行胸腔穿刺術引流出黃色胸腔積液,胸水常規:白細胞總數3600×106/L、李凡他實驗 +,多核>單核;胸水生化:總蛋白10.5 g/L,葡萄糖 9.28 mmol/L,腺苷脫氨酶 15.85 U/L,乳酸脫氫酶 119.0 U/L,氯 109.0 mmol/L。胸水脫落細胞:見大量淋巴細胞、紅細胞,少量間皮細胞及噬細胞,未見惡性細胞。因未能明確診斷,遂行內科胸腔鏡探查:見右側臟層胸膜與壁層胸膜黏膜多發隆起,表面覆蓋有壞死,于黏膜隆起處多次鉗夾組織送檢(見圖2)(A、B)。病理回報(右側壁層胸膜活檢)見多量慢性肉芽腫性炎,周邊有少量纖維素樣滲出,并見有較多慢性炎細胞浸潤,不除外結節病(見圖3)(A、B)。明確診斷為胸膜肺結節病,給予口服醋酸潑尼松片25mg/d治療,1周后患者呼吸困難癥狀較前略有改善,1個月后患者癥狀基本消失,復查胸部CT:右肺門軟組織影未見明顯變化,右肺下葉結節減小,右側胸腔積液完全吸收(見圖4)(A、B),激素逐漸減量,2個月后復查胸部CT,結節較前減小,右側胸膜增厚(見圖5)(A、B),半年后復查胸部CT:雙肺結節影較前減少,右肺下葉結節影較前減小。右側胸膜增厚(見圖6)(A、B),停藥觀察。

圖1 A、B 胸部CT雙肺見多發結節狀高密度影,較大者位于右肺下葉(IM42),邊緣毛糙,牽拉胸膜,右側胸腔內見液體密度影

圖2 A、B 內科胸腔鏡下見右側臟層胸膜與壁層胸膜黏膜多發隆起,表面覆蓋有壞死
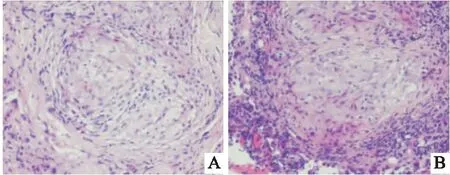
圖3 A、B病理 HE染色(×200)多量慢性肉芽腫性炎,周邊少量纖維素樣滲出,并見較多慢性炎細胞浸潤
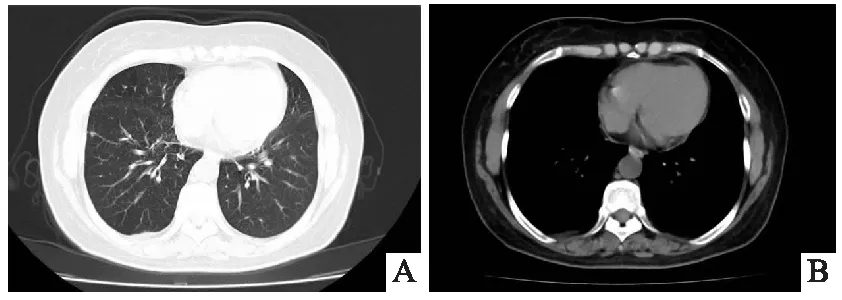
圖4 A、B 胸部CT 雙肺可見結節狀高密度影,較大者位于右肺下葉(IM32),直徑約5 mm,縱隔可見多發淋巴結顯示,兩側胸腔未見液體密度影
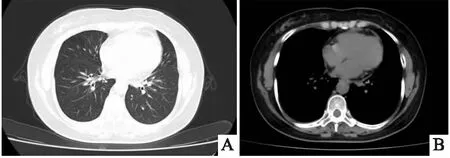
圖5 A、B 胸部CT 雙肺可見散在結節影,最大者于右肺下葉(IM35)直徑約3mm。右側胸膜增厚

圖6 A、B 胸部CT 雙肺結節影較前減少,右肺下葉結節影較前較小。右側胸膜增厚
討 論
結節病(PPS)是一種原因不明的非壞死性肉芽腫性疾病,可累及全身多系統,肺和淋巴系統最常受累,其病理特征主要表現為非干酪樣壞死性肉芽腫性改變。有文獻稱約90%的結節病可累及于肺部,胸膜組織受累少見[1]。外國學者在上世紀90年代初已經提出PPS的概念[2],但在國內尚未有明確的診斷標準。肺結節病需要依靠病理組織活檢結果確診,然當其累及胸膜時,其病理表現極易與結核性胸膜炎的慢性干酪樣肉芽腫性炎相混淆。但近年來通過對內科胸腔鏡技術的廣泛開展,人們對PPS的認識不斷提高,診斷率不斷上升。Huggins[3]等對國外181例結節病患者進行研究,發現伴有胸腔積液表現的患者占2.8%,并且只有1.1%是由胸膜結節所致,提出結節病患者的胸腔積液可能與結節病無關的觀點。孫永昌等[4]對國內發表的結節病病例進行總結,發現結節病胸膜病變的發生率為3.4%~16.7%。結節病的病因與發病機制目前仍無確切的說法,其病因考慮可能與慢性炎癥、免疫、遺傳及環境等多種因素相關[5]。此外有研究表明Th17細胞不僅參與結節病中肺泡/肉芽腫生成的過程,也參與了肺纖維化的過程,在激素治療過程中可能也發揮著重要作用[6]。
PPS主要表現為胸膜增厚、胸膜結節、胸腔積液和氣胸,其中胸膜增厚和胸膜結節常同時出現,胸腔積液相對少見,氣胸則多出現于疾病晚期,可能與肉芽腫侵犯胸膜,導致胸膜破裂有關[5]。其臨床表現以胸膜病變的常見癥狀為主,比如低熱、咳嗽、氣促、胸悶、胸痛、呼吸困難等,部分患者在查體時可發現腫大的淺表淋巴結。部分患者實驗室檢查可出現白細胞減少,血沉增快,C反應蛋白升高等。亦有研究表示腫標中CA125會輕度升高,腺苷脫氨酶可能降低。以胸腔積液為主要臨床表現的PPS患者,胸水常為滲出性,部分可遷延為纖維素性胸膜炎。
PPS的胸部影像學表現多為肺門及縱隔淋巴結腫大,單雙側均可出現。國外學者將其胸部X線表現分為4期[7],國內病例Ⅱ期多見,其胸部CT多表現為肺門、縱隔淋巴結增大伴有胸腔積液[8]。PPS患者內科胸腔鏡下多表現為大小不等的結節,彌漫性分布于壁層、臟層胸膜上,呈白色、灰白色或粉紅色,甚至可累及膈肌,同時可伴有結節周圍胸膜充血水腫。若患者存在有內科胸腔鏡探查的禁忌時,纖維支氣管鏡活檢及淺表淋巴結穿刺活檢,也可以幫助診斷該病。PPS的活檢病理組織多表現為非干酪性壞死性肉芽腫性炎,免疫組化及抗酸染色均為陰性。PPS的確診以病理組織活檢結果為金標準,同時應結合患者臨床表現、實驗室化驗及影像學等輔助檢查,排除其他肉芽腫性疾病。其治療方案與結節病基本一致,糖皮質激素一般可以獲得較好的療效,部分患者需同時聯用免疫抑制劑、細胞毒性藥物等。但注意使用中必須要嚴格隨訪,根據患者狀態調整激素用量,避免激素相關性肺結核的發生[9]。
本例患者初期表現為胸悶、氣短等典型胸腔積液壓迫肺組織的癥狀,但因患者未前往醫院進行正規診治,無法判斷患者當時病情嚴重程度。入院時胸部CT表現為雙肺多發結節,右肺門軟組織影及縱隔淋巴結腫大,右側大量胸腔積液,易誤診為肺癌。胸水為黃色滲出液,內科胸腔鏡下表現為壁層及臟層胸膜彌漫性分布的白色結節,大小不等,易與結核性胸膜炎或肺癌等惡性腫瘤的胸膜轉移相混淆。
由此可見,PPS的臨床表現無特殊性,僅靠臨床癥狀、影像學表現及實驗室指標極易誤診為結核或惡性腫瘤,進行組織活檢的病理結果是確診該病的可靠手段。本例患者入院后經胸腔穿刺術未能明確診斷,行內科胸腔鏡下組織病理活檢后明確診斷為PPS,給予激素治療有效,定期復查胸部CT見右肺門軟組織影、兩肺結節及縱隔淋巴結較前明顯縮小或消失。證明內科胸腔鏡對于胸膜疾病的診斷而言是一種行之有效的技術手段,當胸腔積液患者經胸腔穿刺術不能明確診斷其病因時,可考慮行內科胸腔鏡進行檢查,以免延誤疾病的診斷及治療。

