三黃紫參油治療濕疹作用機制探討
楊永健,李麗娟,龐永誠,萬青,熊瑤
1 昆明市中醫醫院 云南昆明 650000 2 昆明市西山區永昌衛生服務中心 云南昆明 650000
濕疹(eczema),是一種發生于真皮淺層及表皮的病因不明的炎癥性皮膚病,臨床分急性(原發性和多形性皮疹)、慢性(苔蘚樣變)、亞急性三個時期,其發病可能與慢性感染灶、內分泌及代謝改變、血液循環障礙、神經精神因素、食物、吸入物、生活環境等內外因素因素相互作用有關,少數可能由遲發性過敏反應介導[1,2]。濕疹是一種常見病、多發病,我國社區人群發病率7.50%[3]~9.26%[4],兒童發病率高達18.71%[5]。濕疹發作時瘙癢難耐,易反復發作,通常需要長期用藥,給患者家庭造成巨大經濟負擔,嚴重影響患者身心健康[6]。目前,控制癥狀、減少復發、提高患者生活質量是濕疹的治療原則,外用糖皮質激素、外用鈣調磷酸酶抑制劑、抗組胺藥是一線治療藥物[7]。鈣調磷酸酶抑制劑使用初期可致皮膚灼熱感、刺痛感和瘙癢加重;抗組胺藥可出現困倦、嗜睡等;長期外用糖皮質激素可致局部皮膚萎縮、毛細血管擴張、色素沉著、激素依賴性皮炎等局部并發癥,盡管全身不良反應風險較低[8],但濕疹皮膚的藥物經皮吸收率增加[9]導致下丘腦-垂體-腎上腺軸抑制、血糖升高、血壓升高等全身不良反應風險升高。通常,一線治療藥物可快速控制輕中度濕疹發作,但濕疹的反復發作性、藥物的短期和長期不良反應以及患者對不良反應的焦慮,使患者依從性降低、用藥不規范,導致病情進一步的惡化遷延,導致患方負擔增加。
中醫藥,廣泛用于濕疹治療,具有療效好、不良反應少的優勢,可明顯緩解癥狀、減少復發,提高患者生活質量,減輕患者身心和經濟負擔[10]。
濕疹,中醫屬“濕瘡”范疇,張仲景·《金匱要略》稱“浸淫瘡”,歷代醫家據發病部位不同又有“旋耳瘡”“臍瘡”“腎囊風”等稱謂。論其病機,總由稟性不耐,風濕熱之邪客于肌膚而成;或因脾胃虛弱、運化失調;或進食發物;或情志不遂等[2,11-13]。急性者以濕熱為主;亞急性者多與脾虛不運、濕邪留戀有關;慢性者因病久傷血、血虛生風生燥,肌膚失去濡養而成[14]。
三黃紫參油是作者所擬外用方,以黃芩、黃連、黃柏等九味中藥同芝麻油用紫外線燈消毒后泡制2周而成。方中三黃(黃芩、黃連、黃柏)、白鮮皮、紫草、艾葉清熱燥濕,紫草、丹參凉血,丹參、雞血藤養血生新,三七、雞血藤、紫草、丹參活血通絡。全方共奏清熱燥濕祛邪、活血養血生新之效。芝麻油劑,制備簡便,清潔、軟化、保護濕疹皮膚[1],且有強抗氧化活性[15]。此方功效主治與濕疹病機相投,故臨床治療濕疹療效良好。
因濕疹病因不明,且三黃紫參油作用機制不明,故本研究運用中藥網絡藥理學方法[16],對三黃紫參油治療濕疹的潛在活性成分、作用靶點及有關分子通路分析總結,為該方提供細胞分子層面的理解。
材料與方法
1 藥物治療疾病的關鍵成分、靶點預測,構建構建藥物-成分-靶點-疾病網絡拓撲網
使用TCMSP數據庫(https://tcmsp-e.com/)搜索三黃紫參油組方藥物的活性成分和靶點,根據成分ADME參數進行篩選,相對分子量(MW)≤800U(分子量≤800U的藥物表皮透入性大[9,17]),藥物相似性( DL)≥0.18篩選藥物主要活性成分和對應靶點。通過Uniprot 數據庫(https://www.uniprot.org/) 將篩選出的靶蛋白名稱轉化為Gene names并標準化。
以濕疹的英語名稱“eczema”在DisGeNET(https://www.disgenet.org/)數據庫中進行檢索,設置疾病相關性≥0.1獲取濕疹相關的疾病靶點。
應用python語言處理三黃紫參油化學成分靶點和濕疹相關的疾病靶點,獲得三黃紫參油組分與濕疹交集靶點,即為三黃紫參油治療濕疹的關鍵靶點,并繪制韋恩圖;在STRING 數據庫 (https://stringdb.org/ ),輸入關鍵靶點,查詢關鍵靶點信息。
使用python語言通過關鍵靶點提取關鍵成分、藥物數據,合并數據導入 Cytoscape 3.7.2 軟件,構建“藥物-成分-靶點-疾病”網絡。
2 關鍵成分的藥物經皮滲透性預測
研究表明[18],Potts-Guy模型的預測性能最佳,使用Potts-Guy模型的預測各關鍵成分的藥物經皮 滲 透 性。Potts-Guy模 型:Log Kp=0.71 log Kow -0.0061MW-6.3。
3 關鍵靶點基因功能(GO)功能富集分析和KEGG 通路富集分析
將藥物-疾病共同靶基因導入 DAVID 6.8 數據庫(https://david.ncifcrf.gov/),限定物種為“Homo Sapiens”,獲取靶基因功能GO和KEGG富集通路,取P<0.05,分析生物過程(BP)、細胞組分(CC)、分子功能( MF)、KEGG通路,繪制柱狀圖。
結 果
1 藥物治療疾病的關鍵成分、靶點預測,構建藥物-成分-靶點-疾病網絡拓撲網
在TCMSP檢索三黃紫參油組方得到有效成分106種,如槲皮素、烏索酸、次黃芩素等;作用靶點388個,如前列腺素G/H合酶1、白介素-6等。在Dis-GeNET檢索“eczema”得到濕疹的251個疾病靶點,如絲聚合蛋白原、白介素6受體、白介素13、腫瘤壞死因子等。應用python語言處理藥物靶點和疾病靶點,得到8個共同靶點,即三黃紫參油治療濕疹的關鍵靶點,繪制韋恩圖,見圖1;在STRING 數據庫查詢關系靶點信息,制表,見表1。

表1 關鍵靶點名稱和功能
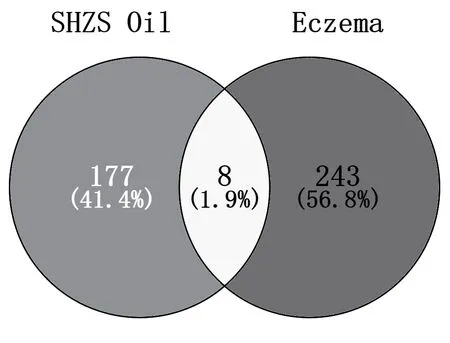
圖1 濕疹與三黃紫參油活性成分靶點
分析、整理數據,導入 Cytoscape 3.7.2 軟 件,得到“藥物-成分-靶點-疾病-通路”網絡,分析數據,導入 Cytoscape 3.7.2 軟 件,得到“藥物-成分-靶點-疾病”網絡,左邊綠色小圈表示三黃紫參油的9種藥物組成,藥物圈外圍淺藍色大圈表示三黃紫參油治療濕疹的17種關鍵成分,右邊黃色矩形為濕疹,矩形和雙圈之間的青色圈表示三黃紫參油治療濕疹的8個關鍵靶點,見圖2。

圖2 藥物-成分-靶點-通路-疾病拓撲網絡
2 關鍵成分的藥物經皮滲透性預測
在TCMSP數據庫查詢關鍵成分相關理化性質,Potts-Guy模型預測顯示17種關鍵成分均具有較好的藥物經皮滲透性。見表2。
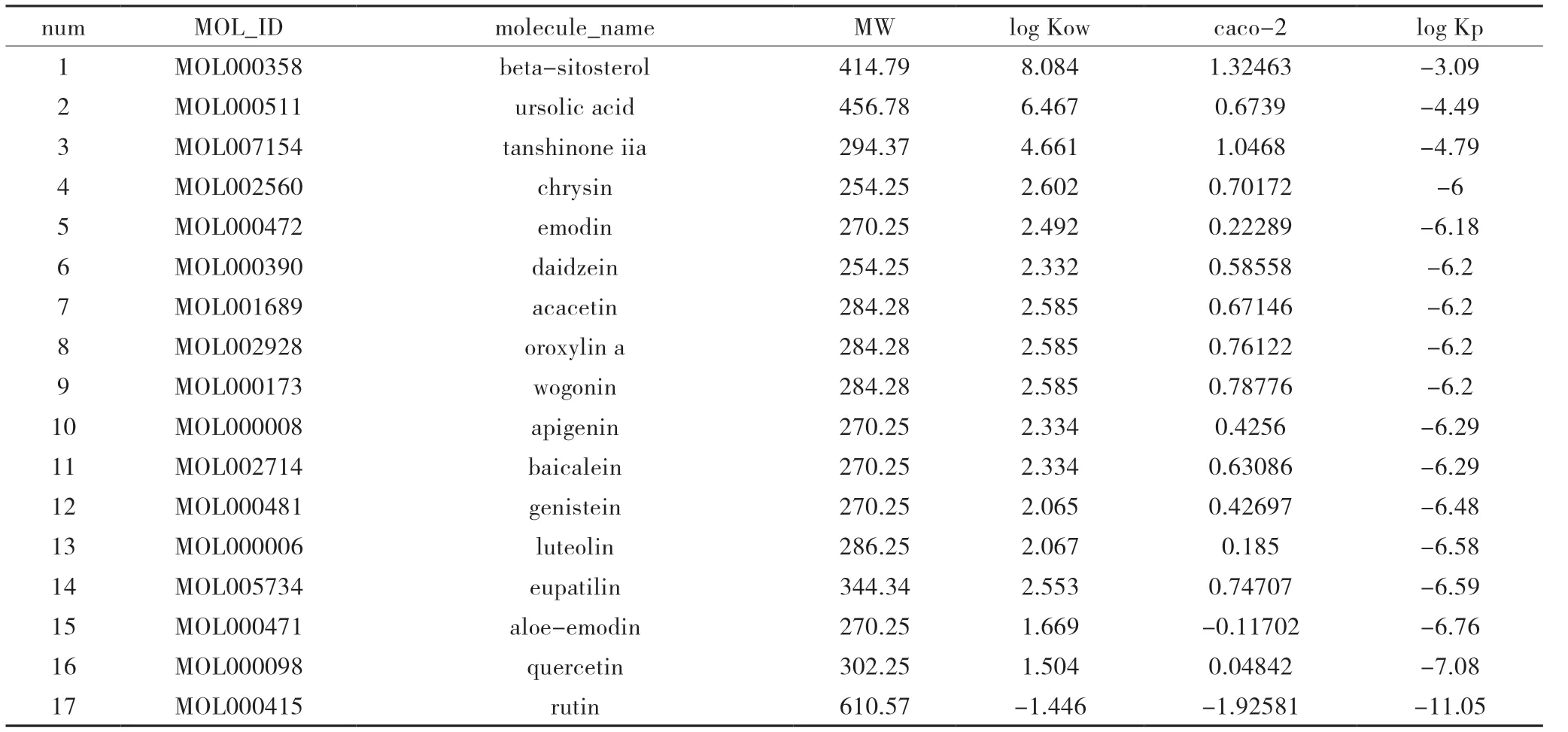
表2 有效成分腸上皮通透性和藥物經皮滲透性
3 關鍵靶點基因功能(GO)富集分析和KEGG 通路富集分析
在 DAVID 數據庫中對三黃紫參油-濕疹疾病的8個共同靶標進行 GO 富集分析(P<0.05)和KEGG通路富集分析(P<0.05),得到生物學過程BP(Biological Process)15個,細胞組分CC(Cellular Component)2個,分子功能MF(Molecular Function)1個,KEGG通路3條,可視化處理后見圖3。
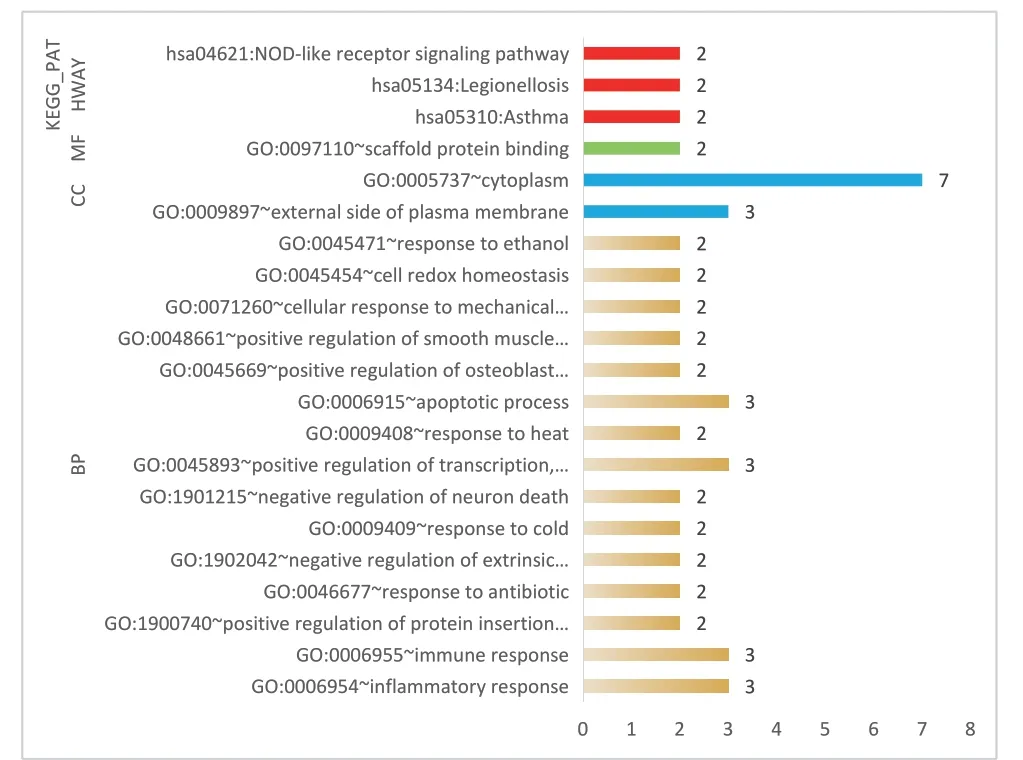
圖3 GO和KEGG通路富集分析
4 GO 富集分析分析
生物過程(BP),共同作用靶點富集在炎癥應答(inflammatory response),免 疫 應 答(immune response),凋亡信號通路中線粒體膜蛋白插入的正調控(positive regulation of protein insertion into mitochondrial membrane involved in apoptotic signaling pathway),抗生素反應(response to antibiotic),通過死亡域受體對外部凋亡信號通路的調控(negative regulation of extrinsic apoptotic signaling pathway via death domain receptors),冷刺激反應(response to cold),神經元凋亡負調控(negative regulation of neuron death),轉錄正調控(positive regulation of transcription),DNA模板(DNA-templated),熱刺激反應(response to heat),凋亡過程(apoptotic process),成骨細胞分化的正調控(positive regulation of osteoblast differentiation),平滑細胞增殖的正調控(positive regulation of smooth muscle cell proliferation),細胞對機械刺激的反應(cellular response to mechanical stimulus),細胞氧化還原內穩態(cell redox homeostasis),乙醇刺激反應(response to ethanol)。細胞組分(CC)富集在質膜外側(external side of plasma membrane)和細胞質(cytoplasm)。分子功能(MF),富集在支架蛋白結合(scaffold protein binding)。
KEGG通路富集在哮喘(Asthma),軍團桿菌病(Legionellosis),NOD樣受體信號通路(NOD-like receptor signaling pathway)。
討 論
三黃紫參油功以清熱燥濕祛邪、活血養血生新,與濕疹病機相投,芝麻油劑有清潔、軟化、保護、抗氧化活性等作用,故對濕疹具有較好臨床療效。三黃紫參油治療濕疹的復雜,現作者從以下一個方面進一步闡述。
三黃紫參油可能通過調控炎癥應答、免疫應答以治療濕疹。濕疹本質上是真皮淺層及表皮炎癥,其不同階段實際是炎癥動態演變過程中的不同時期[1];IV型遲發型變態反應參與濕疹發病[1],由T淋巴細胞介導,輔助性T細胞(Th1/Th2)的分化失衡在濕疹的發生發展中具有重要作用[19-23]。三黃紫參油治療濕疹的關鍵靶點中,IL6、IL13、MS4A2富集在炎癥應答、免疫應答的生物學過程:白介素6(IL6),參與淋巴細胞和單核細胞的分化,是生成T(H)17細胞所必需的;白介素13(IL13),抑制炎癥細胞因子的產生,與IL2協同調節干擾素合成,可能是調節炎癥和免疫反應的關鍵;高親和力免疫球蛋白受體亞基β(MS4A2),是與免疫球蛋白的Fc區結合的高親和力受體,多價抗原對FCER1的聚集是肥大細胞完全應答所必需的,也調節重要的淋巴因子的分泌。三黃紫參油成分可能通過IL6、IL13、MS4A2對炎癥應答、免疫應答、淋巴細胞等起到關鍵的調控作用,從而達到治療濕疹的作用。
三黃紫參油可能通過調控皮膚及皮下組織細胞基本進程以治療濕疹。CASP8, AHR, TP63富集在凋亡過程,IL6, IL13富集在平滑細胞增殖的正調控。芳基碳氫化合物受體(AHR),導鹵代芳烴的生化和毒性作用,參與細胞周期調控,可能在許多組織的發育和成熟中發揮重要作用;腫瘤蛋白質63(TP63),在上皮形態發生的調控中發揮作用。三黃紫參油成分可能通過CASP8、AHR、TP63、IL6、IL13以調控上皮細胞形態,調控皮膚及皮下組織細胞的增殖、生長、成熟、退化、凋零等細胞基本進程而治療濕疹。
三黃紫參油可能通過調控皮膚細胞對冷刺激、熱刺激、機械性刺激、乙醇刺激等外部刺激的應答及局部血液循環以治療濕疹。濕疹病因不明,可能與多種內部因素(如血液循環障礙)、外部因素(如寒冷、炎熱等周圍環境,魚蝦、等食物,酒精、肥皂等化學物質)有關[1,14]。IL6、CASP8富集于冷刺激應答,IL6、NOS3富集于熱刺激應答,CASP8、IL13富集于細胞對機械刺激的反應,CASP8、IL13富集于乙醇刺激反應。內皮型一氧化氮合酶(NOS3),其生存的NO參與血管平滑肌松弛,可介導血管內皮生長因子(VEGF)誘導的冠狀血管生成,可通過激活血小板促進血液凝固。三黃紫參油可能通過IL6、CASP8、NOS3、IL13以調控皮膚對外部刺激的應答及局部血液循環以治療濕疹。
綜上所述,三黃紫參油中有17種關鍵成分具治療濕疹作用,這些成分具有較好的經皮滲透性,他們通過多靶點、多通路發揮治療濕疹的作用。表明三黃紫參油在濕疹上的有效性和中醫理論的正確性。由于中西醫理論的差異性,數據平臺和軟件的限制,本研究也存在局限性。

