脂肪細胞外泌體調節NOX4/TGF-β1/Smad信號通路促進老年自發性高血壓大鼠心肌纖維化
孔巴提·沙提別克 孟巖 王紅
(新疆醫科大學第一附屬醫院綜合內二科,新疆 烏魯木齊 830054)
心肌纖維化是高血壓、心力衰竭、心肌炎等多種心血管疾病發展到一定階段后常見的病理特征〔1〕,其主要表現為心肌成纖維細胞異常增殖,細胞外基質異常沉積,心肌組織中膠原比例增加,導致心肌收縮和舒張障礙〔2〕。高血壓可導致心臟負擔加重,引起膠原在細胞間質和血管周圍沉積而加重心肌纖維化〔3〕。已有研究表明,肥胖與心血管疾病密切相關,且常見于老年高血壓患者,可導致高血壓患者左心室肥大〔4〕,但肥胖對老年高血壓患者心肌纖維化的影響尚不明確。外泌體是一類由活細胞分泌的粒徑在50~150 nm的胞外囊泡,可攜帶母細胞的信息經體液運輸作用于近端和遠端組織而影響病理生理進程,并且已有研究表明脂肪細胞外泌體與心力衰竭等心血管疾病密切相關〔5〕,而其對老年高血壓患者心肌纖維化的影響尚未有明確報道,本研究旨在探討脂肪細胞外泌體對老年自發性高血壓大鼠心肌纖維化的影響。
1 材料與方法
1.1材料 鼠前脂肪細胞3T3-L1購自中國科學院上海生命科學研究所;DMEM培養基購自Gibco公司;12月齡SHR大鼠10只和12月齡WKY大鼠5只均購自新疆醫科大學動物實驗中心;白細胞介素(IL)-6、IL-10、腫瘤壞死因子(TNF)-α酶聯免疫吸附試驗(ELISA)檢測試劑盒購自福麥斯生物技術有限公司;超氧化物歧化酶(SOD)、活性氧(ROS)檢測試劑盒購自南京建成生物工程研究所;cDNA合成試劑盒、qPCR檢測試劑盒購自ABM公司;3-異丁基-1-甲基黃嘌呤(IBMX)購自美國Sigma公司;p-細胞質果蠅蛋白質(Smad)、Smad、尼克酰胺腺嘌呤氧化酶(NOX)4、轉化生長因子(TGF)-β1、3-磷酸甘油醛脫氫酶(GAPDH)抗體、山羊抗兔二抗均購自CST公司。
1.2脂肪細胞的培養與誘導 取液氮保存的3T3-L1前脂肪細胞于37℃水浴鍋中快速解凍,加入等體積的DMEM培養基稀釋后,1 000 r/min離心5 min,細胞重懸后于37℃、5%CO2培養箱中培養,細胞生長匯合率達80%時進行傳代。將前脂肪細胞誘導分化為成熟的脂肪細胞,具體步驟為:取對數生長期的3T3-L1細胞,調整細胞密度為5×103個/ml,接種于12孔板,首先加入誘導培養基A(每100 ml DMEM培養基加入10 μl 10 mmol/L地塞米松溶液、100 μl 0.5 IBMX溶液、100 μl 10 mg/ml胰島素溶液)誘導4 d,然后換成誘導培養基B(每100 ml DMEM培養基加入100 μl 10 mg/ml胰島素溶液)誘導4 d,然后換成DMEM完全培養基培養4 d即可進行后續實驗。
1.3脂肪細胞外泌體的提取與鑒定 誘導成熟的3T3-L1細胞使用含10%的無外泌體胎牛血清的DMEM培養基培養48 h,收集細胞培養上清,采用差速離心法提取外泌體,具體步驟為:將所收集的細胞上清分裝到10 ml的離心管中,首先3 000 r/min,4℃離心15 min,去除死細胞;然后6 000 r/min離心40 min,去除細胞碎片;10 000 r/min離心1 h,取上清;100 000 r/min離心1 h,收集沉淀即為外泌體,用400 μl磷酸鹽緩沖液(PBS)重懸外泌體,并放在-80℃保存。
采用透射電鏡觀察外泌體的形態結構,具體步驟為:稀釋外泌體至蛋白濃度為0.5 mg/ml。將透射電鏡所用的銅網平放到稱量紙上,滴加20 μl上述外泌體溶液,于紅外燈下烘烤10 min;烘干后再滴加2滴磷鎢酸,繼續烘烤10 min,吸棄多余液體,于投射電鏡下觀察外泌體結構。
Western印跡檢測外泌體表面生物標志物CD9、CD63、腫瘤易感基因(TSG)101,具體步驟為:取100 μl外泌體加入50 μl的放射免疫沉淀試驗(RIPA)裂解液,于冰上裂解30 min,12 000 r/min,離心15 min后,取上清,即為外泌體總蛋白。采用二喹啉甲酸(BCA)蛋白定量試劑盒進行蛋白定量,取外泌體蛋白裂解液進行十二烷基硫酸鈉-聚丙烯酰胺凝膠電泳(SDS-PAGE),經轉膜,封閉后CD9、CD63、TSG101一抗孵育過夜,然后二抗孵育,洗膜后,曝光成像。
1.4動物分組及給藥 實驗動物分為對照組(WKY大鼠)、SHR組(SHR大鼠)、exosome組(SHR大鼠),每組5只。exosome組大鼠尾靜脈注射0.5 μg/μl的成熟脂肪細胞外泌體溶液100 μl,每周注射1次,對照組和SHR組注射等體積的生理鹽水,實驗共4 w。
1.5各組收縮壓(SBP)及左心室重量指數(LVI)測定 給藥治療前及給藥后分別采用大鼠RBP-1型大鼠尾動脈血壓心率測定儀測量各組SBP。治療結束后頸椎脫臼處死,解剖取心肌組織,取左心室稱重,并計算LVI。
1.6心肌膠原容積分數(CVF)和血管周圍膠原面積(PVCA)檢測 取左心室中段橫截面心肌組織于組織固定液中固定24 h,取固定后的組織用清水清洗,依次經過70%、80%、90%、95%及無水乙醇梯度水化后,將組織分2次浸入二甲苯中,每次10 min,然后依次將組織浸入軟石蠟和硬石蠟中各2次,每次30 min,然后將組織浸入石蠟液中,冷卻至凝固,并于切片機上制備組織切片,制備的切片分別進行蘇木素-伊紅(HE)染色和Masson染色,HE染色用于觀察心肌組織病理變化;Masson染色觀察心肌組織膠原;采用 CISA-1000計算機圖像分析系統進行分析,CVF=膠原面積/總面積;PVCA=壁內小動脈管腔周圍膠原面積/動脈管腔面積。
1.7ELISA檢測血清炎癥因子IL-6、IL-10、TNF-α 治療結束后,各組大鼠眼眶取血,室溫靜置1 h后,3 500 r/min,4℃離心15 min,取上層血清,按照ELISA試劑盒方法檢測血清炎癥因子TNF-α、IL-1β、IL-6水平,主要步驟為:鋪好一抗的96孔板內加入40 μl待測樣品和10 μl生物素標記抗體后,在加入100 μl辣根過氧化物酶標記抗體,37℃孵育75 min,清洗96孔板后加入顯色劑顯色,終止后于450 nm波長處測吸光度,根據標準曲線計算血清TNF-α、IL-10、IL-6含量。
1.8心肌組織SOD、ROS、羥脯氨酸檢測 實驗結束后取各組大鼠心肌組織100 mg,于冰上勻漿均勻后,3 000 r/min離心10 min,取上清液,根據SOD和ROS檢測試劑盒說明書,檢測各組心肌組織SOD、ROS、羥脯氨酸水平。
1.9qPCR檢測心肌組織過氧化物酶體增殖物激活受體(PPAR)γ表達 取液氮保存的心肌組織加入Trizol研磨至組織完全裂解,取研磨液加入200 μl氯仿,靜置5 min后,于12 000 r/min,4℃離心15 min,轉移上層水相,加入500 μl異丙醇,12 000 r/min,4℃離心10 min,去上清,1 ml 75%乙醇清洗RNA沉淀后,20 μl RNA-free水重懸RNA沉淀,55℃水浴10 min,即為總RNA。使用primer premier5.0軟件設計PPARγ引物,按照cDNA合成試劑盒和RT-qPCR試劑盒進行逆轉錄和RT-qPCR,采用ΔΔCT法計算PPARγ的表達量。β-actin 上游引物:5′-TATGACTTAGTTGCGTTACACC-3′,下游引物:5′-CCTTCACCGTTCCAGTTT-3′;PPARγ上游引物:5′-TCCGTGATGGAAGACCACTC-3′,下游引物:5′-CCCTTGCATCCT TCACAAGC-3′。
1.10Western印跡檢測各組心肌組織p-Smad、Smad、NOX4、TGF-β1表達水平 取各組心肌組織50 mg加入250 μl RIPA裂解液和2.5 μl的苯甲基磺酰氟(PMSF)蛋白酶抑制劑,勻漿器在冰上勻漿后12 000 r/min,4℃離心10 min,取上清,即為心肌組織總蛋白。采用BCA蛋白定量,然后蛋白沸水浴加熱變性,然后進行SDS-PAGE,轉膜,用5%的脫脂牛奶對聚偏氟乙烯(PVDF)膜封閉2 h,然后以1∶1 000比例稀釋后的p-Smad、Smad、NOX4、TGF-β1一抗4℃孵育過夜,TBST洗膜后二抗室溫孵育1.5 h,再用TBST洗膜后按照電化學發光(ECL)試劑盒說明書配制發光液,并將PVDF膜浸入發光液中反應30 s,曝光并拍照。
1.11統計學方法 采用SPSS19.0軟件進行方差分析、t檢驗。
2 結 果
2.1外泌體鑒定結果 采用差速離心法提取的外泌體粒徑在50~100 nm,具有“杯托”樣結構,符合外泌體的結構特征;Western印跡檢測顯示,提取到的外泌體表達Alix、Tsg101、CD9 3種外泌體標志蛋白,見圖1、圖2。
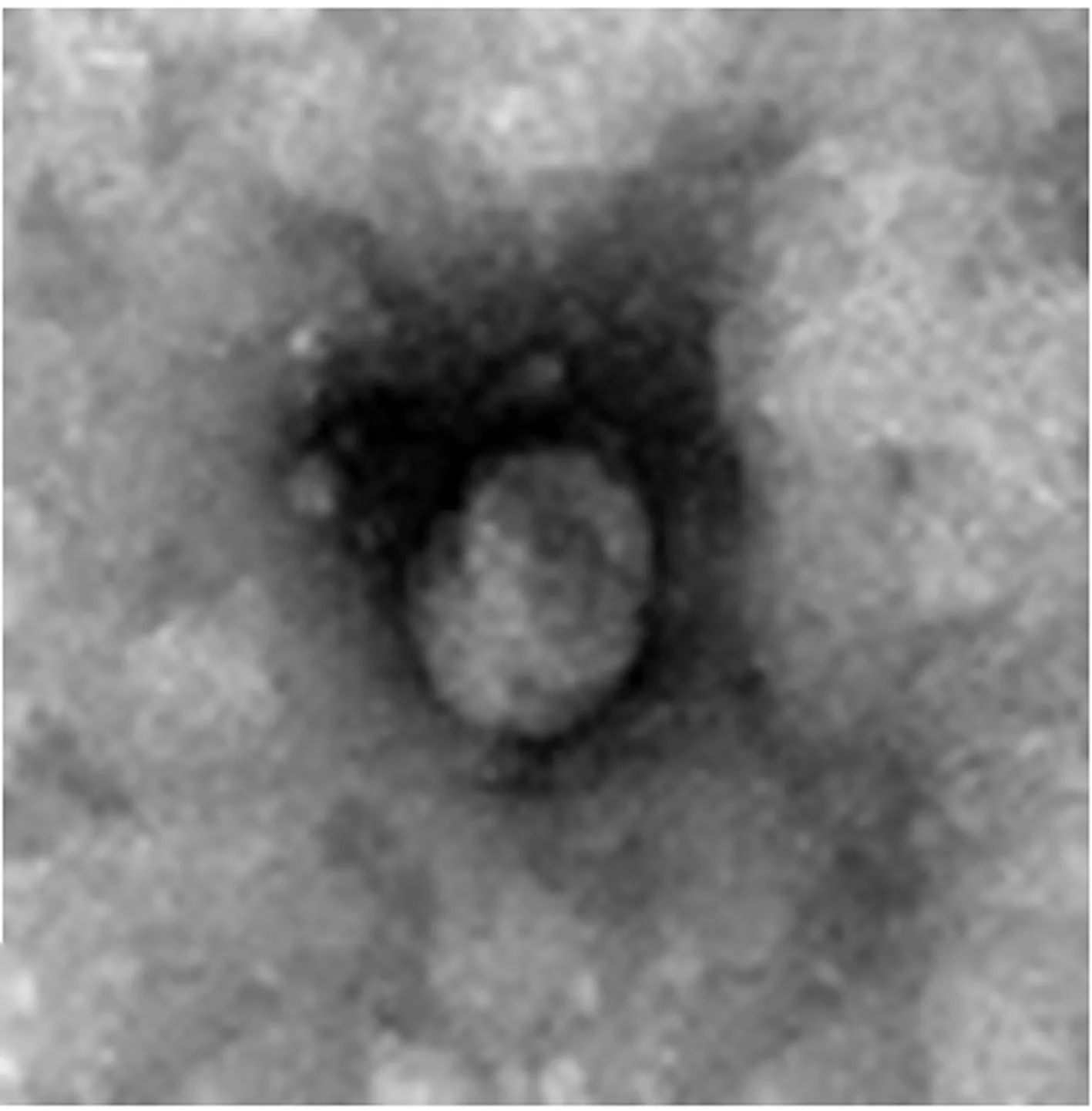
圖1 外泌體投射電鏡拍攝結果(×100)
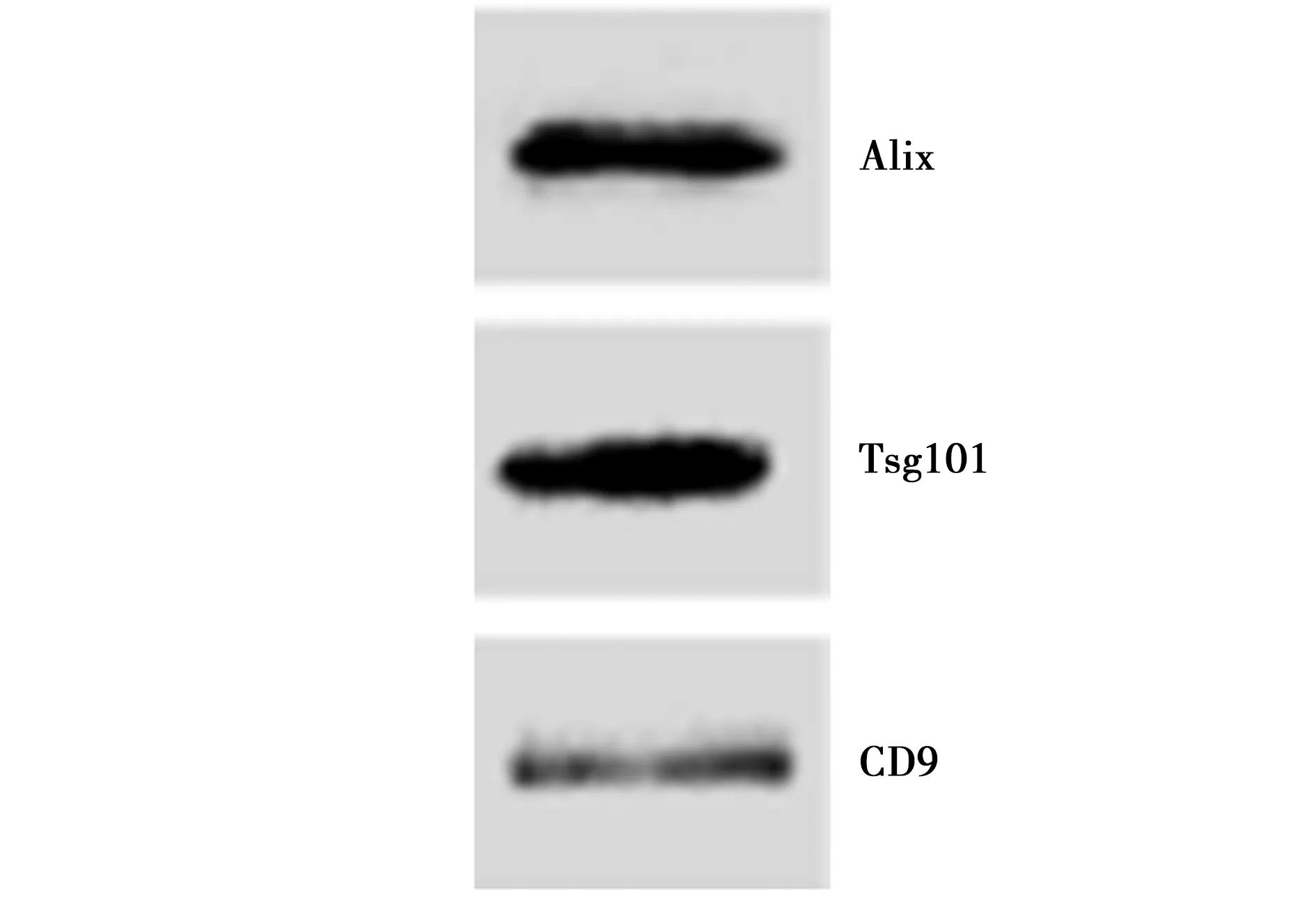
圖2 Western印跡檢測外泌體標志蛋白
2.2脂肪細胞外泌體影響老年自發性高血壓大鼠SBP和LVI 與對照組比較,SHR組SBP和LVI水平均顯著升高(P<0.05);與SHR組比較,exosome組SBP和LVI水平均顯著升高(P<0.05),見表1。提示脂肪細胞外泌體能夠促進SBP和LVI,加重高血壓及心臟損傷。
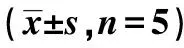
表1 各組SBP和LVI水平比較
2.3脂肪細胞外泌體對各組心肌組織病理變化的影響 HE染色結果(圖3)顯示,對照組心肌結構完整、心肌纖維排列整齊、沒有炎癥細胞浸潤等病理變化;SHR組心肌纖維排列不規則、出現心肌纖維斷裂、心肌細胞呈肥大狀態、有少量炎癥細胞浸潤、心肌組織病變明顯;exosome組心肌纖維排列紊亂且疏松,纖維斷裂現象嚴重,心肌細胞肥大嚴重、有大量的炎癥細胞浸潤、細胞核分布不規則,與SHR組相比,心肌組織損傷嚴重,提示脂肪細胞外泌體能夠加重老年高血壓大鼠心肌組織病變。
2.4脂肪細胞外泌體對各組心肌CVF和PVCA的影響 根據Masson染色結果(圖4),心肌細胞呈紅色,膠原組織呈綠色,對照組大鼠心肌組織排列整齊,膠原組織分布稀疏,血管周圍膠原分布較少;SHR組心肌組織排列較整齊,膠原纖維及血管周圍膠原分布較多;exosome組心肌組織中膠原分布大量增加,膠原纖維網斷裂,血管周圍膠原大量增加,提示心肌纖維化嚴重。相比于對照組,SHR組CVF和PVCA顯著增加(P<0.05),提示高血壓能夠誘發老年大鼠心肌纖維化;相比于SHR組,exosome組CVF和PVCA亦顯著增加(P<0.05),提示脂肪細胞外泌體能夠促進老年高血壓大鼠心肌纖維化。見表2。
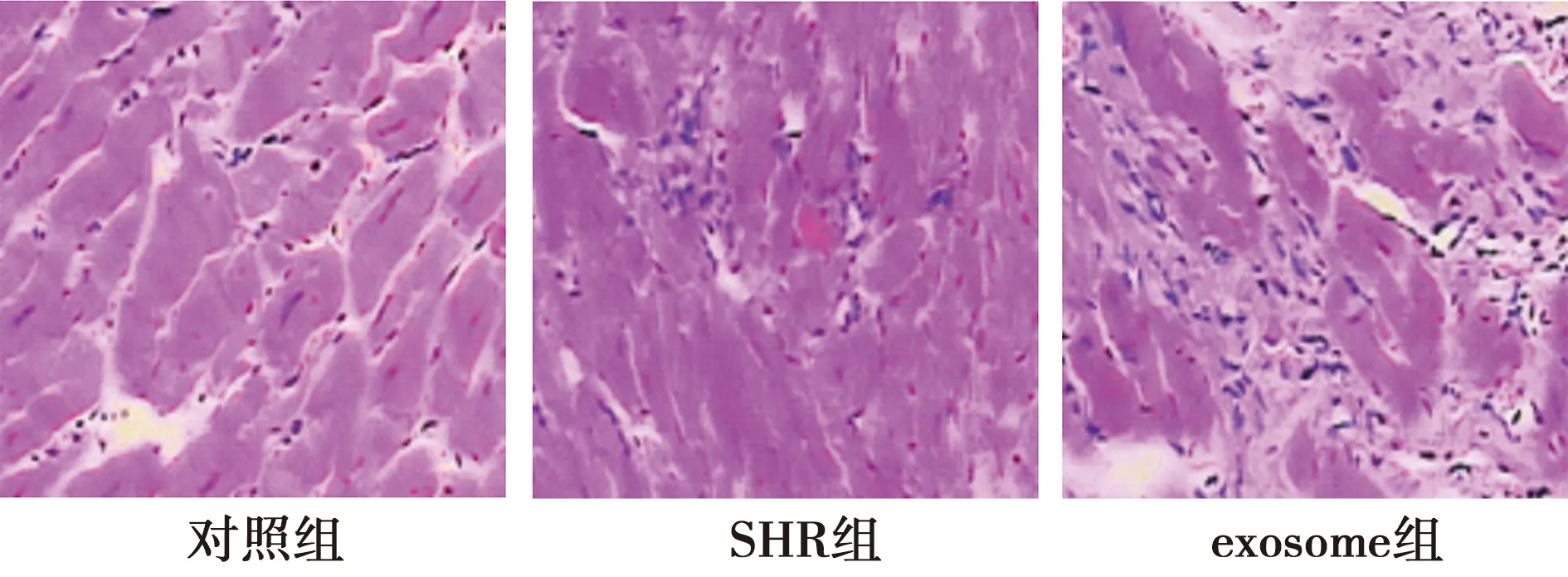
圖3 各組心肌組織HE染色結果(×200)
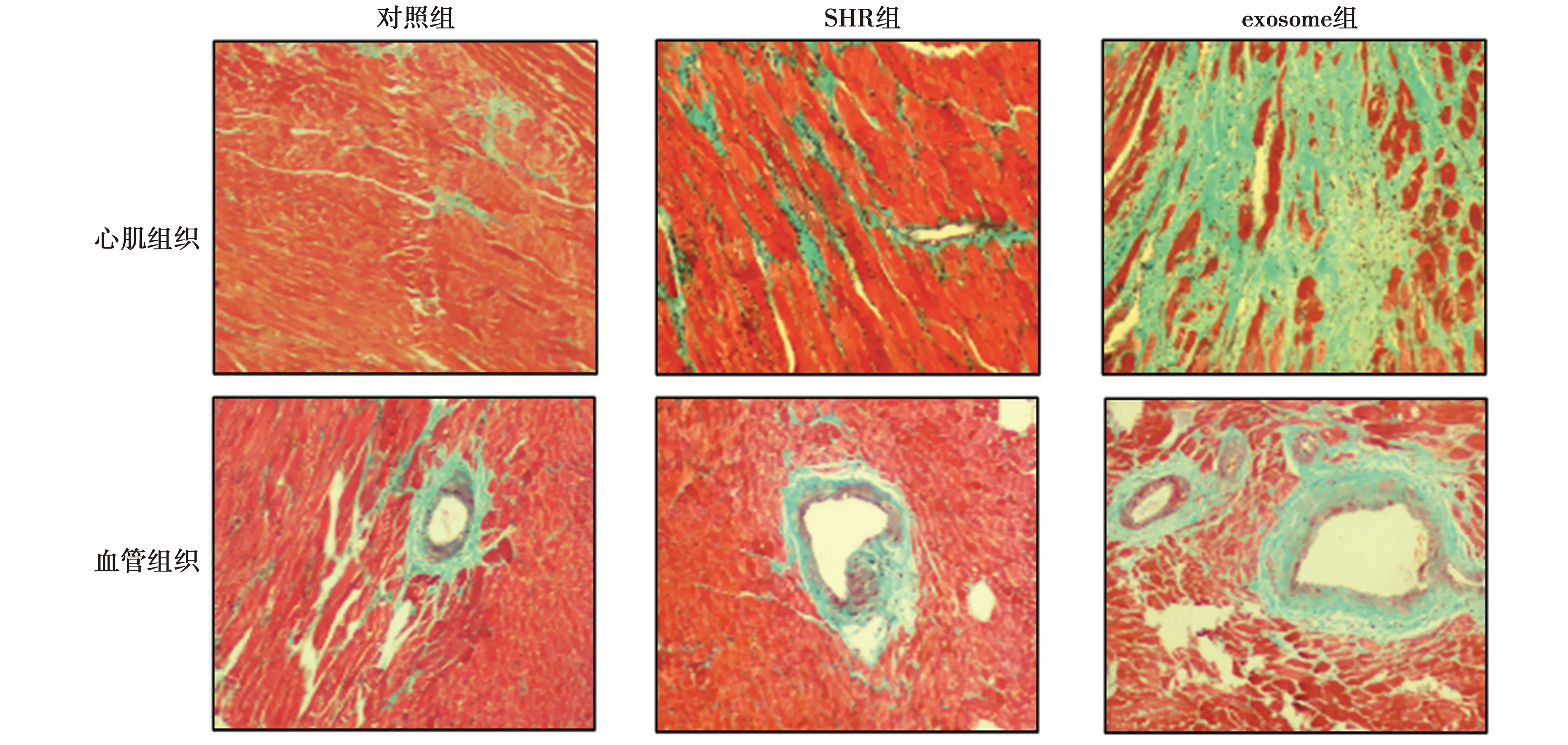
圖4 各組大鼠心肌組織Masson染色結果(×200)
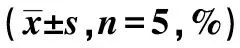
表2 各組CVF和PVCA水平比較
2.5脂肪細胞外泌體對各組血清炎癥因子的影響 相比于對照組,SHR組IL-6、IL-10、TNF-α水平顯著上升(P<0.05),相比于SHR組,exosome組血清IL-6、IL-10、TNF-α水平亦顯著上升,見表3,說明脂肪細胞外泌體能夠顯著促進老年高血壓大鼠體內炎癥反應。
2.6脂肪細胞外泌體對各組心肌組織SOD、 ROS、羥脯氨酸的影響 SHR組心肌組織SOD、 ROS、羥脯氨酸顯著高于對照組(P<0.05),說明高血壓能夠引起老年高血壓大鼠心肌組織SOD、 ROS、羥脯氨酸含量增加;exosome組心肌組織SOD、 ROS、羥脯氨酸水平亦顯著高于SHR組(P<0.05),見表4,提示脂肪細胞外泌體能夠上調大鼠心肌組織SOD、 ROS、羥脯氨酸水平。

表3 各組IL-6、IL-10、TNF-α水平比較
2.7脂肪細胞外泌體對各組心肌組織PPARγ表達的影響 SHR組心肌組織PPARγ表達量顯著低于對照組(P<0.05),exosome組心肌組織PPARγ表達量顯著低于SHR組(P<0.05),見表5,提示脂肪細胞外泌體能夠顯著抑制PPARγ表達。
2.8脂肪細胞外泌體對心肌組織NOX4、TGF-β1表達及Smad磷酸化的影響 相比于對照組,SHR組心肌組織NOX4、TGF-β1表達水平顯著增加(P<0.05),Smad磷酸化水平顯著增加(P<0.05);相比于SHR組,exosome組心肌組織中NOX4、TGF-β1表達水平顯著增加(P<0.05),Smad磷酸化水平顯著增加(P<0.05),見表5,圖5,提示脂肪細胞外泌體能夠通過促進NOX4/ TGF-β1/Smad而促進老年高血壓大鼠心肌纖維化的發展。
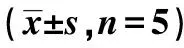
表4 各組SOD、 ROS、羥脯氨酸水平比較
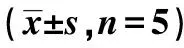
表5 各組PPARγ、NOX4、TGF-β1、p-Smad/Smad水平比較

圖5 各組心肌組織NOX4、TGF-β1表達及Smad磷酸化檢測結果
3 討 論
心肌纖維化是高血壓等心血管疾病共同的病理變化,心肌纖維化可導致心臟收縮和舒張功能障礙、心力衰竭、心律失常、心室重構等〔6〕,因而緩解心肌纖維化是治療心力衰竭和心律失常等心血管疾病的重要措施。已有研究表明,肥胖與冠心病、動脈粥樣硬化的心血管疾病密切相關,肥胖是高血壓的重要誘因之一,且多發于老年高血壓患者,控制肥胖能夠有效緩解高血壓〔7〕。外泌體是一類由多種活細胞分泌的納米級囊泡,已有研究表明脂肪細胞外泌體可影響體內代謝〔8〕。本研究結果說明脂肪細胞可能通過外泌體而加重心肌纖維化。肥胖是高血壓的危險因素之一,且肥胖可加重高血壓患者體內的炎癥,研究表明,體內脂肪代謝異常可導致炎癥,進而引起血管內皮的收縮,并且激活交感神經和腎素-血管緊張素-醛固酮系統,進而促進高血壓的發展〔9〕,本研究發現脂肪細胞外泌體能夠加重老年高血壓大鼠體內炎癥反應。氧化應激與高血壓的發生、發展密切相關〔10〕。氧化應激既引起血管壁增厚和血管腔狹窄,又損傷內皮細胞,導致內皮功能障礙,血管舒張性降低,增加血管收縮,引起外周血管阻力增加和血壓升高〔11,12〕,進而加重心肌纖維化,本研究發現,脂肪細胞外泌體能夠增加老年高血壓大鼠心肌組織SOD、ROS水平,即加重心肌組織的氧化應激。PPARγ 是核受體 PPARs 的一個亞家族,主要表達于心肌組織中,可調控脂類代謝相關基因的表達,PPARγ被激活后能夠增強促進脂肪酸儲存基因的表達,例如脂肪酸轉運蛋白、脂肪酸結合蛋白等,降低血脂水平及增強脂類代謝,臨床上高血壓與高脂血癥常同時發生,相互影響〔13,14〕,本研究結果提示脂肪細胞外泌體可能通過抑制PPARγ的表達而影響血脂代謝及高血壓的發生發展。
NOX4可促進心臟成纖維細胞轉化為肌成纖維細胞,進而促進心臟的纖維化,并且NOX4表達上調會引起TGF-β1表達上調,Smad家族蛋白中,Smad2和Smad3是TGF-β1介導纖維化發生的下游分子,可促進心肌組織膠原蛋白的合成〔15~17〕,本研究發現,脂肪細胞外泌體能夠上調NOX4、TGF-β1及Smad的表達,即激活NOX4/TGF-β1/Smad信號通路。
綜上,脂肪細胞外泌體可治療老年高血壓大鼠體內炎癥、氧化應激反應及心肌纖維化,其影響心肌纖維化的機制為激活NOX4/TGF-β1/Smad信號通路。

