重視素養為本的高三復習“碳元素及其化合物”教學實踐
——以高考熱門考點“碳中和”為例
江蘇 居亞芬 王 菁
一、問題的提出
1.社會高度關注“碳中和”
2021年全國兩會期間,“碳達峰”和“碳中和”被首次寫入政府工作報告,因其對氣候變化、經濟發展和公民個人生活密切相關,所以社會關注度非常高。
“碳中和”是指企業、團體或個人在一定時間內直接或間接產生的CO2排放總量,通過CO2去除手段,如植樹造林、節能減排、產業調整等,抵消掉這部分碳排放,達到“凈零排放”的目的。
2.高考熱門試題情境“碳中和”
《中國高考評價體系說明》中倡導真實問題情境的創設,以激發學生學習的興趣。“碳中和”成為了2021年高考中多個省份、多門學科的熱門情境,同時該主題可關聯最新的科學研究進展,已經受到高三師生的關注。例如被形象稱為“液體陽光”計劃的中國科學家研發的全球首套千噸級太陽能燃料合成項目,作為試題情境出現在2021年全國甲卷理綜的28題和35題,展示我國在綠色發展和清潔能源開發上的成果。由此筆者精選例題,開展了一節有關“碳中和”概念的高三復習課,此類項目式課堂模式可以類推到其他元素化合物復習課。
【例1】(2021·全國乙卷·7)我國提出爭取在2030年前實現碳達峰、2060年前實現碳中和,這對于改善環境、實現綠色發展至關重要。“碳中和”是指CO2的排放總量和減少總量相當。下列措施中能促進碳中和最直接有效的是( )
A.將重質油裂解為輕質油作為燃料
B.大規模開采可燃冰作為新能源
C.通過清潔煤技術減少煤燃燒污染
D.研發催化劑將CO2還原為甲醇
【答案】D
【解析】本題以“碳中和”為情境,考查如何利用化學技術減少碳排放。重質油裂解為輕質油不能減少CO2排放總量,A項錯誤;可燃冰的使用會產生CO2,B項錯誤;清潔燃煤技術主要是減少粉塵、SO2等污染,不能很有效地減少CO2排放,C項錯誤;D項通過氧化還原真正實現了CO2的資源化利用。本題基于學生的學情,向學生普及了多種實現“碳中和”的化學技術,引導學生關注化學對國家科學、經濟和社會發展的貢獻。
二、“碳中和”課堂教學實踐
【環節一】CO2的來源
[真實情境引入]化石能源耗得多,導致地球變暖的元兇CO2也生成得多。隨著人類的活動,全球變暖氣候問題突出,也在影響著人們的生活方式,帶來越來越多的問題。限制碳排放必然對全球經濟發展產生重大的影響,特別是對我國這樣油氣資源相對較少、煤炭資源相對豐富的國家,減排壓力更加嚴峻。
【學習任務1】小組活動:尋找CO2的來源。
[小組匯報]化石燃料的大量燃燒,汽車尾氣的大量排放,生物的呼吸作用,電器的間接釋放,水果行業CO2的使用,有機物在分解、發酵、腐爛、變質的過程中都會生成CO2。
[目的]讓學生了解學科與工業生產、生活、自然之間的緊密聯系,從而對解決實際問題具有重要意義。
【學習任務2】小組活動:說說你知道的CO2的用途。
[小組匯報]①CO2不支持燃燒且密度比空氣大,可用于滅火,是常用滅火劑。
②化工上CO2是一種重要原料,大量用于生產純堿(Na2CO3)、碳酸氫鈉(NaHCO3)、尿素[CO(NH2)2]、碳酸氫銨(NH4HCO3)等。
③生產碳酸飲料、啤酒、汽水等。
④現代化倉庫里常充入CO2,防止糧食蟲蛀和蔬菜腐爛,延長其保存期。
⑤固態的CO2即“干冰”,可作制冷劑,可用于人工降雨,還可以做食品速凍保鮮劑。
⑥烘焙食品行業中作膨松劑。
⑦在農業上,作肥料增進植物的光合作用,促進農作物生長。與氮循環類似,碳循環對自然界也有著重要的作用。
[教師]正視CO2的存在,任何物質都有兩面性。然而我國現在面臨著節能減排的重任,可以從哪些方面有效的實現“碳中和”?
【學習任務3】小組活動:說說你掌握的碳中和的化學技術。
【環節二】節能減排
方法1:碳捕集與封存
人類能做的就是植樹造林,通過土壤、森林和海洋等吸收空氣中的CO2。
方法2:建立低碳系統
(1)碳核算
碳核算是針對所有可能產生CO2的來源,進行企業排放源清查與數據搜集,以了解企業CO2排放源及量化所搜集的數據信息,是邁向實現低碳管理的第一步。
(2)能源轉型
我國已經進入工業化后期,固定投資增速拐點顯現,城鎮化速率放緩,第三產業比重超過50%,經濟結構的深刻變革已然成為逐步與減少碳排放的最大底氣。煤炭在能源使用的占比重過高(57.6%)是導致碳排放強度過高的重要原因。能源轉型開始較早,但脫離煤炭開展較為緩慢。
[小組1]通過清潔煤炭技術可在一定程度上減少煤燃燒造成的污染。
[小組2]新能源汽車、各種儲能設施等作為能源革命的一部分,將會伴隨清潔能源技術的成熟而迅速發展。
[小組3]不斷發展風、光、核、氫等非化石能源,減少煤、石油、天然氣等化石能源的使用帶來的污染。
[資料呈現]1979年碳達峰的歐盟、2005年碳達峰的美國,都承諾在2050年實現凈零排放,分別用了71年和45年。而中國有著“2030年前實現碳達峰,2060年前實現碳中和”的目標,只有30年。
[教師]想用更高的效率、更短的時間完成發達國家同樣的任務,我們還能作什么?
方法3:想辦法將CO2變廢為寶,轉化為工業所需的含碳化合物。
【環節三】CO2的資源化利用
【學習任務4】從含碳元素物質的多樣性、價態觀、氧化還原等角度,設想不同價態含碳物質的相互轉化。
[小組1]通過氧化還原反應可直接將CO2轉化為碳單質、CO或有機化合物(如甲醇、甲酸、甲酸甲酯等)。
[小組2]通過氧化還原反應可結合電化學原理將CO2轉化為其他資源進行充分利用。
【例2】(2019·江蘇卷·20節選)電解法轉化CO2可實現CO2資源化利用。電解CO2制HCOOH的原理示意圖如圖1所示。

圖1
①寫出陰極CO2還原為HCOO-的電極反應式:____________________。
②電解一段時間后,陽極區的KHCO3溶液濃度降低,其原因是____________________。

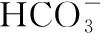
【解析】①根據電解原理,陰極上發生得電子、化合價降低的過程。
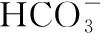
[小組3]利用CO2是酸性氧化物,可用堿或堿性氧化物吸收將其轉化為其他化工原料。
例如,用氨水吸收CO2轉化為化肥碳銨等。CaO可在較高溫度下捕集CO2,在更高溫度下將捕集的CO2釋放利用。
三、真題賞析
【學習任務5】通過2021年各地高考真題賞析,從理論環節真正進入實踐環節,同時對2022年高考的備考做出一定的思考。
[落實素養]用真實的情境引入,培養學生的創新精神和實踐能力。
【例3】(2021·廣東省選擇性考試·9)火星大氣中含有大量CO2,一種有CO2參加的新型全固態電池有望為火星探測器供電。該電池以金屬鈉為負極,碳納米管為正極,放電時( )
A.負極上發生還原反應
B.CO2在正極上得電子
C.陽離子由正極移向負極
D.將電能轉化為化學能
【答案】B
【解析】本題的情境是搭載最新的火星探測計劃,通過CO2的資源化利用為火星探測器供電。原電池原理將化學能轉化為電能,D錯誤;負極發生氧化反應,A項錯誤;正極得電子,B項正確;為形成閉合電路,陽離子移向正極,C項錯誤。本題創設真實的問題情境,借力原電池實現碳中和,引導學生通過所學的化學基本原理和方法,去解決實際面對的化學問題。
【例4】(2021·全國甲卷·28)二氧化碳催化加氫制甲醇,有利于減少溫室氣體二氧化碳。回答下列問題:

總反應的ΔH=________kJ·mol-1;若反應①為慢反應,圖2各示意圖中能體現上述反應能量變化的是________(填標號),判斷的理由是。

A

B

C

D

圖3
①用各物質的平衡分壓表示總反應的平衡常數,表達式Kp________;
②圖中對應等壓過程的曲線是________,判斷的理由是________;
③當x(CH3OH)=0.10時,CO2的平衡轉化率α=________,反應條件可能為________或________。
【答案】(1)-49 A ΔH為負值,反應放熱,因此生成物總能量低于反應物總能量 反應①為慢反應,所以反應①的活化能大于反應②。

②b 總反應ΔH<0,升高溫度時平衡向逆反應方向移動,甲醇的物質的量分數變小
③33.3% 5×105Pa,210℃ 9×105Pa,250℃
【解析】(1)根據蓋斯定律,反應①+②可得二氧化碳加氫制甲醇的總反應的ΔH=ΔH1+ΔH2=-49 kJ·mol-1。該反應的總反應為放熱反應,因此生成物總能量低于反應物總能量,B項和D項圖形不符。反應①為慢反應,因此反應①的活化能高于反應②,因此示意圖中能體現反應能量變化的是A項。

③設起始n起始(CO2)=1 mol,n起始(H2)=3 mol;設反應中轉化的n轉化(CO2)=xmol,n轉化(H2)=3xmol;則平衡時n平衡(CO2)=1-xmol,n平衡(H2)=3-3xmol,n平衡(CH3OH)=xmol,n平衡(H2O)=xmol,當平衡x(CH3OH)=0.10時,經計算CO2的平衡轉化率α=33.3%。由圖3可知,滿足平衡時x(CH3OH)=0.10的條件有:5×105Pa,210℃或9×105Pa,250℃。
本題考查選擇性必修《化學反應原理》模塊中有關平衡的三段式計算、外界條件對化學反應速率和化學平衡的影響等基本知識,引導考生認識并體會化學學科對社會發展的作用。
四、教學反思
1.教師視角
《普通高中化學課程標準(2017年版2020年修訂)》中對氯、硫、氮及其重要化合物的主要性質、在生產生活中的應用做出了具體要求,但碳元素并不在內。然而以素養為主的高中教學,希望每一個學生從自身做起,形成綠色低碳的生活方式,并且能對與化學有關的社會熱點問題做出正確的價值判斷,能積極參與到相關化學問題的實踐中。
教師從碳中和的全球輿論關注,引導學生關注人類面臨的與化學有關的社會問題,通過分析碳源和碳匯認識到國家能源結構急需轉型,進一步引導學生從源頭上實現零減排放,同時多角度實現對CO2的資源化利用,培養學生的社會責任感,最終讓學生深刻認識化學對解決社會實際問題所作出的重大貢獻。
2.學生視角
學生在這堂課中不僅僅是解決了幾道高考真題,而是充分認識到自己所學的化學知識與技能并不是紙上談兵,可以真正落實到生產、生活實際問題的解決中去。也許目前的想法還是理論性較多,實踐難度大,但是極大地鼓勵了學生勇于創新的精神。
3.針對2022年高考的備考指導
(1)讓教學回歸基礎
高考試題的呈現更加靈活化和創新性,旨在杜絕機械的刷題模式。本節課展示的項目式教學模式:對元素化合物的復習和考查不再拘泥于書本中的方程式和性質,而是從物質的多樣性、價態觀、氧化還原等角度創造性進行物質的相互轉化。高中化學基礎知識的考查并不是直接考概念定義,而是將基礎知識融合到物質的合成與轉化、物質的結構與性質、實驗探究等方面,對學生有著更高的要求。
(2)加強信息提取與加工能力
學生都知道審題的重要性,讀題時劃下關鍵字詞和該題的重要原料和目標,問題都是圍繞一個目標而設置的。例如高考真題中圖表的呈現,學生需獲取圖中數據信息,再進行深層次的推導,進行適當的加工。
(3)加強邏輯推理和歸納能力
教師通過創設由淺到深的問題情境,加強對學生邏輯推理能力的考查。例如2021年全國甲卷第28題中通過化學反應原理分析陌生的圖表和數據,能在信息加工的基礎上利用所學知識,分析或選擇反應條件。
本文系常州市教育科學“十三五”規劃立項課題:學科核心素養視域下的高中化學課型及教學策略研究(課題編號:CJK-L2020020)的階段性研究成果之一。

