不同激素對蝴蝶蘭葉片類原球莖誘導的影響
朱飛雪 程玉江 寇艷玲 齊陽陽 郭麗

摘要:為提高蝴蝶蘭葉片類原球莖的誘導率,以蝴蝶蘭雜交品種01、02、03、04、05、06、07和08增殖階段組培苗頂部幼嫩葉片為實驗材料,采用1/2MS為基本培養基,添加不同激素種類并設置不同濃度梯度,以探討6-芐基腺嘌呤(6-BA)、腺嘌呤(Ad)、萘乙酸( NAA)、噻苯隆(TDZ)及其組合對蝴蝶蘭葉片類原球莖誘導的影響。結果表明:單獨使用6-BA類原球莖誘導率較低,TDZ的刺激作用強于6-BA;細胞分裂素和生長素的配合使用效果較好,且不同品種所需激素配比具有差異。其中,01、07品種最佳的誘導培養基為1/2MS+TD20.5mg.L-1,誘導率分別為75.3%、82%; 02品種最佳的誘導培養基為1/2MS+TD20.5mg.L-1'+NAAO.1mg.L-1,其誘導率為24%; 04、05、08品種最佳的培養基為1/2MS+TD22mg.L-1+NAAO.1mg.L-1,誘導率分別為75.7%、60.7%、73.3%;03、06品種最佳的培養基為1/2MS+6-BA5mg.L一1+NAAlmg.L一1+Ad3mg.L一1,誘導率分別為440/、50.7%。
關鍵詞:蝴蝶蘭;激素;葉片;類原球莖;誘導率
蝴蝶蘭是單子葉植物綱天門冬目蘭科蝴蝶蘭屬多年生附生植物,主要分布在泰國、菲律賓、馬來西亞、印度尼西亞及中國臺灣等地。其花形奇特,花姿高雅,色澤艷麗,花期持久,有“蘭中皇后”的美譽[1],在國內外花卉市場中,蝴蝶蘭因其花大色艷備受歡迎。因此,蝴蝶蘭已成為蘭科中栽培最廣泛、產業化技術最成熟和最受歡迎的花卉之一,具有廣闊的市場前景[2],隨著人們欣賞水平的提高,人們對花型、花色提出了更高的要求,這就要求蝴蝶蘭育種家能在短時間內選育出符合市場需求的新品種[3]。
蝴蝶蘭多以雜交育種為主,但后代花色變異過大,育種周期又過長[4];而轉基因育種目標性強[5],育種周期短[6],已開始在蝴蝶蘭新品種選育中廣泛應用[7-8]。在轉基因育種中合適目標基因選擇、高效遺傳轉化體系是獲得蝴蝶蘭轉基因植物的前提條件[9]。蘭科轉基因植物成功的關鍵在于促進細胞組織再生為植株。研究發現,由蝴蝶蘭種子[10]、葉片[11]、花梗、腋芽[12]甚至是根部誘導而得到的球形細胞,類似于幼胚發育成的體細胞——類原球莖,在合適的條件下可以再生為完整的植株。因此,在蝴蝶蘭轉基因的研究當中,類原球莖最常被選為受體材料。而原球莖的誘導率是決定轉基因成功的關鍵,很多學者選擇利用蝴蝶蘭葉片誘導出類原球莖。黃磊等[13]、馬生健等[14]、喬永旭等[15]利用蝴蝶蘭葉片來誘導類原球莖,但是類原球莖的誘導率均不高。可見,類原球莖誘導的難度仍然很大,建立一個高效、穩定的類原球莖誘導體系是亟需的,也在蝴蝶蘭組培快繁體系中始終占有重要地位[16]。為此,本實驗以蝴蝶蘭雜交品種01、02、03、04、05、06、07、08增殖階段組培苗頂部幼嫩葉片為實驗材料,以1/2MS為基本培養基,添加不同種類的激素,以期探究適合蝴蝶蘭葉片誘導原球莖的激素種類、濃度以及配比組合,為蝴蝶蘭原球莖誘導高頻再生體系的建立及轉基因育種提供依據。
一、材料與方法
(一)實驗材料
實驗材料為蝴蝶蘭8個栽培品種,代號分別為01(黃花紅心)、02(小黃花)、03(黃花)、04(小白花)、05(白底紅點)、06(四季紅)、07(紅玫瑰)、08(黑花)共八個品種。
(二)實驗方法
切取幼嫩葉片基部0.5 - 1.0cm,正面朝上,接種于以1/2 MS為基本培養基,添加不同濃度的6- BA、TDZ、NAA、Ad,共15種處理,見表1。并附加20%的椰子汁,瓊脂5.0g.L-l,糖20g.L-,pH值5.8。每個處理設三個重復,每個重復接種50個葉片。培養溫度26+1℃,光照強度500 - 600lx散射光,光照時間16h/d,培養50d后統計結果。
(三)數據分析
培養50d后,統計每瓶葉片誘導出的類原球莖、葉片發黃死亡的數量,計算出其類原球莖誘導率以及葉片黃化死亡率(文中簡稱黃死率)。誘導率(%)及黃化死亡率(%)的計算公式如下。 誘導率(%)=類原球莖數/外植體數X100% 黃化死亡率(%)=黃化死亡數/外植體數X100% 實驗統計數據采用Excel和SPSS16.0軟件處理分析。 二、結果與分析 (一)不同濃度6-BA對葉片類原球莖誘導的影響 不同濃度6-BA處理下,不同品種的葉片類原球莖的誘導率不同,結果見表2。由表2可以看出,01-07品種隨著6-BA濃度的增加,類原球莖的誘導率也逐漸增加。8個品種中,01、07品種在6-BA濃度為8mg.L-1時,類原球莖誘導率最高,分別為35.3%和30.0%。尤其07號品種,經方差分析,其誘導率顯著高于其它兩個處理。02、04、08品種的誘導率最低,在6-BA濃度(mg.L-1)為3、5時,誘導率均為o;當升至8mg.L-時,02、04品種的誘導率分別增加至11%和6%,08品種的誘導率仍然是0。從實驗結果可以得出,高濃度的6-BA有利于誘導出葉片原球莖。但是,從表2中可以看出,01品種在3個濃度上較高的原球莖誘導率為35.3%、30.0%、26.0%,其它幾個品種則更低,均不超過20.0%。表明單獨使用6-BA誘導出的葉片原球莖數量較少。
由表2還能看出,除了6-BA濃度會影響葉片原球莖的誘導之外,品種之間的差異也較大,尤其是08品種,即使6-BA濃度增加至8mg.L-1,其誘導率仍然是0。
(二)6-BA與NAA組合對葉片原球莖誘導的影響
在添加3、5、8 (mg.1-1) 6-BA的基礎上,添加Img.L-1的NAA處理下的葉片原球莖的誘導率不同,結果見表3。
從表3可以看出,01、03、08品種,在NAA濃度為Img.L-1時,其葉片原球莖誘導率隨著6-BA濃度的增加而增加,最高的誘導率為01號品種,當6-BA濃度為8mg.L-1時,其誘導率為46.0%;其次為03品種,其最高誘導率為36.0%。04、05、07品種,在3個處理上的葉片原球莖誘導率都很低,尤其是04、05品種,其誘導率均為0。
由此可見,除了6-BA、NAA會影響葉片原球莖的誘導之外,品種之間的差異對誘導率影響也較大,不同品種,葉片原球莖誘導所需激素種類及配比也不同,這和第一個實驗結果一致。
(三)6-BA、NAA和Ad組合對葉片原球莖誘導的影響
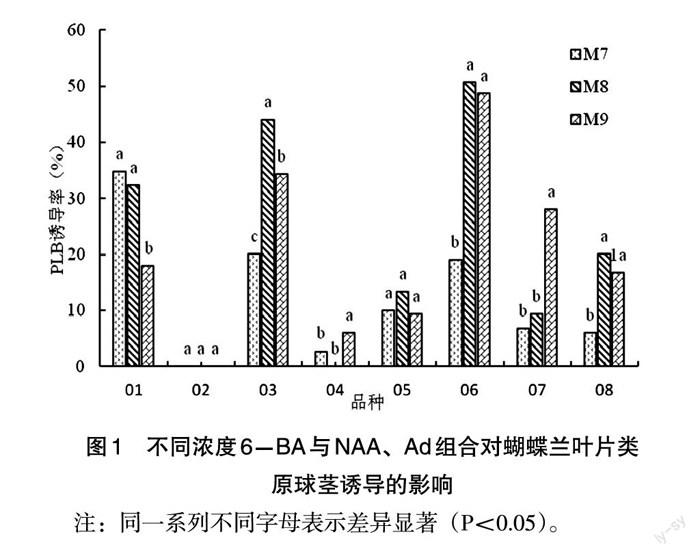
6-BA與NAA、Ad配合使用時,蝴蝶蘭葉片類原球莖的誘導率不同,見圖l。由圖1可以看出,03、04、05、06、07、08品種,三種激素協同作用較明顯,其中03、05、06品種在6-BA5mg.L-1+NAAlmg.L-1+Ad 3mg.L“時,類原球莖誘導率分別由使用6-BA和NAA組合的36.0%、3.3%、26.7%提高到44.0%,13.0%、50.7%;04、07、08品種,其誘導率隨著6-BA濃度增加而逐漸增加;01品種三者協同作用不明顯,隨著6-BA濃度的增加,其誘導率逐漸降低,且誘導率低于其他處理;02品種三者協同作用較差,在三個處理上,其誘導率均為0。
(四)TDZ、NAA對葉片誘導的影響
TDZ對蝴蝶蘭葉片類原球莖誘導具有顯著作用,其與NAA的配合使用表現較強的協同效應,結果見表4。除01、07品種在單獨使用TDZ 0.5 mg.L-1時,達到最大誘導率75.3%、82.0%外,其他品種均在TDZ、NAA配合使用時有最大誘導率。經方差分析,07品種在單獨使用TDZ 0.5 mg.L-l時,其葉片類原球莖誘導率顯著高于其他幾個處理。04、05、08品種,在TDZ2 mg.L-l+NAA 0.1mg.L-1時,類原球莖誘導率最高,分別為76.7%、60.7%、72.7%,方差分析表明,這三個品種在這個處理上的葉片類原球莖誘導率顯著高于其他幾個處理。02、03、06品種在TDZ 0.5 mg.L-l+NAA 0.1mg.L-1時類原球莖誘導率最高,分別為24.0%、28.0%、26.0%,從表4中可以看出,這三個品種在這6種培養基上,其誘導率均較低,從而說明除激素種類、濃度影響類原球莖誘導率外,品種之間的差異對其影響也較大。
實驗過程中觀察發現,品種不同,葉片黃化死亡率不同(見表5)。由表5可以看出,在M11處理上,其葉片黃化死亡率最低,最高的為03品種,其黃化死亡率為17.0%,其他幾個品種均為0。由表5還可以看出,品種之間差異較大,01、02、06在幾個處理中其黃化死亡率均為0,03品種的黃化死亡率較高,其他幾個品種在不同處理上黃化死亡率不同。
在這6個處理中,從接種到結果統計觀察發現,接種外植體的外觀表現無明顯差異,一般是接種1-2周后,葉片切口變黃或變黑,未見褐化;2-3周后,無明顯變化或個別葉片有黃化、褐化;3-4周后,黃化、褐化葉片增多,生成物出現;4-6周,生成物數逐漸增多,褐化、黃化葉片也增多。50d后葉片誘導生成物明顯出現類原球莖。
三、討論
對不同植物種類而言,能否誘導類原球莖的發生,主要取決于植物自身基因型和誘導條件兩個方面。培養基種類、激素種類與配比、糖分比例及光照等都是需要考慮的誘導條件,其中,激素種類與配比對誘導效果影響最大。在蝴蝶蘭[17-18]、石斛蘭[19-20]、大花蕙蘭[21-22]和文心蘭[23-24]等蘭花類原球莖誘導過程中,細胞分裂素(6-BA、Ad或KT)與生長素(2,4-D、NAA、IBA)組合有不同誘導效果。
本實驗中使用6-BA、6-BA與NAA組合、6-BA與NAA和Ad組合誘導蝴蝶蘭葉片原球莖,單獨使用6-BA,在8個品種中,01-07號品種隨著濃度的增加,原球莖的誘導率也在增加,其中01、07品種在6-BA濃度為8mg.L-1時,類原球莖誘導率最高,分別為35.3%和30.0%。02、04、08品種的誘導率最低,在6-BA濃度(mg.L-1)為3、5時,誘導率均為0;當6-BA濃度為8mg.L-l時,02、04品種的誘導率分別增加至11.0%和6.0%,08品種的誘導率仍然是0。從實驗結果可以得出,高濃度的6-BA有利于誘導出葉片類原球莖,這和喬永旭等[25]、張玉等[26]的研究結果一致。
TDZ因其極高的生物活性,被廣泛應用于植物類原球莖的誘導[27],也被認為是在蘭科植物類原球莖誘導過程中最有效的激素,付雙彬等[28]在誘導虎頭蘭原球莖時,單獨加入3mg.L-1,在30d時即可使80%的組培苗誘導產生類原球莖,而在90d后則可使其達到100%。在本實驗中,單獨使用TDZ和使用TDZ與NAA組合兩種處理,實驗結果發現,TDZ對蝴蝶蘭葉片誘導具有顯著作用,其與NAA的配合使用,表現較強的協同效應。這與李娜等[29]的結果一致。除01、07品種在單獨使用TDZ 0.5 mg.L-1時,達到最大誘導率外,其誘導率分別為75.3%、82%,其他品種均在TDZ、NAA配合使用時有最大誘導率。其中04、05、08品種,在TD22 mg.L-l+NAA O.lmg.L-1時,原球莖誘導率最高,分別為76.7%、60.7%、73.3%;02、03、06品種在TDZ 0.5mg.L-+NAA O.lmg.L-1時原球莖誘導率最高,分別為24.0%、28.0%、26.0%。品種不同,誘導率差異也較大,因此,除了激素種類、濃度會影響原球莖誘導率外,品種不同葉片誘導所需激素種類及配比也不同。
參考文獻:
[1]韓思儀,崔永一,蝴蝶蘭原球莖組織防褐化研究[J].江蘇農業科學,2019,47(13):67-71.
[2]謝利,劉芳,易懋升,等.蝴蝶蘭倍性與葉部和花部性狀的相關性[J].華南農業大學學報,2014,35(05):82-87.
[3]楊錄軍,王俊,趙玉安,等.蝴蝶蘭葉片離體培養胚胎組織的發生[J].陜西農業科學,2013f06):7-10.
[4]顧德峰,趙春莉,宋彥君,等,蝴蝶蘭無性快繁規模化生產的研究[J].園藝學報,2007,34(01):193-196.
[5]莊東紅,曲瑩,徐大熊,等.蝴蝶蘭若干品種(系)的染色體數和形態分析[J].園藝學報,2007,34(05):1257-1262.
[6]劉學慶,王秀峰,樸永吉,蝴蝶蘭不同品種耐冷特性的報告[J].園藝學報,2007,34(02):425-430.
[7]許傳俊,周文靈,陳冬茵,等,蝴蝶蘭多酚氧化酶基因克隆及其序列分析[J].同藝學報,2009,36(12):1799-1804.
[8]許傳俊,孫敘卓,李玲,等.蝴蝶蘭抗壞血酸過氧化物酶基因克隆及其表達研究[J].園藝學報,2012,39(04):769-776.
[9]高壯壯.蝴蝶蘭再生體系建立及轉藍色形成基因研究[D].咸陽:西北農林科技大學,2020.
[10]張和臣,董曉宇,王利民,等,以蝴蝶蘭種子萌發的原球莖為受體的遺傳轉化體系構建[J]河南農業科學,2016,45(08):107-111+124.
[11]卜朝陽,蔣慧萍,滿若君.蝴蝶蘭花梗離體培養及葉片誘導類原球莖研究[J].江蘇農業科學,2008(03):147-150.
[12]張彥妮,邊紅琳,陳立新,蝴蝶蘭幼嫩花梗組織培養和快速繁殖[J].草業科學,201 1,28(04):590-596.
[13]黃磊,陳之林,吳坤林,等,切割方式和外植體大小對蝴蝶蘭葉片誘導類原球莖的影響[J].熱帶亞熱帶植物學報,2009,17(03):261-266.
[14]馬生健,楊艷梅,不同激素對蝴蝶蘭幼葉誘導原球莖的影響[J].廣東農業科學,201 1,38(10):36-37.
[15]喬永旭,張永平,陳超,等,蝴蝶蘭組培苗類原球莖的誘導與分化[J]北方園藝,2010(04):13 8-141.
[16]于旋.蝴蝶蘭類原球莖農桿菌介導的轉基因體系構建[D].杭州:浙江農林大學,2015.
[17]崔廣榮,侯喜林,張子學,等,蝴蝶蘭葉片離體培養胚狀體的發生及組織學觀察[J].園藝學報,2007,34(02):431-436.
[18]聶菁,劉麗鳳,任海虹,等,蝴蝶蘭類原球莖誘導、增殖及植株再生條件初步研究[J]山西大學學報(自然科學版),2016,39(02):318-324.
[19]陸順教,易雙雙,冷青云,等.秋石斛原球莖途徑再生體系的建立[J].分子植物育種,2017,15(03):1014-1021.
[20]任海虹,王景雪,聶菁.鐵皮石斛原球莖高效再生體系的研究[J].中草藥,2017,48(19):4057-4061.
[21]袁芳,宋凱杰,楊澤東,等,鐵皮石斛莖段類原球莖的誘導及植株再生[J]東北農業科學,2019,44(04):66-71.
[22]吳開云,黃敏仁,王明庥.大花蕙蘭幼苗葉片誘導類原球莖[J]分子植物育種,2007,5(03):341-346.
[23]徐萌,郭紹霞,孫麗,等,大花蕙蘭原球莖誘導、增殖與分化影響因素研究[J].北方園藝,2016,(16):108-110.
[24]陳曉旋,李洪波,葉春海,等,文心蘭類原球莖的誘導與增殖技術的優化[J]熱帶作物學報,2010,31(09):1464-1468,
[25]喬永旭.蝴蝶蘭類原球莖的誘導[J]東北林業大學學報,201 1,39(03):34-36.
[26]張玉,李艷敏,張和臣,等,蝴蝶蘭葉片誘導類原球莖初探[J].河南農業科學.2012,41(02):126-128+135.
[27]姜福星,劉鳳欒,趙梁軍,植物類原球莖的研究與應用[J].核農學報,2012.26(03):0478-0483.
[28]付雙彬,池夢薇,楊燕萍,等,虎頭蘭類原球莖誘導、增殖及保存[J]北方園藝,2020(10):71-77.
[29]李娜,楊蕾蕾,陳朋,等,蜻蜓石斛類原球莖的誘導與植株再生系統建立[J].植物生理學報,2021,57(12):166-171.
基金項目:2020年河南省科技廳科技攻關重點研發與推廣專項“野生薄皮快繁體系及工廠化育苗關鍵技術的研究”,項目編號:212102110188;2021年河南農業職業學院自然科學基金項目“大巖桐花粉活力檢測及貯藏關鍵技術研發與應用”,項目編號:HNACKY-2021-03;2021年河南農業職業學院科研創新人才項目“新優景觀植物藍花丹快繁體系及工廠化育苗的研究”,項目編號:HNACSRHR-2021-04。
作者簡介:朱飛雪(1979-),女,河南平頂山人,碩士,講師,研究方向:園林植物種質資源與育種。
(責任編輯曹雯梅)

