某院頭孢菌素類藥物皮試管理規定實施前后皮試情況對比
閆琴琴 吳雪
摘要:目的 為醫療機構規范頭孢菌素類藥物皮試的執行標準提供參考。方法 調取2018年4月—2019年3月(實施前)、2019年4月—2020年3月(實施后)各病區使用過頭孢菌素的病例,對兩組皮試率及過敏反應發生情況進行回顧性分析。結果? ? 實施皮試管理規定后,全院頭孢菌素皮試率由97.81%下降至70.71%,前后比較差異有統計學意義(P<0.01),其中臨床藥師重點參與宣教干預的婦、產、兒科病區皮試率分別從99.91%降至6.58%、98.9%降至8.13%、100%降至17.37%。說明書明確規定需皮試的品種用量較前下降33.28%。兩組過敏反應發生率并無明顯差異(P>0.05)。結論? ? 為保證醫療質量和醫療安全,頭孢菌素類藥物皮試亟待規范。建議取消頭孢普遍篩查,做好詳細詢問過敏史和防范救治措施更為重要。
關鍵詞:頭孢菌素;皮試;過敏反應
中圖分類號:R978.1? ? ? 文獻標志碼:A
Comparison of skin test before and after the implementation of the regulations on the skin test of cephalosporins in a hospital
Yan Qin-qin and Wu Xue
(Department of Pharmacy, the 924th Hospital of PLA Joint Service Support Force, Guilin 541002)
Abstract Objective To provide references for medical institutions to standardize the implementation of standard cephalosporin drug skin test. Methods From April 2018 to March 2019 (before the implementation) and from April 2019 to March 2020 (after the implementation), the data of patients who had received cephalosporin in each ward were collected. The skin test and the occurrence of allergic reactions in the two groups were analyzed retrospectively. Results After the implementation of the skin test management regulations, the skin test rate of cephalosporin in the whole hospital decreased from 97.81% to 70.71%, and the difference was statistically significant (P<0.01). The skin test rate in the gynecology, obstetrices, and pediatrics wards mainly involved in the direct education intervention decreased from 99.91% to 6.58%, 98.9% to 8.13%, and 100% to 17.37%, respectively. The specification clearly stipulated that the amount of varieties to be skin tested was 33.28% lower than before. There was no significant difference in the incidence of allergic reactions between the two groups (P>0.05). Conclusion In order to ensure medical quality and safety, skin test of cephalosporins should be standardized urgently. It is recommended to cancel the universal cephalosporin screening, and it is more important to inquire about the history of allergy and provide preventive treatment measures.
Key words Cephalosporin; Skin test; Allergic reaction
頭孢菌素類藥物因其抗菌譜廣、組織穿透力強、不良反應少等特點廣為臨床應用。使用頭孢菌素類藥物前是否需要進行皮膚過敏試驗(以下簡稱“皮試”),目前國內外仍尚有爭議。《中華人民共和國藥典臨床用藥須知》(2015版)中對此未做明確規定,不同廠家藥品說明書的要求也表述各異,從而造成不同醫院、同一醫院不同病區之間頭孢菌素皮試執行的情況差異較大。目前美國和歐洲大部分國家不進行皮試[1]。日本2004年學術組織建議停用頭孢菌素等抗菌藥物皮試[2],2009年回顧過敏反應統計后再次肯定不做皮試決定。頭孢菌素皮試的影響因素較多,皮試液的品種、濃度、配制、操作規范等沒有統一標準,因此頭孢菌素皮試預測價值極低[3-4]。目前頭孢類藥物皮試假陽性率、假陰性率均高,皮試符合率僅小于30%[5]。因此,常規進行頭孢菌素類藥物皮試的意義不大。
中國人民解放軍聯勤保障部隊第九二四醫院從2019年4月起發布并實施《藥物皮膚過敏試驗管理規定》(以下簡稱“皮試管理規定”),對頭孢類藥物是否需要皮試做了明確規定。本文對比分析自皮試管理規定實施前后1年各病區頭孢菌素皮試率下降情況,以及過敏反應發生情況,旨在為規范頭孢菌素皮試提供參考。
1 資料與方法
1.1 一般資料
中國人民解放軍聯勤保障部隊第九二四醫院皮試管理規定如下:(1)有以下情況者需皮試:①本院現有品規藥品說明書明確要求進行皮試的,如:頭孢噻肟、頭孢米諾、頭孢甲肟;②既往有明確β-內酰胺類抗生素速發型過敏反應史的患者;③既往有頭孢菌素過敏史的患者,因臨床情況確需使用時,應盡量選用化學結構側鏈差異大的其他頭孢以減少或避免交叉過敏反應的發生,且使用前應用擬用藥品做皮試;皮試和使用前應知情告之并請患者填寫相關知情同意書。(2)說明書中無要求的,皮試不列為常規[6]。
以2018年4月—2020年3月在中國人民解放軍聯勤保障部隊第九二四醫院住院并使用頭孢菌素類針劑的患者為研究對象進行回顧性分析。
1.2 方法
1.2.1 分組
將研究對象分為兩組。干預前組:皮試管理規定發布實施前1年即2018年4月—2019年3月的樣本數;干預后組:皮試管理規定發布實施后1年即2019年4月—2020年3月的樣本數。干預方法:臨床藥師進行以下幾方面宣教:①認識皮試的局限性;②詳細詢問過敏史比皮試更重要,甄別真假過敏;③做好處置速發型過敏反應的充分準備。從美康合理用藥信息支持系統分別提取上述兩組使用過頭孢菌素類針劑的樣本數,以及其中進行皮試的樣本數。計算皮試率(皮試率=行皮試樣本數/使用過頭孢菌素類針劑樣本數×100%)。統計兩組說明書明確規定需皮試的品種的用量。
排除標準:去除使用過注射用頭孢噻肟、注射用頭孢米諾鈉、注射用鹽酸頭孢甲肟3種說明書要求皮試的樣本。
1.2.2 統計分析
統計兩組過敏反應發生樣本數,數據主要來自醫護人員上報不良反應監測系統。發生在給藥后數分鐘到1 h的統計為速發型過敏,大于1 h的為遲發型。對兩組過敏反應進行對比分析。
1.3 統計學方法
選擇統計學軟件SPSS20.0進行統計數據分析,其中計數資料以n(%)形式表示,采用卡方(χ2)兩組數據皮試率、過敏反應發生率予以檢驗,P<0.05表示差異有統計學意義。
2 結果
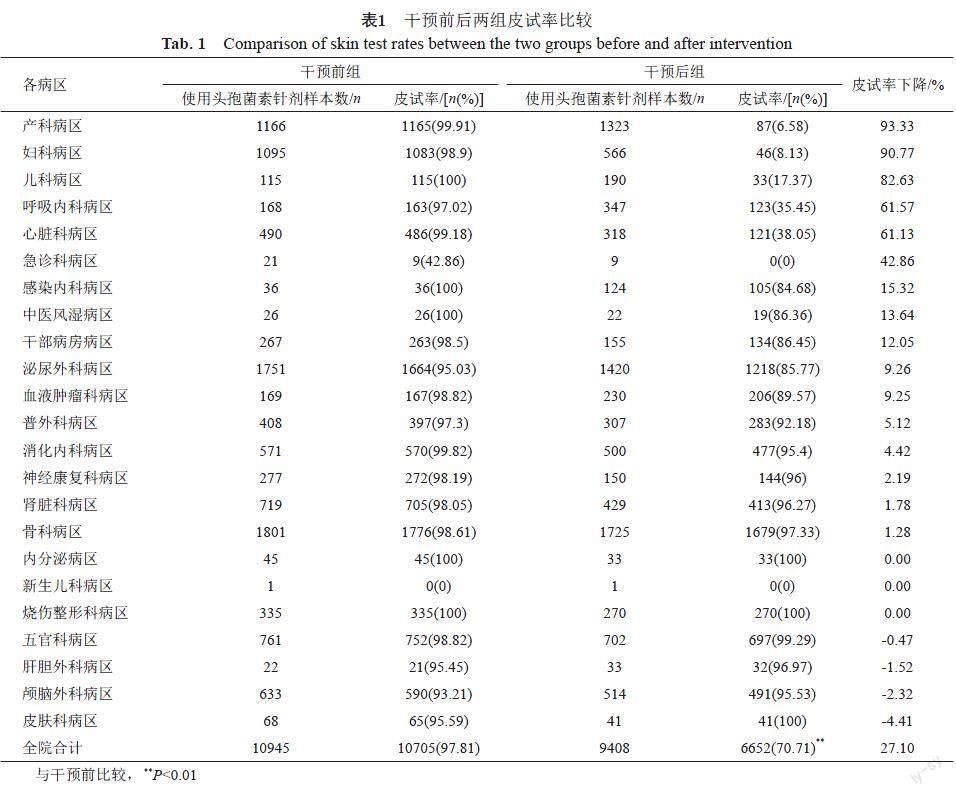
2.1 干預前后兩組皮試率對比
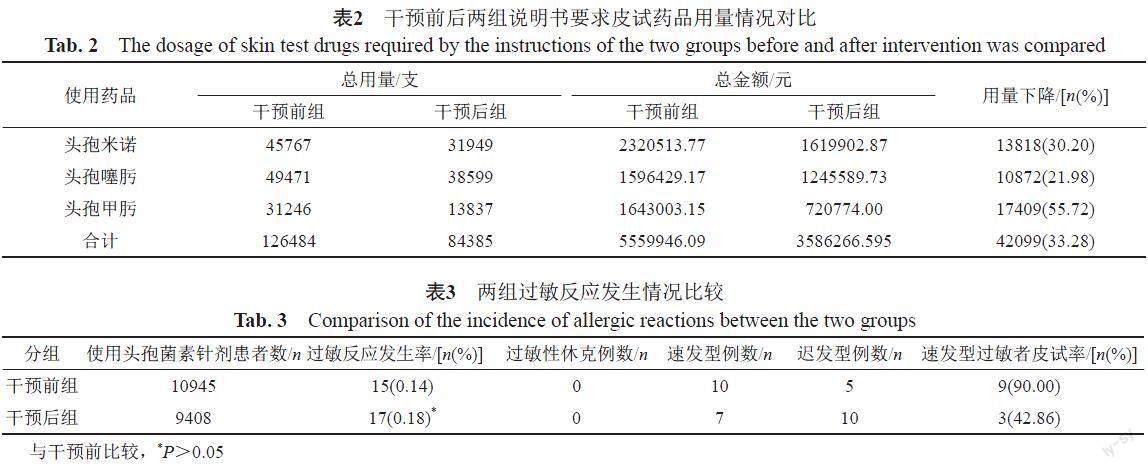
實施皮試管理規定后全院總體皮試率下降,與實施前對比,差異明顯,具有統計學意義(P<0.01)(表1)。干預后醫生盡量選擇說明書不要求皮試的品種,要求皮試品種用量下降(表2)。
2.2 兩組過敏反應比較
收集干預前后兩組頭孢過敏不良反應共32例,男性11例,女性21例,年齡最小者9個月,最大72歲。過敏史:1例有磺胺類藥物過敏史,22例無過敏史,9例不詳。使用藥物為:頭孢美唑2例,頭孢哌酮舒巴坦2例,頭孢曲松5例,頭孢他啶2例,頭孢噻肟10例,頭孢呋辛2例,頭孢甲肟1例,頭孢唑肟2例,頭孢唑林3例。過敏反應表現均主要為:皮疹瘙癢、蕁麻疹29例,寒顫發冷2例,面部潮紅心慌胸悶1例。兩組過敏反應發生率無明顯差異(P>0.05)(表3)。
3 討論
實施皮試管理規定后,中國人民解放軍聯勤保障部隊第九二四醫院頭孢菌素皮試率較實施前下降27.1%。其中婦、產、兒科下降均達80%以上,尤其產科除一些有既往過敏史的患者予以皮試外,其余患者均不再行皮試,皮試率下降達93%。這與中國人民解放軍聯勤保障部隊第九二四醫院臨床藥師多次在婦產兒等科室進行皮試相關宣教工作密切相關。通過對各科室皮試率統計分析,仍有部分病區皮試開展高達100%,這主要與醫護人員對頭孢過敏反應認識欠缺,對過敏史判斷草率,認為進行皮試可以規避醫患糾紛,進行自我保護有關。臨床藥師應重點加強用藥宣教,提高醫、護、藥等專業人員對頭孢過敏反應的認識。
不同于青霉素類藥物,頭孢菌素過敏反應機制目前尚未完全闡明,并且藥物皮試僅能預測速發型過敏反應,對遲發型過敏反應不具備預測價值[3]。本文兩組的過敏反應發生例數并無明顯差異,說明減少皮試并未導致過敏不良反應的增加。干預前組發生速發型過敏反應者中,90%的患者用藥前曾進行過皮試且皮試結果均為陰性,由此也可以反映出頭孢皮試的假陰性率較高,皮試結果對過敏與否的預測價值有限。頭孢皮試的普遍篩查將大幅縮窄患者治療選擇,尤其是兒童,本身能選擇的品種少。皮試假陽性必然導致不必要的高檔廣譜、不良反應多的抗生素的濫用,如碳青霉烯類、糖肽類以及喹諾酮類,氨基糖苷類等。同時增加患者經濟負擔以及增加護士工作量。
對于使用前是否需要皮試,有些藥品說明書表述不明確,如注射用鹽酸頭孢甲肟說明書示“建議在注射前做皮膚過敏反應試驗”,此表述臨床難以把握,且容易產生糾紛。另外同一藥品不同廠家對皮試的要求也不一樣,我國市場上銷售的幾十種注射用頭孢曲松鈉制劑說明書中,部分規定需要進行皮試,部分則并未做常規要求。為便于臨床應用,中國人民解放軍聯勤保障部隊第九二四醫院也將說明書是否明確皮試作為修改抗菌藥物目錄的一項參考標準,如采取將頭孢甲肟品種剔除目錄,引進上海羅氏頭孢曲松等措施。
本研究也存在局限性:①因本次研究樣本較少,尤其是不良反應,可能有些無相關記錄或未上報導致統計不全。可收集多地區多家醫院樣本數據,評價頭孢類藥物皮試的利與弊,從而明確頭孢是否需要皮試的臨床實踐。②對頭孢菌素類之間交叉過敏未作相關研究。③因為條件限制,未對相關藥物經濟學進行過多評價。
頭孢菌素去皮試目前在全國多家醫院形成制度,國家有關部門也將發布β-內酰胺類抗生素皮膚試驗指導原則。另外國家應加強規范頭孢菌素類藥物生產質量標準,規范藥品說明書的制定。各醫療機構也可根據自身情況制定皮試管理規定,以規范頭孢菌素類藥物的皮試執行,保障患者用藥安全及醫護人員醫療行為的合法性。
參 考 文 獻
[1]鄭波. 客觀對待頭孢菌素類抗生素的皮試[J]. 中華內科雜志, 2014, 53(6): 435-436.
[2]厚生勞動省醫藥食品局. 醫藥品. 醫療用具等安全性情報[EB/OL]. (2004-10)[2014-03-06]. http://www.mhlw.go.p/houdou/2004/10/h1028-2a.html.
[3]重慶市藥事管理質量控制中心. 重慶市頭孢菌素類抗菌藥物皮膚過敏試驗共識[EB/OL].(2018-12-7). http://guide.medlive.cn/.
[4]趙曙剛, 汪林嬌. 基于藥品說明書對β-內酰胺類抗生素皮膚過敏試驗臨床意義的探討和建議[J]. 中國醫藥科學, 2020, 10(5): 27-31.
[5]北京藥學會抗生素專業委員會. 頭孢類抗菌藥物皮膚過敏試驗高端論壇專家共識[J]. 臨床藥物治療雜志, 2008, 6(4): 1-2.
[6]浙江省醫院藥事管理質控中心. 浙江省頭孢菌素類抗生素皮膚過敏試驗指導意見[EB/OL].(2018-9-19). http://guide.medlive.cn/.

