小鼠IL-1Ra蛋白的原核表達及其多克隆抗體制備
戰俊澎 鄒德穎 常江 楊馨 郭珣 張凱 劉益辛 胡盼 盧士英 李巖松 柳增善 任洪林


摘要:以小鼠脾臟cDNA為模板,用降落PCR擴增IL-1Ra基因片段,IL-1Ra基因片段長約為537 bp。將IL-1Ra擴增片段和原核表達載體pET-30a(+)連接構建重組表達質粒,在37 ℃誘導表達,重組表達的小鼠IL-1Ra蛋白的分子質量為19 ku。用純度較好的小鼠IL-1Ra重組蛋白免疫兔子,制備特異性多克隆抗體;測定多克隆抗體的效價達到1 ∶4 096 000。經Western-Blot鑒定該抗體可與Raw264.7細胞中表達的小鼠IL-1Ra天然蛋白發生特異性結合。利用實時熒光定量PCR和Western-Blot檢測表明布魯氏菌S2弱毒株感染Raw264.7細胞(小鼠單核巨噬細胞)后小鼠IL-1Ra上調表達。本研究成功制備了小鼠IL-1Ra重組蛋白和兔抗多克隆抗體,為深入探討小鼠IL-1Ra與布魯氏菌感染之間的關系提供工具。
關鍵詞:小鼠;IL-1Ra;原核表達;多克隆抗體;IL-1Ra重組蛋白
中圖分類號:S858.91 ??文獻標志碼: A
文章編號:1002-1302(2022)09-0037-06
白介素-1(IL-1)家族是最早報道的細胞因子家族之一,由8個細胞因子(IL-1β、IL-1α、IL-18、IL-33、IL-36α、IL-36β、IL-36γ、IL-37)和3個受體拮抗劑(IL-1Ra、IL-36Ra、IL-38)組成[1]。IL-1Ra是IL-1的1個結構變體,與 IL-1R 結合的親和力幾乎與IL-1相同,但不能激活細胞[2-3]。盡管IL-1及IL-1Ra與 IL-1RⅠ 具有相似的親和力,但是由于少數IL-1與IL-1RⅠ結合便足以完全激活細胞免疫應答,而且多數細胞中IL-1RⅠ表達水平較高,在表達 IL-1Ra 的細胞中至少需要100~1 000倍過量的IL-1Ra才能抑制50%的IL-1反應[4-5]。IL-1Ra 包括4個亞型,1個分泌型(sIL-Ra1)和3個胞內型(icIL-1Ra1、icIL-1Ra2、icIL-1Ra3),其中sIL-Ra1和icIL-1Ra1與IL-1R結合良好,而icIL-1Ra3與受體結合能力較弱[6]。IL-1Ra可以減輕被注射脂多糖(LPS)的兔子產生嚴重的低血壓,并在免疫復合物誘導的炎癥性腸病動物模型中減輕IL-1介導的腸道炎癥和壞死,證明IL-1Ra在一些病理情況下有助于逆轉IL-1所引起的炎癥反應[7-8]。
IL-1β與IL-1Ra已經證明在維持腸道穩態,炎癥性腸病(IBD)和炎癥性結直腸癌(CRC)的發病機制中存在2種不同的甚至相反的功能[9-10]。過量的IL-1釋放會引起嚴重的炎癥反應及自身免疫類疾病[11]。而IL-1Ra重組蛋白與不同藥物聯用可以有效治療一些疾病,目前IL-1Ra也可應用于基因治療[12]。目前已有研究證明,IL-1Ra重組蛋白對治療類風濕關節炎是有效果的[13]。筆者所在課題組前期通過構建布魯氏菌強毒株、弱毒株感染綿羊白細胞層抑制性消減雜交(SSH)cDNA文庫,篩選到2種差異表達的基因——IL-1β和 IL-1Ra,并證明了布魯氏菌S2疫苗株與野毒株感染可引起這2個基因差異表達[14]。且目前國內外未見同時針對IL-1β及IL-1Ra與布魯氏菌之間關系的研究報道,因此對IL-1Ra分子特征與生理病理功能的研究將有助于探究其與布魯氏菌感染之間的關系。
本研究擬通過構建重組質粒pET-30a-Ra并進行原核表達,對重組蛋白進行純化,免疫動物制備抗小鼠IL-1Ra重組蛋白的多克隆抗體,以期探究小鼠IL-1Ra與布魯氏菌感染之間的關系。
1 材料與方法
試驗在吉林大學人獸共患病研究所細菌實驗室內進行,試驗時間為2020年7月至2021年9月。
1.1 材料
布魯氏菌S2弱毒株、原核表達載體pET-30a(+),大腸桿菌BL21(DE3)和大腸桿菌DH5α感受態細胞、Raw264.7細胞由筆者所在實驗室保存;SPF級雌性兔子購自遼寧長生生物技術股份有限公司;TRIzol、反轉錄試劑盒,ES-Taq酶,DL2000 DNA maker,限制性內切酶NdeⅠ、XhoⅠ,T 4 DNA 連接酶和pMDTM18-T Vector Cloning Kit均購自TakaRa公司;質粒小提試劑盒和膠回收試劑盒購自天根生物科技(北京)有限公司;彩虹預染蛋白marker和M5 HiPer ECL Western HRP Substrate(超敏ECL發光液)購自北京聚合美生物科技有限公司;弗氏不完全和弗氏完全佐劑購自美國Sigma公司;TMB顯色液A液和B液購自北京梅科萬德生物科技有限公司;HRP標記的山羊抗兔IgG抗體購自安諾倫生物科技有限公司。
1.2 引物設計與合成
鼠源IL-1Ra基因的CDS序列(登錄號:NM 001039701.3)來源于NCBI數據庫。引物序列如下:上游引物,5′-GGAATTCCATATGCGCCCTTCTGGGAAAAGACCCTGCAAGATGCAAGCCTTCA-3′;下游引物,5′-CCGCTCGAGCTAATGGTGATGGTGATGATGTTGGTCTTCCTGGAAGTAGAACTT-3′(下劃線部分分別為NdeⅠ和XhoⅠ酶切位點)。引物合成自吉林省庫美生物科技有限公司。
1.3 目的片段的擴增
用TRIzol法提取小鼠脾臟總RNA,用反轉錄試劑盒反轉錄合成cDNA,-80 ℃分裝,保存。以小鼠脾臟cDNA為模板,降落PCR擴增得到小鼠IL-1Ra基因的CDS區序列。PCR反應總體系為 20 μL:模板2 μL,2×Es Taq MasterMix(Dye) 10 μL,上下游引物各1 μL,ddH 2O 6 μL。降落PCR擴增程序為:95 ℃ 7 min;95 ℃ 1 min、72 ℃ 40 s、72 ℃ 1 min,每1個循環降低1 ℃,共23個循環;94 ℃ 1 min、60 ℃ 40 s、72 ℃ 1 min,共25個循環;72 ℃ 10 min。1.0%瓊脂糖凝膠電泳驗證產物正確后,用膠回收試劑盒回收目的片段。將純化好的目的片段與pMD-18T載體連接后轉化入DH5α感受態細胞,用西林瓶涂布于含有氨芐的LB固體平板上,37 ℃培養12 h后挑取單個菌落進行菌液PCR鑒定,將鑒定正確的菌株送去測序,鑒定正確的質粒命名為pMD-18T-Ra。3C7D4F95-0118-493B-927E-EE6BECA5C702
1.4 pET-30a-Ra重組質粒的構建
從測序正確的重組菌株和保種的pET-30a(+)菌株中提取質粒。將pMD-18T-Ra質粒和 pET-30a(+) 空質粒分別用NdeⅠ和XhoⅠ這2種限制性核酸內切酶在37 ℃進行雙酶切5 h,利用T 4 DNA連接酶將IL-1Ra與pET-30a(+)載體 16 ℃ 過夜連接,連接產物轉化至DH5α感受態細胞,用西林瓶涂布于含有卡那霉素的LB固體平板上,37 ℃培養12 h后挑取單個菌落進行菌液PCR鑒定,取正確的重組質粒進一步用NdeⅠ和xhoⅠ進行雙酶切驗證,將鑒定正確的菌液送去測序,將正確的質粒命名為pET-30a-Ra。
1.5 IL-1Ra重組蛋白的誘導表達及可溶性分析
將重組克隆質粒pET-30a-Ra轉入BL21(DE3)感受態細胞中,用西林瓶涂布于含有卡那霉素的LB固體平板上,挑取單克隆菌株,接種于LB液體培養基中培養并測序。小鼠IL-1Ra表達菌分別在37 ℃和16 ℃,加入終濃度為1 mmol/L異丙基硫代半乳糖苷(IPTG)對菌液進行誘導表達。一段時間后收集菌體重懸(緩沖液:50 mmol/L Tris-HCl(pH值7.6)、10%甘油、0.5 mol/L NaCl、10 mmol/L咪唑)后并超聲破碎,分別對上清和包涵體進行聚丙烯酰氨凝膠(SDS-PAGE)電泳,分析目的蛋白表達形式,確定目的蛋白上清表達的最佳表達條件。
1.6 IL-1Ra重組蛋白的純化
將pET-30a-Ra陽性菌液以1 ∶100接種至 1 L 含卡那霉素的液體LB培養基中,按照“1.5”節誘導表達步驟進行誘導表達。超聲破碎后的細菌裂解液12 000 r/min離心40 min,取上清與 Ni-NTA Beads 于4 ℃孵育結合1 h,分別用含有不同咪唑濃度(40、60、80、150、250 mmol/L)的洗脫緩沖液(50 mmol/L Tris-HCl(pH值7.6)、10%甘油、0.5 mmol/L NaCl、10 mmol/L咪唑)進行梯度洗脫,分別收集洗脫液進行SDS-PAGE電泳鑒定,以確定將目的蛋白洗脫下來的緩沖液咪唑濃度。純化好的蛋白裝進透析袋中,在磷酸緩沖鹽溶液(PBS緩沖液)中24 h內透析4次,PEG2000濃縮后用BCA標準蛋白試劑盒檢測蛋白濃度為1.2 mg/mL。
1.7 多克隆抗體制備
免疫前耳緣靜脈采集陽性血清,將重組IL-1Ra蛋白采用背部皮下多點注射的方式免疫新西蘭大白兔,每次間隔7 d,共免疫5次。初次免疫時800 μg重組蛋白與弗氏完全佐劑等體積混合均勻,之后的加強免疫用400 μg重組蛋白與弗氏不完全佐劑等體積混勻,5次免疫后3 d耳緣靜脈采集血液分離血清。
1.8 多克隆抗體效價的測定
采用間接酶聯免疫吸附試驗(ELISA)測定采集分離血清中的抗體效價。用重組IL-1Ra蛋白? 5 μg/mL 100 μL/孔包被ELISA酶標板,37 ℃培養箱包被2 h;PBST洗滌3次,5%脫脂乳(5 g脫脂奶粉溶解于100 mL PBST中) 200 μL/孔,37 ℃封閉 1 h;PBST洗滌3次,將兔抗IL-1Ra多克隆抗體進行倍比稀釋,免疫前血清作為對照的陰性血清,100 μL/孔,37 ℃孵育1 h;PBST洗滌3次,HRP標記的山羊抗兔IgG抗體1 ∶4 000倍稀釋,100 μL/孔,37 ℃孵育1 h;PBST洗滌3次,將TMB顯色A液和B液等體積混合,100 μL/孔,37 ℃避光 8 min,加入終止液,50 μL/孔,立即使用酶標儀450 nm波長處測量D值。
1.9 多克隆抗體反應原性鑒定
收集Raw264.7細胞沉淀,用混合好的RIPA裂解液(1%PMSF)裂解細胞,4 ℃ 10 000 r/min 離心10 min,吸取上清后加入蛋白上樣緩沖液,煮沸 10 min,經SDS-PAGE電泳后轉印至聚偏二氟乙烯(PVDF)膜上,將PVDF浸沒在5%脫脂乳(5 g脫脂奶粉溶解于100 mL TBST中)中在水平搖床上室溫封閉2 h,將多克隆抗體1 ∶500倍稀釋作為一抗,4 ℃ 過夜孵育,TBST洗滌3次,每次10 min;HRP標記山羊抗兔IgG抗體1 ∶5 000倍稀釋作為二抗,室溫孵育1 h,TBST洗滌4次,每次10 min;超敏ECL發光液顯色。
1.10 布魯氏菌S2弱毒株感染宿主細胞后對小鼠IL-1Ra表達的影響
以細胞數 ∶細菌數=1 ∶100的劑量感染Raw264.7細胞,并以PBS組為對照組,收集0、4、8、12、24 h樣品,用qPCR檢測小鼠IL-1Ra基因的mRNA水平變化,用蛋白質印跡法(Western-Blot)檢測小鼠IL-1Ra蛋白表達水平變化。引物序列見表1。PCR擴增程序:95 ℃ 2 min;95 ℃ 30 s,60 ℃ 30 s,72 ℃ 32 s,共40個循環,每個樣本設置3個重復孔。采用2-ΔΔC T法對試驗結果進行統計分析。
1.11 統計分析
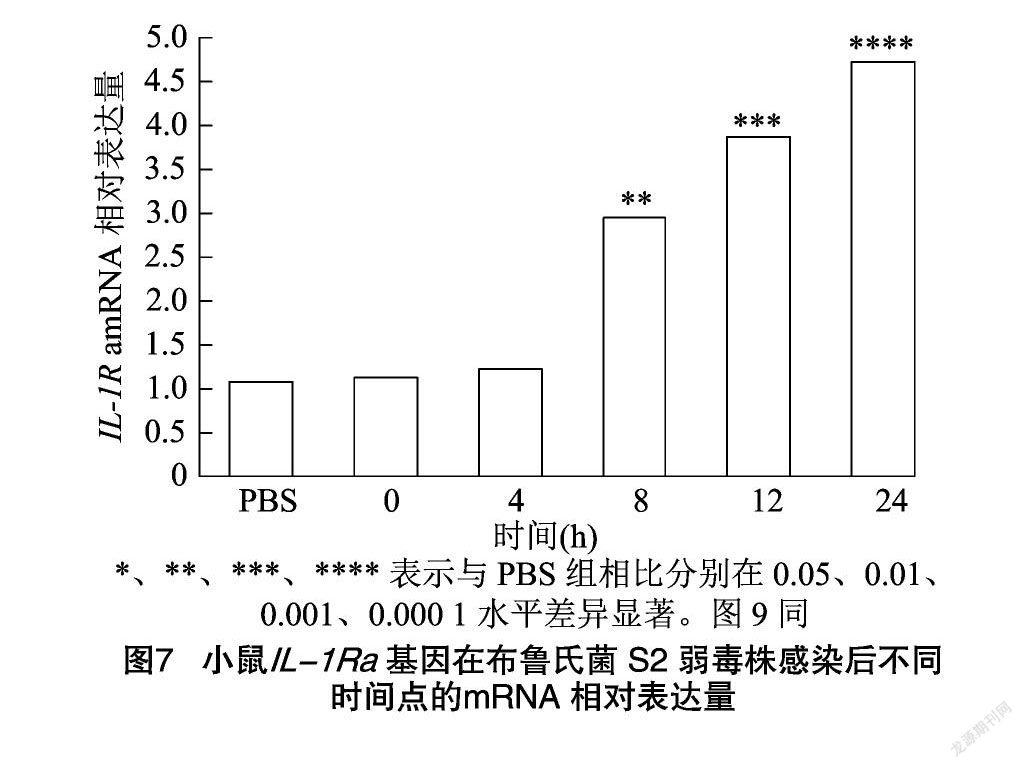
采用GraphPad Prism 7.0軟件進行統計學分析,P<0.05、P<0.01、P<0.001、P<0.000 1分別表示在0.05、0.01、0.001、0.000 1水平差異顯著,分別用*、**、***、****表示。
2 結果與分析
2.1 小鼠IL-1Ra基因擴增
瓊脂糖凝膠電泳顯示,在537 bp處有明亮的條帶(圖1),與預期大小相符。
2.2 pET-30a-Ra重組質粒的構建
對重組質粒pET-30a-Ra經NdeⅠ和XhoⅠ進行雙酶切鑒定,可以看到1條5 400 bp的條帶和1條537 bp 的條帶(圖2),片段大小符合預期,經測序表明重組質粒與目的基因序列比對完全一致,證明pET-30a-Ra原核表達載體構建成功。3C7D4F95-0118-493B-927E-EE6BECA5C702
2.3 IL-1Ra重組蛋白的誘導表達
從圖3可以看出,重組蛋白在37、 16 ℃均能誘導表達且重組蛋白在上清中的表達量都高于包涵體, 但是37 ℃時重組蛋白的表達量高,因此誘導條件確定為終濃度1 mmol/L IPTG,37 ℃誘導 8 h,此時重組蛋白主要以上清形式表達,分子量約為19 ku。
2.4 IL-1Ra重組蛋白的純化
SDS-PAGE結果顯示,用40 mmol/L咪唑洗3遍后再用60 mmol/L咪唑洗2遍,對雜蛋白的洗滌效果最好,最后用250 mmol/L咪唑可以將重組蛋白完全洗脫下來,此時重組蛋白的純度較好(圖4)。
2.5 多克隆抗體的制備及抗體效價的測定
利用純化的IL-1Ra重組蛋白免疫兔子制備多克隆抗體,采用間接ELISA法測定5次免疫后多克隆抗體的效價已經達到1 ∶4 096 000(圖5),表明純化的IL-1Ra重組蛋白能夠誘導新西蘭大白兔產生高效價的抗體。
2.6 多克隆抗體反應原性鑒定
Western-Blot 結果顯示,制備的多克隆抗體能夠很好地識別Raw264.7中表達的天然IL-1Ra蛋白(圖6),該抗體可以用于檢測布魯氏菌感染Raw264.7細胞后IL-1Ra蛋白的變化。
2.7 布魯氏菌S2弱毒株感染宿主細胞后對小鼠IL-1Ra表達的影響
運用qPCR技術檢測不同時間點小鼠IL-1Ra基因mRNA表達水平變化,與PBS組相比,8、12、24 h 小鼠IL-1Ra基因表達量顯著升高,在24 h時達到峰值(圖7)。Western-Blot檢測結果發現,與PBS組相比,4、8、12、24 h小鼠IL-1Ra蛋白的表達量均顯著升高,其上升趨勢與mRNA轉錄結果一致,與預期結果相符(圖8、圖9)。
3 討論與結論
IL-1與IL-1Ra的平衡在炎癥性腸病(IBD)中起重要作用,在疾病早期IL-1就在結腸中產生,且IL-1水平與組織炎癥程度相關,在炎癥消退之前,結腸中IL-1Ra的水平是IL-1的10倍[15]。在該動物模型中,加入IL-1Ra的中和抗體會導致炎癥延長和死亡率增加,表明了內源性IL-1Ra抗炎的重要性,且外源加入IL-1Ra重組蛋白可以抑制炎癥[16-17]。大量IBD動物模型的研究表明,IL-1 和IL-1Ra的差異表達與IBD之間存在一定的相關性,且隨著病情的好轉,IL-1、IL-1Ra表達異常也得到緩解。筆者所在課題組前期通過構建布魯氏菌強毒株、弱毒株感染綿羊白細胞層抑制性消減雜交(SSH)cDNA文庫,篩選到差異表達基因IL-1β與IL-1Ra[12],并且建立了IL-1β及其拮抗因子的熒光定量PCR檢測方法[18],雙熒光ELISA檢測方法[19]和雙T線膠體金免疫層析試紙條檢測方法[20],初步探討了IL-1β與IL-1Ra之間關系對布魯氏菌病自然感染與疫苗免疫的鑒別診斷作用,提示 IL-1Ra 與布魯氏菌感染之間可能存在某種聯系。因此,為了建立區別鑒定布魯氏菌病自然感染與疫苗免疫的檢測方法,掌握IL-1Ra分子特征與生理病理功能至關重要。
本研究針對小鼠的IL-1Ra基因構建了原核表達重組質粒pET-30a-Ra,成功獲得了可溶性表達的小鼠IL-1Ra重組蛋白,通過鎳柱純化后,經 SDS-PAGE 驗證獲得純度較好的重組蛋白。將純化后的重組蛋白作為免疫原免疫兔子獲得多克隆抗體,經間接ELISA測定,兔抗多克隆抗體效價能夠達到1 ∶4 096 000,經過Western-Blot檢測結果表明,多克隆抗體能夠特異性識別Raw264.7細胞中表達的天然IL-1Ra蛋白,可用于檢測布魯氏菌弱毒株感染Raw264.7細胞后小鼠IL-1Ra的表達水平,為進一步研究小鼠IL-1Ra與布魯氏菌感染的關系提供了良好的試驗材料。
參考文獻:
[1]Garlanda C,Dinarello C A,Mantovani A.The interleukin-1 family:back to the future[J]. Immunity,2013,39(6):1003-1018.
[2]Arend W P. Interleukin-1 receptor antagonist[M]//Advances in immunology Volume 54.Amsterdam:Elsevier,1993:167-227.
[3]Arend W P,Malyak M,Guthridge C J,et al. Interleukin-1 receptor antagonist:role in biology[J]. Annual Review of Immunology,1998,16:27-55.
[4]Benedetti F,Dallaspezia S,Melloni E M T,et al. Effective antidepressant chronotherapeutics (sleep deprivation and light therapy) normalize the IL-1β:IL-1ra ratio in bipolar depression[J]. Frontiers in Physiology,2021,12:740686.
[5]郭 興. 綿羊白介素1β及其受體拮抗因子全長cDNA克隆、分子特性及差異表達分析[D]. 長春:吉林大學,2015:6.
[6]Haskill S,Martin G,van Le L,et al. cDNA cloning of an intracellular form of the human interleukin 1 receptor antagonist associated with epithelium[J]. Proceedings of the National Academy of Sciences of the United States of America,1991,88(9):3681-3685.3C7D4F95-0118-493B-927E-EE6BECA5C702
[7]Muro M,Mrowiec A. Interleukin (IL)-1 gene cluster in inflammatory bowel disease:is IL-1RA implicated in the disease onset and outcome?[J]. Digestive Diseases and Sciences,2015,60(5):1126-1128.
[8]水一鳴,劉楠楠,郭 興,等. 羊IL-1Ra基因全長cDNA克隆及生物信息學分析[J]. 中國畜牧獸醫,2018,45(3):598-603.
[9]Arend W P. The balance between IL-1 and IL-1Ra in disease[J]. Cytokine & Growth Factor Reviews,2002,13(4/5):323-340.
[10]Aksentijevich I,Masters S L,Ferguson P J,et al. An autoinflammatory disease with deficiency of the interleukin-1-receptor antagonist[J]. The New England Journal of Medicine,2009,360(23):2426-2437.
[11]Horai R,Saijo S,Tanioka H,et al. Development of chronic inflammatory arthropathy resembling rheumatoid arthritis in interleukin 1 receptor antagonist-deficient mice[J]. The Journal of Experimental Medicine,2000,191(2):313-320.
[12]Saad K,Abdallah A E M,Abdel-Rahman A A,et al. Polymorphism of interleukin-1β and interleukin-1 receptor antagonist genes in children with autism spectrum disorders[J]. Progress in Neuro-Psychopharmacology and Biological Psychiatry,2020,103:109999.
[13]Altomare A,Corrado A,Maruotti N,et al. The role of Interleukin-1 receptor antagonist as a treatment option in calcium pyrophosphate crystal deposition disease[J]. Molecular Biology Reports,2021,48(5):4789-4796.
[14]唐 峰. 布魯氏菌強弱毒株感染羊白細胞層SSH cDNA文庫建立及CD96分子初步研究[D]. 長春:吉林大學,2013.
[15]Dionne S,Hiscott J,DAgata I,et al. Quantitative PCR analysis of TNF-α and IL-1β mRNA levels in pediatric IBD mucosal biopsies[J]. Digestive Diseases and Sciences,1997,42(7):1557-1566.
[16]Isaacs K L,Sartor R B,Haskill S.Cytokine messenger RNA profiles in inflammatory bowel disease mucosa detected by polymerase chain reaction amplification[J]. ZooKeys,1992,103(5):1587-1595.
[17]Harrell C R,Markovic B S,Fellabaum C,et al. The role of Interleukin 1 receptor antagonist in mesenchymal stem cell-based tissue repair and regeneration[J]. BioFactors,2020,46(2):263-275.
[18]水一鳴. IL-1β和IL-1Ra雙熒光ELISA檢測方法的建立及其初步應用[D]. 長春:吉林大學,2018.
[19]遲 丹. 綿羊白介素1β及其受體拮抗因子熒光定量PCR檢測方法的建立與應用[D]. 長春:吉林大學,2016.
[20]鞠丹迪. IL-1Ra/IL-1β試紙條檢測方法建立及其在布魯氏菌病感染與免疫鑒別診斷中的應用探討[D]. 長春:吉林大學,2019.3C7D4F95-0118-493B-927E-EE6BECA5C702

