野生羅非魚響應低溫脅迫的腦組織轉錄組測序分析
徐欣玉 劉潔 夏慧敏 陳麗婷 李鵬飛 肖俊 陸穎
摘要:【目的】比較低溫脅迫下野生羅非魚和養殖吉富羅非魚的基因表達模式,揭示野生羅非魚低溫應答的特有分子調控機制,為后續開展野生羅非魚耐冷親本大范圍篩選打下基礎。【方法】挑選規格相近的野生羅非魚和養殖吉富羅非魚進行梯度降溫試驗,水溫先以1 ℃/12 h的速度從26 ℃降至14 ℃,并保持288 h(12 d),于26 ℃、20 ℃及14 ℃保持0、120和288 h等5個時間點分別解剖羅非魚采集腦組織樣品,構建cDNA文庫后以Illumina HiSeq×Ten測序平臺進行雙端測序及比較轉錄組分析,并采用實時熒光定量PCR對具有重要功能的差異表達基因(DEGs)進行表達驗證。【結果】野生羅非魚在11 ℃時開始出現死亡個體,但在8 ℃時仍有50.0%的存活個體,說明野生羅非魚較養殖吉富羅非魚具有更強的低溫耐受能力。在14 ℃的長時間低溫脅迫過程中,養殖吉富羅非魚腦組織中表達顯著上調的差異表達基因數量約是野生羅非魚的10倍,即養殖吉富羅非魚的應激反應遠比野生羅非魚強烈。KEGG信號通路富集分析結果顯示,養殖吉富羅非魚和野生羅非魚在14 ℃保持120和288 h的上調差異表達基因均富集到核糖體發生、內質網蛋白加工及剪接體信號等信號通路上,野生羅非魚的上調差異表達基因還額外富集到核苷酸切除修復、N-糖基化生物合成和DNA復制信號等通路上。與養殖吉富羅非魚相比,在野生羅非魚中發現577個特有的差異表達基因,主要富集在NOD受體信號通路、凋亡和內吞等通路上,且表現為NOD受體信號通路被啟動,而細胞凋亡受抑制。在野生羅非魚中,參與NOD受體信號通路的關鍵功能基因(Nemo、NFκB、p38、JNK和IL-1β)在長時間低溫脅迫中均維持在一個較高的表達水平,而內吞途徑關鍵基因的表達上升倍數也明顯高于養殖吉富羅非魚。【結論】野生羅非魚通過避免過度的應激反應和維持低水平代謝的細胞穩定以減輕低溫脅迫對機體的損傷,并持續啟動NOD受體信號通路及內吞途徑以維持其免疫能力,而具有較養殖羅非魚更強的低溫耐受力。
關鍵詞: 羅非魚;腦組織;低溫脅迫;差異表達基因(DEGs);轉錄組測序
中圖分類號: S917.4;S965.125? ? ? ? ? ? ? ? ? ? ? ? ? ? 文獻標志碼: A 文章編號:2095-1191(2022)03-0704-10
Transcriptome sequencing analysis of the brain tissues responding to low temperature stress in wild tilapia
XU Xin-yu LIU Jie XIA Hui-min CHEN Li-ting LI Peng-fei XIAO Jun LU Ying
(1Key Laboratory of Exploration and Utilization of Aquatic Genetic Resources (Shanghai Ocean University), Shanghai 201306, China; 2Key Laboratory of Freshwater Aquatic Genetic Resources, Ministry of Agriculture and Rural Affairs, (Shanghai Ocean University),Shanghai? 201306, China; 3Guangxi Academy of Fishery Sciences/Guangxi Key
Laboratory of? Aquatic Genetic Breeding and Healthy Aquaculture, Nanning, Guangxi? 530021, China; 4Guangxi Academy of Sciences/Guangxi Engineering Research Center for Fishery Major Diseases Control and Efficient
Healthy Breeding Industrial Technology, Nanning, Guangxi? 530007, China)
Abstract:【Objective】To investigate regulatory mechanism of the responses to low temperature stress in wild tilapia, comparing to that of the cultured tilapia, so as to contribute to screen cold tolerant parents from wild tilapia in the future.【Method】A wild and a cultured tilapia populations with similar sizes were selected for a gradient low temperature stress test that the water temperature was decreased from 26 ℃ to 14 ℃ at the rate of 1 ℃/12 h and kept at 14 ℃ for 288 h (12 d). The brain tissues were collected at 26 ℃, 20 ℃ and 14 ℃ for 0, 120 and 288 h during this period, respectively, and were dissected. The prepared cDNA libraries were sequenced using Illumina HiSeq×Ten platform. A comparative transcriptome analysis was carried out to identify differentially expressed genes (DEGs) between the stressed and control tissues. Expression of the critical genes involved in the responses to low temperature stress were verified with a qRT-PCR analysis. 【Result】Death of wild tilapia individuals initially occurred at 11 ℃ and still 50.0% of them were alive at 8 ℃, indicating that the wild tilapia had a better tolerance to low temperature than the cultured tilapia.During the long-term low temperature stress at 14 ℃, DEGs expression in cultured tilapia brain tissue was about 10 times higher than that in wild tilapia, indicating that the stress response of cultured tilapia was much stronger. KEGG pathway enrichment analysis results showed that the up-regulated DEGs of cultured GIFT tilapia and wild tilapia maintained at 14 ℃ for 120 and 288 h were both enriched in ribosome formation, endoplasmic reticulum protein processing and spliceosome signaling pathways. The up-regulated DEGs of wild tilapia were additionally enriched in nucleotide excision repair, N-glycosylation biosynthesis and DNA replication pathways. Compared with the cultured Tilapia, there were 577 unique DEGs in wild Tilapia, which were mainly enriched in the NOD receptor signaling pathway, apoptosis, endocytosis and other pathways. The NOD receptor signaling pathway was activated, and apoptosis was inhibited. In wild tilapia, the key functional genes involved in Nod-like receptor signal pathway, such as Nemo, NFκB, P38, JNK and IL-1β, maintained a high expression under the long-term low temperature stress. Meanwhile,the key genes employed in the endocytosis pathway had the much higher expression than the cultured tilapia. 【Conclusion】Wild tilapia has stronger cold tolerance than cultured tilapia by avoiding excessive stress response and maintaining low-level metabolic cell stability to alleviate the damage of low temperature stress on the body, as well as continuing to activate NOD receptor signaling pathways and endocytosis pathways to maintain their immunity.D702AD90-53E9-41CC-98A9-65C771A49FD3
Key words: tilapia; brain tissue; low temperature stress; DEGs; transcriptome sequencing
Foundation items:National Key Research and Development Program of China“Technological Innovation of Blue Granary”(2018YFD0900101, 2018YFD0900601); Guangxi Freshwater Fish Industry Innovation Team of National Mo-dern Agricultural Industry Technology System(nycytxgxcxtd-2021-08-03)
0 引言
【研究意義】羅非魚隸屬于慈鯛科(Cichlidae)羅非魚屬(Oreochromis),是全球重要的經濟養殖魚類,具有繁殖能力強、生長速度快、抗病力強及食性雜等優點(鄭雄等,2019;李柳清等,2020)。羅非魚起源于非洲的熱帶亞熱帶地區,屬于暖水性魚類,在越冬期間會增加能量損耗,導致其免疫力下降甚至死亡(Abdel-Ghany et al.,2021),制約著其養殖區域的向北拓展。野生羅非魚較養殖羅非魚具有更強的低溫耐受能力,因此開展野生羅非魚低溫應激分子機制研究,有助于篩選具有較強耐低溫能力的野生品系作為雜交育種親本,以拓展羅非魚養殖區域。【前人研究進展】寒冷是水生環境中魚類的主要應激源。近年來,已有學者運用轉錄組測序及其他組學研究方法探究冷應激反應下不同魚類的基因表達模式(Mininni et al.,2014;Qian and Xue,2016)。Long等(2012)對斑馬魚(Danio rerio)幼蟲的研究發現,在冷應激條件下顯著差異表達的基因主要參與RNA剪接、核糖體生物合成和蛋白質分解等通路。Xu等(2018)在對冷應激存活黃姑魚(Nibea albiflora)的研究中發現,其腦和肌肉組織中參與分子—分子相互作用、信號轉導、碳水化合物代謝、脂質代謝、消化系統及內分泌系統等通路的基因表達均顯著上調,可能與應激信號轉導、能量代謝和應激誘導的細胞膜變化等生理過程相關。Sun等(2019)研究表明,在受低溫脅迫的石斑魚(Epinephelus coioides)肝臟轉錄組中,其應激反應涉及細胞黏附分子、PPAR信號通路及脂肪酸延長等途徑。Wen等(2019)通過對低溫脅迫后的暗紋東方鲀(Takifugu fasciatus)肝臟組織進行多組學分析,建立的mRNA—蛋白質—代謝物相互作用網絡證實分子互作網絡主要參與脂肪酸代謝、膜轉運、信號轉導及DNA損傷和修補等代謝過程。Liu等(2020)通過對低溫脅迫8月齡虎皮魚的腦、鰓、肝臟和肌肉組織進行轉錄組測序,發現參與晝夜節律、類固醇和脂肪酸生物合成等途徑的基因在低溫脅迫下其表達模式均發生改變,并證實泛素介導的蛋白質降解可能是虎皮魚應對急性冷應激過程的關鍵。針對羅非魚而言,不同羅非魚品種的耐低溫能力也存在明顯差異,其致死溫度范圍在8.9~10.5 ℃(唐章生等,2012)。在羅非魚耐受低溫應激的分子調控機制研究中,Chen等(2002)研究認為免疫相關基因對羅非魚的耐寒能力存在影響,當羅非魚處于12.0 ℃時其血漿腎上腺素增加,血清皮質醇水平顯著升高,血清中的高皮質醇水平對魚體免疫產生抑制作用;Ammar等(2018)對尼羅羅非魚在夏季和冬季的基因表達差異進行分析,發現冬季IV型防凍基因在其腸道、鰓、皮膚、脾臟、肝臟和腦組織中的表達量明顯上調;Nitzan等(2019)對冷應激下的奧利亞羅非魚鰓組織和肝臟進行轉錄組測序,發現基因在局部黏附和細胞—細胞外基質(ECM)相互作用通路中的表達下調,而在蛋白酶體及各種細胞內蛋白水解活性信號通路中的表達上調。可見,羅非魚的低溫應答過程主要表現在免疫、節律、信號傳導、DNA修補和基礎物質合成或降解等相關代謝途徑的基因啟動,且主要發生在免疫器官、消化器官及中樞控制器官——腦。腦是調控低溫脅迫下應激反應的關鍵器官(Song and McDowell,2020),機體對于冷刺激的耐受機制是在神經系統的主導下進行。【本研究切入點】選擇合適的親本,采用臨界非損傷性的溫度適應選育方法有可能改善子代羅非魚耐低溫能力(肖俊等,2014;杜雪松等,2019),但從育種角度而言迫切需要耐低溫性狀能穩定遺傳的親本,并將其耐低溫性狀引入現有的優良家系中。野生羅非魚是耐寒研究和育種實踐的良好材料,開展野生羅非魚低溫應激反應的分子生物學研究對加速羅非魚抗寒性育種進程具有重要意義。【擬解決的關鍵問題】選擇野生羅非魚進行低溫脅迫試驗,并以養殖的吉富羅非魚為對照,通過Illumina HiSeq×Ten測序平臺對羅非魚的腦組織進行轉錄組測序,比較低溫脅迫下2種羅非魚的基因表達模式,旨在揭示野生羅非魚低溫應答的特有分子調控機制,為后續開展野生羅非魚耐冷親本大范圍篩選打下基礎。
1 材料與方法
1. 1 降溫試驗及樣品采集
成年野生羅非魚采自廣西崇左市扶綏縣左江流域(東經107°54′14.76″,北緯22°38′2.76″),選用規格相近的養殖吉富羅非魚為對照(唐永凱等,2010)。隨機挑選野生羅非魚和吉富羅非魚各30尾,26 ℃下暫養60 d后進行降溫預試驗。參考Healy等(2017)、Giordano等(2021)的降溫試驗方法,使水溫先以1 ℃/12 h的速度從26 ℃降至8 ℃,降溫過程中每2 h記錄1次水溫及羅非魚死亡數量。正式取樣時,使水溫先以1 ℃/12 h的速度從26 ℃降至14 ℃,并保持288 h(12 d),于26 ℃、20 ℃及14 ℃保持0、120和288 h等5個時間點分別解剖羅非魚采集腦組織樣品,各時間點均取2尾羅非魚作為平行重復。按取樣水溫和時間,吉富羅非魚樣品分別命名為G26、G20、G14H0、G14H120和G14H288,野生羅非魚樣品分別命名為W26、W20、W14H0、W14H120和W14H288。采集的腦組織立即凍存于液氮中備用。D702AD90-53E9-41CC-98A9-65C771A49FD3
1. 2 RNA提取與測序
采用TRIzol試劑提取羅非魚腦組織總RNA,在安捷倫生物分析儀芯片RNA 7500 Series II上檢測其質量和濃度。使用TruSeq RNA樣品制備試劑盒(Illumina)從每個樣品中提取3 μg總RNA,轉錄合成cDNA后構建平均插入片段大小為300~500 bp的測序文庫,然后以Illumina HiSeq×Ten測序平臺進行雙端測序。
1. 3 轉錄組測序數據處理與分析
使用Trimomatic v0.32對測序獲得的原始序列(Raw reads)進行檢測和過濾(Bolger et al.,2014),過濾掉低質量序列及接頭序列后得到有效序列(Clean reads)。通過HISAT v2.1.0將Clean reads比對到尼羅羅非魚參考基因組(GenBank登錄號GCA_000002035.4)上(Kim et al.,2019;Tao et al.,2021),再使用Cufflinks 2.2.1計算基因表達量(FPKM)(Trapnell et al.,2012),以R語言軟件包edgeR篩選差異表達基因(Differentially expressed genes,DEGs)(Chen et al.,2016),篩選條件:[log2 Fold Change]≥1和P<0.05。通過KEGG數據庫對差異表達基因進行功能注釋及信號通路分析(Kanehisa et al.,2016),并用R語言軟件包ggplot2對結果進行可視化處理(Ginestet,2011)。
1. 4 實時熒光定量PCR驗證
采用實時熒光定量PCR對NOD受體、內吞及凋亡等信號通路上的17個差異表達基因進行表達驗證。使用反轉錄試劑盒(TaKaRa)將各樣品的RNA反轉錄合成cDNA,以β-actin基因為內參基因,使用FastStart Universal SYBR? Green Master(ROX)試劑在CFX96 Real-Time PCR Detection System定量PCR儀(Bio-Rad)上進行實時熒光定量PCR檢測。每個樣品測定3個平行,采用2-△△Ct法計算目的基因相對表達量。
2 結果與分析
2. 1 羅非魚低溫存活率測定結果
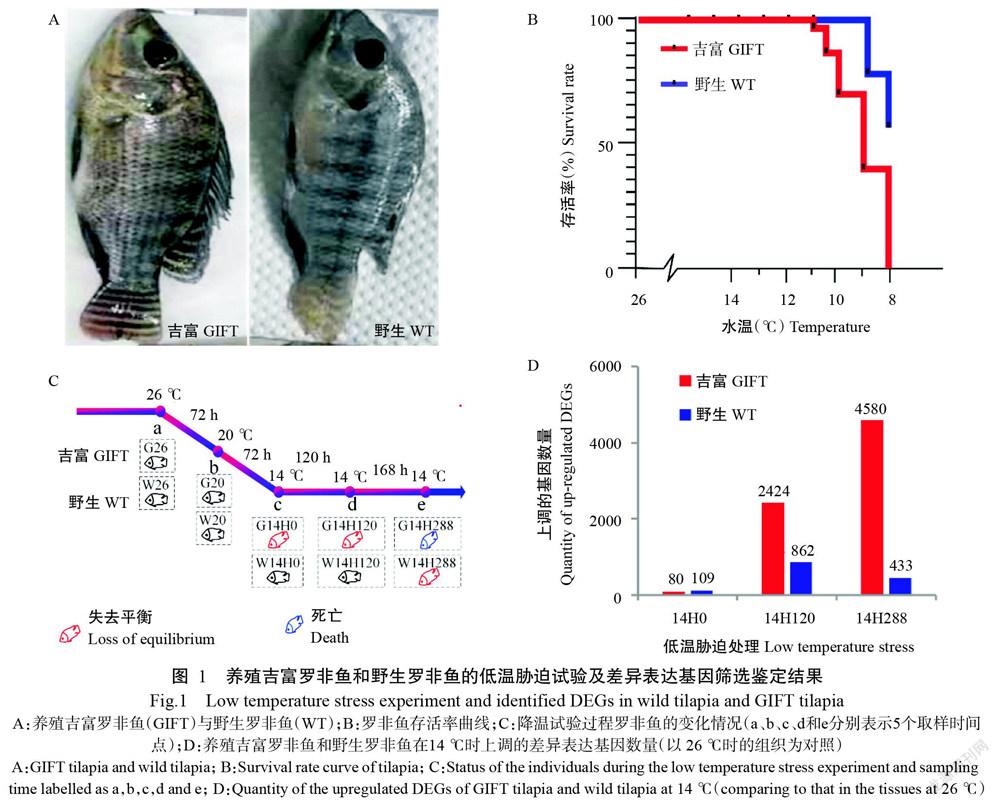
在低溫預試驗中,統計梯度降溫過程中各時間點養殖吉富羅非魚和野生羅非魚的存活數量,計算存活率。結果顯示,養殖吉富羅非魚在水溫降至14 ℃時開始出現個體失去平衡的現象,在水溫降至11 ℃時出現個體死亡,并于8 ℃時全部死亡(圖1)。相比之下,野生羅非魚雖然在14 ℃時出現失去平衡的個體,并于11 ℃時開始出現死亡個體,但在8 ℃時仍有50.0%的存活個體,說明野生羅非魚較養殖吉富羅非魚具有更強的低溫耐受能力。
2. 2 羅非魚腦組織轉錄組測序結果
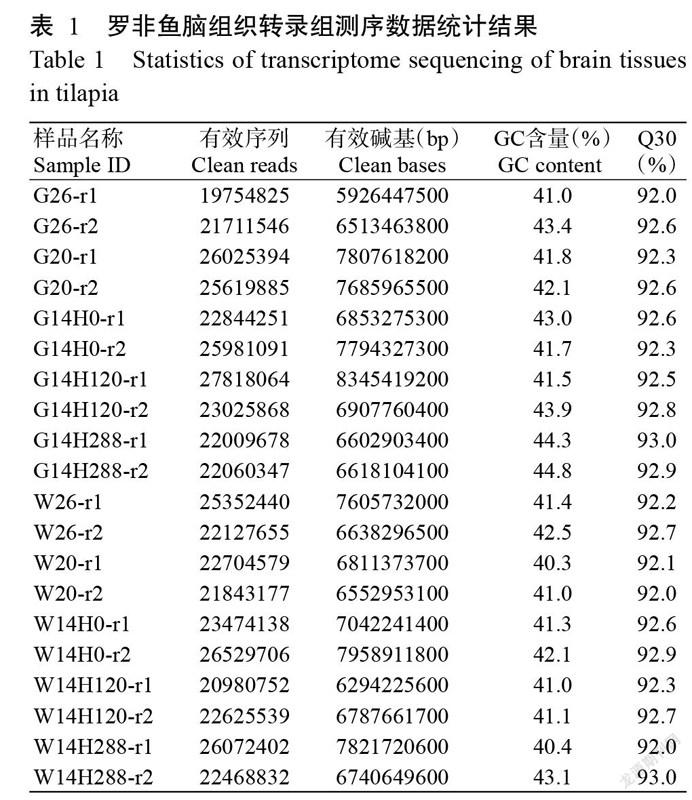
對養殖吉富羅非魚和野生羅非魚5個時間點的腦組織共20個樣本進行轉錄組測序,經質控后共獲得141.31 Gb的Clean reads。測序堿基達Q30(測序堿基準確率達99.9%)的比例超過92.0%(表1),即測序準確率較高。將各樣品的Clean reads比對到尼羅羅非魚參考基因組上,其比對率均在69.5%以上,最高為94.2%,滿足后續分析的要求。
2. 3 低溫脅迫下羅非魚腦組織差異表達基因功能注釋分析結果
為認定野生羅非魚的種屬關系,將26 ℃的野生型羅非魚轉錄組測序數據比對到7種羅非魚[奧利亞羅非魚(NC_013750.1)、紅羅非魚(NC_014060.1)、布氏異羅非魚(NC_023470.1)、莫桑比克羅非魚(AY597335.1)、 尼羅羅非魚(GU477624.1)、齊氏羅非魚(KM658974.1)和維多利亞綠羅非魚(NC_026109.1)]的線粒體基因組上,結果發現比對到紅羅非魚的數目最多,故推測該野生羅非魚與紅羅非魚的親緣關系最為接近。對G14H0 vs G26、G14H120 vs G26、G14H288 vs G26、W14H0 vs W26、W14H120 vs W26和W14H288 vs W26等6對樣品的基因表達量進行比較分析,鑒定出各組差異表達基因中的上調差異表達基因如圖1-D所示。其中,野生羅非魚W14H288和W14H120共有的上調差異表達基因數量為162個,而養殖吉富羅非魚G14H288和G14H120共有的上調差異表達基因數量為1686個,約是野生羅非魚的10倍。野生羅非魚W14H288特有的上調差異表達基因是200個,而養殖吉富羅非魚G14H288特有的上調差異表達基因為2909個,也是野生羅非魚的10倍以上,說明長期處于14 ℃下養殖吉富羅非魚的應激反應遠比野生羅非魚強烈。
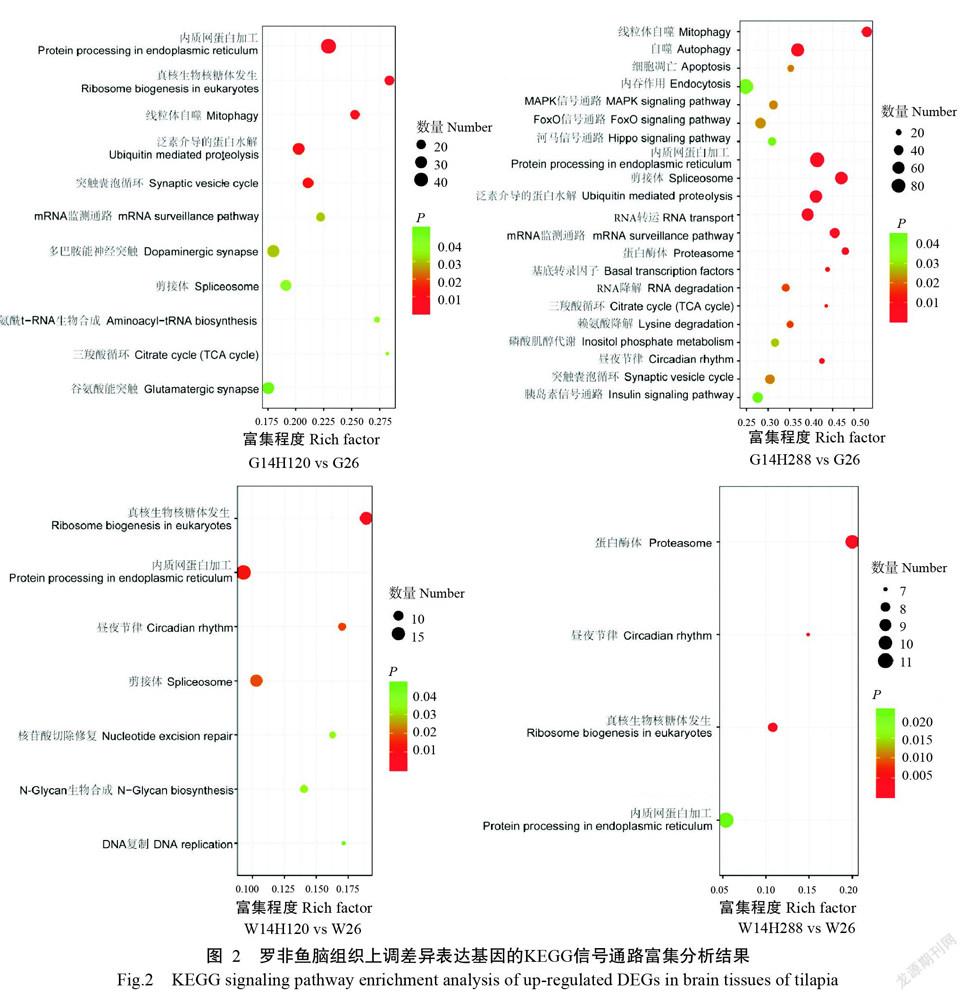
KEGG信號通路富集分析結果(圖2)顯示,養殖吉富羅非魚和野生羅非魚在14 ℃保持120和288 h的上調差異表達基因均富集到核糖體發生、內質網蛋白加工及剪接體信號等信號通路上,可能與應激狀態下機體利用這些蛋白作為應激狀態的供能物質有關。富集到晝夜節律信號通路上與本研究觀察到低溫脅迫下羅非魚運動和攝食節奏急劇變慢的現象相符(Li et al.,2020;Zou et al.,2021);富集到蛋白酶體等信號通路上,則可能與清除細胞內冷應激下產生的異常蛋白有關(Yu et al.,2021)。與養殖吉富羅非魚相比,野生羅非魚的上調差異表達基因還額外富集到核苷酸切除修復、N-聚糖生物合成和DNA復制信號等通路上,可能參與冷應激過程中的損傷修復(Huang et al.,2021)。養殖吉富羅非魚的這些差異表達基因則富集到自噬、線粒體自噬、細胞凋亡、泛素介導蛋白水解及賴氨酸降解等信號通路上,可能與長期低溫脅迫下能量利用途徑的改變有關,并激活自噬和細胞凋亡途徑,將細胞內一些不重要的蛋白及細胞器分解以維持細胞的基本存活。可見,野生羅非魚在長期低溫脅迫下主要通過避免過度的應激反應、及時啟動修復和減弱細胞調亡等機制,以獲得較養殖羅非魚更強的耐低溫能力。D702AD90-53E9-41CC-98A9-65C771A49FD3
2. 4 低溫脅迫下野生羅非魚的基因表達模式
為了解野生羅非魚特有的低溫應激機制,對14 ℃脅迫下僅在野生羅非魚中上調的差異表達基因進行分析。在計算得到野生羅非魚在14 ℃下各時間點上調差異表達基因(W14H0 vs W26、W14H120 vs W26和W14H288 vs W26)的基礎上,將這些差異表達基因中在相同時間點的養殖吉富羅非魚腦組織也發生顯著上調(G14H0 vs G26、G14H120 vs G26和G14H288 vs G26)的基因舍去,即去除養殖吉富和野生羅非魚在相同時間點共有的上調差異表達基因后,得到在對應時間點僅在野生羅非魚中上調的差異表達基因。通過篩選共得到這3個時間點僅在野生羅非魚中發生表達變化的差異表達基因有577個,且主要富集在NOD受體信號通路(Nod-like receptor signal pathway,map04621)、凋亡(Apoptosis,map 04210)和內吞(Endocytosis,map04144)等通路上。對這些差異表達基因所參與的生物反應過程進行深入分析,發現在野生羅非魚中存在NOD受體信號通路被啟動而細胞凋亡受抑制的平衡(圖3)。
結合參與這3條信號通路上關鍵差異表達基因的實時熒光定量PCR驗證結果(圖4),發現在NOD受體信號通路上,野生羅非魚的B細胞編碼κ輕鏈多肽抑制基因(Nemo)顯著上調,并激活下游的核轉錄因子kappa B1(NFκB)、絲裂原活化蛋白激酶(p38)和C-Jun氨基末端激酶(JNK)等,促進炎癥相關因子白細胞介素-1β(IL-1β)表達上升,進而啟動天然免疫和炎癥反應(Elabd et al.,2020),且這些基因在長期低溫脅迫中均維持在一個較高的表達水平。在該過程中,養殖吉富羅非魚的這些基因幾乎沒有參與全程的冷應激反應,尤其是NOD受體信號通路上的Nemo基因一直未被啟動;而參與這一途徑的其他基因中只觀察到p38和IL-1β在個別時間點因未知原因突然劇烈升高,但隨后又迅速恢復至原有水平。在細胞調亡途徑中,重要抑制因子顆粒酶B(GZMB)在野生羅非魚呈顯著上升,而抑制細胞調亡的發展(Yang et al.,2021)。此外,野生羅非魚的蛋白酪氨酸磷酸酶非受體型13(ptpn13)和細胞凋亡相關半胱氨酸肽酶2(casp2)等基因參與細胞調亡調控表達量上升的倍數明顯小于養殖吉富羅非魚,細胞調亡可能在一定程度上受到抑制,而有利于避免過度應激的發生。在內吞途徑中,大部分野生羅非魚關鍵基因表達上升的倍數也明顯高于養殖吉富羅非魚,對及時清理細胞內的不良物質及維持細胞穩定均有利。故推測野生羅非魚較養殖吉富羅非魚具有更強的耐低溫能力是通過避免過度應激反應及維持低水平代謝的細胞穩定來實現。
3 討論
水溫對魚類的生長、繁殖、代謝、生理功能和行為活動均產生重要影響(Somero,2010;Ma et al.,2014;Yang and Ma,2016)。雖然魚類可通過廣泛的調節代謝及生理生化適應過程應對一定范圍內的水溫變化,但不適當的環境溫度仍然會產生負面影響(陳子桂等,2018;Xu et al.,2018)。冷應激下,機體的穩態調節是在神經系統主導下,由下丘腦—腺垂體—甲狀腺系統(HPT)、下丘腦—腺垂體—腎上腺皮質系統(HPA)和機體交感—腎上腺髓質系統(SAM)配合相關激素的作用共同實現,其原理較復雜(Oyola and Handa,2017)。腦組織對冷應激敏感,已有研究表明熱帶魚的腦組織較冷水魚的腦組織對熱刺激更具穩定性,但對冷刺激不穩定(Lu et al.,2019)。在低溫應激后,金魚出現躲避游泳的現象是由一種存在魚類后腦組織中的神經元細胞參與調控進而激活聽覺傳入所引起(Silva et al.,2019)。在鯉魚中,低溫會減少腦組織的血容量,防止低溫血液進入大腦而影響感覺運動神經的活性(van den Burg et al.,2005)。可見,腦是魚類冷敏感檢測的理想組織。
現有關于羅非魚對低溫應答機制的研究主要是通過長時間的低溫脅迫及觀察基因表達變化來實現。Nitzan等(2019)對具有相同遺傳背景的吉富羅非魚進行降溫試驗(從24 ℃降溫至12 ℃并保持),根據存活時間將吉富羅非魚分為冷耐受魚和冷敏感魚,發現冷敏感魚的差異表達基因數量多于冷耐受魚。本研究中,冷敏感的養殖吉富羅非魚在14 ℃保持120和288 h時表達顯著上調的基因數量遠多于低溫耐受能力較強的野生羅非魚,僅在冷應激早期(14 ℃保持0 h)對冷應激的響應基因稍多一些,說明野生羅非魚對低溫環境的應答啟動更迅速,但在長期冷應激反應過程中對低溫更敏感的養殖吉富羅非魚中具有溫度依賴性表達的基因遠多于野生羅非魚。從上調表達基因的功能注釋結果來看,Nitzan等(2019)發現鰓組織中糖酵解、糖異生及肝臟中氨基酸生物合成通路上的某些基因在耐冷魚類中呈下調表達。本研究發現在野生羅非魚的上調差異表達基因主要富集到核苷酸切除修復和N-糖基化的生物合成等通路上,而在能量代謝途徑基本上呈下調趨勢,表明能量代謝的減弱有利于魚類應對寒冷環境。
根據已有關于低溫脅迫對羅非魚免疫系統的影響研究可知,長時間冷應激反應會直接導致其免疫力下降(Ndong et al.,2007),引起血液中兒茶酚胺、皮質醇、腎上腺素、去甲腎上腺素和腎上腺素激的水平上升,從而抑制白細胞的吞噬作用,降低抗體水平(Chen et al.,2002)。此外,SGT1 和 ATG1等免疫相關基因在低溫脅迫下呈下調表達的現象可能會影響過氧化物酶體、吞噬體和自噬的調節(Yang et al.,2015)。這是由于過度應激反應引發的免疫能力下降,極大增加了羅非魚在低溫環境下的病原體感染風險。本研究發現,在低溫脅迫下野生羅非魚的應激反應明顯弱于養殖吉富羅非魚,可能促使免疫反應和細胞凋亡在一定程度上受到抑制,避免對機體的損傷。然而,在對免疫相關基因的分析中發現由p38、JNK、IL-1β、ptpn13和casp2等關鍵功能基因共同參與的NOD受體信號通路在長期低溫脅迫野生羅非魚腦組織中始終保持著較高的水平,暗示著NOD受體信號通路可能在野生羅非魚低溫應答中發揮關鍵作用。在NOD受體信號通路上,Nemo基因顯著上調,再激活下游的NFκB、p38和JNK基因等,促進炎癥相關因子IL-1β表達上升,進而啟動天然免疫和炎癥反應(Velmurugan et al.,2019;Elabd et al.,2020),可能對維持野生羅非魚的生存具有重要意義。就低溫誘導的細胞凋亡或程序性死亡而言,GZMB是細胞凋亡過程中起關鍵作用的生物酶,其表達水平能反映細胞凋亡的程度。本研究結果表明,野生羅非魚可能通過激活GZMB基因,抑制核纖層蛋白,達到間接減弱因核膜完整性喪失而導致的細胞凋亡,從而表現出更強的耐寒性。因此,控制免疫過度反應和細胞調亡程度,且又保持局部的免疫能力,可能是野生羅非魚具有較強耐低溫能力的原因之一。D702AD90-53E9-41CC-98A9-65C771A49FD3
來自野生群體的優良性狀,始終是良種選育的重要性狀來源 ,而攜帶有這些優良性狀的野生家系是雜交育種的重要親本材料(Li et al.,2021)。本研究對養殖吉富羅非魚和野生羅非魚進行耐寒能力測定,比較分析二者在低溫致死極限下的差異,并通過轉錄組測序分析揭示野生羅非魚低溫脅迫下細胞凋亡、內吞和NOD受體等信號通路相關基因的表達模式,明確了導致羅非魚不同低溫耐受能力的分子調控機制,為今后篩選耐寒能力強的野生羅非魚品種打下基礎。
4 結論
野生羅非魚通過避免過度應激反應和維持低水平代謝的細胞穩定以減輕低溫脅迫對機體的損傷,并持續啟動NOD受體信號通路及內吞途徑以維持其免疫能力,即野生羅非魚較養殖羅非魚具有更強的耐受低溫能力。
參考文獻:
陳子桂,何金釗,楊明偉,林崗,甘習軍,馬華威,馮鵬霏. 2018. 烏蘇里擬鲿對水溫環境的適應性[J]. 南方農業學報,49(4):800-805. [Chen Z G,He J Z,Yang M W,Lin G,Gan X J,Ma H W,Feng P F. 2018. Water temperature adaptability of Pseudobagrus ussuriensis[J]. Journal of Southern Agriculture,49(4):800-805.] doi:10.3969/j.issn. 2095-1191.2018.04.28.
杜雪松,林勇,梁國琨,黃姻,賓石玉,陳忠,覃俊奇,趙怡. 2019. 兩種羅非魚的耐寒性能比較[J]. 廣西師范大學學報(自然科學版),37(3):174-179. [Du X S,Lin Y,Liang G K,Huang Y,Bin S Y,Chen Z,Qin J Q,Zhao Y. 2019. Comparision of low temperature resistant performance between two tilapia[J]. Journal of Guangxi Normal University(Natural Science Edition),37(3):174-179.] doi:10.16088/j.issn.1001-6600.2019.03.020.
李柳清,羅永巨,肖俊,黃一帆,陰晴朗,王志芳,檀午芳. 2020. 人工添加酵母硒對吉富羅非魚肌肉蛋白、脂肪及氨基酸的影響[J]. 南方農業學報,51(11):2856-2864. [Li L Q,Luo Y J,Xiao J,Huang Y F,Yin Q L,Wang Z F,Tan W F. 2020. Effects of artificial addition of yeast selenium on protein,fat and amino acids in muscle of GITF tilapia[J]. Journal of Southern Agriculture,51(11):2856-2864.] doi:10.3969/j.issn.2095-1191.2020.11.030.
唐永凱,李建林,俞菊華,陳雪峰,李紅霞. 2010. 吉富羅非魚MSTN基因結構及其多態性與生長性狀的相關性[J]. 中國水產科學,17(1):44-51. [Tang Y K,Li J L,Yu J H,Chen X F,Li H X. 2010. Genetic structure of MSTN and association between its polymorphisms and growth traits in genetically improved farmed tilapia(GIFT)[J]. Journal of Fishery Sciences of China,17(1):44-51.]
唐章生,盧其西,林勇,賓石玉,彭婷,鐘舒紅,甘西. 2012. 不同低溫條件下吉富羅非魚的耐受性研究[J]. 廣西師范大學學報(自然科學版),30(1):105-110. [Tang Z S,Lu Q X,Lin Y,Bin S Y,Peng T,Zhong S H,Gan X. 2012. Tolerance of GIFT tilapia(Oreochromis niloticus) under different low temperature stress[J]. Journal of Guangxi Normal University(Natural Science Edition),30(1):105-110.] doi:10.16088/j.issn.1001-6600.2012.01.010.
肖俊,甘西,羅永巨.? 2014. 羅非魚育種研究進展[J]. 湖南科技大學學報(自然科學版),29(1):106-112. [Xiao J,Gan X,Luo Y J. 2014. The progress of tilapia breeding[J]. Journal of Hunan University of Science & Technology (Natural Science Edition),29(1):106-112.] doi:10.13582/ j.cnki.1672-9102.2014.01.022.
鄭雄,趙立朝,吳志強,張潔,黃亮亮,汪開成,張曼. 2019. 廣西右江流域野生羅非魚種群及其雜合性研究[J]. 南方農業學報,50(12):2797-2805. [Zheng X,Zhao L C,Wu Z Q,Zhang J,Huang L L,Wang K C,Zhang M. 2019. Wild tilapia population and its hybridization in Youjiang River,Guangxi[J]. Journal of Southern Agriculture,50(12):2797-2805.] doi:10.3969/j.issn.2095-1191.2019.12. 23.D702AD90-53E9-41CC-98A9-65C771A49FD3
Abdel-Ghany H M,Salem M E S,Ezzat A A,Essa M A,Helal A M,Ismail R F,El-Sayed A F M. 2021. Effects of different levels of dietary lipids on growth performance,liver histology and cold tolerance of Nile tilapia(Oreochromis niloticus)[J]. Journal of Thermal Biology,96:102833.? doi:10.1016/j.jtherbio.2020.102833.
Ammar A Y,El Nahas A F,Mahmoud S,Barakat M E,Hassan A M. 2018. Characterization of type IV antifreeze gene in Nile tilapia(Oreochromis niloticus) and influence of cold and hot weather on its expression and some immune-related genes[J]. Fish Physiology and Biochemi-stry,44(2):515-525. doi:10.1007/s10695-017-0450-4.
Bolger A M,Lohse M,Usadel B. 2014. Trimmomatic:A flexible trimmer for Illumina sequence data[J]. Bioinformatics (Oxford,England),30(15):2114-2120. doi:10.1093/bioinformatics/btu170.
Chen W H,Sun L T,Tsai C L,Song Y L,Chang C F. 2002. Cold-stress induced the modulation of catecholamines,cortisol,immunoglobulin M,and leukocyte phagocytosis in tilapia[J]. General and Comparative Endocrinology,126(1):90-100. doi:10.1006/gcen.2001.7772.
Chen Y S,Lun A T L,Smyth G K. 2016. From reads to genes to pathways: Differential expression analysis of RNA-Seq experiments using Rsubread and the edgeR quasi-likelihood pipeline[version 2; peer review:5 app-roved][J]. F1000Research,5:1438. doi:10.12688/f1000 research.8987.2.
Elabd H,Wang H P,Shaheen A,Matter A. 2020. Astragalus membranaceus nanoparticles markedly improve immune and anti-oxidative responses;and protection against Aeromonas veronii in Nile tilapia Oreochromis niloticus[J]. Fish & Shellfish Immunology,97:248-256. doi:10. 1016/j.fsi.2019.12.025.
Ginestet C. 2011. ggplot2:Elegant graphics for data analysis[J]. Journal of the Royal Statistical Society,174(1):245-246. doi:10.1111/j.1467-985X.2010.00676_9.x.
Giordano D,Corti P,Coppola D,Altomonte G,Xue J M,Russo R,di Prisco G,Verde C. 2021. Regulation of globin expression in Antarctic fish under thermal and hypoxic stress[J]. Marine Genomics,57:100831. doi:10.1016/j.margen.2020.100831.
Healy T M,Brayant H J,Schulte P M. 2017. Mitochondrial genotype and phenotypic plasticity of gene expression in response to cold acclimation in killifish[J]. Molecular Ecology,26(3):814-830. doi:10.1111/mec.13945.
Huang Y,Zhang H L,Li Z L,Du T,Chen Y H,Wang Y,Ni H H,Zhang K M,Mai J,Hu B X,Huang J H,Zhou L H,Yang D,Peng X D,Feng G K,Tang J,Zhu X F,Deng R. 2021. FUT8-mediated aberrant N-glycosylation of B7H3 suppresses the immune response in triple-negative breast cancer[J]. Nature Communications,12(1):2672. doi:10. 1038/s41467-021-22618-x.D702AD90-53E9-41CC-98A9-65C771A49FD3
Kanehisa M,Sato Y,Kawashima M,Furumichi M,Tanabe M. 2016. KEGG as a reference resource for gene and protein annotation[J]. Nucleic Acids Research,44(D1):D457-D462. doi:10.1093/nar/gkv1070.
Kim D,Paggi J M,Park C,Bennett C,Salzberg S L. 2019. Graph-based genome alignment and genotyping with HISAT2 and HISAT-genotype[J]. Nature Biotechnology,37(8):907-915. doi:10.1038/s41587-019-0201-4.
Li B J,Zhu Z X,Qin H,Meng Z N,Lin H R,Xia J H. 2020. Genome-wide characterization of alternative splicing events and their responses to cold stress in tilapia[J]. Frontiers in Genetics,11:244. doi:10.3389/fgene.2020.00244.
Li S,Guo H,Chen Z Y,Jiang Y,Shen J Y,Pang X,Li Y. 2021. Effects of acclimation temperature regime on the thermal tolerance,growth performance and gene expression of a cold-water fish,Schizothorax prenanti[J]. Journal of Thermal Biology,98:102918. doi:10.1016/j.jtherbio.2021.102918.
Liu L L,Zhang R,Wang X W,Zhu H,Tian Z H. 2020. Transcriptome analysis reveals molecular mechanisms responsive to acute cold stress in the tropical stenothermal fish tiger barb(Puntius tetrazona)[J]. BMC Genomics,21(1):737. doi:10.1186/s12864-020-07139-z.
Long Y,Li L C,Li Q,He X Z,Cui Z B. 2012. Transcripto-mic characterization of temperature stress responses in larval zebrafish[J]. PLoS One,7(5):e37209. doi:10.1371/ journal.pone.0037209.
Lu D L,Ma Q,Wang J,Li L Y,Han S L,Limbu S M,Li D L,Chen L Q,Zhang M L,Du Z Y. 2019. Fasting enhan-ces cold resistance in fish through stimulating lipid cata-bolism and autophagy[J]. The Journal of Physiology,597(6):1585-1603. doi:10.1113/JP277091.
Ma Z H,Guo H Y,Zheng P L,Wang L,Jiang S G,Qin J G,Zhang D C. 2014. Ontogenetic development of digestive functionality in golden pompano Trachinotus ovatus (Linnaeus 1758)[J]. Fish Physiology and Biochemistry,40(4):1157-1167. doi:10.1007/s10695-014-9912-0.
Mininni A N,Milan M,Ferraresso S,Petochi T,Marco P D,Marino G,Livi S,Romualdi C,Bargelloni L,Patarnello T. 2014. Liver transcriptome analysis in gilthead sea bream upon exposure to low temperature[J]. BMC Genomics,15(1):765. doi:10.1186/1471-2164-15-765.
Ndong D,Chen Y Y,Lin Y H,Vaseeharan B,Chen J C. 2007. The immune response of tilapia Oreochromis mossambicus and its susceptibility to Streptococcus iniae under stress in low and high temperatures[J]. Fish & Shellfish Immunology,22(6):686-694. doi:10.1016/j.fsi.2006.08. 015.
Nitzan T,Kokou F,Doron-Faigenboim A,Slosman T,Biran J,Mizrahi I,Zak T,Benet A,Cnaani A. 2019. Transcriptome analysis reveals common and differential response to low temperature exposure between tolerant and sensitive blue tilapia(Oreochromis aureus)[J]. Frontiers in Genetics,10:100. doi:10.3389/fgene.2019.00100.D702AD90-53E9-41CC-98A9-65C771A49FD3
Oyola M G,Handa R J. 2017. Hypothalamic-pituitary-adrenal and hypothalamic-pituitary-gonadal axes:Sex differences in regulation of stress responsivity[J]. Stress (Amsterdam,Netherlands),20(5):476-494. doi:10.1080/10253890.2017. 1369523.
Qian B Y,Xue L Y. 2016. Liver transcriptome sequencing and de novo annotation of the large yellow croaker (Lari-michthy crocea) under heat and cold stress[J]. Marine Genomics,25:95-102. doi:10.1016/j.margen.2015.12.001.
Silva K E,Rosner J,Ullrich N J,Chordas C,Manley P E,Moulton E A. 2019. Pain affect disrupted in children with posterior cerebellar tumor resection[J]. Annals of Clinical and Translational Neurology,6(2):344-354. doi:10.1002/acn3.709.
Somero G N. 2010. The physiology of climate change:How potentials for acclimatization and genetic adaptation will determine ?winners? and ?losers?[J]. Journal of Experimental Biology,213(6):912-920. doi:10.1242/jeb.037 473.
Song J W,McDowell J R. 2020. Comparative transcriptomics of spotted seatrout (Cynoscion nebulosus) populations to cold and heat stress[J]. Ecology and Evolution,11(3):1352-1367. doi:10.1002/ece3.7138.
Sun Z Z,Tan X H,Xu M L,Liu Q Y,Ye H Q,Zou C Y,Ye C X. 2019. Liver transcriptome analysis and de novo annotation of the orange-spotted groupers(Epinephelus coioides) under cold stress[J]. Comparative Biochemistry and Physiology. Part D:Genomics & Proteomics,29:264-273. doi:10.1016/j.cbd.2018.12.008.
Tao W J,Xu L H,Zhao L,Zhu Z X,Wu X,Min Q W,Wang D H,Zhou Q. 2021. High-quality chromosome-level genomes of two tilapia species reveal their evolution of repeat sequences and sex chromosomes[J]. Molecular Eco-logy Resources,21(2):543-560. doi:10.1111/1755-0998. 13273.
Trapnell C,Roberts A,Goff L,Pertea G,Kim D,Kelley D R,Pimentel H,Salzberg S L,Rinn J L,Pachter L. 2012. Differential gene and transcript expression analysis of RNA-Seq experiments with TopHat and Cufflinks[J]. Nature Protocols,7(3):562-578. doi:10.1038/nprot.2012.016.
van den Burg E H,Peeters R R,Verhoye M,Meek J,Flik G,van der Linden A. 2005. Brain responses to ambient temperature fluctuations in fish:Reduction of blood volume and initiation of a whole-body stress response[J]. Journal of Neurophysiology,93(5):2849-2855. doi:10.1152/jn.01113.2004.
Velmurugan B K,Chan C R,Weng C F. 2019. Innate-immune responses of tilapia(Oreochromis mossambicus) exposure to acute cold stress[J]. Journal of Cellular Physio-logy,235(9):6325-6325. doi:10.1002/jcp.28270.D702AD90-53E9-41CC-98A9-65C771A49FD3
Wen X,Hu Y D,Zhang X Y,Wei X Z,WANG T,Yin S W. 2019. Integrated application of multi-omics provides insights into cold stress responses in pufferfish Takifugu fasciatus[J]. BMC Genomics,20(1):563. doi:10.1186/s12864-019-5915-7.
Xu D D,You Q C,Chi C F,Luo S Y,Song H B,Lou B,Takeuchi Y.? 2018. Transcriptional response to low temperature in the yellow drum(Nibea albiflora) and identification of genes related to cold stress[J]. Comparative Biochemistry and Physiology. Part D:Genomics & Proteomics,28:80-89. doi:10.1016/j.cbd.2018.07.003.
Yang C G,Jiang M,Wen H,Tian J,Liu W,Wu F,Gou G W. 2015. Analysis of differential gene expression under low-temperature stress in Nile tilapia(Oreochromis niloticus) using digital gene expression[J]. Gene,564(2):134-140. doi:10.1016/j.gene.2015.01.038.
Yang H,Su J J,Meng W X,Chen X Y,Xu Y,Sun B. 2021. MiR-518a-5p targets GZMB to extenuate vascular endothelial cell injury induced by hypoxia-reoxygenation and thereby improves myocardial ischemia[J]. International Heart Journal,62(3):658-665. doi:10.1536/ihj.20-619.
Yang Q B,Ma Z H. 2016. Effect of temperature on growth,survival and occurrence of skeletal deformity in the gol-den pompano Trachinotus ovatus larvae[J]. Indian Journal of Fisheries,63(1):74-82. doi:10.21077/ijf.2016.63. 1.51490-10.
Yu T,Zhang J G,Cao J S,Cai Q,Li X,Sun Y,Li S N,Li Y L,Hu G H,Cao S L,Liu C H,Wang G Q,Wang L S,Duan Y J. 2021. Leaf transcriptomic response mediated by cold stress in two maize inbred lines with contrasting tolerance levels[J]. Genomics,113(2):782-794. doi:10. 1016/j.ygeno.2021.01.018.
Zou H F,Shi M M,Liu L F,Yuan H M,Zhang Y,Zhang X S,Lu W Q. 2021. Diel rhythm of urotensin I mRNA expression and its involvement in the locomotor activity and appetite regulation in olive flounder Paralichthys olivaceus[J]. Comparative Biochemistry and Physiology. Part B:Biochemistry & Molecular Biology,256:110627. doi:10.1016/j.cbpb.2021.110627.
(責任編輯 蘭宗寶)D702AD90-53E9-41CC-98A9-65C771A49FD3

