草地貪夜蛾腸道細菌分離鑒定與功能初探
陳亞平 杜鄂巍 李亞紅 魯智慧 李浩 桂富榮
摘要:【目的】明確草地貪夜蛾幼蟲腸道細菌的種類和功能,以詮釋腸道細菌對草地貪夜蛾寄主植物適應性的影響,為揭示草地貪夜蛾的寄主適應機制及進一步預測其寄主譜擴張趨勢提供依據。【方法】采用傳統的微生物分離純化方法對草地貪夜蛾腸道細菌進行分離純化,對分離獲得的細菌菌株進行16S rRNA序列同源性分析鑒定;利用篩選培養基對產生纖維素酶、木聚糖酶、果膠酶及對苯酚有代謝能力的菌株進行初篩,并進一步用DNS法測定相關菌株產纖維素酶、木聚糖酶和果膠酶的酶活性,用含苯酚的無機鹽培養基培養菌株,檢測菌株的苯酚降解效率。【結果】共分離獲得45株細菌菌株,經同源序列比對分析,45株細菌菌株分屬于3門5屬8種,分別是厚壁菌門(Firmicutes)的葡萄球菌屬(Staphylococcus)和芽孢桿菌屬(Bacillus),變形菌門(Proteobacteria)的克雷伯氏菌屬(Klebsiella)和不動桿菌屬(Acinetobacter),放線菌門(Acinobacteria)的短桿菌屬(Curtobacterium),其中克雷伯氏菌屬的豐度最高。45株菌株中有產纖維素酶菌株11株,酶活力最高的是變棲克雷伯氏菌菌株K3,為0.105±0.007 U/mL;產木聚糖酶菌株10株,酶活力最高的是枯草芽孢桿菌菌株B9,為1.090±0.468 U/mL;產果膠酶菌株5株,酶活力最高的是變棲克雷伯氏菌菌株K27,為0.193±0.047 U/mL;降解苯酚的菌株9株,降解速率最高的是沙福芽孢桿菌菌株B8,為(0.347±0.042)%。【結論】草地貪夜蛾幼蟲腸道細菌的產酶菌株多樣性較高,推測這是導致草地貪夜蛾寄主譜廣,對寄主為害嚴重的原因之一。
關鍵詞: 草地貪夜蛾;腸道細菌;分離鑒定;酶活測定;苯酚降解
中圖分類號: S433.4? ? ? ? ? ? ? ? ? ? ? ? ? ? ? 文獻標志碼: A 文章編號:2095-1191(2022)03-0821-09
Isolation,identification and functional analysis of intestinal bacteria of Spodoptera frugiperda
CHEN Ya-ping DU E-wei LI Ya-hong LU Zhi-hui LI Hao GUI Fu-rong
(1Plant Protection College,Yunnan Agricultural University/State Key Laboratory for Conservation and Utilization
of Bioresources in Yunnan, Kunming, Yunnan? 650201, China; 2 Yunnan Plant Protection and Plant
Inspection Station, Kunming, Yunnan? 650034, China)
Abstract:【Objective】To clarify the species and functions of intestinal bacteria of Spodoptera frugiperda and explain the effects of intestinal bacteria on the adaptability of S. frugiperda to host plants,so as to provide a theoretical basis for revealing the host adaptation mechanism of S. frugiperda and predict the expansion trend of host spectrum. 【Method】The intestinal bacteria of S. frugiperda were isolated and purified using the microbial isolation and purification methods,and the 16S rRNA gene sequence homology analysis was performed on the isolated bacterial strains. The strains that produced cellulase,xylanase,pectinase and metabolized phenol were preliminarily screened. And the cellulase,xylanase,pectinase production activities and metabolism of phenol were analyzed through DNS method. The strains were cultured in phenol-containing inorganic salt medium to detect their phenol degradation efficiency. 【Result】A total of 45 bacterial strains were isolated by comparative homologous sequence analysis,and they belonged to 5 genera of Firmicutes,Proteobacteria,and Acinobacteria,namely,Staphylococcus,Bacillus,Klebsiella,Acinetobacter and Colletotrichum,among which Klebsiella had the highest abundance. Among the 45 strains,11 strains could produce cellulase and K3 of Klebsiella had the highest enzyme activity of 0.105±0.007 U/mL; 10 strains could produce xylanase and B9 of Bacillus had the highest enzyme activity of 1.090±0.468 U/mL; 5 strains could produce pectinase K27 of Klebsiella had the highest enzyme activity of 0.193±0.047 U/mL; 9 strains could degrade phenol and B8 of Bacillus had the highest degradation rate of (0.347±0.042)%. 【Conclusion】Diversity of enzyme-producing strains of intestinal bacteria in S. frugiperda larvae is speculated to be one of the reasons for the wide host spectrum and serious damage to the host.
Key words: Spodoptera frugiperda; intestinal bacteria; isolation and identification; enzyme activity determination; phenolic degradation
Foundation items: National key Research and Development Program of China (2021YFD1400701)
0 引言
【研究意義】草地貪夜蛾(Spodoptera frugiperda)屬鱗翅目(Lepidoptera)夜蛾科(Noctuidae),原產于美洲熱帶和亞熱帶地區,是聯合國糧農組織全球預警的跨境遷飛性重大害蟲,目前已入侵全球100多個國家和地區(蘇湘寧等,2020;Gui et al.,2020),給各地農業產業造成毀滅性打擊。該蟲于2019年1月侵入我國云南江城,是近年來入侵我國的重大農業害蟲之一,位列農業農村部發布的一類農作物十大害蟲之首。2020年草地貪夜蛾在我國27個省1423個縣發生,發生面積超過133萬ha,對我國糧食作物的安全生產構成極大威脅(田良恒等,2021;Wu et al.,2021)。草地貪夜蛾造成嚴重危害的重要原因之一是其寄主范圍廣,達76科353種(Montezano et al.,2018),且其寄主譜還在不斷擴大,據報道,生姜、煙草和茶葉等多種具有較高經濟價值的經濟作物均是其潛在寄主(Lü et al.,2021)。草地貪夜蛾能在各種復雜的棲境中定殖和為害,與其較廣的寄主譜及對寄主植物的有效利用密切相關,而腸道細菌在其對寄主的適應過程中發揮著重要作用。因此,研究草地貪夜蛾腸道可培養細菌群落結構和功能,有助于進一步研究腸道細菌在昆蟲對寄主植物適應中的作用,為草地貪夜蛾的防控打下基礎。【前人研究進展】昆蟲腸道內的大量共生菌與其昆蟲宿主一起作為一個共生體受到自然選擇作用,在不同的環境及取食條件中,逐漸塑造出一個使昆蟲機體適應環境及食物的腸道微生物群落,并且可能通過垂直傳遞被保留下來(Wilson et al.,2010),而腸道微生物也同時直接影響著昆蟲宿主的生理活動,這些微生物與昆蟲一起協同完成許多重要的功能。如可為昆蟲提供營養(李丹紅等,2017),蚜蟲取食植物韌皮汁液,這些汁液缺乏蚜蟲生存所必須的氨基酸,而蚜蟲腸道共生菌則為其合成這些必須的營養物質(Wilson et al.,2010);在昆蟲生長過程中必不可少的維生素,直接來源于食物的量無法滿足其正常發育,不足的部分可由腸道細菌合成來進行補充(Jing et al.,2020)。對寄主植物營養成分的降解也主要由腸道微生物來完成,前人采用傳統微生物分離方法從棉鈴蟲、小菜蛾和家蠶腸道中分離得到的可培養細菌有水解纖維素、木聚糖、果膠、淀粉和脂肪的能力(Anand et al.,2010;Briones-Roblero et al.,2017;Gandotra et al.,2018)。此外,昆蟲對寄主植物進行利用還需應對植物內含有的次生代謝物質和防御性物質(Xu et al.,2016),如玉米根蟲腸道細菌可保護其免受大豆葉片中的半胱氨酸蛋白酶抑制劑的毒害,使玉米根蟲能在食源缺乏的情況下取食大豆葉片(Chu et al.,2013);從舞毒蛾腸道中分離的不動桿菌屬細菌可降解其主要寄主山楊分泌的有毒性的酚苷類化合物,從而保護昆蟲在取食后不受毒性影響(Mason et al.,2016);毛健夜蛾的主要寄主植物是富含生物堿的石蒜科植物,其腸道內的克雷伯氏菌能降解生物堿,在其腸道內還分離到酪黃腸球菌,能耐受植物分泌的乳膠,可能對昆蟲的腸道具有保護作用(Vilanova et al.,2016)。現已有研究關注到草地貪夜蛾的腸道微生物,研究內容多集中在草地貪夜蛾的分布區域和入侵階段等因素對其腸道細菌群落的影響(唐運林等,2019;張凌英等,2020;張詩晟等,2020)。【本研究切入點】目前,草地貪夜蛾對寄主植物的適應能力與其腸道細菌功能之間的關系尚未見相關報道。【擬解決的關鍵問題】采用傳統的微生物分離純化方法對草地貪夜蛾的腸道細菌進行分離培養及鑒定,并驗證其對自身無法降解的食物成分(纖維素、木聚糖、果膠及酚類)的降解能力,為草地貪夜蛾腸道細菌響應寄主植物的不同營養成分及次生物質脅迫研究提供參考,也為揭示其寄主適應機制及進一步預測寄主譜擴張趨勢提供依據。
1 材料與方法
1. 1 試驗材料
1. 1. 1 供試蟲源 草地貪夜蛾采自云南省玉溪市(東經101°58′,北緯23°35′,海拔421 m),在實驗室內用自主栽培的玉米葉片飼養10代以上[飼養溫度(27±0.5)℃,相對濕度(70±5)%,光周期L∶D=16 h∶8 h]。成蟲羽化后,以1∶1的雌雄比配對,取同一雌蟲產下的卵粒進行試驗。
1. 1. 2 主要試劑及培養基 LB培養基:蛋白胨10 g,酵母提取物5 g,NaCl 10 g,瓊脂15 g,水1 L;營養瓊脂培養基(NA):牛肉膏3 g,蛋白胨10 g,NaCl 5 g,瓊脂15 g,水1 L;沙門菌培養基(SS):牛肉粉5 g,蛋白胨5 g,三號膽鹽3.5 g,瓊脂15 g,乳糖10 g,檸檬酸鈉8.5 g,硫代硫酸鈉8.5 g,檸檬酸鐵1 g,中性紅0.025 g,煌綠0.00033 g,水1 L;纖維素篩選培養基:羧甲基纖維素鈉10 g,蛋白胨1 g,(NH)SO 4 g,NaCl 1 g,KHPO 2 g,MgSO·7HO 0.4 g,瓊脂20 g,水1 L,pH 7.0;木聚糖篩選培養基:木聚糖8 g,酵母粉1 g,(NH)SO 4 g,KHPO 2 g,NaCl 0.5 g,MgSO·7HO 0.5 g,瓊脂20 g,水1 L,pH 7.0;果膠篩選培養基:果膠粉10 g,酵母粉1 g,(NH)SO 4 g,KHPO 1 g,KCl 0.5 g,MgSO·7HO 0.4 g,FeSO 0.01 g,瓊脂20 g,水1 L,pH 7.0;苯酚降解培養基:苯酚0.1 g,KHPO 1 g,KHPO 0.3 g,MgSO·7HO 0.1 g,NaCl 1 g,NHNO 1 g,瓊脂20 g,水1 L,pH 7.0;纖維素酶鑒定培養基:羧甲基纖維素鈉5 g,(NH)SO 2 g,NaCl 1 g,KHPO 2 g,MgSO·7HO 0.2 g,CaCl 0.1 g,瓊脂20 g,水1 L,pH 7.0;木聚糖酶鑒定培養基:木聚糖5 g,(NH)SO 2 g,KHPO 2 g,NaCl 1 g,MgSO·7HO 0.2 g,瓊脂20 g,水1 L,pH 7.0;果膠酶鑒定培養基:果膠粉5 g,(NH)SO 2 g,KHPO 1 g,NaNO 3 g,KCl 0.5 g,MgSO·7HO 0.4 g,FeSO 0.01 g,瓊脂20 g,水1 L,pH 7.0;無機鹽培養基(MSM):苯酚0.1 g,KHPO 1 g,KHPO 0.3 g,MgSO·7HO 0.1 g,NaCl 1 g,NHNO 1 g,水1 L,pH 7.0。
1. 2 試驗方法
1. 2. 1 草地貪夜蛾中腸細菌分離 取5頭健康且生長發育程度較一致的草地貪夜蛾5齡幼蟲,饑餓處理24 h左右使其排空腸道內食物殘渣。用無菌水沖洗后浸入75%酒精溶液中1 min,然后用無菌水清洗蟲體3次,放入滅菌培養皿中,用尖頭鑷輕輕拉拽以取出完整的腸道,去除前腸、后腸及馬氏管,將中腸置于2 mL無菌凍存管中,加入少量磷酸緩沖液后用鑷子輕輕搗碎,勻漿,補充磷酸緩沖液至1 mL。將含草地貪夜蛾中腸的懸液分別稀釋至10-3、10-4和10-5后備用,并各取100 μL分別涂布于LB、NA和SS固體培養基上(黃秀梨和辛明秀,2008),各設3次重復,置于30 ℃培養箱培養24~48 h。選取菌落數量適中的培養皿,用接種環挑取不同形態特征的單菌落,經5次劃線得到純培養菌株,置于2 mL液體培養基凍存管中,30 ℃下180 r/min恒溫搖床培養24 h,添加50%的甘油后置于-80 ℃超低溫冰箱中保存(鄭亞強等,2017)。
1. 2. 2 草地貪夜蛾腸道細菌DNA提取及PCR擴增
按照DNA提取試劑盒[天根生物科技(北京)有限公司]的操作步驟提取腸道細菌DNA。以提取得到的細菌基因組DNA為模版,使用通用引物27F(5'-AGAGTTTGATCCTGGCTCAG-3')/1492R(5'-CTA CGGCTACCTTGTTACGA-3')進行16S rRNA PCR擴增。反應體系25.0 μL:RCR Mix 12.5 μL,DNA模板1.0 μL,上、下游引物各1.0 μL,ddH2O補足至25.0 μL。擴增程序:94 ℃預變性5 min;94 ℃ 30 s,52 ℃ 30 s,72 ℃ 50 s,進行30個循環;72 ℃延伸10 min。反應完成后,用1%瓊脂糖凝膠電泳檢測后送至上海擎科生物科技有限公司進行測序。
1. 2. 3 草地貪夜蛾腸道細菌菌株分子鑒定及系統發育分析 對所有樣本的有效標簽進行聚類,默認相似性大于97%即定義為一個操作分類單元(Operational taxonomic unit,OTU),統計各分類水平的物種在每個樣本中的相對豐度。將可培養分離的菌株獲得的16S rRNA序列與GenBank中已知序列進行BLAST同源比對,下載GenBank中同源性較高序列,利用MEGA X10.0.2,使用鄰接法(Neighbor-joining,NJ)進行1000次補償計算,構建系統發育進化樹。
1. 2. 4 草地貪夜蛾腸道細菌對纖維素、木聚糖和果膠降解功能分析 將分離純化獲得的菌株分別點接到纖維素篩選培養基、木聚糖篩選培養基和果膠篩選培養基(黃秀梨和辛明秀,2008),每株菌株設3個重復,將各培養基平板倒置于恒溫培養箱中30 ℃培養72 h,篩選出能在上述培養基中生長的菌株。將篩選培養基上生長的菌株分別點接至纖維素酶鑒定培養基、果膠酶鑒定培養基和木聚糖酶鑒定培養基,并放置于恒溫箱中30 ℃培養7 d后,分別使用剛果紅、溴酚藍和盧戈式碘液進行染色,觀察菌落周圍是否產生透明圈。將有產酶活性的菌株,分別采用DNS法測定相關菌株產纖維素酶、木聚糖酶和果膠酶的酶活性。
1. 2. 5 草地貪夜蛾腸道細菌對苯酚的降解功能分析 將分離純化獲得的菌株接種到苯酚降解培養基上。將培養基平板倒置于恒溫培養箱中30 ℃培養72 h。將能在苯酚降解培養基上生長的菌株接種到含苯酚的無機鹽培養基中于37 ℃下200 r/min搖床培養,采用分光光度計比色法檢測苯酚降解效率。
1. 3 統計分析
試驗數據應用SPSS 19.0進行單因素方差分析(One-way ANOVA),采用Duncan’s多重比較分析各菌株間同一種酶活性的差異。
2 結果與分析
2. 1 草地貪夜蛾腸道細菌分離結果
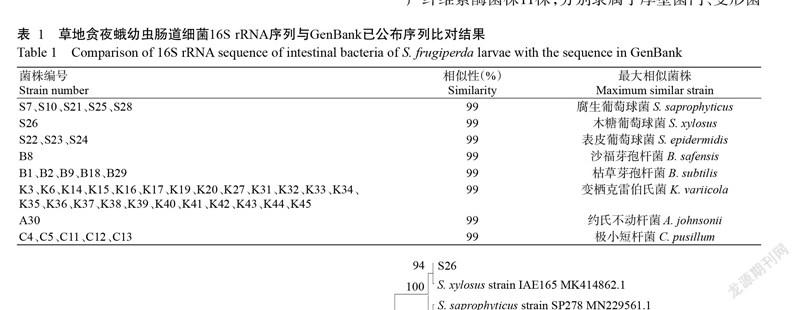
從各類培養基上共獲得菌落形態相異的45株菌株,將獲得的16S rRNA序列與GenBank數據庫中已知序列進行比對,結果見表1。45條序列與5個屬的16S rRNA序列同源性較高,序列相似性在99%以上,菌株分別屬于3門5屬8種,分別為:厚壁菌門(Firmicutes)的葡萄球菌屬(Staphylococcus)和芽孢桿菌屬(Bacillus);變形菌門(Proteobacteria)的克雷伯氏菌屬(Klebsiella)和不動桿菌屬(Acinetobacter);放線菌門(Acinobacteria)的短桿菌屬(Curtobacterium)。
2. 2 草地貪夜蛾腸道細菌系統發育分析結果
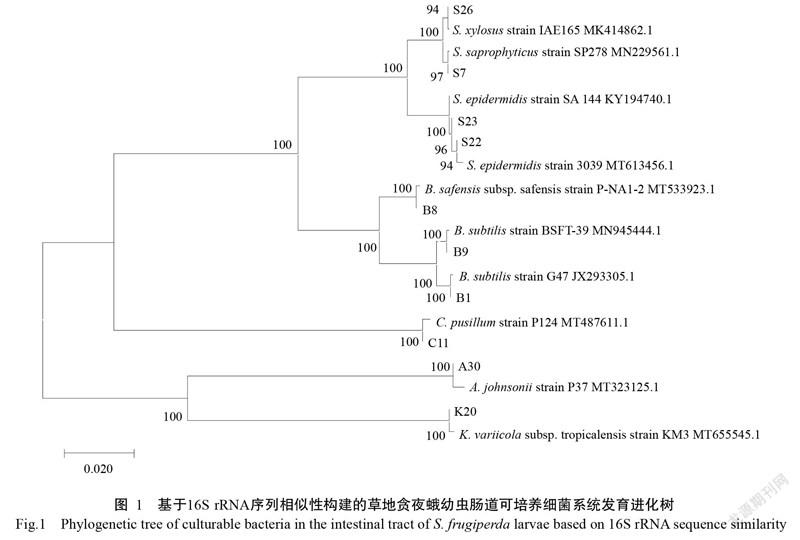
對測序獲得的草地貪夜蛾腸道細菌16S rRNA序列進行系統進化分析,結果(圖1)表明,其腸道細菌主要由兩大類群組成,系統發育進化樹共分為兩大支:菌株S7、S22、S23和S26與其他已知的葡萄球菌屬菌株聚為一小支,B1、B8和B9與其他芽孢桿菌屬的菌株聚為一小支,這2個分支構成厚壁菌門,并與放線菌門短桿菌屬的菌株C11聚為一大支;克雷伯氏菌屬的菌株K20與不動桿菌屬的菌株A30聚為變形菌門的一大支。
2. 3 草地貪夜蛾腸道細菌產纖維素酶、木聚糖酶和果膠酶活性分析結果
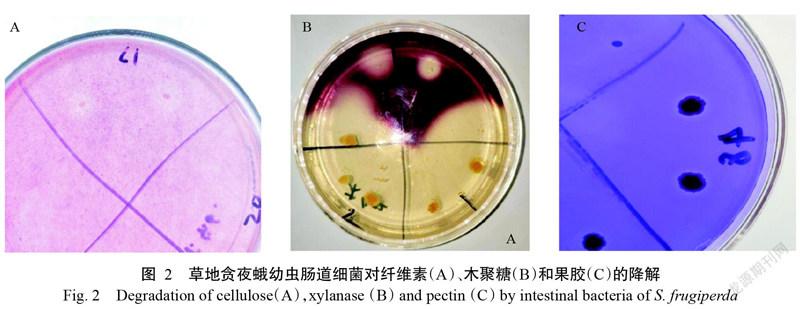
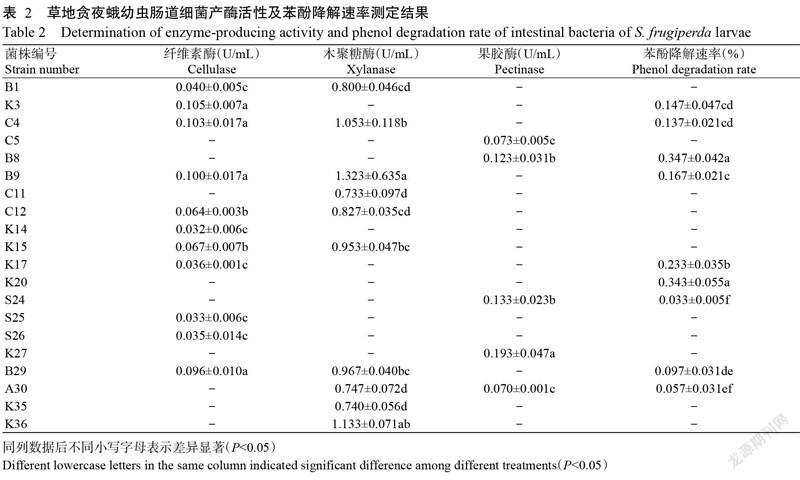
將分離獲得的45株細菌菌株分別接種到纖維素酶、果膠酶和木聚糖酶篩選培養基上,共篩選出產酶菌株19株(圖2),占總分離菌株數的42.2%。其中,產纖維素酶菌株11株,分別隸屬于厚壁菌門、變形菌門和放線菌門中葡萄桿菌屬的腐生葡萄球菌和木糖葡萄球菌,芽孢桿菌屬的枯草芽孢桿菌,克雷伯氏菌屬的變棲克雷伯氏菌,短桿菌屬的極小短桿菌;10株產木聚糖酶菌株,分別隸屬于厚壁菌門、變形菌門和放線菌門中芽孢桿菌屬的枯草芽孢桿菌,克雷伯氏菌屬的變棲克雷伯氏菌,不動桿菌屬的約氏不動桿菌,短桿菌屬的極小短桿菌;5株產果膠酶菌株,分別隸屬于厚壁菌門、變形菌門和放線菌門中葡萄球菌屬的表皮葡萄球菌,芽孢桿菌屬的枯草芽孢桿菌,克雷伯氏菌屬的變棲克雷伯氏菌,不動桿菌屬的約氏不動桿菌,短桿菌屬的極小短桿菌(表2)。
將產酶菌株分別接種至LB液體發酵培養基中,于30 ℃下250 r/min培養3 d后測定其發酵液中相關酶活性,結果(表2)顯示,產纖維素酶活性最高的菌株是變棲克雷伯氏菌K3,為0.105±0.007 U/mL,其次為C4、B9和B29,4株菌株間產纖維素酶活性差異不顯著(P>0.05,下同),且均顯著高于其他產纖維素酶菌株的酶活性(P<0.05,下同);產木聚糖酶活性最高的菌株是枯草芽孢桿菌B9,為1.323±0.635 U/mL,顯著高于K36菌株外的其他產木聚糖酶菌株的酶活性;產果膠酶活性最高的菌株是變棲克雷伯氏菌K27,為0.193±0.047 U/mL,顯著高于其他產果膠酶菌株的酶活性。
2. 4 草地貪夜蛾腸道細菌對苯酚降解能力分析結果
分離獲得的45株細菌菌株中有9株可降解苯酚(表2),分別隸屬于厚壁菌門、變形菌門和放線菌門中葡萄桿菌屬的表皮葡萄球菌,芽孢桿菌屬的沙福芽孢桿菌和枯草芽孢桿菌,克雷伯氏菌屬的變棲克雷伯氏菌,不動桿菌屬的約氏不動桿菌,短桿菌屬的極小短桿菌。其中,沙福芽孢桿菌B8對苯酚的降解速率最高,為(0.347±0.042)%,顯著高于K20菌株外的其他7株菌株。
3 討論
昆蟲與寄主植物的協同進化機制較多,其中腸道微生物群落在其協同進化過程中發揮著重要作用,如對植物細胞壁的降解、營養物質代謝及植物防御性次生物質的耐受等。研究發現,白蟻的腸道細菌為白蟻提供了高活性的纖維素酶,催化植物細胞壁轉化為可利用的發酵產品,以彌補其自身缺乏木質纖維素降解基因的不足(Warnecke et al.,2007),從而使昆蟲能補充其自身生長所需的營養;此外,白蟻的腸道細菌還可將宿主產生的含氮廢棄物或大氣氮合成氨,提供給昆蟲必須的氨基酸和維生素(Calderón-Cortés et al.,2012)。果膠是構成植物細胞壁的重要成分,Jing等(2014)在意大利蜜蜂的腸道中發現了能降解果膠的共生菌。酚類是植物中最廣泛也是最重要的一種防御性次生物質,會影響昆蟲對食物的消化吸收并誘導活性氧產生,活性氧對許多鱗翅目昆蟲有很強的毒性。夏曉峰(2014)發現小菜蛾在食物消化過程中,腸桿菌能對進入中腸的有毒酚類進行有效降解,而這些腸道細菌對特定食物進行分解代謝、提高宿主繁殖力及其與昆蟲宿主基因間的交流互補,促使昆蟲隨著寄主植物發生協同進化(Bevins and Salzman,2011),因此,從昆蟲腸道細菌的角度來研究昆蟲的食性具有重要意義。
本研究采用傳統微生物分離純化方法,從草地貪夜蛾5齡幼蟲中腸中分離得到分屬3門5屬8種的45株細菌菌株,測序結果顯示,45株菌株中有25株屬于變形菌門,15株屬于厚壁菌門,5株屬于放線菌門。在門水平上,本研究中變形菌門和厚壁菌門是草地貪夜蛾幼蟲中腸細菌中的優勢門,與其他昆蟲腸道細菌的優勢類群一致,說明昆蟲腸道細菌的結構具有一定的保守性。在屬和種水平上,本研究發現草地貪夜蛾幼蟲腸道優勢細菌隸屬克雷伯氏菌屬,與前人對重慶及云南其他地區的研究結果一致。唐運林等(2019)從重慶地區的草地貪夜蛾幼蟲腸道中分離到8個屬的細菌,其中克雷伯氏菌屬豐度最高;李青晏等(2020)對云南蒙自的草地貪夜蛾幼蟲和成蟲中腸細菌進行分離培養,發現幼蟲腸道中克雷伯氏菌屬豐度最高;張志紅等(2020)研究表明,云南芒市草地貪夜蛾幼蟲腸道的優勢種細菌為變棲克雷伯氏菌。而Acevedo等(2016)采用傳統微生物培養方法對美國草地貪夜蛾種群進行研究,發現其3齡幼蟲腸道中主要的細菌種類為菠蘿泛菌、德維希腸桿菌、奎尼沃納沙雷氏菌、解鳥氨酸拉烏爾菌、產酸克雷伯氏菌和分散泛菌;Almeida等(2017)從巴西草地貪夜蛾腸道中發現7屬10種細菌,其中鉛黃腸球菌和蒙氏腸球菌為優勢種。國內外草地貪夜蛾種群幼蟲腸道可培養細菌種類與優勢種類的差異,可能與地理環境有關。
此外,入侵云南的草地貪夜蛾種群基因型是C型(玉米型) (張磊等,2019;Gui et al.,2020),在云南主要為害玉米,而克雷伯氏菌普遍存在于玉米的根莖及種植土壤中,與植物在長期進化過程中形成了密切的合作關系(李夢嬌等,2014),提示云南草地貪夜蛾腸道克雷伯氏菌可能來源于寄主植物或由寄主植物介導的根際土壤。在本研究中,產纖維素酶和果膠酶活性最高的腸道菌株也為克雷伯氏菌,表明草地貪夜蛾取食玉米后克雷伯氏菌可在其腸道中穩定定殖并協助宿主昆蟲提高對寄主植物的利用效率。已有研究證實植食性昆蟲的微生物出現在寄主植物上和植物根際土壤中,是由于植物可直接影響其種植土壤的微生物群落結構,繼而影響昆蟲腸道微生物組成,昆蟲腸道微生物、植物共生微生物及植物根際土壤微生物之間可能發生傳遞(Chi et al.,2005;Sugio et al.,2015)。Priya等(2012)研究發現,棉鈴蟲幼蟲腸道細菌群落的結構與其寄主植物葉際細菌群落相似,表明寄主植物是昆蟲腸道細菌的重要來源。然而,寄主植物及其內生菌在進入昆蟲腸道后協助昆蟲適應多樣化的寄主植物的生理代謝機制尚需進一步探究。
本研究在分離獲得的45株細菌中篩選得到20株產酶和苯酚降解菌株,能降解纖維素的有3門4屬5種11株,能降解木聚糖的有3門4屬4種10株,能降解果膠的有3門5屬5種5株,能降解苯酚的有3門5屬6種9株,產酶菌株多樣性較高,并且數量在分離獲得的腸道細菌中所占比例較高。同屬鱗翅目的家蠶幼蟲腸道細菌產纖維素酶菌株分別有葡萄球菌屬、芽孢桿菌屬和不動桿菌屬(李冠楠等,2014);小菜蛾腸道細菌中則主要由腸桿菌和肉桿菌來執行食物消化及對植物酚類解毒代謝的功能(夏曉峰,2014);椰心葉甲腸道菌群只有芽孢桿菌屬能降解纖維素和木聚糖,此外帶化紅球菌能降解木聚糖(章雨璐等,2021)。相比而言,草地貪夜蛾腸道細菌中可行使營養成分降解及植物次生物質代謝的細菌種類更豐富,這可能是導致草地貪夜蛾對寄主適應性強且食性高度多樣化的潛在原因。鄭亞強等(2017)從馬鈴薯塊莖蛾腸道分離出4門8屬的細菌菌株,對纖維素、木聚糖和果膠等3種大分子物質均無降解能力,但獲得多株具有較強淀粉酶活性的菌株,這可能是馬鈴薯塊莖蛾為適應高淀粉食物而形成的特有菌屬;椰子織蛾多取食棕櫚科植物的老硬葉片,其中纖維素、木聚糖等難降解物質占比高于幼嫩葉片,涂艷等(2020)從椰子織蛾腸道中分離培養出多株具有較高纖維素酶及木聚糖酶活性的菌株,表明腸道細菌功能與其主要取食的寄主植物部位及營養成分有直接關系。
4 結論
通過傳統微生物分離純化方法從草地貪夜蛾幼蟲腸道分離獲得3門5屬8種共45株細菌,其中有20株細菌可行使營養成分降解及植物次生物質代謝的功能,產酶菌株的多樣性較高,推測這是導致草地貪夜蛾寄主譜廣,對寄主為害嚴重的原因之一。
參考文獻:
黃秀梨,辛明秀. 2008. 微生物學實驗指導[M]. 北京:高等教育出版社:31-32. [Huang X L,Xin M X. 2008. A guide to microbiology experiment[M] Beijing:Higher Education Press:31-32.]
李丹紅,王譽,楊紅. 2017. 高效降解木質纖維素的白蟻腸道微生物組[J]. 微生物學報,57(6):876-884. [Li D H,Wang Y,Yang H. 2017. Gut microbiome of wood-feeding termites[J]. Acta Microbiologica Sinica,57(6):876-884.] doi:10.13343/j.cnki.wsxb.20170076.
李冠楠,夏雪娟,趙歡歡,隆耀航,唐文超,辛佳,李漢歌,朱勇. 2014. 家蠶腸道細菌菌落形態與產消化酶相關性研究[J]. 西南師范大學學報(自然科學版),39(12):53-57. [Li G N,Xia X J,Zhao H H,Long Y H,Tang W C,Xin J,Li H G,Zhu Y. 2014. On intestinal bacteria colony morphology of silkworm and enzyme-producing correlation[J]. Journal of Southwest China Normal University (Natural Science Edition),39(12):53-57.] doi:10.13718/ j.cnki.xsxb.2014.12.011.
李夢嬌,彭晟,徐紹忠,余代宏,趙明富,文國松. 2014. 克雷伯氏菌在農業與環境治理上的應用[J]. 生物技術進展,4(6):415-420. [Li M J,Peng S,Xu S Z,Yu D H,Zhao M F,Wen G S. 2014. Application of Klebsiella spp. in agriculture and environmental management[J]. Current Biotechnology,4(6):415-420.] doi:10.3969/j.issn.2095-2341.2014.06.07.
李青晏,唐運林,蔣睿軒,張永紅,朱峰,白興榮,顧偌鋮,吳燕燕,吳玉嬌,陳潔,李田,李春峰,韋俊宏,潘國慶,周澤揚. 2020. 云南地區草地貪夜蛾腸道細菌的分離及鑒定[J]. 西南大學學報(自然科學版),42(1):1-8. [ Li Q Y,Tang Y L,Jiang R X,Zhang Y H,Zhu F,Bai X R,Gu R C,Wu Y Y,Wu Y J,Chen J,Li T,Li C F,Wei J H,Pan G Q,Zhou Z Y. 2020. Isolation and identification of gut bacteria of Spodoptera frugiperda feeding on maize in Yunnan,China[J]. Journal of Southwest University (Na-tural Science Edition),42(1):1-8.] doi:10.3969/j.issn.2095- 1191.2020.06.007.
蘇湘寧,廖章軒,李傳瑛,黃少華,李峰博,劉偉玲,章玉蘋. 2020. 廣東草地貪夜蛾對2種常用農藥的抗藥性及助劑和增效劑對農藥毒力的影響[J]. 南方農業學報,51(6):1274-1281. [Su X N,Liao Z X,Li C Y,Huang S H,Li F B,Liu W L,Zhang Y P. 2020. Resistance of Spodoptera frugiperda in Guangdong against two commonly used pesticides and the effects of auxiliaries and synergist on toxicity to pesticides[J]. Journal of Southern Agriculture,51(6):1274-1281.] doi:10.3969/j.issn.2095-1191. 2020.06.004.
唐運林,吳燕燕,顧偌鋮,鄒祥明,張禎,牛小慧,王澤樂,陳潔,吳玉嬌,李田,李春峰,韋俊宏,潘國慶,周澤揚. 2019. 重慶地區草地貪夜蛾腸道細菌的分離鑒定[J]. 西南大學學報(自然科學版),41(7):8-14. [Tang Y L,Wu Y Y,Gu R C,Zou X M,Zhang Z,Niu X H,Wang Z L,Chen J,Wu Y J,Li T,Li C F,Wei J H,Pan G Q,Zhou Z Y. 2019. Isolation and identification of gut bacteria of Spodoptera frugiperda that migrated to Chongqing Area[J]. Journal of Southwest University(Natural Science Edition),41(7):8-14.] doi:10.13718/j.cnki xdzk 2019. 07.002.
田良恒,張利芬,白素芬,尹新明,李欣. 2021. 棉鈴蟲齒唇姬蜂對入侵害蟲草地貪夜蛾的寄生效能[J]. 河南農業大學學報,55(3):442-447. [Tian L H,Zhang L F,Bai S F,Yin X M,Li X. 2021. Parasitism potency of Campoletis chlorideae on the invasive pest Spodoptera frugiperda[J]. Journal of Henan Agricultural University,55(3):442-447.] doi:10.16445/j.cnki.1000-2340.20210414.002.
涂艷,呂寶乾,章雨露,蔣方一丁,齊可欣. 2020. 椰子織蛾幼蟲腸道細菌的初步分離鑒定及功能分析[J]. 生物安全學報,29(4):258-263. [Tu Y,Lü B Q,Zhang Y L,Jiang F Y D,Qi K X. 2020. Preliminary identification and functional analysis of larval gut bacteria in Opisina arenosella Walker[J]. Journal of Biosafety,29(4):258-263.] doi:10.3969/j.issn.20951787.2020.04.005.
夏曉峰. 2014. 小菜蛾中腸微生物多樣性及其功能研究[D]. 福州:福建農林大學. [Xia X F. 2014. Organizational diversity and functional characterization of microbiota in the midgut of diamondback moth,Plutella xylostella (L.)[D]. Fuzhou:Fujian Agriculture and Forestry University.]
張磊,柳貝,姜玉英,劉杰,吳孔明,蕭玉濤. 2019. 中國不同地區草地貪夜蛾種群生物型分子特征分析[J]. 植物保護,45(4):20-27. [Zhang L,Liu B,Jiang Y Y,Liu J,Wu K M,Xiao Y T. 2019. Molecular characterization analysis of fall armyworm populations in China[J]. Plant Protection,45(4):20-27.] doi:10.16688/j.zwbh.2019296.
張凌英,蘇造堂,徐天梅,張志紅,鄭亞強,桂富榮,陳斌. 2020. 云南普洱江城縣草地貪夜蛾幼蟲腸道中可培養細菌的分離及鑒定[J]. 環境昆蟲學報,42(1):60-67. [Zhang L Y,Su Z T,Xu T M,Zhang Z H,Zheng Y Q,Gui F R,Chen B. 2020. Isolation and identification of culturable intestinal bacteria of Spodoptera frugiperda in Jiangcheng,Puer,Yunnan Province[J]. Journal of Environmental Entomology,42(1):60-67.] doi:10.3969/j.issn.1674-0858. 2020.01.8.
張詩晟,蔡海林,張瀟筱,楊中俠. 2020. 湖南常德地區草地貪夜蛾腸道細菌的鑒定及其寄主分析[J]. 湖南農業大學學報(自然科學版),46(3):319-323. [Zhang S S,Cai H L,Zhang X X,Yang Z X. 2020. Identification of the intestinal bacteria in Spodoptera frugiperda collected from Changde Area and analysis of potential host plants[J]. Journal of Hunan Agricultural University (Natural Scien-ces),46(3):319-323.] doi:10.13331/j.cnki.jhau.2020.03. 010.
張志紅,張凌英,趙英杰,蘇造堂,陳思穎,肖關麗,李維薇,陳斌. 2020. 云南省芒市草地貪夜蛾幼蟲腸道可培養細菌種類及對抗生素的敏感性[J]. 南方農業學報,51(6):1293-1299. [Zhang Z H,Zhang L Y,Zhao Y J,Su Z T,Chen S Y,Xiao G L,Li W W,Chen B. 2020. Species and antibiotic sensitivity of culturable gut bacteria of Spodoptera frugiperda larvae from Mangshi,Yunnan[J]. Journal of Southern Agriculture,51(6):1293-1299.] doi:10.3969/j.issn.2095-1191.2020.06.007.
章雨璐,呂寶乾,楊帆,涂艷,蔣方一丁,齊可欣,李紫城. 2021. 椰心葉甲腸道微生物的分離鑒定及功能分析[J]. 熱帶作物學報,42(4):1066-1070. [Zhang Y L,Lü B Q,Yang F,Tu Y,Jiang F Y D,Qi K X,Li Z C. 2021. Isolation,identification and functional analysis of intestinal microorganisms of Brontispa longissimi Gestro[J]. Chinese Journal of Tropical Crops,42(4):1066-1070.] doi:10.3969/ j.issn.1000-2561.2021.04.023.
鄭亞強,杜廣祖,李亦菲,陳斌,李正躍,肖關麗. 2017. 馬鈴薯塊莖蛾腸道細菌分離鑒定及其對植物源大分子化合物的降解作用[J]. 環境昆蟲學報,39(3):525-532. [Zheng Y Q,Du G Z,Li Y F,Chen B,Li Z Y,Xiao G L. 2017. Isolation and identification of bacteria from larval gut of the potato tuberworm,Phthorimaea operculella (Zeller) and the degradation for plant-based macromolecular compounds[J]. Journal of Environmental Entomology,39(3):525-532.] doi:10.3969/j.issn.1674-0858.2017.03.5.
Acevedo F E,Peiffer M,Tan C W,Jones A G,Hoover K,Stanley B A,Wang J,Rosa C,Luthe D,Felton G. 2016. Fall army worm-associated gut bacteria modulate plant defense response[J]. Molecular Plant-Microbe Ireractions,30(2):127-137. doi:10.1094/MPMI-11-16-0240-R.
Almeida L G,Moraes L A B,Trigo J R,Omoto C, C?nsoli F L. 2017. The gut microbiota of insecticide-resistant insects houses insecticide-degrading bacteria:A potential source for bitotechnolgical exploitation[J]. PLoS One,12(3):0174754. doi:10.1371/journal.pone.0174754.
Anand A A P,Vennison S J,Sankar S G,Prabhu D I G,Vasan P T,Raghuraman T,Geoffrey C J,Vendan S E. 2010. Isolation and characterization of bacteria from the gut of Bombyx mori that degrade cellulose,xylan,pectin and starch and their impact on digestion[J]. Journal of Insect Science,10:1-20. doi:10.1673/031.010.10701.
Bevins C L,Salzman N H. 2011. Paneth cells,antimicrobial peptides and maintenance of intestinal homeostasis[J]. Nature Reviews Microbiology,9(5):356-368. doi:10. 1038/nrmicro2546.
Briones-Roblero C I,Rodríguez-Díaz R,Santiago-Cruz J A,Zú?iga G,Rivera-Ordu?a F N. 2017. Degradation capacities of bacteria and yeasts isolated from the gut of Dendroctonus rhizophagus(Curculionidae:Scolytinae)[J]. Folia Microbiologica,62(1):1-9. doi:10.1007/s12223-016-0469-4.
Calderón-Cortés N,Quesada M,Watanabe H,Cano-Camacho H,Oyama K. 2012. Endogenous plant cell wall digestion:A key mechanism in insect evolution[J]. Annual Review of Ecology,Evolution,and Systematics,43(1):45-71. doi:10.1146/ANNUREV-ECOLSYS-110411-160312.
Chi F,Shen S H,Cheng H P,Jing Y X,Yanni Y G,Dazzo F B. 2005. Ascending migration of endophytic rhizobia,from roots to leaves,inside rice plants and assessment of benefits to rice growth physiology[J]. Applied Environmental Microbiology,71(11):7271-7278. doi:10.1007/ 1-4020-3570-5_92.
Chu C C,Spencerb J L,Curzia M J,Zavala J A,Seufferheld M J. 2013. Gut bacteria facilitate adaptation to crop rotation in the western corn rootworm[J]. Proceedings of the National Academy of Sciences of the United States of America,110(29):11917-11922. doi:10.1073/pnas.130188 6110.
Gandotra S,Bhuyan P M,Gogoi D K,Kumar A,Subramanian S. 2018. Screening of nutritionally important gut bacteria from the Lepidopteran insects through qualitative enzyme assays[J]. Proceedings of the National Academy of Scien-ces,India Section B:Biological Sciences,88(1):329-337. doi:10.1007/s40011-016-0762-7.
Gui F R,Lan T M,Zhao Y,Guo W,Dong Y,Fang D M,Liu H,Li H,Wang H L,Hao R S,Cheng X F,Li Y H,Yang P C,Sahu S K,Chen Y P,Cheng L,He S Q,Liu P,Fan G Y,Lu H R,Hu G H,Dong W,Chen B,Jiang Y,Zhang Y W,Xu H H,Lin F,Slipper B,Postma A,Jackson M,Abate B A,Tesfaye K,Demie A L,Bayeleygne M D,Degefu D T,Chen F,Kuria P K,Kinyua Z M,Liu T X,Yang H M,Huang F N,Liu X,Sheng J,Kang L. 2020. Genomic and transcriptomic analysis unveils population evolution and development of pesticide resistance in fall armyworm Spodoptera frugiperda[J]. Protein & Cell. doi:10.1007/s13238-020-00795-7.
Jing T Z,Qi F H,Wang Z Y. 2020. Most dominant roles of insect gut bacteria:Digestion,detoxification,or essential nutrient provision?[J]. Microbiome,8(1):38-58. doi:10. 1186/s40168-020-00823-y.
Jing X F,Wong A C N,John M,Colvin J,McKenzie C L,Douglas A E. 2014. The bacterial communities in plant phloem-sap-feeding insects[J]. Molecular Ecology,23(6):1433-1444. doi:10.1111/mec.12637.
Lü D B,Liu X Y,Dong Y L,Yan Z Z,Zhang X,Wang P,Yuan X Q,Li Y P. 2021. Comparison of gut bacterial communities of fall armyworm(Spodoptera frugiperda) reared on different host plants[J]. International Journal of Molecular Sciences,22(20):11266. doi:10.3390/ijms 222011266.
Mason C J,Lowe-Power T M,Rubert-Nason K F,Lindroth R L,Raffa K F. 2016. Interactions between bacteria and aspen defense chemicals at the phyllosphere-herbivore interface[J]. Journal of Chemical Ecology,42(3):193-201. doi:10.1007/s10886-016-0677-z.
Montezano D G,Sosa-Gómez D R,Paula-Moraes S V,Sousa-Silva J C,Hunt T E,Specht A, Roque-Specht V F,Peterson J A. 2018. Host plants of Spodoptera frugiperda (Lepidoptera:Noctuidae) in the Americas[J]. African Entomology,26(2):286-300. doi:10.4001/003.026.0286.
Priya N G,Ojha A,Kajla M K,Raj A,Rajagopal R. 2012. Host plant induced variation ingut bacteria of Helicoverpa armigera[J]. PLoS One, 7(1):e30768. doi:10.1371/journal.pone.0030768.
Sugio A,Dubreuil G,Giron D,Simon J C. 2015. Plant-insect interactions under bacterial influence:Ecological implications and underlying mechanisms[J]. Journal of Experimental Botany,66(2):467-478. doi:10.1093/jxb/eru435.
Vilanova C,Baixeras J,Latorre A,Manuel P. 2016. The gene-ralist inside the specialist:Gut bacterial communities of two insect species feeding on toxic plants are dominated by Enterococcus sp.[J]. Frontiers in Microbiology,7:1005. doi:10.3389/fmicb.2016.01005.
Warnecke F,Luginbühl P,Ivanova N,Ghassemian M,Richardson T H,Stege J T,Cayouette M,McHardy A C,Djordjevic G,Aboushadi N,Sorek R,Tringe S G,Podar M,Martin H G,Kunin V,Dalevi D,Madejska J,Kirton E,Platt D,Szeto E,Salamov A,Barry K,Mikhailova N,Kyrpides N C,Matson E G,Ottesen E A,Zhang X,Hernández M,Murillo C,Acosta L G,Rigoutsos I,Tamayo G,Green B D,Chang C,Rubin E M,Mathur E J,Robertson D E,Hugenholtz P,Leadbetter J R. 2007. Metagenomic and functional analysis of hindgut micro-biota of a wood-feeding higher termite[J]. Nature,450(7169):560-565. doi:10.1038/nature06269.
Wilson A C C,Ashton P D,Calevro F,Charles H,Colella S,Febvay G,Jander G,Kushlan P F,Macdonald S J,Schwartz J F,Thomas G H,Douglas A E. 2010. Genomic insight into the amino acid relations of the pea aphid Acyrthosiphon pisum with its symbiotic bacterium Buchnera aphidicola[J]. Insect Molecular Biology,19(S2):249-258. doi:10.1111/j.1365-2583.2009.00942.x.
Wu P X,Wu F M,Fan J Y,Zhang R Z. 2021. Potential economic impact of invasive fall armyworm on mainly affected crops in China[J]. Journal of Pest Science,94(4):1065-1073. doi:10.1007/S10340-021-01336-9.
Xu L T,Lu M,Sun J H. 2016. Invasive bark beetle-associated microbes degrade a host defensive monoterpene[J]. Insect Science,23(2):183-190. doi:10.1111/1744-7917.12255.
(責任編輯 麻小燕)

