腹腔鏡下原發灶切除術在轉移性結直腸癌中的應用
侯丁丁,秦春和,楊國山,張子超,趙 力
(清華大學第一附屬醫院普通外科,北京,100016)
15%~25%的結直腸癌患者在結直腸癌確診前或確診時發現遠處轉移(包括肝、肺、腹膜、卵巢、非區域淋巴結等),即同時性轉移性結直腸癌(metastatic colorectal cancer,mCRC)[1]。目前國內外指南一般將原發灶切除術推薦應用于:(1)初始可切除的同時性mCRC;(2)同時性mCRC原發灶伴有出血、穿孔、梗阻等腫瘤相關并發癥[2-3]。對于原發灶無癥狀或輕微癥狀的初始不可切除同時性結直腸癌肝轉移不應行預防性原發灶切除術,目前也已達成共識[4]。但對于初始不可切除的mCRC,經過積極的全身治療,如果轉移灶達到部分緩解穩定狀態,我們中心仍建議行原發灶切除術[5]。此外,對于原發灶術式的選擇,轉移灶處于不可切除狀態下,傳統認為即使原發灶可行根治手術,但仍無法使患者全身達到無疾病狀態,因此既往對于不可切除的mCRC行原發灶切除術時,姑息性原發灶切除術占多數。但近年文獻報道,對于mCRC行高位淋巴結清掃術能進一步改善患者總生存期(overall survival,OS)。我們結合清華大學第一附屬醫院普通外科對同時性mCRC行腹腔鏡下原發灶根治性切除術的臨床資料進行探討,以期為同時性mCRC原發灶切除術的分層處理提供臨床依據。
1 資料與方法
1.1 納入與排除標準 選擇2016年1月至2021年8月清華大學附屬第一醫院普通外科收治的同時性mCRC患者。納入標準:(1)同時性mCRC;(2)手術切除標本證實原發灶病理為腺癌或黏液腺癌;(3)初始轉移部位僅限肝或/和肺;(4)腹腔鏡下原發灶根治性切除術(D3淋巴結清掃術)。排除標準:(1)美國東部腫瘤協作組評分>2分;(2)異時性mCRC;(3)存在骨、腦、腹膜等轉移瘤;(4)伴有其他腫瘤病史;(5)開腹原發灶切除術;(6)腹腔鏡下原發灶姑息性切除術(D1~D2);(7)隨訪資料不全。
1.2 臨床資料 入組的15例mCRC患者均行腹腔鏡下原發灶根治性切除術,男6例,女9例, 43~73歲,平均(59.60±9.42)歲,其中左半結腸6例,右半結腸9例;基因情況:鼠類肉瘤病毒癌基因突變6例,鼠類肉瘤病毒癌基因同源物B1未見突變,微衛星狀態均為微衛星穩定型;轉移灶局限肝臟11例,局限肺臟2例,肝肺同時轉移2例;肝或肺轉移數量1~5枚8例,5枚以上7例;5例為初始可切除mCRC,其臨床危險評分為3~5分,其中2例初始可切除mCRC患者行新輔助治療后行原發灶切除及同期或二期轉移灶超聲引導下射頻消融術或切除術,達到無疾病狀態,另3例初始可切除患者因原發灶梗阻行原發灶根治性切除術;10例為初始不可切除mCRC(臨床危險評分為3~5分),其中8例先行轉化處理,轉為可切除狀態4例,病情明顯緩解并穩定后行原發灶切除術4例,另2例初始不可切除的患者因腸梗阻先行原發灶根治性切除術,后行轉化處理;入組原發灶切除術均行D3淋巴結清掃術。
1.3 手術方法 根據腫瘤部位分別行全麻下腹腔鏡右半結腸癌、腹腔鏡乙狀結腸癌、腹腔鏡下直腸癌根治性切除術等。(1)腹腔鏡右半結腸癌根治性手術(尾側入路):患者取頭低足高并左傾位,以回盲部為標志,尋找小腸系膜根部在右髂窩附著處,仔細辨認右輸尿管后,由此切開進入右Toldt間隙(圖1A),拓展間隙外側至升結腸、結腸肝曲后方,內側至腸系膜上靜脈右側,向上展開至十二指腸降段、胰頭及胰腺鉤突前方(圖1B)。展開并暴露右半結腸系膜腹側,以腸系膜上靜脈為標志,先行辨認斜行隆起的回結腸血管蒂,結腸系膜于其下方(圖1C),并與前面解剖的右Toldt間隙貫通;自腸系膜上靜脈前縱行切開結腸系膜,解剖腸系膜上靜脈,依次分離回結腸血管、右結腸動脈(圖1D,部分患者出現)、結腸中血管,并于根部結扎離斷,沿腸系膜上靜脈暴露胃結腸干并離斷右結腸靜脈。打開胃結腸韌帶進入小網膜囊(圖1E),找到胃系膜與結腸系膜之間融合間隙并分離(圖1F),向下翻轉橫結腸,拓展橫結腸右后間隙,并與前面解剖的右Toldt間隙相通。取上腹部正中長約5 cm切口,將標本完整游離后放置體外,再行回腸、橫結腸的端側吻合,斷端及吻合口加固縫合。(2)肝多發轉移瘤初始不可切除轉化為可切除:取右上腹倒L形切口,自劍突下至右腋前線,長約20 cm,兩側肝臟拉鉤輔助顯露肝臟,依次離斷肝圓韌帶,游離鐮狀韌帶、冠狀韌帶,離斷左右三角韌帶及肝腎韌帶,徹底將肝臟游離,直視下處理病灶,肝轉移瘤用超聲刀配合電刀切除,切緣距腫瘤邊緣約1 cm(圖2A~圖2D);位置較深、預計切除困難或切除損傷肝體積較多時,配合術中超聲引導下行肝轉移瘤射頻消融術。(3)以肺多發轉移瘤經轉化處理后,大部分腫瘤消失,殘余病灶進行射頻消融術(圖2E、圖2F):患者靜脈麻醉后CT定位,常規消毒鋪巾,利多卡因逐層浸潤麻醉,射頻消融針于定位處垂直進針,CT下掃描見射頻消融針穿入轉移瘤,50 W功率射頻消融5 min,邊緩慢退針邊低功率消融針道,CT掃描未見氣胸及胸腔積液,局部加壓包扎。

圖1 A:超聲刀剪開小腸系膜在右髂窩附著處(箭頭示右側輸尿管);B:拓展至十二指腸及胰腺前方間隙(粗箭頭示十二指腸降段,細箭頭示胰腺);C:打開回結腸下方系膜(箭頭示回結腸血管);D:沿腸系膜上靜脈方向解剖出右結腸動脈(粗箭頭示腸系膜上靜脈,細箭頭示右結腸動脈);E:打開胃結腸韌帶進入小網膜囊;F:分離胃系膜與結腸系膜之間融合間隙(粗箭頭示胃系膜,細箭頭示橫結腸系膜)

圖2 A:肝轉移瘤基線狀態;B:肝轉移瘤經過轉化處理后,肝轉移瘤較前縮小;C:肝轉移瘤經轉化后,達到可切除狀態;D:肝轉移瘤切除術后狀態;E:肺轉移瘤基線狀態;F:肺轉移瘤經轉化后較前明顯縮小
1.4 觀察指標 (1)手術時間、術中出血量、清掃淋巴結數量、術后開始飲水時間、手術至化療開始時間、術后住院時間;(2)術后并發癥情況,主要包括吻合口漏、吻合口出血及吻合口狹窄;(3)OS:指由疾病診斷至死亡或隨訪截至時間,生存時間按月計算,隨訪截至2021年11月15日。
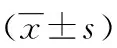
2 結 果
手術時間155~590 min(部分患者手術時間較長,因同期行肝轉移瘤切除術或射頻消融術),平均(311.67±131.04)min;術中出血量50~200 mL,平均(126.67±53.00)mL;清掃淋巴結4~46枚,平均(17.80±11.95)枚;術后首次飲水時間1~5 d,平均(2.40±1.12)d;術后住院6~33 d,平均(14.33±8.64)d;手術至全身化療開始時間14~47 d,平均(24.14±8.26)d,其中1例患者行術前完全新輔助治療。術后1例右半結腸癌術后吻合口水腫導致吻合口輕度狹窄,出現不完全性腸梗阻,經過保守治療后好轉。截至隨訪日期,3例患者死亡,OS 7~70個月,平均(18.73±17.30)個月。
3 討 論
2021年中國臨床腫瘤學會指南將mCRC分為初始可切除mCRC及初始不可切除mCRC,目前關于mCRC已達成以下共識:(1)對于初始可切除mCRC,作為R0切除的一部分,臨床危險評分0~2分時,可同期或分期切除原發灶、轉移灶;臨床危險評分3~5分時,建議先行新輔助治療,本研究中2例臨床危險評分>3分,經治療后達到無疾病狀態。(2)對于初始不可切除mCRC,目前國內外指南一般將原發灶切除術推薦應用于原發灶伴嚴重出血、穿孔、梗阻等腫瘤相關并發癥時[2]。本研究中共5例mCRC患者因腸梗阻先行腹腔鏡下原發灶切除術,因為此類并發癥往往會導致全身治療的延遲[6]。
原發灶無癥狀或輕微癥狀的初始不可切除同時性結直腸癌肝轉移不應行原發灶切除術,爭議在于此類患者行原發灶切除術能改善OS[7-8]。關于初始不可切除的mCRC前瞻性研究,日本進行的JCOG1007(iPACS)隨機對照研究發現,原發灶切除術后行化療與單純化療相比并無生存獲益(25.9個月 vs. 26.7個月,P=0.69),不建議對于原發灶無癥狀的初始不可切除的mCRC行原發灶切除術[9]。但iPACS研究中患者未經過規范的全身治療篩查,未將腫瘤快速進展的生物學行為較差的群體篩選出來,未能認識到對系統治療反應是目前篩查腫瘤生物學行為的最佳手段。
我中心認為,對于此類患者需經標準的全身強烈的轉化方案后肝轉移灶緩解并處于穩定狀態,病灶能達到明顯的部分緩解(3~4個月),并維持在穩定狀態一段時間(2~3個月)[10];患者體力狀況好,美國東部腫瘤協作組評分0~1分;原發灶切除術采用腹腔鏡方式,與開腹手術相比,可減少術后3級以上并發癥(如吻合口漏、腸梗阻、切口感染、肺部感染、腹腔感染等),保障系統治療的開始[11]。我們通過腹腔鏡行原發灶切除術,術后僅1例因吻合口水腫導致不全腸梗阻,經保守治療后好轉。此外,除1例術前完全新輔助治療患者外,余14例術后開始化療時間為(24.14±8.26)d,均能保障早期開始術后全身治療。本研究中4例初始不可切除的mCRC患者,經轉化處理后,轉移灶明顯緩解并穩定,行原發灶切除術,術后轉入維持治療階段。此外,還應考慮到晚期腫瘤對患者心理狀態的影響[12],對于mCRC患者,適當時機切除原發灶可增加患者治療腫瘤的信心,術后患者依從性明顯提高。
多項研究發現,不論原發灶是否伴有腫瘤相關癥狀,對于mCRC,腹腔鏡下姑息性原發灶切除術較開腹手術均具有優勢[13-14]。當轉移灶處于不可切除狀態下,傳統認為即使原發灶可行根治手術,但仍無法使患者全身達到無疾病狀態,因此對于不可切除的mCRC行原發灶切除術時,往往行姑息性原發灶切除術[15]。但Ishihara等[16]通過探討為1 982例不可切除的mCRC患者行原發灶切除術與淋巴結清掃術對預后的影響,發現行原發灶切除術的患者中,行D3 淋巴結清掃術的患者中位OS明顯好于非D3 淋巴結清掃術的患者(17.2個月vs.13.7個月,P<0.0001)。我們為15例原發灶行根治性切除術,截至隨訪日期,OS為(18.73±17.30)個月,優于上述的17.2個月。此外,Furuhata等[17]發現,即使為不可切除mCRC的患者行姑息性原發灶切除術,接受高位淋巴結清掃術較低位淋巴結清掃術也能顯示出更好的中位OS(13.0個月vs. 11.5個月,P=0.041)。因此,為不可切除mCRC行原發灶切除術時,盡可能切除更多的區域淋巴結,可能改善患者長期OS。此外,通過對原發灶與轉移灶的根治性切除,可使有區域淋巴結轉移的mCRC患者與無區域淋巴結轉移的患者5年OS達到相同的生存結果(24.3% vs. 19.5%;P=0.890)[18]。
我們建議,對于同時性mCRC的原發灶應做到分層處理,以最大程度地提高患者OS、改善生活質量。(1)伴有原發灶腫瘤相關并發癥時,可先行切除原發灶,以便后續全身治療的開展;(2)對于初始可切除的患者,作為R0切除的一部分,可同期或分期切除原發灶;(3)對于原發灶無腫瘤相關癥狀的初始不可切除者,建議先行全身治療篩查后,轉化成功時,再按照初始可切除狀態處理;如轉化后轉移灶明顯緩解并穩定,即貫徹基于全身治療反應的局部治療策略,可行原發灶切除術;如強烈的全身轉化方案后腫瘤仍快速進展,再對機體行有創傷的原發灶切除術,無益于提高OS、改善生活質量,建議此類患者進入多學科討論。文獻提示,對mCRC行D3淋巴結清掃優于D1~D2淋巴結清掃術,不論原發灶有無并發癥,腹腔鏡手術均優于開腹手術;因此我們建議,在快速康復理念指導下行腹腔鏡原發灶根治性切除術,盡可能做到D3淋巴結清掃,術后吻合口并發癥少,可早期開始全身治療,并且經過原發灶切除后患者對未來治療充滿自信,依從性提高。當然,本研究尚存在入組例數較少、無同期隨機對照、未能充分展開說明全身治療在治療過程中的價值、部分患者術后隨訪時間較短等不足,期待更多大規模臨床隨機對照研究進一步證實。

