急性心肌梗死并發急性腎損害的危險因素分析
張云輝,鄧仙炳,陳校春(陽江市中醫醫院急診科,廣東陽江 529500)
急性心肌梗死(AMI)屬臨床常見病癥,發病率逐年上升[1-2]。AMI 常常并發急性腎損傷(AKI),嚴重影響患者生活質量[3-4]。以往研究認為AMI 會影響心功能,增加泵衰竭的發生幾率,引發AKI[5-6]。機體血管緊張素II 的釋放量增加,引起血管收縮,將加重腎臟損傷[7-8]。研究表明,高齡、肺水腫或心源性休克者AKI 的發生風險高[9-10]。本研究分析前壁/前側壁梗死與AKI之間的關系,探討AMI-AKI 的危險因素。
1 資料和方法
1.1 一般資料
選取2018 年1 月至2021 年3 月在我院治療的AMI 患者195 例,其中男118 例,女77 例;年齡54~85歲,平均年齡(65.8±9.2)歲。納入標準:(1)AMI 診斷符合2018 年急性心肌梗死全球統一定義中的標準[11];(2)發病至入院時間不超過24 h;(3)入組前未行經皮冠狀動脈介入治療(PCI)治療;(4)患者及家屬知情同意。排除標準:(1)有心臟、腎臟移植史者;(2)終末期腎臟疾病或已行血液透析治療者;(3)合并有惡性腫瘤、血液系統疾病、自身免疫系統疾病等其他嚴重疾病。本研究符合《世界醫學協會赫爾辛基宣言》相關要求。
1.2 方法
195 例AMI 患者根據是否并發AKI(根據2012 年KIDGO 指南診斷標準)分為AKI 組和非AKI 組。收集及分析兩組患者的年齡,入院后血壓、血脂及鉀(K)、鈉(Na)、鈣(Ca)、磷(P)、鎂(Mg)水平;發病至入院時間;Killip 分級;肌酸激酶(CK)、肌酸激酶MB 同工酶CK-MB)、谷丙轉氨酶(ALT)、谷草轉氨酶(AST)水平;左室射血分數(LVEF)值。根據12 導聯心電圖檢查,ST 段抬高特征判斷梗死部位,若是抬高段為V1~V5或V3~V5,為前壁梗死;若是抬高段為V1~V3,為前間壁梗死;若是抬高段為V5~V7,為前側壁梗死;若是抬高段為Ⅱ、Ⅲ與aVF,為下壁梗死,統計前壁/前間壁梗死比例。收集入院24 h 內行超聲心動圖檢查資料,取心尖四腔切面以改良的Simpson 法計算LVEF 值[12]。利用logistic 回歸模型分析上述因素與AMI 患者并發AKI 的相關性。
1.3 統計學處理
采用SPSS 22.0 軟件,選用t檢驗、χ2檢驗及logistic回歸分析數據,檢驗水準:α=0.05。
2 結果
2.1 臨床資料
195 例AMI 患者并發27 例AKI,AKI 發生率為13.9%。AKI 組患者年齡明顯高于非AKI 組患者(P<0.05);AKI 組患者發病至入院時間≥6 h 比例明顯高于非AKI 組(P<0.05),表1、2。

表1 兩組臨床資料比較 例(%)

表2 兩組患者的年齡、體質量指數及血壓的比較
2.2 心臟參數指標
AKI 組LVEF 明顯低于非AKI 組(P<0.05),而KilliP 分級≥3 級、前壁/前間壁梗死比例明顯高于非AKI 組(P<0.05),見表3。

表3 兩組患者心臟參數指標比較
2.3 實驗室指標
AKI 組患者CK、CK-MB 明顯高于非AKI 組患者(P<0.05),見表4。
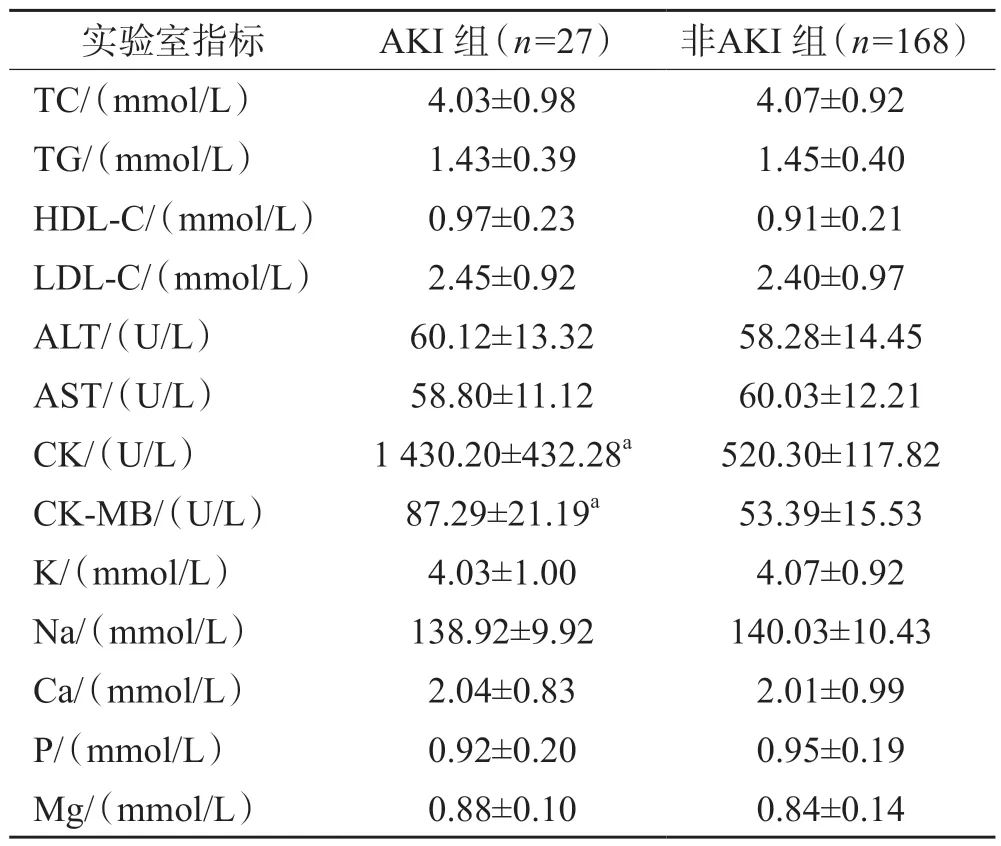
表4 兩組患者實驗室指標比較
2.4 多因素分析
將上述有統計學意義指標作為自變量,是否并發AKI 作為因變量進行logistic 回歸分析,結果顯示:年齡、發病至入院時間≥6 h、Killip 分級≥3 級、前壁/前側壁梗死及CK-MB 是AMI 患者并發AKI 的危險因素(OR=1.657、1.619、2.059、1.397 和1.359,P<0.05),見表5。
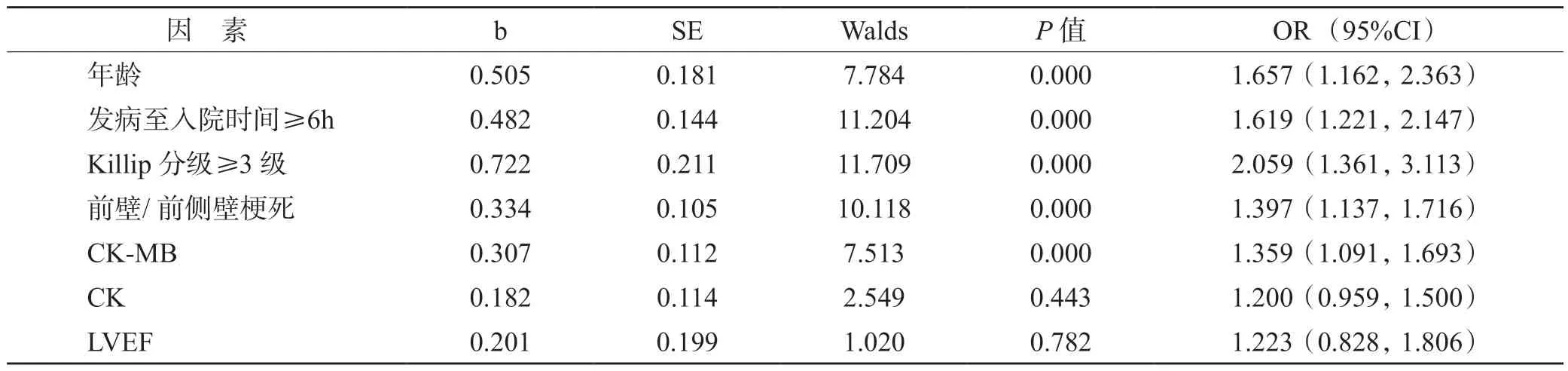
表5 多因素分析
3 討論
AMI 患者常并發AKI,此類患者的預后差,病死率也高[13]。以往研究發現,AMI 后發生AKI 的危險因素有入院時間長、基礎腎功能差、入院時Killip 分級≥3級、有高血壓病史等等,尚沒有綜合分析年齡、Killip分級、前壁/前側壁梗死等多種因素與AKI 發生風險的關系[14]。有研究顯示并發AKI 患者的年齡明顯比單純性 AMI 患者大[15]。年齡增長,患者機體的免疫功能降低,易發動脈粥樣硬化,高齡患者的腎功能降低,腎灌注量易受到影響。本研究結果顯示:發病至入院時間越長,AKI 發生風險越大。因此,加強對患者的健康教育,使其掌握一定的院前急救醫療知識對于改善AMI本身的轉歸,減少AKI 的發生率有重要意義。
本研究結果顯示:AKI 組LVEF 明顯低于非AKI組(P<0.05)。LVEF 降低引起心搏出量降低,中心靜脈壓及腹內壓增高,腎臟有效血流量降低,易誘發AKI。AMI 發生過程中形成的血栓可對冠狀動脈血流造成影響,可使心肌缺血,繼而影響心臟收縮功能,這種缺血還可增加左心室壓力,造成短暫高血壓,反映到腎臟上,誘發腎臟小動脈收縮并發生硬化,造成管腔狹窄,引起腎缺血,造成腎損傷。此外,AMI 患者還常出現動脈粥樣硬化,腎動脈粥樣硬化發生后,造成腎臟管腔狹窄,引起腎嚴重缺血,容易發生AKI[16]。AKI 患者早期癥狀不明顯,若不及時發現并干預,將會延誤病情,錯失最佳治療時機[17]。客觀評價AMI 患者左心室功能變化,對診斷及判斷患者預后具有重要意義。
有文獻顯示,入院時Killip 分級≥3 級的患者發生AKI 的風險是其他患者的數倍[18]。本研究亦得出類似結果,且分析了CK、CK-MB 水平及前壁/前間壁梗死比例對于患者預后的影響,發現前壁/ 前間壁梗死比例明顯高于非AKI 組,AKI 組患者CK、CK-MB 水平明顯高于非AKI 組患者。AKI 組的前壁/前間壁梗死比例高于非AKI 組,可能與廣泛前壁心肌梗死患者的血流動力學常不穩定,易出現心源性休克及心力衰竭相關,導致腎灌注不足、腎缺血而誘發AKI。還有大量證據表明[19],中性粒細胞釋放的特定有毒產物可對腎臟造成損害。本研究發現AKI 組CK 和CK-MB 水平顯著高于非AKI 組。CK 和CK-MB 水平升高加重AMI患者的炎癥反應,加速AMI 后心肌損傷和心肌細胞凋亡,引起腎組織損傷并誘發AKI。前壁的心律失常多于后壁,病死率也相應增加。前壁AMI 側支循環較多,后壁常常被其累及,誘發Benzol-Jarisch 反射,迷走神經反射程度加大,常造成房室結動脈供血障礙,導致心律失常及房室傳導阻滯,誘發心力衰竭[20]。不僅LVEF低,而且每搏輸出量也可能會相應減少,可導致腎灌注不足,并引起中心靜脈壓和腹內壓升高,使腎臟的有效血流量減少,誘發AKI。
而本研究發現,血脂、血壓指標及ALT、AST、K、Na、Ca、P、Mg 等不是AMI 患者發生AKI 的危險因素。AKI 的發生機制中有炎癥反應和氧化應激反應的參與,研究發現AKI 患者血漿細胞因子和氧化應激標志物水平升高[21]。AMI 引起的疼痛、焦慮和左心室功能損害,可激活交感神經系統,使去甲腎上腺素的釋放量增加,并與間充質干細胞表達的β3 腎上腺素能受體結合以調節相關生物學途徑,引起外周血中性粒細胞和單核細胞分泌增加,同時使大量白細胞聚集滲入腎臟,引起腎臟炎癥改變。
logistic 回歸分析顯示:年齡、發病至入院時間≥6 h、Killip 分級≥3 級、前壁/ 前側壁梗死及CK-MB 是AMI 患者并發AKI 的危險因素。今后應將重視此評價體系的應用,對患者進行積極的干預和治療,降低AKI的發生率。本研究還存在一些不足。首先,本研究中的病例來自同一家醫院,且是回顧性驗證;其次,本研究僅考慮患者的院內結局,未進行隨訪,對遠期預后尚缺乏研究,需在今后的進一步研究中予以補充。

