預(yù)氧化工藝對含溴飲用水消毒副產(chǎn)物生成的影響
嚴好婷,俞昊天,陳玉敏,留嘉婧,葉東東,毛玉琴
(浙江樹人學(xué)院生物與環(huán)境工程學(xué)院,浙江杭州 310015)
目前,飲用水水源中存在的有機污染問題仍然比較突出,常規(guī)的飲用水處理工藝對可溶性有機物(DOM)的去除能力有限[1],越來越多的水廠在傳統(tǒng)工藝前增設(shè)預(yù)氧化工藝以加強對DOM的去除[2]。預(yù)氯化是國內(nèi)外水廠最早且應(yīng)用最廣泛的預(yù)氧化工藝,但是預(yù)氯化后會產(chǎn)生致畸、致癌的消毒副產(chǎn)物(DBPs)[3],因此,臭氧、二氧化氯、高錳酸鉀等預(yù)氧化工藝逐漸被水廠用于替代預(yù)氯化工藝。單獨使用這些預(yù)氧化工藝不會生成DBPs,但是有可能會引進一些其他的問題,如二氧化氯預(yù)氧化后生成亞氯酸鹽和氯酸鹽[4],同樣威脅健康。另外,臭氧和二氧化氯還能夠氧化有機物的雙鍵和芳香結(jié)構(gòu),改變有機物性質(zhì)[5],進而影響后續(xù)氯消毒過程中DBPs的生成。肖融等[6]研究表明,臭氧能夠?qū)⑺械牟糠钟袡C物氧化成含類甲基酮等結(jié)構(gòu)的化合物,這是形成三鹵甲烷(THMs)的一種主要前體物,使得后續(xù)氯消毒過程中THMs生成量顯著增加。但也有研究表明,臭氧預(yù)氧化可以有效消除DBPs的主要前體物,減少后續(xù)氯消毒工藝中的氯耗,從而減少鹵乙酸(HAAs)、THMs和二鹵乙腈(DHANs)等DBPs的生成[7]。水源水中有機物特性以及氧化劑類型的不同可能會對DBPs的形成產(chǎn)生很大的影響,但目前關(guān)于不同預(yù)氧化工藝對后續(xù)氯消毒過程中DBPs生成影響的定量對比研究還比較缺乏。
此外,溴離子普遍存在于自然界水體中,長江下游和微山湖的溴離子質(zhì)量濃度一般在200~400 μg/L,黃河下游的溴離子質(zhì)量濃度一般在100~150 μg/L[8-9]。溴離子的大量出現(xiàn)會導(dǎo)致預(yù)氧化工藝對DBPs生成特性的影響更加復(fù)雜。以臭氧預(yù)氧化為例:一方面,臭氧預(yù)氧化工藝可以通過降解水中有機質(zhì)除去部分DBPs前體物[10];另一方面,臭氧的強氧化特性也可能會使水中溴離子形成溴酸鹽,并且促使由其所形成的DBPs進一步向溴代DBPs轉(zhuǎn)變[11-12]。相比于同結(jié)構(gòu)的氯代DBPs,溴代DBPs具有更高的細胞毒性和基因毒性[13],然而目前關(guān)于預(yù)氧化工藝對含溴水體DBPs生成特性的研究還相當(dāng)少。因此,本研究以預(yù)氧化工藝中的臭氧和二氧化氯預(yù)氧化為代表,通過定量研究對比了這兩類預(yù)氧化工藝對含溴水體中DBPs生成和分配的影響,并將預(yù)氧化工藝、溴離子與DBPs聯(lián)系在一起,以期為更好地保障飲用水安全提供依據(jù)和對策。
1 試驗材料和方法
1.1 水樣配制
1.2 試驗方法與儀器
臭氧預(yù)氧化試驗采用臭氧發(fā)生器(新大陸,NLO-20)通過高壓放電法每天即時制備飽和臭氧水,試驗裝置和制備過程參照Yang等[9]的文獻。二氧化氯儲備液的制備參照《生活飲用水標準檢驗方法 消毒劑指標》(GB/T 5750.11—2006),利用亞氯酸鈉和稀硫酸反應(yīng)制得。臭氧和二氧化氯采用等當(dāng)量濃度投加的方式,具體投加量如表1所示,反應(yīng)20 min后測定氧化劑余量,立即加入等化學(xué)反應(yīng)劑量的硫代硫酸鈉淬滅。取一定體積的水樣進行常規(guī)水質(zhì)指標的測定,剩余水樣進行加氯培養(yǎng)測定THMs、HAAs、DHANs等DBPs的生成勢。加氯培養(yǎng)條件為:pH值為8.0±0.2,恒溫培養(yǎng)箱溫度為(20±1) ℃,培養(yǎng)時間為24 h,氯投加量采用過量投加的方式,保證最大需氯量的水樣(一般為原水)培養(yǎng)24 h后的余氯質(zhì)量濃度大于1 mg/L。培養(yǎng)完成后立即測定各水樣的余氯含量,并隨即加入等化學(xué)反應(yīng)劑量的硫代硫酸鈉淬滅余氯,最后進行液液萃取測定DBPs。
臭氧濃度的檢測采用靛藍法測定臭氧在610 nm處的吸光度;二氧化氯濃度采用Hach二氧化氯測定儀(Pocket ColorimeterTMII)并利用DPD分光光度法進行測定,每次試驗前均需先對二氧化氯濃度進行測定后再使用;溴離子和溴酸鹽濃度利用瑞士萬通Metrohm 761型離子色譜儀測定;UV254的測定儀器為上海美普達UV-1800型分光光度計;DOC采用日本島津公司的TOC-VCPH型總有機碳分析儀進行測定;THMs和DHANs濃度利用EPA 551.1標準方法測定,儀器采用安捷倫公司的氣相色譜儀(Agilent 7890A,USA),配備電子捕獲(ECD)檢測器,使用DB-1毛細管柱(30 m×0.25 mm×0.25 μm);HAAs色譜分離采用DB-1701毛細管柱(30 m× 0.25 mm×0.25 μm),HAAs濃度的測定利用美國環(huán)保署(EPA)552.3 標準方法,儀器采用安捷倫公司的氣相色譜儀(Agilent 7890A,USA),其輔助儀器為電子捕獲(ECD)檢測器。

表1 實驗室自配水的氧化劑投加量和當(dāng)量濃度Tab.1 Oxidant Dosage and Normal Concentration of Experimental Raw Water
2 結(jié)果與討論
2.1 預(yù)氧化對常規(guī)水質(zhì)指標的影響
SUVA值是水樣的UV254與DOC的比值,通常被用于表征DBPs前體物和水中有機物所含腐植酸類物質(zhì)的量[10]。SUVA值與化合物中的芳香度和疏水性化合物數(shù)量呈正相關(guān)關(guān)系[14],即SUVA值越高,DBPs的生成潛能越大。如圖1所示,SUVA值隨著臭氧投加量的提高而出現(xiàn)了明顯的降低態(tài)勢,SUVA值為4.26~8.51 L/(mg·m),下降率約為49.9%。但二氧化氯投加量的增加對SUVA值的降低無顯著影響,SUVA值為8.18~8.69 L/(mg·m),下降率僅有5.9%。SUVA值在不同氧化劑當(dāng)量濃度條件下,臭氧對SUVA的去除效率遠高于二氧化氯。然而,臭氧和二氧化氯預(yù)氧化后DOC基本不變,說明對于腐植酸類物質(zhì),這兩種氧化工藝均不能將其徹底礦化生成CO2和H2O。水樣的DOC不變,SUVA值顯著下降,表明預(yù)氧化改變了腐植酸類物質(zhì)結(jié)構(gòu),將大分子疏水性的有機物轉(zhuǎn)變?yōu)樾》肿佑H水性有機物,這與之前文獻中的研究結(jié)果吻合[15]。
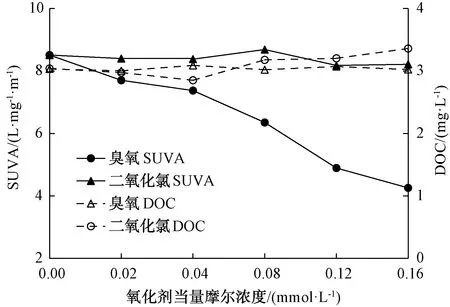
圖1 不同氧化劑當(dāng)量濃度下SUVA和DOC的變化Fig.1 Variation of SUVA and DOC under Different Oxidant Normal Concentrations
2.2 DBPs的生成和分布
在本研究所檢測的DBPs中,HAAs中的一氯乙酸(MCAA)、一溴乙酸(MBAA)和三溴乙酸(TBAA)濃度基本低于檢出限,因此不予考慮。如圖2所示,臭氧和二氧化氯對THMs、HAAs和DHANs總生成潛能的影響規(guī)律基本一致。THMs和HAAs總生成潛能隨著臭氧和二氧化氯投加量的增加呈現(xiàn)先增加后減少的趨勢[圖2(a)~圖2(d)]。這可能是由于臭氧和二氧化氯的強氧化作用使得一些難以和氯直接反應(yīng)的大分子物質(zhì)轉(zhuǎn)變?yōu)榭梢院吐确磻?yīng)的小分子物質(zhì),增加了DBPs的前體物[16]。然而,隨著臭氧和二氧化氯投加量的進一步提高,這些前體物可能繼續(xù)被臭氧和二氧化氯氧化分解,不能再充當(dāng)DBPs的前體物,從而導(dǎo)致THMs和HAAs總生成潛能的降低。DHANs中的CN官能團極易被氧化,隨著臭氧和二氧化氯投加量的增大,DHANs的生成量呈下降趨勢[圖2(e)~圖2(f)]。
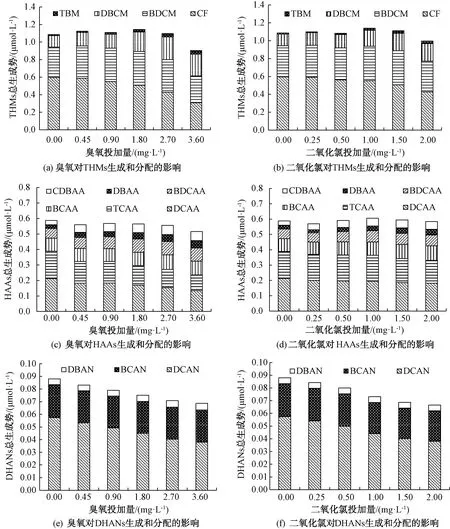
圖2 氧化劑投加量對DBPs生成和分布的影響Fig.2 Effect of Oxidant Dosage on DBPs Formation and Speciation
在THMs組分構(gòu)成中,三氯甲烷(CF)和一氯二溴甲烷(DBCM)始終為優(yōu)勢物質(zhì)。在臭氧和二氧化氯投加量逐漸增大的情況下,CF的生成量呈現(xiàn)顯著降低趨勢,一溴二氯甲烷(BDCM)降低趨勢則相對稍緩,而對DBCM的生成起促進作用,且三溴甲烷(TBM)生成量也逐漸升高,溴代THMs將逐漸代替氯代THMs成為優(yōu)勢物質(zhì)。DBCM在臭氧投加量由0.90 mg/L升至1.80 mg/L,其生成量的增長率為37.5%;DBCM在二氧化氯投加量從0.50 mg/L升至1.00 mg/L時,增長率約為20.0%。臭氧和二氧化氯對THMs的抑制作用為CF>BDCM>DBCM>TBM[圖2(a)~圖2(b)]。在HAAs組分構(gòu)成中,二氯乙酸(DCAA)和三氯乙酸(TCAA)始終占據(jù)優(yōu)勢地位,隨著臭氧和二氧化氯投加量的增大而逐漸減少,而溴氯乙酸(BCAA)、一溴二氯乙酸(BDCAA)、二溴乙酸(DBAA)和一氯二溴乙酸(CDBAA)生成量呈現(xiàn)增加趨勢[圖2(c)~圖2(d)],這說明在含溴水體中采用預(yù)氧化工藝會增加溴代HAAs生成的風(fēng)險,值得引起注意。
在不同臭氧和二氧化氯投加量下,3種DHANs的生成量均較相近,兩種含溴DHANs[溴氯乙腈(BCAN)和二溴乙腈(DBAN)]的生成量隨著臭氧和二氧化氯投加量的增大基本不變,其中二氯乙腈(DCAN)含量最高,隨著臭氧和二氧化氯投加量的增加,DCAN的生成量與單獨氯消毒相比存在較明顯的下降趨勢,故而DHANs總體生成量也逐漸下降。
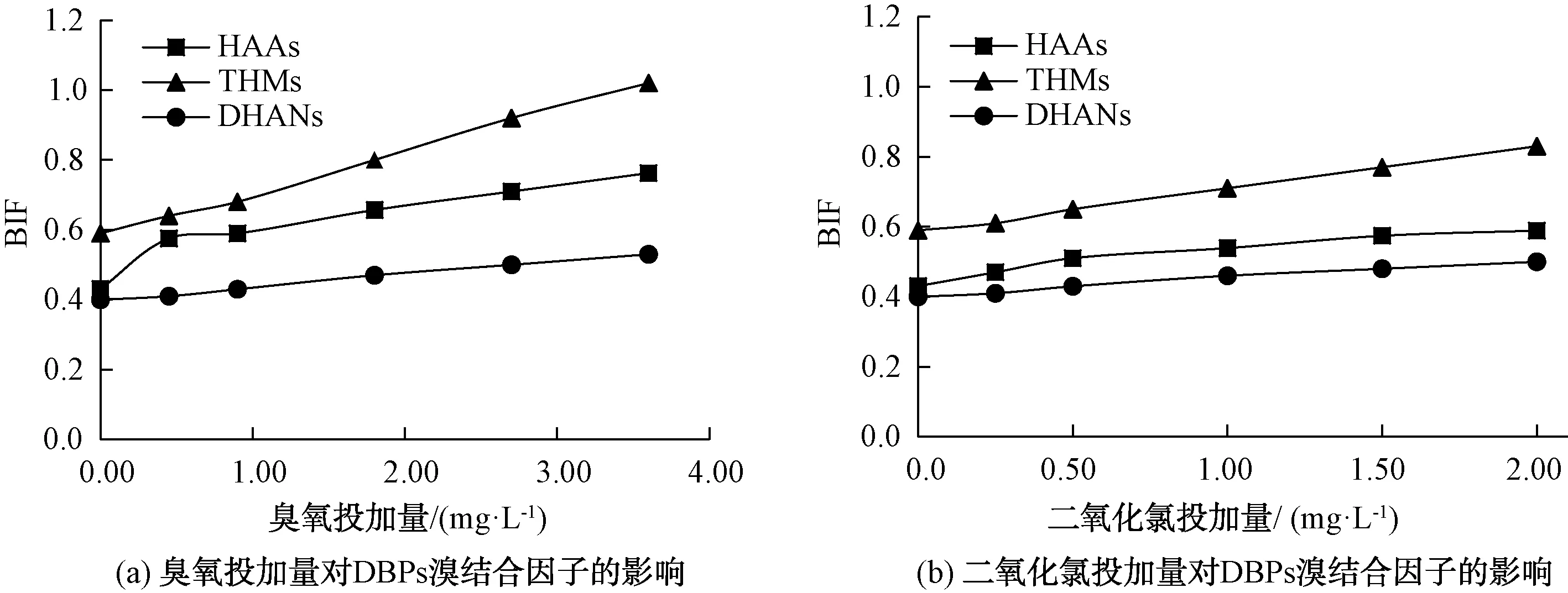
圖3 氧化劑投加量對DBPs溴結(jié)合因子的影響Fig.3 Effect of Oxidant Dosage on DBP Bromine Incorporation Factor
2.3 溴結(jié)合因子
為深入分析臭氧和二氧化氯預(yù)氧化對各類DBPs中溴代組分所占比例的變化狀況,引入溴結(jié)合因子(BIF)對DBPs中溴代組分所占比例進行評估,THMs、HAAs和DHANs的BIF計算如式(1)~式(3)[17]。BIF值越大,表明在DBPs中溴的結(jié)合程度越高,反映出溴代DBPs所占比例也越大[18]。如圖3所示,隨著臭氧和二氧化氯投加量的增大,THMs、HAAs和DHANs的BIF均呈現(xiàn)升高趨勢。當(dāng)臭氧投加量增至3.60 mg/L,THMs、HAAs和DHANs的BIF分別增長了0.43、0.33和0.13;而當(dāng)二氧化氯投加量增至2.00 mg/L,THMs、HAAs和DHANs的BIF分別增長了0.24、0.16和0.10。BIF的升高可能因為臭氧和二氧化氯將原水中芳香族類的疏水性基團逐漸被氧化成小分子親水性基團,而親水性基團更有利于溴的取代。HAAs和DHANs的BIF始終小于THMs的BIF,HAAs、DHANs與THMs相比各組分分配比例受臭氧和二氧化氯投加量影響更小,且THMs、HAAs和DHANs的BIF對于臭氧投加量的變化更敏感。
(1)
(2)
(3)
其中:[BDCM]——一溴二氯甲烷的摩爾濃度,μmol/L;
[DBCM]——一氯二溴甲烷的摩爾濃度,μmol/L;
[TBM]——三溴甲烷的摩爾濃度,μmol/L;
[CF]——三氯甲烷的摩爾濃度,μmol/L;
[BCAA]——溴氯乙酸的摩爾濃度,μmol/L;
[DBAA]——二溴乙酸的摩爾濃度,μmol/L;
[BDCAA]——一溴二氯乙酸的摩爾濃度,μmol/L;
[CDBAA]——一氯二溴乙酸的摩爾濃度,μmol/L;
[TBAA]——三溴乙酸的摩爾濃度,μmol/L;
[DCAA]——二氯乙酸的摩爾濃度,μmol/L;
[TCAA]——三氯乙酸的摩爾濃度,μmol/L;
[DCAN]——二氯乙腈的摩爾濃度,μmol/L;
[BCAN]——溴氯乙腈的摩爾濃度,μmol/L;
[DBAN]——二溴乙腈的摩爾濃度,μmol/L;
BIF(THMs)、BIF(HAAs)、BIF(DHANs)——THMs、HAAs、DHANs的溴結(jié)合因子。
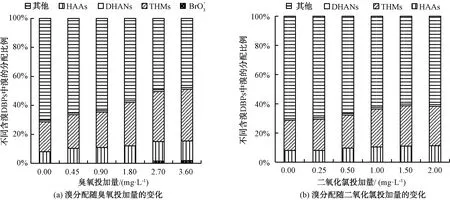
圖4 溴分配隨氧化劑投加量的變化Fig.4 Variation of Bromine Distribution with Different Oxidant Dosage
2.4 預(yù)氧化對溴分配的影響
3 結(jié)論
(1)臭氧和二氧化氯這兩種預(yù)氧化工藝處理含溴水體后對后續(xù)氯消毒過程中THMs、HAAs和DHANs總生成量的變化趨勢基本一致,HAAs和THMs總生成量均隨著臭氧和二氧化氯投加量的增大呈現(xiàn)先增加后減小趨勢,DHANs總生成量隨著氧化劑投加量的增加而減少。從DBPs總量控制的角度出發(fā),建議增大氧化劑的投加量,且高投量的臭氧對DBPs總量生成的抑制作用優(yōu)于二氧化氯預(yù)氧化。
(2)對臭氧和二氧化氯進行預(yù)氧化處理均會促進后續(xù)氯消毒過程中THMs、HAAs和DHANs中溴代組分所占的比例增大,即溴結(jié)合因子增大。氧化劑含量越高,溴結(jié)合因子越大。等當(dāng)量濃度下臭氧預(yù)氧化后,其溴結(jié)合因子增大幅度高于二氧化氯預(yù)氧化。
(3)在含溴水體臭氧-氯和二氧化氯-氯消毒過程中,溴代DBPs的分配比例呈現(xiàn)增加趨勢。在臭氧和二氧化氯投加量較低的情況下,氯能夠迅速將溴離子氧化,而溴的取代效率比氯高很多,導(dǎo)致溴代DBPs大量生成。

