CaCl2和NaHCO3對海水淡化水礦化處理效果的影響及最佳濃度分析
黃 靜,蔡姝崴,王付杉
(1.中國人民解放軍海軍勤務學院海防工程系,天津 300450;2.中國人民解放軍海軍勤務學院基礎部,天津 300450;3.自然資源部天津海水淡化與綜合利用研究所,天津 300192)
真空膜蒸餾技術因其具有運行壓力和工作溫度低、操作簡單安全、水質純凈度高等優點,在水處理領域,尤其是海水淡化方面具有廣泛的應用前景,引起越來越多的科研工作者的關注[1-3]。但是,該技術得到的淡化水缺乏人體所必需的礦物質,長期飲用可能增加患心血管疾病的風險[4]。同時水質呈弱酸性、緩沖能力差,直接進入供水管道后,可能腐蝕管道內的鐵銹或水垢,從而出現“紅水”或“黃水”現象[5]。因此,需要對淡化水進行礦化處理,即通過提高水的硬度、堿度以及調節pH來增加淡化水的緩沖能力,滿足居民的日常飲水需求。
海水淡化水的礦化工藝大致有3種:與其他水源摻混、溶解礦石法、直接投加藥劑法。與其他水源摻混是指淡化水與自來水、苦咸水等礦物質含量豐富的水按比例混合,增加水中礦物質含量和水質的化學穩定性。但摻混水源需要進行預處理,否則可能因含有有害物質而影響人體健康。溶解礦石法是指通過溶解富含CaCO3的礦石,讓礦石中的礦物質進入水中,從而增加水中礦物質離子含量。河北曹妃甸反滲透海水淡化工程即采用該方法對淡化水進行礦化處理[6]。直接投加藥劑法是指直接向海水淡化水中按比例用計量加藥裝置加入所需成分,如NaOH、NaHCO3、Na2CO3、CaO、CaCl2等。印尼Adipala電廠反滲透海水工程采用海水淡化水加藥的礦化技術,但水處理的價格高達0.43元/t,因此該方法大多適用于小型海水淡化系統[6]。典型的直接投加藥劑法的工藝有4種[7],如式(1)~式(4)。
2CO2+Ca(OH)2→Ca(HCO3)2
(1)
Ca(OH)2+Na2CO3→CaCO3+2NaOH
(2)
CaSO4+2NaHCO3→Ca(HCO3)2+Na2SO4
(3)
CaCl2+2NaHCO3→Ca(HCO3)2+2NaCl
(4)
目前,海水淡化水礦化處理的研究主要集中在溶解礦石法上,但這種淡化方法不適合在島礁中應用。因為島礁遠離大陸且面積較小,更適合小型化、移動式的裝置和設備。二氧化碳溶解礦石的設備體積較大;硫酸溶解礦石法由于硫酸的危險性,其運輸、儲存過程難度較大。與其他水源摻混又容易引入人體不需要的離子,這些離子不僅會給人體帶來傷害,而且可能加劇金屬管道的腐蝕,尤其在南方高溫、高濕、高鹽的環境下,設備的腐蝕是一個不可忽視的問題。相比之下,直接投加藥劑法是通過向反滲透海水淡化水中投加食品添加劑來改善水質,采用的食品添加劑有CaO、MgSO4等,這種方法的設備簡單,容易控制投加藥劑量,操作維護簡便,兼具高效性和便攜性,比較合適島礁用水的礦化后處理。但是,查閱資料發現,利用直接投加藥劑法對島礁海水淡化水進行礦化處理的研究很少。
針對上述問題,本試驗采用直接投加藥劑法,利用CaCl2+NaHCO3組合藥劑對淡化水進行礦化處理。研究CaCl2和NaHCO3的投加對水中總溶解性固體(TDS)、pH、Ca2+、氯化物(以Cl-計)、總硬度(TH)和總堿度(TA)的影響,以及達到標準水質要求且滿足水質安全性和健康性時CaCl2和NaHCO3的投加量。礦化水以《生活飲用水衛生標準》(GB 5749—2006)的要求為基本目標[8],其中,TDS質量濃度為200~500 mg/L;pH值在6.5~8.5;Ca2+質量濃度為20~36 mg/L;Cl-質量濃度為50~100 mg/L;Na+質量濃度為20~100 mg/L,最高限值為200 mg/L;TH質量濃度為100~200 mg/L;TA質量濃度>80 mg/L。但是,該標準主要是針對地下水和地表水的水源,而海水淡化水的水質與傳統的自來水有一定差異。也就是說,海水淡化水不僅要滿足《生活飲用水衛生標準》(GB 5749—2006)的基本要求,還要注重水質的健康安全性和衛生安全性,能夠長期滿足健康直飲水的要求。Martin[9]提出,飲用水的TDS理想值是300 mg/L。WHO給出飲用水中TDS的最佳值為250~500 mg/L。因此,本文在滿足基本標準要求的前提下,將TDS的最佳值定為300~500 mg/L。
1 材料與方法
1.1 試驗藥品
試驗以課題組前期真空膜蒸餾淡水為介質[10],所用CaCl2購于天津市科密歐化學試劑有限公司,NaHCO3購于天津市化學試劑批發公司,均為分析純。
1.2 試驗方法及流程
取膜蒸餾產水2 500 mL,分別裝入5個500 mL的塑料瓶中,然后按照64.1、76.2、84.0、98.1、104.0 mg/L的質量濃度加入CaCl2,充分溶解(以Cl-計)并搖勻。然后分別進行電導率、TDS、pH、氯化物(以Cl-計)、Ca2+、TH(以CaCO3計)、TA(以CaCO3計)測試。
取膜蒸餾產水2 500 mL,分別裝入5個500 mL的塑料瓶中,先加入CaCl2(~100 mg/L),然后按照40.2、83.0、138.8、212.0、262.1 mg/L的質量濃度加入NaHCO3,充分溶解并搖勻。然后分別進行電導率、TDS、pH、氯化物(以Cl-計)、Ca2+、TH(以CaCO3計)、TA(以CaCO3計)測試。
1.3 分析儀器及方法
TDS和電導率采用哈希電導率進行手動測量;Na+按照加入NaHCO3的量計算得到;pH、氯化物(以Cl-計)、Ca2+、TH(以CaCO3計)、TA(以CaCO3計)這5項的結果由自然資源部天津海水淡化與綜合利用研究所的檢測中心進行測量。
這5項采用的檢測標準如下[11-13]。pH、氯化物(以Cl-計)、TH(以CaCO3計)采用《生活飲用水標準檢驗方法 感官性狀和物理指標》(GB/T 5750.4—2006)測定;Ca2+采用《工業循環冷卻水中鈣、鎂離子的測定 EDTA滴定法》(GB/T 15452—2009)測定;TA(以CaCO3計)采用《工業循環冷卻水總堿及酚酞堿度的測定》(GB/T 15451—2006)測定。
2 結果和討論
2.1 CaCl2的投加量對礦化效果的影響
向膜蒸餾產水中投加CaCl2,5個水樣的檢測結果如表1所示。膜蒸餾產水中投加不同量的CaCl2時,TDS變化趨勢如圖1所示。TDS整體上隨CaCl2投加量的增加而增加,這是因為CaCl2易溶于水,增加了水中TDS的含量,同樣地,溶液的電導率整體也呈上升趨勢。當CaCl2的投加量從64.1 mg/L增至104.0 mg/L時,水的TDS從最初的(117.80±0.16) mg/L逐漸提高到(182.90±0.08) mg/L,但卻始終低于最小目標值(300 mg/L)。
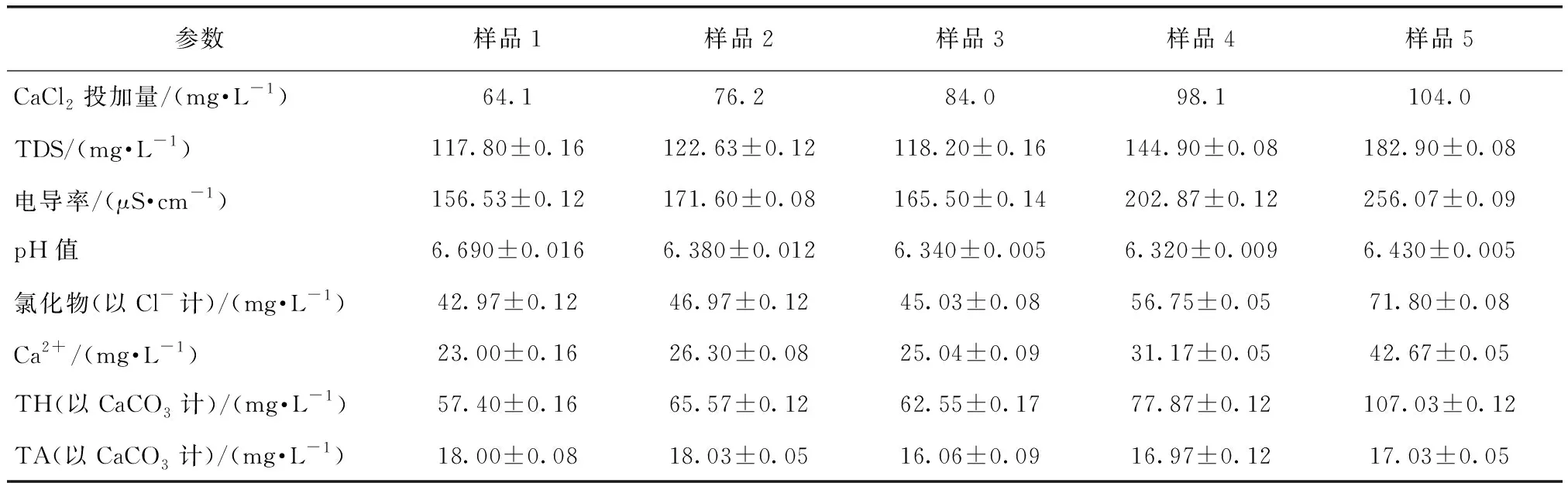
表1 CaCl2的投加量對礦化效果的影響參數Tab.1 Effect Parameters of CaCl2 Dosage on Mineralization
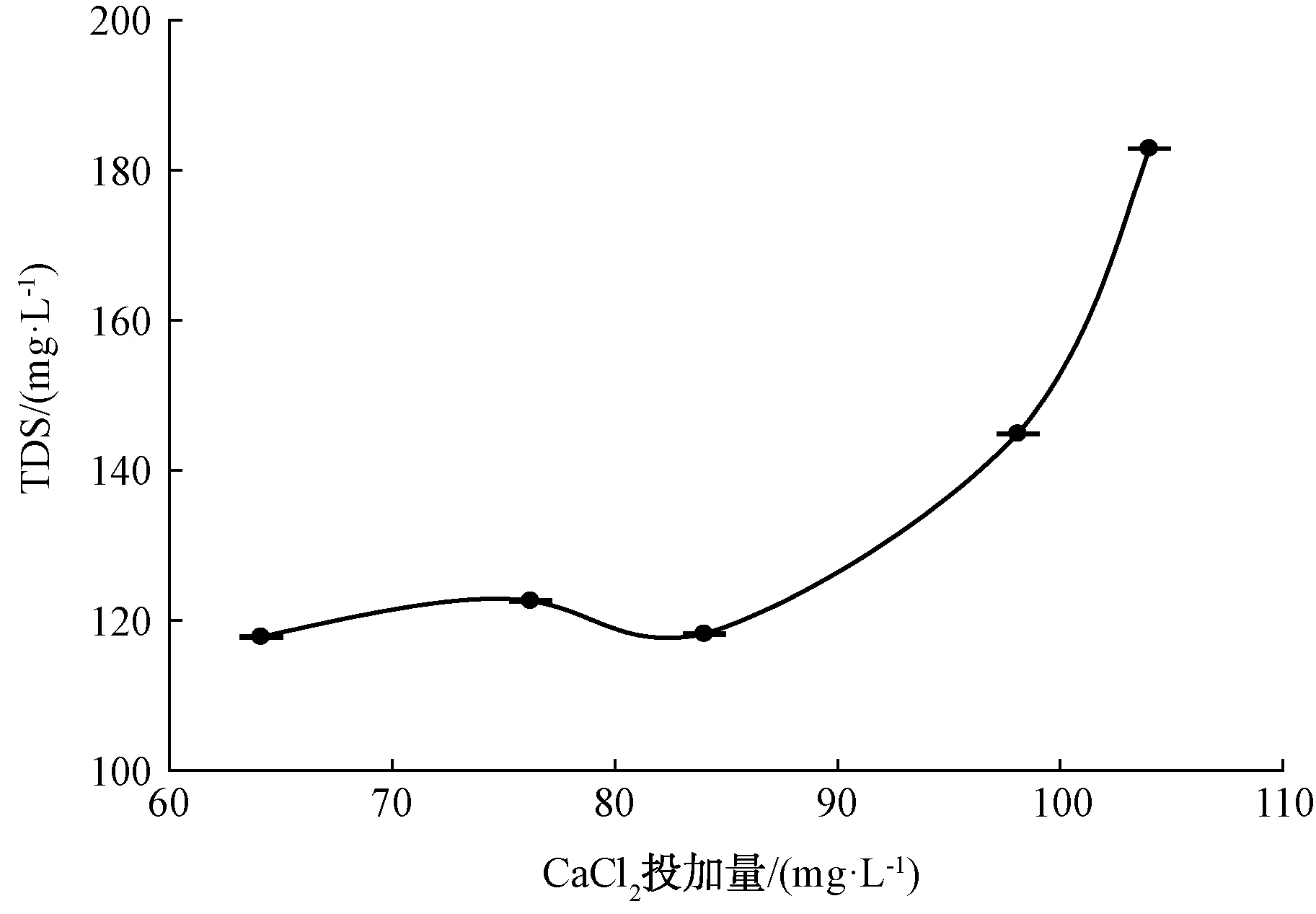
圖1 CaCl2投加量對TDS的影響Fig.1 Influence of CaCl2 Dosage on TDS
膜蒸餾產水中投加不同量的CaCl2時,pH變化趨勢如圖2所示,CaCl2的投加對淡化水pH的影響不大。隨著CaCl2投加量從64.1 mg/L增至98.1 mg/L,淡化水的pH值在(6.690±0.016)~(6.320±0.009)。當CaCl2投加量在64.1~70.9 mg/L時,pH值在6.50~(6.69±0.016),符合飲用水水質要求。
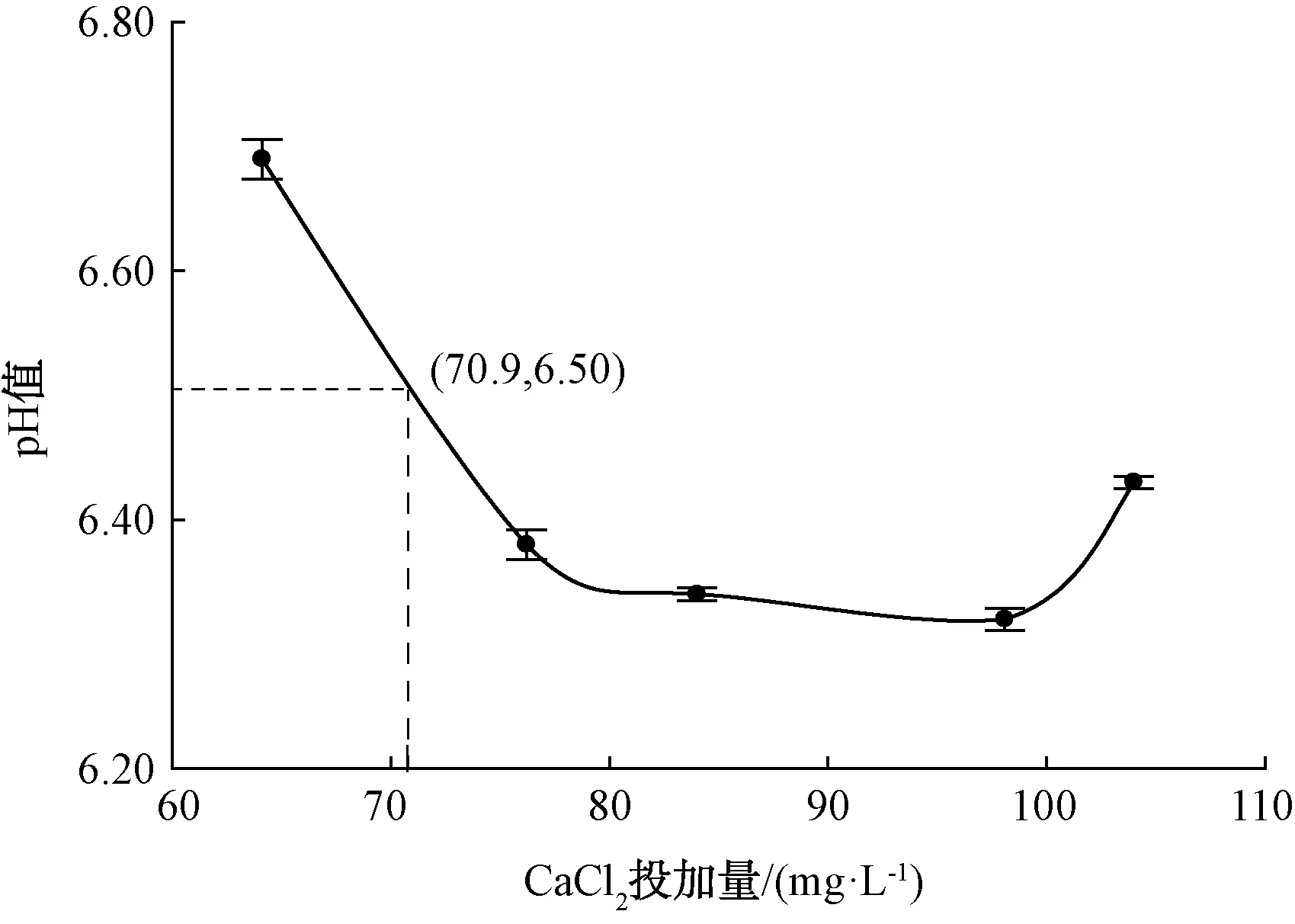
圖2 CaCl2投加量對pH的影響Fig.2 Influence of CaCl2 Dosage on pH
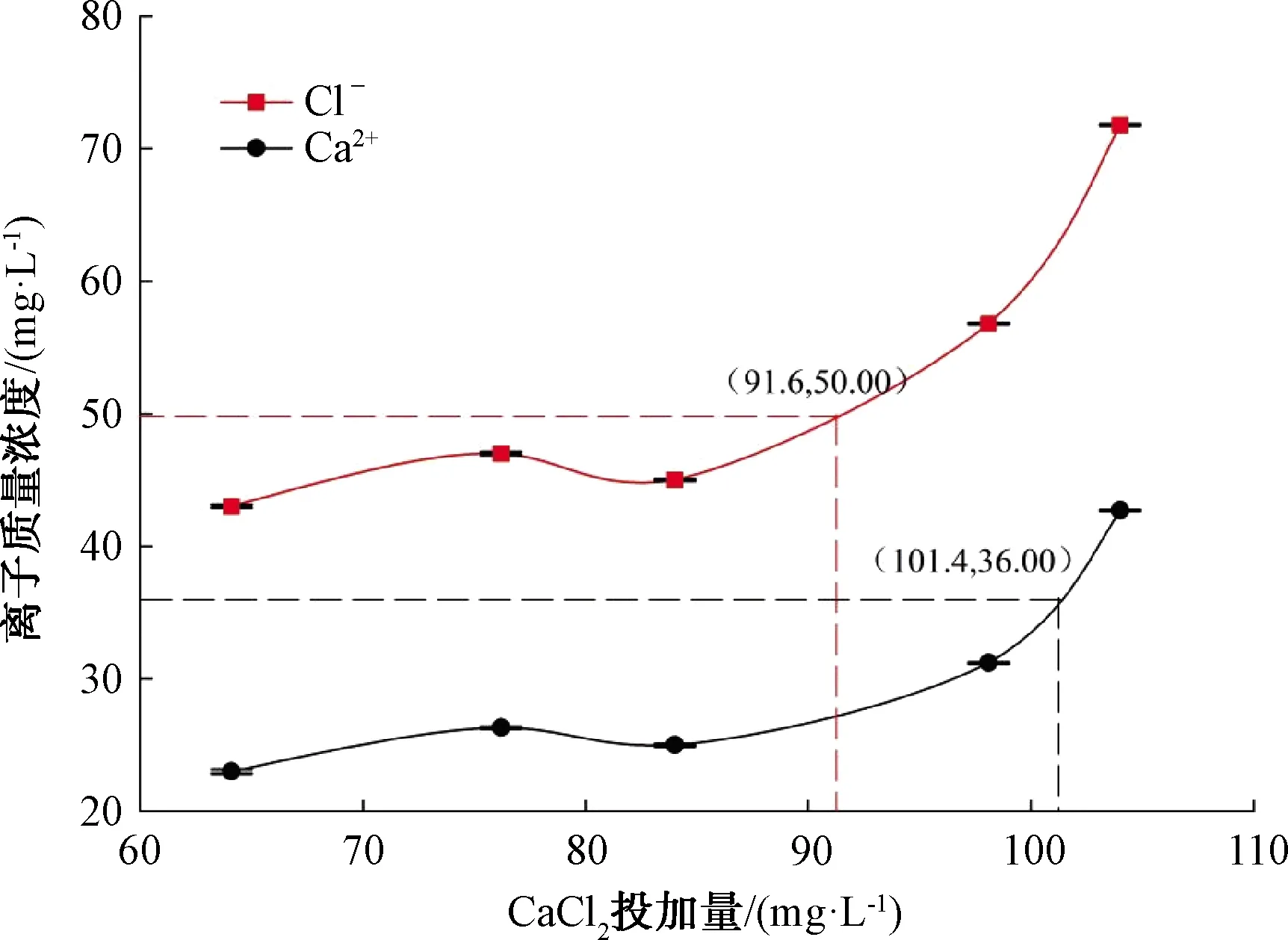
圖3 CaCl2投加量對Ca2+和Cl-的影響Fig.3 Influence of CaCl2 Dosage on Ca2+ and Cl-
膜蒸餾產水中投加不同量的CaCl2時,Cl-和Ca2+含量變化趨勢如圖3所示,CaCl2的投加迅速提高水中氯化物和Ca2+的含量,這是因為CaCl2在溶液中完全電離出Ca2+和Cl-。隨著CaCl2投加量從64.1 mg/L增至104.0 mg/L,Cl-質量濃度從最初的(42.97±0.12) mg/L逐漸提高到(71.80±0.08) mg/L;Ca2+質量濃度從(23.00±0.16) mg/L提高到(42.67±0.05) mg/L。CaCl2投加量提升的開始階段,Cl-和Ca2+含量增加較慢,但當CaCl2增大到一定程度后,二者提升速率明顯增大。當CaCl2質量濃度在91.6~104.0 mg/L時,氯化物的質量濃度在50.00~(71.80±0.08) mg/L;當CaCl2質量濃度在64.1~101.4 mg/L時,Ca2+的質量濃度在(23.00±0.16)~36.00 mg/L,均符合飲用水標準。
膜蒸餾產水中投加不同量的CaCl2時,TH和TA變化趨勢如圖4所示,CaCl2的投加迅速提高TH,但是TA基本不受影響,只是略微有所下降。水的硬度是指溶解在水中的鹽類物質的含量,即鈣鹽與鎂鹽含量的多少,而堿度是指水中能與強酸發生中和作用的物質的總量。CaCl2的加入提高了水中Ca2+的濃度,但是硬度是離子含量綜合體現的結果,所以當CaCl2的投加量為84.0 mg/L,硬度略有降低,但是整體上硬度隨CaCl2的投加而呈增加趨勢。而CaCl2是不與強酸發生反應的物質,對堿度的影響不大。隨著CaCl2投加量從64.1 mg/L增至104.0 mg/L,TH從最初的(57.40±0.16) mg/L逐漸提高到(107.03±0.12) mg/L;TA在(16.06±0.09)~(18.03±0.05) mg/L。只有當CaCl2質量濃度超過102.8 mg/L時,TH才能滿足100~200 mg/L的標準。
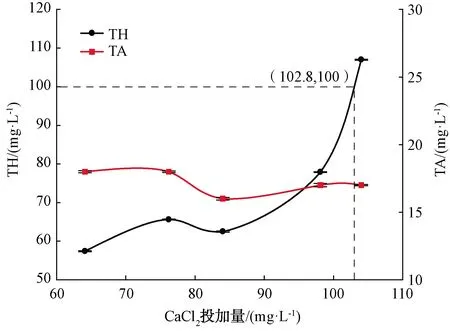
圖4 CaCl2投加量對TH和TA的影響Fig.4 Influence of CaCl2 Dosage on TH and TA
從上述結果可以看出,膜蒸餾產水中投加CaCl2能夠有效提高產水的TH,相應地氯化物和Ca2+的濃度也會增加,但是TDS始終低于理想值,水的pH也略有降低,且對TA幾乎沒有影響。考慮到后面還需要通過投加NaHCO3的方法提高TA,而投加NaHCO3同時會提高pH和TDS。因此,這里只綜合考慮Cl-、Ca2+和TH來確定CaCl2的投加量。
由圖3可知,同時滿足Ca2+和Cl-要求的CaCl2投加量在91.6~101.4 mg/L。而由圖4可知,滿足TH要求的CaCl2投加量不低于102.8 mg/L即可。綜合考慮試驗數據擬合等誤差因素,在下一步NaHCO3調節TA的試驗中,CaCl2的投加量在98.1~103.0 mg/L。
2.2 NaHCO3的投加量對礦化效果的影響
在上述試驗基礎上,先投加102.0~102.2 mg/L的CaCl2,再通過投加不同濃度的NaHCO3的方法調節堿度,同樣配置5個水樣,各參數測量結果如表2所示。
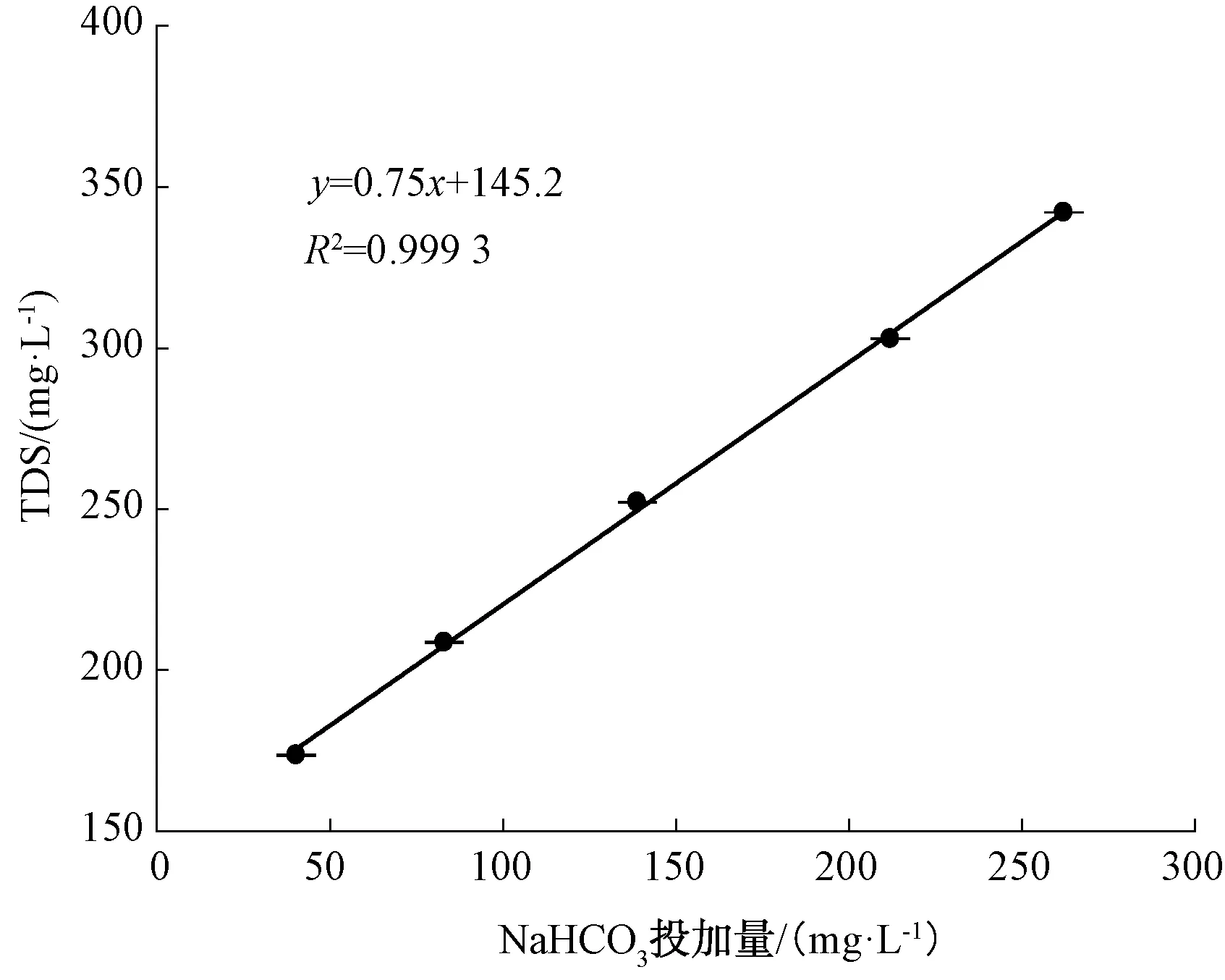
圖5 NaHCO3投加量對TDS的影響Fig.5 Influence of NaHCO3 Dosage on TDS
投加不同量的NaHCO3,TDS變化趨勢如圖5所示,NaHCO3的投加明顯進一步提高水的TDS和電導率,同樣是因為NaHCO3易溶于水,提高了水中溶質的含量。隨著NaHCO3投加量從40.2 mg/L增至262.1 mg/L,TDS從最初的(173.63±0.12) mg/L逐漸提高到(342.10±0.08) mg/L,電導率從(201.60±0.16) μS/cm增至(217.47±0.12) μS/cm。同CaCl2的投加對TDS影響不同,NaHCO3的投加使TDS呈現線性增長。NaHCO3的投加量在206.4~262.1 mg/L時,TDS質量濃度在300~500 mg/L,此時符合《生活飲用水衛生標準》(GB 5749—2006)的基本要求,也能夠滿足健康直飲水的要求。
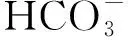
(5)
因此,隨著NaHCO3投加量從40.2 mg/L增至262.1 mg/L,水的pH值先從最初的(6.640±0.008)逐漸提高到(7.450±0.008),隨后稍有降低,降至(7.320±0.016)。根據pH值的限制(6.5~8.5),NaHCO3的投加量在40.2~262.1 mg/L時,皆符合要求,當NaHCO3的投加量為206.4 mg/L時,pH值為7.44。
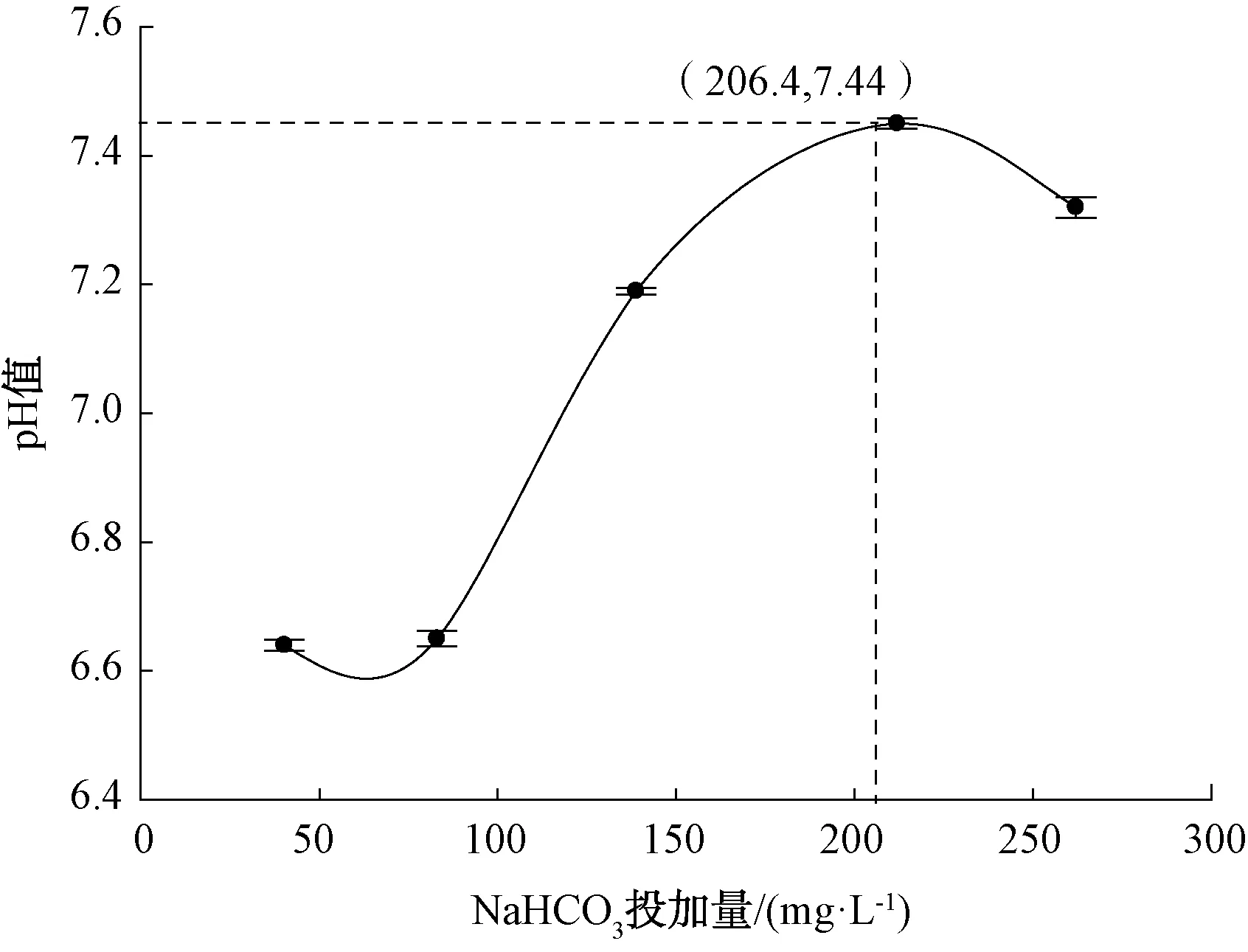
圖6 NaHCO3投加量對pH值的影響Fig.6 Influence of NaHCO3 Dosage on pH Value
投加不同量的NaHCO3水中Cl-和Ca2+濃度變化趨勢如圖7所示,理論上,NaHCO3的投加量不會對水中氯化物和Ca2+的含量造成影響,圖7中也可以看出二者雖然有變化,但是變化幅度很小,可能是由于在第一步投加CaCl2時的微小誤差所引起的。但由于NaHCO3溶于水時完全電離出Na+,使溶液中Na+的質量濃度顯著增加,從(11.03±0.12) mg/L增至(71.70±0.08) mg/L,此時,Cl-的質量濃度為58.44~(62.37±0.05) mg/L,Ca2+的質量濃度為(30.37±0.12)~(32.57±0.12) mg/L,皆符合生活飲用水的水質標準。
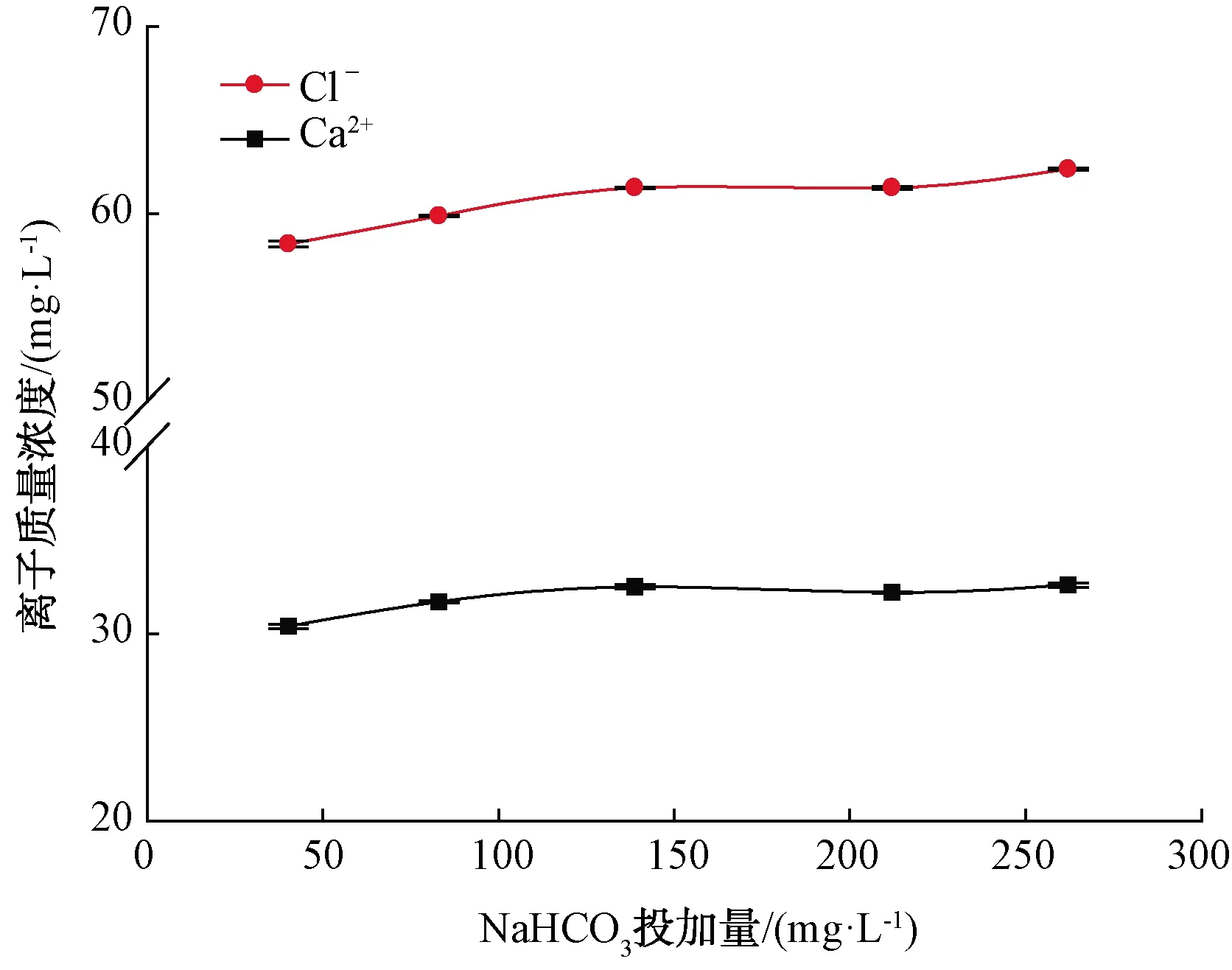
圖7 NaHCO3投加量對Cl-和Ca2+含量的影響Fig.7 Influence of NaHCO3 Dosage on Ca2+ and Cl-
投加不同量的NaHCO3水的TH和TA變化趨勢如圖8所示。NaHCO3的投加顯著提高TA,只投加CaCl2時(圖4),TA質量濃度在(16.06±0.09)~(18.03±0.05) mg/L,投加NaHCO3之后,TA線性增加,這是因為NaHCO3能與強酸發生中和反應,增加了水中能與強酸發生作用的物質的總量,從而提高了TA。NaHCO3的投加量從40.2 mg/L增至262.1 mg/L時,TA從(58.03±0.05) mg/L線性提升到(324.07±0.09) mg/L。而TH變化不大,質量濃度約為100 mg/L。根據《生活飲用水衛生標準》(GB 5749—2006),TA應大于80 mg/L,因此,NaHCO3的質量濃度為58.7~262.1 mg/L,當NaHCO3的質量濃度為206.4 mg/L時,TA為257.41 mg/L。
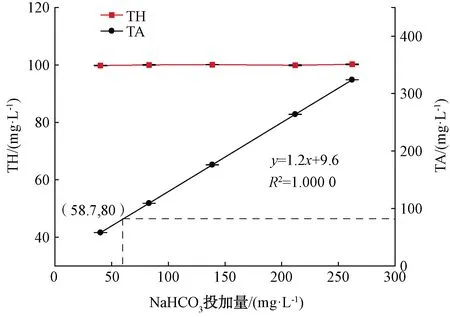
圖8 NaHCO3投加量對TH和TA的影響Fig.8 Influence of NaHCO3 Dosage on TH and TA
由圖5~圖8可知,NaHCO3的投加能夠引入Na+,同時有效提高水的TDS、pH和TA,但是對氯化物、Ca2+和TH基本沒有影響。礦化水不僅要滿足《生活飲用水衛生標準》(GB 5749—2006)的要求,還要能夠滿足衛生安全性和健康安全性的要求,因此,在CaCl2的投加量為102.0~102.2 mg/L的前提下,繼續投加NaHCO3質量濃度在206.4~262.1 mg/L時為最佳投料量。
3 結論
針對島礁供水問題,采用直接投加藥劑法對真空膜蒸餾產水進行礦化處理。分析CaCl2和NaHCO3的投加對淡化水水質的影響,探討既達到標準水質要求又滿足健康直飲水要求下CaCl2和NaHCO3的投加量,得出以下結論。
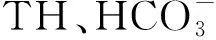
(2)在CaCl2的投加量為102.0~102.2 mg/L的前提下,繼續投加NaHCO3質量濃度在206.4~262.1 mg/L,得到的礦化水的各項指標如下:TDS為300.0~342.1 mg/L;pH值為7.32~(7.45±0.08);Ca2+質量濃度為32.04~(32.57±0.12) mg/L;Cl-質量濃度為61.36~(62.31±0.05) mg/L;Na+質量濃度為56.71~(71.70±0.08) mg/L;TH質量濃度為100 mg/L;TA質量濃度為257.41~(324.07±0.09) mg/L。各項指標都能達到《生活飲用水衛生標準》(GB 5749—2006)的要求,也能滿足健康直飲水的要求。
(3)本項研究為島礁海水淡化水的礦化處理提供了一定的借鑒,也為與其他處理方法聯用提供了一定的依據。

