何首烏及首烏藤中二蒽酮類成分研究進展△
楊建波,汪祺a,高慧宇,王雪婷,宋云飛,王瑩,程顯隆,魏鋒*,靳洪濤,段寶忠,馬雙成*
1.中國食品藥品檢定研究院,北京 100050;2.中國醫學科學院 藥物研究所,北京 100050;3.大理大學 藥學院,云南 大理 671000
何首烏為蓼科植物何首烏Polygonum multiflorumThunb.的干燥塊根,為著名傳統補益類中藥,有生和制何首烏之分,生何首烏具有解毒、消癰、截瘧、潤腸通便等功效;制何首烏具有補肝腎、益精血、烏須發、強筋骨等功效[1]183-184。首烏藤,別名夜交藤,為何首烏的干燥藤莖,秋、冬二季采割,除去殘葉,捆成把或趁鮮切段,干燥,具有養血安神、祛風通絡的功效,可用于治療失眠多夢、血虛身痛、風濕痹痛和皮膚瘙癢等[1]277-278。何首烏和首烏藤均為我國傳統中藥,其中何首烏為傳統中草藥的“四大仙草”之一,被廣泛應用于治療烏發及脫發、補肝腎和調血脂的中藥制劑和保健食品之中[2]。文獻報道[3-12],何首烏和首烏藤中主要含有蒽醌類(單核蒽醌和雙核蒽醌)、二苯乙烯類、黃酮類和多酚類等成分。但是,近年來關于服用何首烏、首烏藤及其相關制劑所引發的肝損傷不良反應報道較多,已經引起國內外科研人員的高度關注[13-14]。
本課題組首次從何首烏中分離得到雙核蒽醌,即二蒽酮類成分,藥理研究結果顯示其也具有一定的肝毒性[15-17],提示其可能與何首烏造成肝損傷有一定的相關性。因此,本文對何首烏及首烏藤中二蒽酮類成分的提取分離、在線鑒別、安全性評價和含量測定等方面進行系統的綜述,為該類成分肝毒性的進一步研究提供參考。
1 二蒽酮類成分的提取分離
本課題組采用大孔吸附樹脂(DM-8 型)、十八烷基硅烷鍵合硅膠(ODS)、Sephadex LH-20、MCI和半制備液相等多種色譜技術,對何首烏70%乙醇提取物進行了系統的分離和純化,從中首次分離得到14 個二蒽酮類成分[6-8],分別為反式-大黃素-大黃素二蒽酮(1)、順式-大黃素-大黃素二蒽酮(2)、polygonumnolide A1(3)、polygonumnolide A2(4)、polygonumnolide A3(5)、polygonumnolide A4(6)、polygonumnolide B1(7)、polygonumnolide B2(8)、polygonumnolide B3(9)、polygonumnolide C1(10)、polygonumnolide C2(11)、polygonumnolide C3(12)、polygonumnolide C4(13)和polygonumnolide E(14)。薄瑞[18]采用水浴回流提取法對首烏藤中的二蒽酮類成分進行提取,獲得70%乙醇提取物;采用D101型大孔吸附樹脂法對首烏藤70%乙醇提取物中的二蒽酮進行了選擇性富集;利用正、反相硅膠和半制備液相等多種色譜技術對其進行系統的分離和純化,從中首次分離得到2 個二蒽酮苷類成分,分別為PMC-a-1(15)與PMC-a-2(16)。
目前,從何首烏及首烏藤中所分離得到16 個二蒽酮類成分主要為大黃素-大黃素型二蒽酮和大黃素-大黃素甲醚型二蒽酮,是通過大黃素的C-10和大黃素甲醚的C-10相互聚合而成,具體結構見圖1。
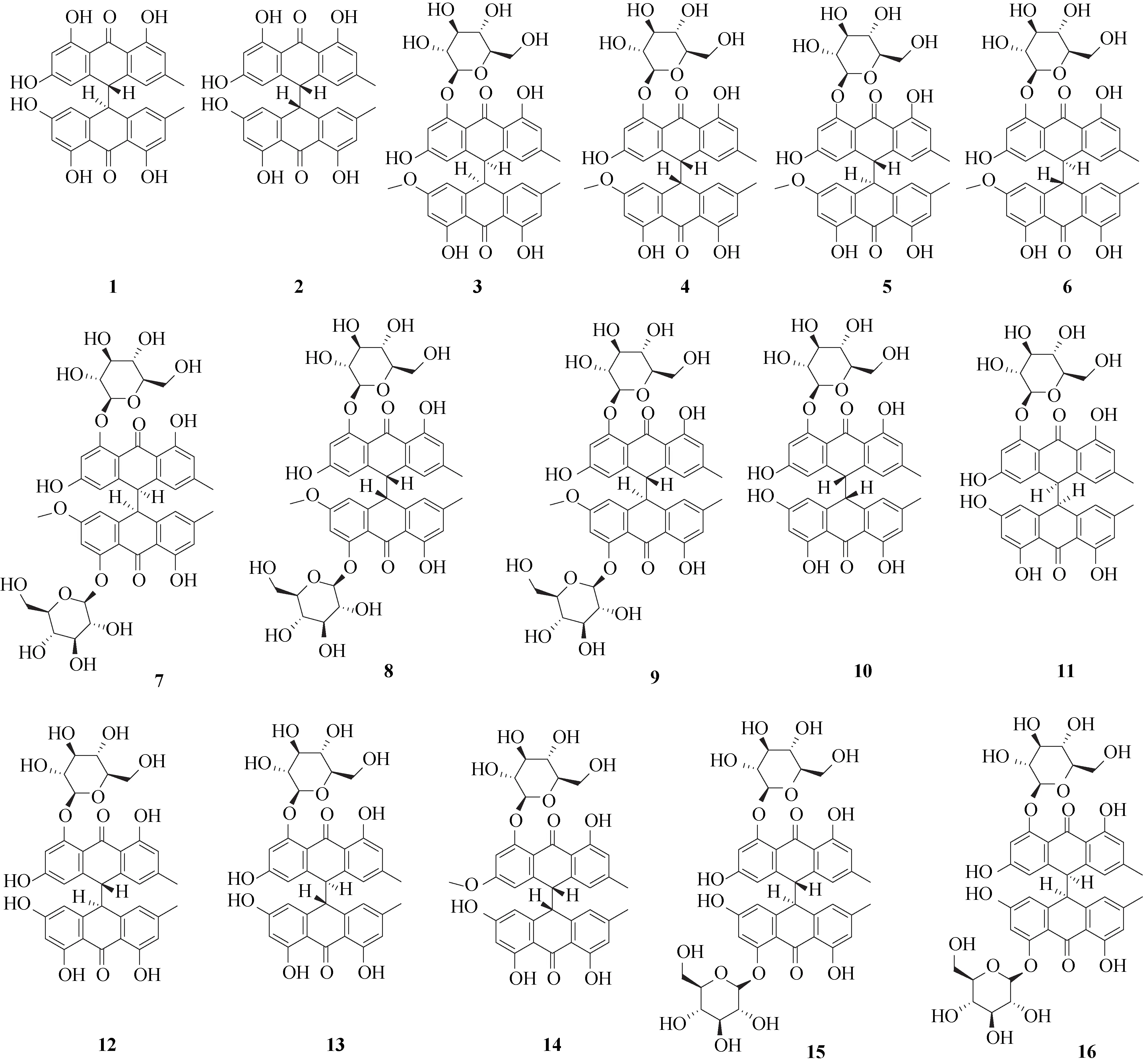
圖1 何首烏和首烏藤中分離得到的二蒽酮單體化合物
2 二蒽酮類成分的在線鑒別
Xu 等[19]運用高效液相色譜-線性離子阱-靜電場軌道阱質譜法(HPLC-LTQ-Orbitrap MS)對廣東德慶產區何首烏的70%乙醇提取液進行分析,通過一級質譜的準分子離子峰和多級質譜碎片信息推測出28 個新的二蒽酮苷類成分,其苷元為大黃素(10→10′)大黃素型二蒽酮(Ⅰ)和大黃素(10→10′)大黃素甲醚型二蒽酮(Ⅱ),其中取代基主要為甲氧基、葡萄糖苷和丙二酰基化的葡萄糖苷等。Yang等[20]通過70%乙醇提取、DM-8型大孔吸附樹脂純化和Sephadex LH-20 凝膠柱色譜富集等方法富集得到何首烏中微量成分二蒽酮類成分,并進一步運用高效液相色譜-紫外檢測器-傅里葉變換離子回旋共振質譜法(HPLC-UV-FTICR-MS)對該組分和分離得到的7個二蒽酮對照品順式-大黃素-大黃素二蒽酮(2)、polygonumnolide A1(3)、polygonumnolide A2(4)、polygonumnolide B1(7)、polygonumnolide C2(11)、polygonumnolide C3(12)和polygonumnolide E(14)進行一級高分辨質譜和多級質譜分析,結果表明何首烏中存在45個二蒽酮類成分,其中30個二蒽酮苷類成分可能為新化合物,主要分為3 種結構類型,分別為大黃素-大黃素型二蒽酮(Ⅰ)、大黃素-大黃素甲醚型二蒽酮(Ⅱ)及大黃素甲醚-大黃素甲醚型二蒽酮(Ⅲ),其差異主要是取代基和C-10/10′的手型中心構型不同,具體見圖2。
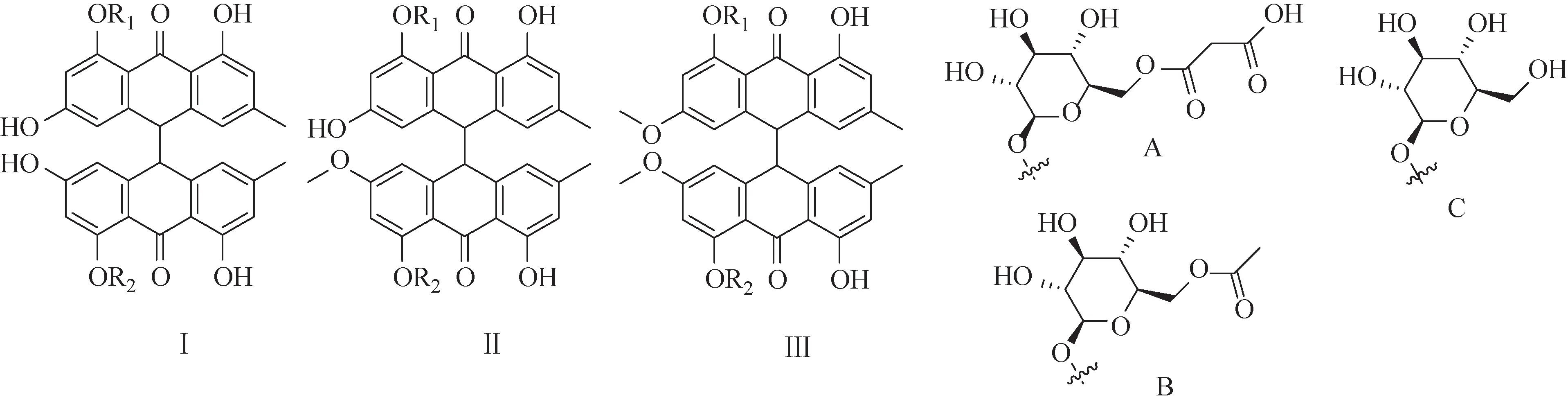
圖2 何首烏和首烏藤中不同類型二蒽酮類成分及其不同取代基類型
薄瑞[18]采用超高效液相色譜串聯四級桿飛行時間質譜法(UPLC-Q-TOF-MS/MS)對富集得到的首烏藤70%乙醇提取物中的二蒽酮類成分進行定性分析,首次從首烏藤中推測出72 個二蒽酮苷類成分和5個二蒽酮苷元成分,主要也分為3種結構類型,分別為Ⅰ、Ⅱ、Ⅲ,其中有29 個二蒽酮苷類成分可能為新化合物。
3 二蒽酮類成分的毒性研究
3.1 不同細胞水平的毒性評價
Yang等[6]對從何首烏中分離得到polygonumnolides A1~A4、polygonumnolides B1~B3(3~9)7個二蒽酮化合物,進行人口腔表皮癌細胞KB 的細胞毒活性評價,發現其半數抑制濃度(IC50)值分別為29.7、35.6、36.8、31.1、82.4、88.6、95.8 μmol·L-1,均表現中等強度的細胞毒活性。Yang 等[7]對從何首烏中分離得到反式-大黃素-大黃素二蒽酮(1)、順式-大黃素-大黃素二蒽酮(2)和polygonumnolides C1~C4(10~13)6 個二蒽酮類化合物進行人正常肝細胞L02的細胞毒活性評價,結果發現化合物10~13作用24 h對L02細胞的IC50值分別為313.05、205.20、294.20、207.35 μmol·L-1,表現中等強度的細胞毒活性。Yang等[21]還對反式-大黃素-大黃素二蒽酮(1)和順式大黃素-大黃素二蒽酮(2)進行人肝癌細胞HepaRG 的細胞毒活性評價,發現其IC50值分別為10.98、15.45 μmol·L-1。薄瑞[18]對從首烏藤分離得到的PMC-a-1(15)進行L02、HepG2細胞的細胞毒活性評價,結果發現其具有中等強度的抑制作用,作用48 h 的IC50值分別為45.25、72.78 μmol·L-1;PMC-a-2 未對HepG2 細胞表現較強的抑制活性,而對L02細胞表現一定的細胞毒活性,作用48 h的IC50值為61.11 μmol·L-1,從而提示二蒽酮類成分可能是何首烏產生肝毒性的組分之一。
3.2 酶水平的抑制作用
膽紅素的異常代謝也是何首烏的臨床不良反應之一。由于尿苷二磷酸(UDP)-葡萄糖醛酸轉移酶1A1(UGT1A1)是唯一負責膽紅素代謝的酶,因此Wang 等[17]研究了二蒽酮化合物對大鼠肝微粒體中UGT1A1的抑制作用,結果發現反式-大黃素-大黃素二蒽酮(1)、順式-大黃素-大黃素二蒽酮(2)和polygonumnolide C2(11)均具有肝微粒體酶的抑制活性,表觀抑制常數(Ki)值分別為0.863、1.083、4.291 μmol·L-1,進一步分析發現二蒽酮類化合物的6/6′位羥基為其潛在的活性基團。汪祺等[22]運用分子對接等技術對何首烏中分離得到的16 個二蒽酮類成分進行了毒性預測,結果發現這些二蒽酮類成分的大鼠經口服給藥的半數致死量(LD50)為125.3~1 239.6 mg·kg-1,從而提示該類成分可能具有潛在的肝毒性。
3.3 模式生物斑馬魚的毒性評價
Yang 等[15]以斑馬魚胚胎發育為評價模型,將受精后2~4 h(2~4 hpf)的斑馬魚胚胎暴露于反式-大黃素-大黃素二蒽酮(1)、順式-大黃素-大黃素二蒽酮(2)和polygonumnolides C1~C4(10~13)等二蒽酮類化合物,結果發現其96 hpf 的LD50值分別為(0.87±0.27)、(0.92±0.37)、(1.13±0.06)、(1.55±0.49)、(14.31±0.00)、(1.73±0.33)mg·L-1,進一步分析發現化合物1、2、10、11和13所觀察到最低作用劑量(LOEL)分別為0.500、0.500、0.250、2.000、2.000 mg·L-1,表明該類成分具有一定的斑馬魚胚胎發育毒性。Li 等[16]采用斑馬魚肝毒性評價模型,以斑馬魚肝區面積、肝區灰度值和卵黃囊的吸收面積等為評價指標,對從何首烏中分離得到的反式-大黃素-大黃素二蒽酮(1)、順式-大黃素-大黃素二蒽酮(2)、polygonumnolide C1(10)和polygonumnolide C4(13)進行肝毒性評價,結果發現游離二蒽酮較結合二蒽酮具有更強的肝毒性,推測二蒽酮類成分可能是何首烏潛在誘發肝毒性的物質基礎之一。
4 二蒽酮類成分的含量分析
Yang 等[21]運用超高效液相色譜-三重四極桿質譜法(UHPLC-QQQ-MS/MS)對從不同產地和市場收集的90 批生何首烏中6 個二蒽酮類成分polygonumnolide C4(13)、polygonumnolide C3(12)、polygonumnolide C1(10)、polygonumnolide C2(11)、反式-大黃素-大黃素二蒽酮(1)和順式-大黃素-大黃素二蒽酮(2)的含量進行分析。結果發現,何首烏中二蒽酮類成分含量差異較大,6 個二蒽酮類化合物質量分數分別為0.03~19.04、0.02~13.86、0.07~15.53、0.034~23.35、0.38~83.67、0.29~67.00 μg·g-1。選擇其中15 批何首烏樣品,按照《中華人民共和國藥典》2015 年版制何首烏項下“清蒸工藝”進行炮制,結果發現,經過24 h炮制后何首烏中6 個二蒽酮類成分的含量下降幅度均超過80%,表明合理和規范炮制的制何首烏中二蒽酮類成分含量大幅下降。對從市場收集的86 批制首烏中6個二蒽酮類成分含量進行分析,結果發現,其質量分數分別為0.02~13.03、0.05~8.94、0.02~7.23、0.03~12.75、0.10~28.54、0.14~27.79 μg·g-1。如果以炮制24 h 制何首烏中6 個二蒽酮類成分的含量來分析市場中制何首烏的質量,發現65%以上市場中銷售的制何首烏可能存在炮制不規范的問題,需要進一步深入調查與研究。
薄瑞[18]發現首烏藤中所存在的72 個二蒽酮苷類成分主要分為3 種類型,其中大黃素-大黃素二蒽酮和大黃素-大黃素甲醚二蒽酮具有m/z254、416、458的特征離子,而大黃素甲醚-大黃素甲醚二蒽酮具有m/z268、537 的特征離子,運用UPLC-Q-TOF-MS/MS,以半定量的方式初步評價了首烏藤中各類型的二蒽酮的相對含量。結果發現,在首烏藤中Ⅰ和Ⅱ型的二蒽酮類成分的含量占比相對較高,分別為54.69%和41.58%,而Ⅲ型的二蒽酮類成分的含量占比較低,為3.73%。
5 討論
何首烏及首烏藤中二蒽酮類成分主要為2 個分子大黃素和/或大黃素甲醚蒽酮通過蒽環碳原子連接而成的化合物,主要通過C-10 和C-10′中位連接,多以單鍵連接。本課題組通過傳統的提取分離與純化技術首次從何首烏中分離得到二蒽酮類成分,并對其進行了L02、HepG2、HepRG 等細胞毒性評價及UGT1A1 酶、模式生物斑馬魚等毒性評價,結果發現該類成分具有潛在的肝毒性,可能為何首烏中肝毒性組分之一。然而該類成分為何首烏及首烏藤中微量成分,具有數量多和單一成分含量低等特點,所以通過傳統的提取與分離獲得較為費時費力,故有必要對其開展全合成研究,解決樣品量不足的問題。目前,對何首烏及首烏藤中二蒽酮類成分的毒性評價主要集中在體外細胞和模式生物斑馬魚模型,這些模型與哺乳動物模型存在一定的差異,所以有必要對其進行小鼠急性毒性與大鼠長期毒性評價等實驗,有助于進一步系統地闡明該類成分的肝毒性。
與此同時,二蒽酮類成分還廣泛存在于蓼科植物大黃、豆科植物番瀉葉和藤黃科植物貫葉連翹中,該類成分還具有較好的瀉下作用[23],且具有抗腫瘤[24]、抗病毒[25]和抗抑郁[26]等活性,所以有必要對何首烏及首烏藤中的二蒽酮類成分進行系統的提取分離和結構鑒定,進一步對其有效性進行評價,從而有助于評價含二蒽酮類成分中藥的安全性與有效性,為臨床安全、合理用藥提供參考。

